| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Furano [1] | |||
| Nombre IUPAC sistemático 1,4-Epoxibuta-1,3-dieno 1-Oxaciclopenta-2,4-dieno | |||
| Otros nombres Oxol Oxa [5] anuleno 1,4-epoxi-1,3-butadieno 5-Oxacyclopenta-1,3-dieno 5-Oxacyclo-1,3-pentadieno furfuran óxido Divinylene | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.003.390 | ||
| KEGG | |||
PubChem CID | |||
| UNII | |||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 4 H 4 O | |||
| Masa molar | 68,075 g · mol −1 | ||
| Apariencia | Líquido volátil incoloro | ||
| Densidad | 0,936 g / ml | ||
| Punto de fusion | −85,6 ° C (−122,1 ° F; 187,6 K) | ||
| Punto de ebullición | 31,3 ° C (88,3 ° F; 304,4 K) | ||
| -43,09 · 10 −6 cm 3 / mol | |||
| Peligros | |||
| Ficha de datos de seguridad | Pennakem | ||
| Frases R (desactualizadas) | R26 / 27/28 , R45 | ||
| Frases S (desactualizadas) | S16 , S37 , S45 , S28 | ||
| NFPA 704 (diamante de fuego) |  3 4 1 | ||
| punto de inflamabilidad | −36 ° C (−33 ° F; 237 K) | ||
autoignición temperatura | 390 ° C (734 ° F; 663 K) | ||
| Límites explosivos | Inferior: 2,3% Superior: 14,3% a 20 ° C | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis mediana ) | > 2 g / kg (rata) | ||
| Compuestos relacionados | |||
Heterociclos relacionados | Pirrol tiofeno | ||
Compuestos relacionados | Tetrahidrofurano (THF) 2,5- Dimetilfurano Benzofurano Dibenzofurano | ||
| Estructura | |||
Grupo de puntos | C 2v | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
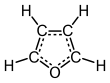
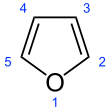
El furano es un compuesto orgánico heterocíclico , que consta de un anillo aromático de cinco miembros con cuatro átomos de carbono y un átomo de oxígeno . Los compuestos químicos que contienen tales anillos también se denominan furanos.
El furano es un líquido incoloro, inflamable y altamente volátil con un punto de ebullición cercano a la temperatura ambiente. Es soluble en disolventes orgánicos comunes , incluidos alcohol , éter y acetona , y es ligeramente soluble en agua . [2] Su olor es "fuerte, etéreo; parecido al cloroformo ". [3] Es tóxico y puede ser cancerígeno en humanos. El furano se utiliza como punto de partida para otras especialidades químicas . [4]
Historia [ editar ]
El nombre "furano" proviene del latín furfur , que significa salvado . [5] (El furfural se produce a partir del salvado). El primer derivado de furano que se describió fue el ácido 2-furoico , de Carl Wilhelm Scheele en 1780. Otro derivado importante, el furfural , fue informado por Johann Wolfgang Döbereiner en 1831 y caracterizado nueve años después por John Stenhouse . El propio furano fue preparado por primera vez por Heinrich Limpricht en 1870, aunque lo llamó "tetrafenol" (como si fuera un análogo de cuatro carbonos del fenol , C 6 H 6 O).[6] [7]
Producción [ editar ]
Industrialmente, el furano se fabrica mediante la descarbonilación del furfural catalizada con paladio o mediante la oxidación del 1,3-butadieno catalizada con cobre : [4]
En el laboratorio, el furano se puede obtener a partir del furfural mediante oxidación a ácido 2-furoico, seguido de descarboxilación . [8] También se puede preparar directamente por descomposición térmica de materiales que contienen pentosa y sólidos celulósicos , especialmente madera de pino .
Síntesis de furanos [ editar ]
La síntesis de Feist-Benary es una forma clásica de sintetizar furanos, aunque se han desarrollado muchas síntesis. [9] Uno de los métodos de síntesis más simples de furanos es la reacción de 1,4-dicetonas con pentóxido de fósforo (P 2 O 5 ) en la síntesis de Paal-Knorr . La reacción de formación de tiofeno de 1,4-dicetonas con el reactivo de Lawesson también forma furanos como productos secundarios. Existen muchas rutas para la síntesis de furanos sustituidos. [10]
Química [ editar ]
El furano es aromático porque uno de los pares de electrones solitarios en el átomo de oxígeno está deslocalizado en el anillo, creando un sistema aromático 4 n + 2 (ver la regla de Hückel ) similar al benceno . Debido a la aromaticidad, la molécula es plana y carece de dobles enlaces discretos . El otro par solitario de electrones del átomo de oxígeno se extiende en el plano del sistema de anillo plano. La hibridación sp 2 es para permitir que uno de los pares solitarios de oxígeno resida en un orbital p y así permitirle interactuar dentro del sistema π .
Debido a su aromaticidad, el comportamiento del furano es bastante diferente al de los éteres heterocíclicos más típicos como el tetrahidrofurano .
- Es considerablemente más reactivo que el benceno en las reacciones de sustitución electrofílica , debido a los efectos donadores de electrones del heteroátomo de oxígeno. El examen de los contribuyentes de resonancia muestra el aumento de la densidad electrónica del anillo, lo que conduce a un aumento de las tasas de sustitución electrofílica. [11]
- El furano actúa como dieno en las reacciones de Diels-Alder con dienófilos deficientes en electrones , como el ( E ) -3-nitroacrilato de etilo. [12] El producto de reacción es una mezcla de isómeros con preferencia por el isómero endo :
- La reacción de Diels-Alder de furano con arinos proporciona los correspondientes derivados de dihidronaftalenos , que son intermedios útiles en la síntesis de otros compuestos aromáticos policíclicos . [13]
- La hidrogenación de furanos secuencialmente produce dihidrofuranos y tetrahidrofuranos .
- En la reacción de Achmatowicz , los furanos se convierten en compuestos de dihidropirano .
- El pirrol se puede preparar industrialmente haciendo reaccionar furano y amoniaco en presencia de catalizadores ácidos sólidos , tales como SiO 2 y Al 2 O 3 . [14]
Seguridad [ editar ]
El furano se encuentra en los alimentos comerciales tratados térmicamente y se produce mediante la degradación térmica de los componentes naturales de los alimentos. [15] [16] Se puede encontrar en café tostado , café instantáneo y alimentos procesados para bebés . [16] [17] [18] La investigación ha indicado que el café hecho en café espresso fabricantes , y café hecho de cápsulas contiene más furano que la formulada en tradicionales cafetera de goteo , aunque los niveles son todavía dentro de los límites de salud seguros. [19]
La exposición al furano en dosis aproximadamente 2000 veces el nivel proyectado de exposición humana a los alimentos aumenta el riesgo de tumores hepatocelulares en ratas y ratones y tumores de los conductos biliares en ratas. [20] Por tanto, el furano está catalogado como posible carcinógeno humano . [20]
Ver también [ editar ]
- BS 4994 - Resina de furano como FRP termoendurecible para equipos de plantas de procesos químicos
- Furanocumarina
- Furanoflavonoide
- Furanosa
- Ácido furantetracarboxílico
- Anillos aromáticos simples
- Ácidos grasos furanos
- Tetrahidrofurano
Referencias [ editar ]
- ^ Nomenclatura de la química orgánica: Recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: La Real Sociedad de Química . 2014. p. 392. doi : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
- ^ Jakubke, Hans Dieter; Jeschkeit, Hans (1994). Enciclopedia concisa de química . Walter de Gruyter. págs. 1–1201 . ISBN 0-89925-457-8.
- ^ Publicación del DHHS (NIOSH) núm. 2016-171 , p. 2, consultado Nov 2019
- ^ a b Hoydonckx, ÉL; Van Rhijn, WM; Van Rhijn, W .; De Vos, DE; Jacobs, PA "Furfural y derivados". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a12_119.pub2 .
- ^ Senning, Alexander (2006). Diccionario de quimioetimología de Elsevier . Elsevier. ISBN 0-444-52239-5.
- ^ Limpricht, H. (1870). "Ueber das Tetraphenol C 4 H 4 O" . Berichte der Deutschen Chemischen Gesellschaft . 3 (1): 90–91. doi : 10.1002 / cber.18700030129 .
- ^ Rodd, Ernest Harry (1971). Química de los compuestos de carbono: un tratado moderno e integral . Elsevier.
- ^ Wilson, WC (1941). "Furan" . Síntesis orgánicas .; Volumen colectivo , 1 , p. 274
- ^ Hou, XL; Cheung, HY; Hon, TY; Kwan, PL; Lo, TH; Tong, SY; Wong, HN (1998). "Síntesis regioselectiva de furanos sustituidos". Tetraedro . 54 (10): 1955-2020. doi : 10.1016 / S0040-4020 (97) 10303-9 .
- ^ Katritzky, Alan R. (2003). "Síntesis de furanos 2,4-disustituidos y 2,3-benzo-1,3a, 6a-triazapentalenos sustituidos con 4,6-diarilo" (PDF) . Arkivoc . 2004 (2): 109. doi : 10.3998 / ark.5550190.0005.208 .
- ^ Bruice, Paula Y. (2007). Química orgánica (5ª ed.). Upper Saddle River, Nueva Jersey: Pearson Prentice Hall. ISBN 978-0-13-196316-0.
- ^ Masesane, I .; Batsanov, A .; Howard, J .; Modal, R .; Acero, P. (2006). "El enfoque de oxanorborneno para los derivados 3-hidroxi, 3,4-dihidroxi y 3,4,5-trihidroxi del ácido 2-aminociclohexanocarboxílico" . Revista Beilstein de Química Orgánica . 2 (9): 9. doi : 10.1186 / 1860-5397-2-9 . PMC 1524792 . PMID 16674802 .
- ^ Filatov, MA; Baluschev, S .; Ilieva, IZ; Enkelmann, V .; Miteva, T .; Landfester, K .; Aleshchenkov, SE; Cheprakov, AV (2012). "Tetraariltetraantra [2,3] porfirinas: síntesis, estructura y propiedades ópticas" (PDF) . J. Org. Chem . 77 (24): 11119–11131. doi : 10.1021 / jo302135q . PMID 23205621 . Archivado desde el original (PDF) el 19 de febrero de 2020.
- ^ Harreus, Albrecht Ludwig. "Pirrol". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a22_453 .
- ^ Anese, M .; Manzocco, L .; Calligaris, S .; Nicoli, MC (2013). "Estrategias de aplicación industrial para mitigar la acrilamida, el furano y el 5-hidroximetilfurfural en los alimentos" (PDF) . Revista de Química Agrícola y Alimentaria . 61 (43): 10209-14. doi : 10.1021 / jf305085r . PMID 23627283 . Archivado desde el original (PDF) el 8 de agosto de 2017.
- ^ a b Moro, S .; Chipman, JK; Wegener, JW; Hamberger, C .; Dekant, W .; Mally, A. (2012). "Furano en alimentos tratados térmicamente: formación, exposición, toxicidad y aspectos de la evaluación de riesgos" (PDF) . Nutrición molecular e investigación alimentaria . 56 (8): 1197-1211. doi : 10.1002 / mnfr.201200093 . hdl : 1871/41889 . PMID 22641279 .
- ^ Autoridad europea de seguridad alimentaria (2011). "Actualización sobre los niveles de furano en los alimentos de los años de seguimiento 2004-2010 y evaluación de la exposición" . Revista EFSA . 9 (9): 2347. doi : 10.2903 / j.efsa.2011.2347 .
- ^ Waizenegger, J .; Winkler, G .; Kuballa, T .; Ruge, W .; Kersting, M .; Alexy, U .; Lachenmeier, DW (2012). "Análisis y evaluación de riesgos del furano en productos de café dirigidos a adolescentes". Aditivos Alimentarios y Contaminantes: Parte A . 29 (1): 19-28. doi : 10.1080 / 19440049.2011.617012 . PMID 22035212 . S2CID 29027966 .
- ^ "Cafeteras espresso: el café en cápsulas contiene más furano que el resto" . Science Daily . 14 de abril de 2011.
- ↑ a b Bakhiya, N .; Appel, KE (2010). "Toxicidad y carcinogenicidad del furano en la dieta humana" (PDF) . Archivos de Toxicología . 84 (7): 563–578. doi : 10.1007 / s00204-010-0531-y . PMID 20237914 . S2CID 19389984 .
Enlaces externos [ editar ]
| Wikimedia Commons tiene medios relacionados con Furan . |
- Métodos sintéticos recientes