| |||
| |||
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Ácido aminoacético | |||
| Otros nombres Ácido 2-aminoetanoico, glicool | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| Abreviaturas | Gly , G | ||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA | 100.000.248 | ||
| Número CE |
| ||
| KEGG | |||
PubChem CID | |||
| UNII | |||
Tablero CompTox ( EPA ) | |||
| |||
| Propiedades | |||
Fórmula química | C 2 H 5 N O 2 | ||
| Masa molar | 75.067 g · mol −1 | ||
| Apariencia | Blanco sólido | ||
| Densidad | 1,1607 g / cm 3 [2] | ||
| Punto de fusion | 233 ° C (451 ° F; 506 K) (descomposición) | ||
solubilidad en agua | 24,99 g / 100 ml (25 ° C) [3] | ||
| Solubilidad | soluble en piridina escasamente soluble en etanol insoluble en éter | ||
| Acidez (p K a ) | 2,34 (carboxilo), 9,6 (amino) [4] | ||
Susceptibilidad magnética (χ) | -40,3 · 10 −6 cm 3 / mol | ||
| Farmacología | |||
Código ATC | B05CX03 ( QUIÉN ) | ||
| Peligros | |||
| Ficha de datos de seguridad | Ver: página de datos | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis mediana ) | 2600 mg / kg (ratón, oral) | ||
| Página de datos complementarios | |||
Estructura y propiedades | Índice de refracción ( n ), constante dieléctrica (ε r ), etc. | ||
Datos termodinámicos | Comportamiento de fase sólido-líquido-gas | ||
Datos espectrales | UV , IR , RMN , MS | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
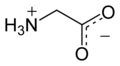
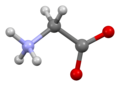
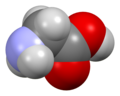
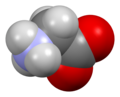
Glicina (símbolo Gly o G ; [5] / ɡ l aɪ s i n / ) [6] es un aminoácido que tiene un solo hidrógeno átomo como su cadena lateral . Es el aminoácido más simple (ya que el ácido carbámico es inestable), con la fórmula química NH 2 - CH 2 - COOH . La glicina es uno de los aminoácidos proteinogénicos . Está codificado por todos los codones.comenzando con GG (GGU, GGC, GGA, GGG). La glicina es parte integral de la formación de hélices alfa en la estructura de la proteína secundaria debido a su forma compacta. Por la misma razón, es el aminoácido más abundante en las triples hélices de colágeno . La glicina también es un neurotransmisor inhibidor : la interferencia con su liberación dentro de la médula espinal (como durante una infección por Clostridium tetani ) puede causar parálisis espástica debido a la contracción muscular desinhibida.
La glicina es un sólido cristalino incoloro y de sabor dulce. Es el único aminoácido proteinogénico aquiral . Puede caber en entornos hidrófilos o hidrófobos , debido a su cadena lateral mínima de un solo átomo de hidrógeno. El radical acilo es glicilo .
Historia y etimología [ editar ]
La glicina fue descubierta en 1820 por el químico francés Henri Braconnot cuando hidrolizó la gelatina hirviéndola con ácido sulfúrico . [7] Originalmente lo llamó "azúcar de gelatina", [8] [9] pero el químico francés Jean-Baptiste Boussingault demostró que contenía nitrógeno. [10] El científico estadounidense Eben Norton Horsford , entonces alumno del químico alemán Justus von Liebig , propuso el nombre "glycocoll"; [11] [12] sin embargo, el químico sueco Berzelius sugirió el nombre más simple "glicina". [13][14] El nombre proviene del griego palabra γλυκύς "sabor dulce" [15] (que también se relaciona con la prefijos glico- y gluco- , como en la glicoproteína y glucosa ). En 1858, el químico francés Auguste Cahours determinó que la glicina era una amina del ácido acético . [dieciséis]
Producción [ editar ]
Aunque la glicina se puede aislar de la proteína hidrolizada, esta no se usa para la producción industrial, ya que se puede fabricar más convenientemente mediante síntesis química. [17] Los dos procesos principales son la aminación de ácido cloroacético con amoníaco , dando glicina y cloruro de amonio , [18] y la síntesis de aminoácidos de Strecker , [19] que es el principal método sintético en los Estados Unidos y Japón. [20] De esta forma se producen anualmente unas 15 000 toneladas . [21]
La glicina también se cogenera como impureza en la síntesis de EDTA , que surge de las reacciones del coproducto de amoníaco. [22]
Reacciones químicas [ editar ]
Sus propiedades ácido-base son las más importantes. En solución acuosa, la glicina en sí es anfótera : a pH bajo, la molécula puede protonarse con una p K a de aproximadamente 2,4 y a pH alto pierde un protón con una p K a de aproximadamente 9,6 (los valores precisos de p K a dependen de la temperatura y fuerza iónica).
La glicina funciona como ligando bidentado para muchos iones metálicos. Un complejo típico es Cu (glicinato) 2 , es decir, Cu (H 2 NCH 2 CO 2 ) 2 , que existe tanto en isómeros cis como trans.
Como molécula bifuncional, la glicina reacciona con muchos reactivos. Estos se pueden clasificar en reacciones centradas en N y centro carboxilato.
La amina sufre las reacciones esperadas. Con los cloruros de ácido se obtiene el ácido amidocarboxílico, como el ácido hipúrico [23] y la acetilglicina. [24] Con ácido nitroso se obtiene ácido glicólico ( determinación de van Slyke ). Con yoduro de metilo, la amina se cuaterniza para dar betaína , un producto natural:
- H
3norte+
CH
2ARRULLO-
+ 3 CANALES 3 I → (CANALES
3)
3norte+
CH
2ARRULLO-
+ 3 HI
La glicina se condensa consigo misma para dar péptidos, comenzando con la formación de glicilglicina :
- 2 H
3norte+
CH
2ARRULLO-
→ H
3norte+
CH
2CONHCH
2ARRULLO-
+ H 2 O
La pirólisis de glicina o glicilglicina da 2,5- dicetopiperazina , la diamida cíclica.
Metabolismo [ editar ]
Biosíntesis [ editar ]
La glicina no es esencial para la dieta humana , ya que se biosintetiza en el cuerpo a partir del aminoácido serina , que a su vez se deriva del 3-fosfoglicerato , pero la capacidad metabólica para la biosíntesis de glicina no satisface la necesidad de síntesis de colágeno. [25] En la mayoría de los organismos, la enzima serina hidroximetiltransferasa cataliza esta transformación a través del cofactor piridoxal fosfato : [26]
- serina + tetrahidrofolato → glicina + N 5 , N 10 -tetrahidrofolato de metileno + H 2 O
En el hígado de los vertebrados , la síntesis de glicina es catalizada por la glicina sintasa (también llamada enzima de escisión de glicina). Esta conversión es fácilmente reversible : [26]
- CO 2 + NH+
4+ N 5 , N 10 -Tetrahidrofolato de metileno + NADH + H + ⇌ Glicina + tetrahidrofolato + NAD +
Además de ser sintetizada a partir de serina, la glicina también puede derivarse de treonina, colina o hidroxiprolina a través del metabolismo entre órganos del hígado y los riñones. [27]
Degradación [ editar ]
La glicina se degrada a través de tres vías. La vía predominante en animales y plantas es la inversa de la vía de la glicina sintasa mencionada anteriormente. En este contexto, el sistema enzimático involucrado generalmente se denomina sistema de escisión de glicina : [26]
- Glicina + tetrahidrofolato + NAD + ⇌ CO 2 + NH+
4+ N 5 , N 10 -tetrahidrofolato de metileno + NADH + H +
En la segunda vía, la glicina se degrada en dos pasos. El primer paso es el reverso de la biosíntesis de glicina a partir de serina con serina hidroximetiltransferasa. Entonces serina se convierte en piruvato por deshidratasa serina . [26]
En la tercera vía de su degradación, glicina se convierte a glioxilato por D-aminoácido oxidasa . Luego, el glioxilato es oxidado por la lactato deshidrogenasa hepática a oxalato en una reacción dependiente de NAD + . [26]
La vida media de la glicina y su eliminación del cuerpo varía significativamente según la dosis. [28] En un estudio, la vida media varió entre 0,5 y 4,0 horas. [28]
La glicina es extremadamente sensible a los antibióticos que se dirigen al folato, y los niveles de glicina en sangre bajan drásticamente al cabo de un minuto de las inyecciones de antibióticos. Algunos antibióticos pueden agotar más del 90% de la glicina a los pocos minutos de su administración. [29]
Función fisiológica [ editar ]
La función principal de la glicina es la de precursora de las proteínas . La mayoría de las proteínas incorporan solo pequeñas cantidades de glicina, una notable excepción es el colágeno , que contiene aproximadamente un 35% de glicina debido a su papel que se repite periódicamente en la formación de la estructura helicoidal del colágeno junto con la hidroxiprolina . [26] [30] En el código genético , la glicina está codificada por todos los codones que comienzan con GG, a saber, GGU, GGC, GGA y GGG.
Como intermedio biosintético [ editar ]
En eucariotas superiores , el ácido δ-aminolevulínico , el precursor clave de las porfirinas , es biosintetizado a partir de glicina y succinil-CoA por la enzima ALA sintasa . La glicina proporciona la subunidad central C 2 N de todas las purinas . [26]
Como neurotransmisor [ editar ]
La glicina es un neurotransmisor inhibidor en el sistema nervioso central , especialmente en la médula espinal , el tronco encefálico y la retina . Cuando se activan los receptores de glicina , el cloruro ingresa a la neurona a través de los receptores ionotrópicos, lo que provoca un potencial postsináptico inhibidor (IPSP). La estricnina es un antagonista fuerte de los receptores ionotrópicos de glicina, mientras que la bicuculina es débil. La glicina es un necesario co-agonista junto con el glutamato para receptores NMDA. En contraste con el papel inhibidor de la glicina en la médula espinal, este comportamiento se facilita en los receptores glutamatérgicos ( NMDA ) que son excitadores. [31] La LD 50 de la glicina es de 7930 mg / kg en ratas (oral), [32] y generalmente causa la muerte por hiperexcitabilidad.
Usos [ editar ]
En los Estados Unidos, la glicina se vende típicamente en dos grados: Farmacopea de los Estados Unidos ("USP") y grado técnico. Las ventas de grado USP representan aproximadamente del 80 al 85 por ciento del mercado estadounidense de glicina. Si se necesita una pureza mayor que el estándar de la USP, por ejemplo para inyecciones intravenosas , se puede usar una glicina de calidad farmacéutica más cara. La glicina de grado técnico, que puede o no cumplir con los estándares de grado de la USP, se vende a un precio más bajo para su uso en aplicaciones industriales, por ejemplo, como agente en la complejación y acabado de metales. [33]
Alimentos para animales y humanos [ editar ]
La glicina no se usa mucho en alimentos por su valor nutricional, excepto en infusiones. En cambio, el papel de la glicina en la química de los alimentos es como aromatizante. Es ligeramente dulce y contrarresta el regusto a sacarina. También tiene propiedades conservantes, quizás debido a su formación de complejos con iones metálicos. Los complejos de glicinato metálico, por ejemplo, glicinato de cobre (II), se utilizan como complementos para piensos. [21]
Materia prima química [ editar ]
La glicina es un intermediario en la síntesis de una variedad de productos químicos. Se utiliza en la fabricación de herbicidas glifosato , [35] iprodiona , glifosina, imiprotrina y eglinazina. [21] Se utiliza como intermedio de un medicamento como el tiamfenicol . [ cita requerida ]
Investigación de laboratorio [ editar ]
La glicina es un componente importante de algunas soluciones utilizadas en el método SDS-PAGE de análisis de proteínas. Sirve como agente tampón, manteniendo el pH y previniendo el daño de la muestra durante la electroforesis. La glicina también se usa para eliminar los anticuerpos que marcan las proteínas de las membranas de transferencia Western para permitir el sondeo de numerosas proteínas de interés del gel SDS-PAGE. Esto permite extraer más datos de la misma muestra, aumentando la confiabilidad de los datos, reduciendo la cantidad de procesamiento de muestras y la cantidad de muestras requeridas. Este proceso se conoce como stripping.
Presencia en el espacio [ editar ]
La presencia de glicina fuera de la tierra se confirmó en 2009, basándose en el análisis de muestras que habían sido tomadas en 2004 por la nave espacial Stardust de la NASA del cometa Wild 2 y posteriormente devueltas a la Tierra. La glicina se había identificado previamente en el meteorito de Murchison en 1970. [36] El descubrimiento de la glicina cometaria reforzó la teoría de la panspermia , que afirma que los "bloques de construcción" de la vida están muy extendidos por todo el Universo. [37] En 2016, se anunció la detección de glicina dentro del cometa 67P / Churyumov-Gerasimenko por la nave espacial Rosetta . [38]
Se ha debatido la detección de glicina fuera del sistema solar en el medio interestelar . [39] En 2008, el Instituto Max Planck de Radioastronomía descubrió las líneas espectrales de una molécula similar a la glicina aminoacetonitrilo en la Gran Molécula Heimat , una nube de gas gigante cerca del centro galáctico en la constelación de Sagitario . [40]
Evolución [ editar ]
Varios estudios evolutivos independientes que utilizan diferentes tipos de datos han sugerido que la glicina pertenece a un grupo de aminoácidos que constituía el código genético temprano. [41] [42] [43] [44] Por ejemplo, las regiones de baja complejidad (en proteínas), que pueden parecerse a los protopéptidos del código genético temprano , están altamente enriquecidas en glicina. [44]
Presencia en alimentos [ editar ]
| Comida | g / 100g |
|---|---|
| Aperitivos, pieles de cerdo | 11.04 |
| Harina de semillas de sésamo (baja en grasas) | 3,43 |
| Bebidas, proteína en polvo (a base de soja ) | 2,37 |
| Semillas, harina de semillas de cártamo, parcialmente desgrasadas | 2.22 |
| Carne, bisonte, vacuno y otros (varias partes) | 1,5-2,0 |
| Postres de gelatina | 1,96 |
| Semillas, calabaza y calabaza granos de semillas | 1,82 |
| Pavo, todas las clases, lomo, carne y piel | 1,79 |
| Pollo, parrillas o freidoras, carne y piel | 1,74 |
| Carne de cerdo, molida, 96% magra / 4% de grasa, cocida, desmenuzada | 1,71 |
| Palitos de tocino y ternera | 1,64 |
| Miseria | 1,63 |
| Crustáceos , langosta espinosa | 1,59 |
| Especias, semillas de mostaza , molidas | 1,59 |
| Salami | 1,55 |
| Nueces, Butternuts , se secaron | 1,51 |
| Pescado, salmón, rosado, enlatado, sólidos escurridos | 1,42 |
| Almendras | 1,42 |
| Pescado, caballa | 0,93 |
| Cereales listos para comer, granola, caseros | 0,81 |
| Puerros (bulbo y parte inferior de la hoja), liofilizados | 0,7 |
| Queso, parmesano (y otros), rallado | 0,56 |
| Soja , verde, cocida, hervida, escurrida, sin sal | 0,51 |
| Pan, proteína (incluye gluten) | 0,47 |
| Huevo, entero, cocido, frito | 0,47 |
| Frijoles blancos, semillas maduras, cocidos, hervidos, con sal | 0,38 |
| Lentejas, semillas maduras, cocidas, hervidas, con sal | 0,37 |
Ver también [ editar ]
- Trimetilglicina
- Neurotransmisor de aminoácidos
Referencias [ editar ]
- ^ El índice Merck: una enciclopedia de productos químicos, fármacos y productos biológicos (11ª ed.), Merck, 1989, ISBN 091191028X, 4386.
- ^ Manual de química y física , CRC Press, 59a edición, 1978
- ^ "Solubilidades y densidades" . Prowl.rockefeller.edu . Consultado el 13 de noviembre de 2013 .
- ^ Dawson, RMC, et al., Datos para la investigación bioquímica , Oxford, Clarendon Press, 1959.
- ^ "Nomenclatura y simbolismo de aminoácidos y péptidos" . Comisión Conjunta IUPAC-IUB sobre Nomenclatura Bioquímica. 1983. Archivado desde el original el 9 de octubre de 2008 . Consultado el 5 de marzo de 2018 .
- ^ "Glicina | Definición de glicina en inglés por los diccionarios de Oxford" .
- ^ Plimmer, RHA (1912) [1908]. Plimmer, RHA; Hopkins, FG (eds.). La composición química de las proteínas . Monografías de bioquímica. Parte I. Análisis (2ª ed.). Londres: Longmans, Green and Co. p. 82 . Consultado el 18 de enero de 2010 .
- ↑ Braconnot, Henri (1820). "Sur la conversion des matières animales en nouvelles substancias par le moyen de l'acide sulfurique" [Sobre la conversión de materias animales en nuevas sustancias mediante ácido sulfúrico]. Annales de Chimie et de Physique . 2ª serie (en francés). 13 : 113-125. ; ver p. 114.
- ^ MacKenzie, Colin (1822). Mil experimentos en química: con ilustraciones de fenómenos naturales; y observaciones prácticas sobre los procesos de fabricación y químicos que se llevan a cabo en la actualidad en el cultivo exitoso de las artes útiles… . Sir R. Phillips y compañía. pag. 557 .
- ^ Boussingault (1838). "Sur la composicion du sucre de gelatina et de l'acide nitro-saccharique de Braconnot" [Sobre la composición del azúcar de la gelatina y del ácido nitro-glucárico de Braconnot]. Comptes Rendus (en francés). 7 : 493–495.
- ^ Horsford, EN (1847). "Glycocoll (azúcar de gelatina) y algunos de sus productos de descomposición" . La Revista Estadounidense de Ciencias y Artes . 2da serie. 3 : 369–381.
- ^ Ihde, Aaron J. (1970). El desarrollo de la química moderna . Corporación de mensajería. ISBN 9780486642352.
- ↑ Berzelius, Jacob (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Informe anual sobre el progreso de la química y la mineralogía) . vol. 47. Tübigen, (Alemania): Laupp. pag. 654. Desde p. 654: "Er hat dem Leimzucker als Basis den Namen Glycocoll gegeben.… Glycin genannt werden, und diesen Namen werde ich anwenden". (Él [es decir, el científico estadounidense Eben Norton Horsford , entonces estudiante del químico alemán Justus von Liebig ] le dio el nombre "glycocoll" a Leimzucker [azúcar de gelatina], una base. Este nombre no es eufónico y tiene además del defecto que choca con los nombres del resto de las bases. Se compone de γλυχυς (dulce) y χολλα (pegamento animal). Dado que esta base orgánica es la única [una] que tiene un sabor dulce, entonces se puede llamar mucho más brevemente "glicina", y usaré este nombre).
- ^ Nye, Mary Jo (1999). Before Big Science: The Pursuit of Modern Chemistry and Physics, 1800-1940 . Prensa de la Universidad de Harvard. ISBN 9780674063822.
- ^ "glicina" . Diccionarios de Oxford . Consultado el 6 de diciembre de 2015 .
- ↑ Cahours, A. (1858). "Recherches sur les acides amidés" [Investigaciones sobre ácidos aminados]. Comptes Rendus (en francés). 46 : 1044–1047.
- ↑ Okafor, Nduka (9 de marzo de 2016). Microbiología y Biotecnología Industrial Moderna . Prensa CRC. ISBN 9781439843239.
- ^ Ingersoll, AW; Babcock, SH (1932). "Ácido hipúrico" . Síntesis orgánicas . 12 : 40.; Volumen colectivo , 2 , p. 328
- ↑ Wiley (14 de diciembre de 2007). Tecnología de alimentos y piensos de Kirk-Othmer, juego de 2 volúmenes . John Wiley e hijos. ISBN 9780470174487.
- ^ "Conferencia de glicina (preliminar)" . USITC. Archivado desde el original el 22 de febrero de 2012 . Consultado el 13 de junio de 2014 .CS1 maint: bot: estado de URL original desconocido ( enlace )
- ^ a b c Drauz, Karlheinz; Grayson, Ian; Kleemann, Axel; Krimmer, Hans-Peter; Leuchtenberger, Wolfgang y Weckbecker, Christoph (2007). "Aminoácidos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH.
- ^ Hart, J. Roger (2005). "Ácido etilendiaminotetraacético y agentes quelantes relacionados". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a10_095 .
- ^ Ingersoll, AW; Babcock, SH (1932). "Ácido hipúrico". Org. Synth . 12 : 40. doi : 10.15227 / orgsyn.012.0040 .
- ^ Herbst, RM; Shemin, D. (1939). "Acetilglicina". Org. Synth . 19 : 4. doi : 10.15227 / orgsyn.019.0004 .
- ↑ Meléndez-Hevia, E; De Paz-Lugo, P; Cornish-Bowden, A ; Cárdenas, ML (diciembre de 2009). "Un eslabón débil en el metabolismo: la capacidad metabólica para la biosíntesis de glicina no satisface la necesidad de síntesis de colágeno". Revista de Biociencias . 34 (6): 853–72. doi : 10.1007 / s12038-009-0100-9 . PMID 20093739 . S2CID 2786988 .
- ↑ a b c d e f g Nelson, David L .; Cox, Michael M. (2005). Principios de bioquímica (4ª ed.). Nueva York: W. H. Freeman. págs. 127, 675–77, 844, 854. ISBN 0-7167-4339-6.
- ^ . PMID 23615880 . Cite journal requiere
|journal=( ayuda );Falta o vacío|title=( ayuda ) - ↑ a b Hahn RG (1993). "Vida media dependiente de la dosis de la glicina". Investigación Urológica . 21 (4): 289-291. doi : 10.1007 / BF00307714 . PMID 8212419 . S2CID 25138444 .
- ^ ACS Chem Biol. 20 de agosto de 2010; 5 (8): 787–795. doi: 10.1021 / cb100096f
- ^ Szpak, Paul (2011). "Ultraestructura y química de la espina de pescado: implicaciones para la tafonomía y el análisis de isótopos estables" . Revista de Ciencias Arqueológicas . 38 (12): 3358–3372. doi : 10.1016 / j.jas.2011.07.022 .
- ^ "Desarrollo reciente en receptores NMDA" . Revista médica china. 2000.
- ^ "Datos de seguridad (MSDS) para glicina" . El Laboratorio de Química Física y Teórica de la Universidad de Oxford. 2005. Archivado desde el original el 20 de octubre de 2007 . Consultado el 1 de noviembre de 2006 .
- ^ "Glicina de Japón y Corea" (PDF) . Comisión de Comercio Internacional de EE. UU. Enero de 2008 . Consultado el 13 de junio de 2014 .
- ^ Casari, BM; Mahmoudkhani, AH; Langer, V. (2004). "Una redeterminación de cis -Aquabis (glycinato-κ 2 N, O ) cobre (II)". Acta Crystallogr. E . 60 (12): m1949 – m1951. doi : 10.1107 / S1600536804030041 .
- ^ Stahl, Shannon S .; Alsters, Paul L. (13 de julio de 2016). Catálisis de oxidación aeróbica en fase líquida: aplicaciones industriales y perspectivas académicas . John Wiley e hijos. ISBN 9783527690152.
- ^ Kvenvolden, Keith A .; Lawless, James; Pering, Katherine; Peterson, Etta; Flores, José; Ponnamperuma, Cyril; Kaplan, Isaac R .; Moore, Carleton (1970). "Evidencia de hidrocarburos y aminoácidos extraterrestres en el meteorito Murchison". Naturaleza . 228 (5275): 923–926. Código Bibliográfico : 1970Natur.228..923K . doi : 10.1038 / 228923a0 . PMID 5482102 . S2CID 4147981 .
- ^ "Bloque de construcción de la vida en cometa - Thomson Reuters 2009" . Reuters . 18 de agosto de 2009 . Consultado el 18 de agosto de 2009 .
- ^ Agencia Espacial Europea (27 de mayo de 2016). "El cometa de Rosetta contiene ingredientes para la vida" . Consultado el 5 de junio de 2016 .
- ^ Snyder LE, Lovas FJ, Hollis JM, et al. (2005). "Un intento riguroso de verificar la glicina interestelar". Astrophys J . 619 (2): 914–930. arXiv : astro-ph / 0410335 . Código bibliográfico : 2005ApJ ... 619..914S . doi : 10.1086 / 426677 . S2CID 16286204 .
- ^ Personal. "Molécula orgánica, similar a un aminoácido, que se encuentra en la constelación de Sagitario el 27 de marzo de 2008 - Science Daily" . Consultado el 16 de septiembre de 2008 .
- ^ Trifonov, EN (diciembre de 2000). "Consenso de orden temporal de aminoácidos y evolución del código triplete" . Gene . 261 (1): 139-151. doi : 10.1016 / S0378-1119 (00) 00476-5 . PMID 11164045 .
- ^ Higgs, Paul G .; Pudritz, Ralph E. (junio de 2009). "Una base termodinámica para la síntesis de aminoácidos prebióticos y la naturaleza del primer código genético" . Astrobiología . 9 (5): 483–490. arXiv : 0904.0402 . Código bibliográfico : 2009AsBio ... 9..483H . doi : 10.1089 / ast.2008.0280 . ISSN 1531-1074 . PMID 19566427 . S2CID 9039622 .
- ^ Chaliotis, Anargyros; Vlastaridis, Panayotis; Mossialos, Dimitris; Ibba, Michael; Becker, Hubert D .; Stathopoulos, Constantinos; Amoutzias, Grigorios D. (17 de febrero de 2017). "La compleja historia evolutiva de las aminoacil-tRNA sintetasas" . Investigación de ácidos nucleicos . 45 (3): 1059–1068. doi : 10.1093 / nar / gkw1182 . ISSN 0305-1048 . PMC 5388404 . PMID 28180287 .
- ^ a b Ntountoumi, Chrysa; Vlastaridis, Panayotis; Mossialos, Dimitris; Stathopoulos, Constantinos; Iliopoulos, Ioannis; Promponas, Vasilios; Oliver, Stephen G; Amoutzias, Grigoris D (4 de noviembre de 2019). "Las regiones de baja complejidad en las proteínas de los procariotas desempeñan importantes funciones funcionales y están muy conservadas" . Investigación de ácidos nucleicos . 47 (19): 9998–10009. doi : 10.1093 / nar / gkz730 . ISSN 0305-1048 . PMC 6821194 . PMID 31504783 .
- ^ "Base de datos nacional de nutrientes para referencia estándar" . Departamento de Agricultura de Estados Unidos. Archivado desde el original el 3 de marzo de 2015 . Consultado el 7 de septiembre de 2009 . Cite journal requiere
|journal=( ayuda )
Lectura adicional [ editar ]
- Kuan YJ, Charnley SB, Huang HC y col. (2003). "Glicina interestelar" . Astrophys J . 593 (2): 848–867. Código bibliográfico : 2003ApJ ... 593..848K . doi : 10.1086 / 375637 .
- Nowak, Rachel. "Aminoácido encontrado en el espacio profundo - 18 de julio de 2002 - New Scientist " . Consultado el 1 de julio de 2007 .
Enlaces externos [ editar ]
| Wikimedia Commons tiene medios relacionados con la glicina . |
- Espectro de glicina MS
- Glicina en PDRHealth.com
- Sistema de escisión de glicina
- Terapia con glicina: ¿una nueva dirección para el tratamiento de la esquizofrenia?
- "Molécula orgánica, similar a un aminoácido, que se encuentra en la constelación de Sagitario" . ScienceDaily . 27 de marzo de 2008.
- Tsai, Guochuan E. (1 de diciembre de 2008). "Una nueva clase de fármacos antipsicóticos: mejora de la neurotransmisión mediada por receptores NMDA" . Tiempos psiquiátricos . 25 (14).
- ChemSub Online (glicina) .
- Los científicos de la NASA han descubierto la glicina, un componente fundamental de la vida, en muestras del cometa Wild 2 devueltas por la nave espacial Stardust de la NASA.