 | |
| Nombres | |
|---|---|
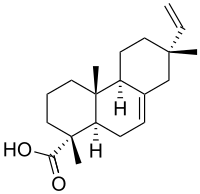
| Nombre IUPAC (1 R , 4a R , 4b S , 7 R , 10a R ) -7-Etenil-1,4a, 7-trimetil-3,4,4b, 5,6,8,10,10a-octahidro-2 H - ácido fenantreno-1-carboxílico | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.163.144 |
| KEGG | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 20 H 30 O 2 | |
| Masa molar | 302,458 g · mol −1 |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El ácido isopimárico (IPA) es una toxina que actúa como un abridor del canal de K + ( canal BK ) activado por Ca 2+ de gran conductancia .
Fuentes [ editar ]
La IPA se origina en muchos tipos de árboles, especialmente las coníferas. [1]
Química [ editar ]
El IPA es uno de los miembros del grupo de los ácidos resinosos y es un diterpeno tricíclico. [1]
Objetivo [ editar ]
El IPA actúa sobre los canales de K + activados por calcio de gran conductancia ( canales BK ). [2] [3]
Modo de acción [ editar ]
Los canales BK están formados por subunidades α y subunidades β accesorias dispuestas en tetrámeros. La subunidad α forma el poro de conducción de iones y la subunidad β contribuye a la activación del canal. La interacción del IPA con el canal BK mejora la sensibilidad al Ca 2+ y / o al voltaje de la subunidad α de los canales BK sin afectar la conductancia del canal. En este estado, los canales de BK todavía pueden ser inhibidos por uno de sus inhibidores, como la caribdotoxina (CTX). [2] [3] La apertura del canal BK conduce a un aumento del flujo de K + que hiperpolariza el potencial de membrana en reposo , reduciendo la excitabilidad de la célula en la que se expresa el canal BK.
Toxicidad [ editar ]
Los estudios sobre los hepatocitos de la trucha arco iris han demostrado que el IPA aumenta la liberación de calcio intracelular , lo que provoca una alteración de la homeostasis del calcio. Esto podría ser importante por la posible toxicidad de la toxina.
Ver también [ editar ]
- Ácido pimarico
Notas [ editar ]
- ^ a b Wilson, AE; Moore, ER; Mohn, WW (1996). "Aislamiento y caracterización de bacterias degradantes del ácido isopimárico de un reactor discontinuo de secuenciación" . Microbiología aplicada y ambiental . 62 (9): 3146–51. PMC 168108 . PMID 8795202 .
- ↑ a b Kaczorowski, GJ; Knaus, HG; Leonard, RJ; McManus, OB; García, ML (1996). "Canales de potasio activados por calcio de alta conductancia; estructura, farmacología y función". Revista de Bioenergética y Biomembranas . 28 (3): 255–67. doi : 10.1007 / bf02110699 . PMID 8807400 .
- ^ a b Imaizumi, Y; Sakamoto, K; Yamada, A; Hotta, A; Ohya, S; Muraki, K; Uchiyama, M; Ohwada, T (2002). "Base molecular de los compuestos de pimarano como nuevos activadores de la subunidad alfa del canal de K (+) activado por Ca (2 +) de gran conductancia". Farmacología molecular . 62 (4): 836–46. doi : 10.1124 / mol.62.4.836 . PMID 12237330 .
Referencias [ editar ]
- Råbergh, Christina MI; Lilius, Henrik; Eriksson, John E .; Isomaa, Boris (1999). "Los ácidos resínicos ácido deshidroabiético y ácido isopimárico liberan calcio de los depósitos intracelulares en los hepatocitos de la trucha arco iris". Toxicología acuática . 46 : 55–65. doi : 10.1016 / S0166-445X (98) 00115-5 .
- Råbergh, CMI; Isomaa, B .; Eriksson, JE (1992). "Los ácidos resínicos ácido deshidroabiético y ácido isopimárico inhiben la captación de ácidos biliares y perturban el transporte de potasio en hepatocitos aislados de trucha arco iris (Oncorhynchus mykiss)". Toxicología acuática . 23 (3-4): 169-179. doi : 10.1016 / 0166-445X (92) 90050-W .