| Cancer de prostata | |
|---|---|
| Otros nombres | Carcinoma de próstata |
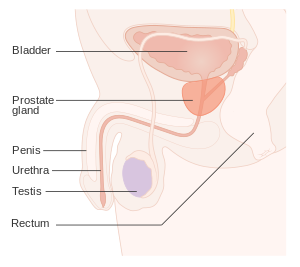 | |
| Posición de la próstata | |
| Especialidad | Oncología , urología |
| Síntomas | Ninguno, dificultad para orinar , sangre en la orina, dolor en la pelvis , la espalda o al orinar [1] [2] |
| Inicio habitual | Edad> 50 [3] |
| Factores de riesgo | Edad avanzada, antecedentes familiares, raza [3] |
| Método de diagnóstico | Biopsia de tejido , imágenes médicas [2] |
| Diagnóstico diferencial | Hiperplasia prostática benigna [1] |
| Tratamiento | Vigilancia activa , cirugía, radioterapia , hormonoterapia , quimioterapia [2] |
| Pronóstico | Tasa de supervivencia a 5 años 99% (EE. UU.) [4] |
| Frecuencia | 1,2 millones de casos nuevos (2018) [5] |
| Fallecidos | 359.000 (2018) [5] |
El cáncer de próstata es un cáncer de próstata . La próstata es una glándula del sistema reproductor masculino que rodea la uretra justo debajo de la vejiga . [6] La mayoría de los cánceres de próstata son de crecimiento lento. [1] [3] Las células cancerosas se pueden diseminar a otras áreas del cuerpo, particularmente a los huesos y los ganglios linfáticos . [7] Es posible que inicialmente no cause síntomas. [1] En etapas posteriores, los síntomas incluyen dolor o dificultad para orinar , sangre en la orina odolor en la pelvis o la espalda. [2] La hiperplasia prostática benigna puede producir síntomas similares. [1] Otros síntomas tardíos incluyen fatiga, debido a niveles bajos de glóbulos rojos . [1]
Los factores que aumentan el riesgo de cáncer de próstata incluyen la edad avanzada, los antecedentes familiares y la raza . [3] Aproximadamente el 99% de los casos ocurren después de los 50 años. [3] Un familiar de primer grado con la enfermedad aumenta el riesgo de dos a tres veces. [3] Otros factores incluyen una dieta rica en carnes procesadas y carnes rojas , [3] mientras que el riesgo de una alta ingesta de productos lácteos no es concluyente. [8] Se ha encontrado una asociación con la gonorrea , aunque no se ha identificado ninguna razón para esta relación. [9]Un mayor riesgo está asociado con las mutaciones BRCA . [10] El diagnóstico se realiza mediante biopsia . [2] Se pueden tomar imágenes médicas para evaluar si hay metástasis . [2]
La detección del cáncer de próstata , incluida la prueba del antígeno prostático específico (PSA), aumenta la detección del cáncer, pero si mejora los resultados es controvertido. [3] [11] [12] [13] Se recomienda la toma de decisiones informada para las personas de 55 a 69 años. [14] [15] Las pruebas, si se llevan a cabo, son más apropiadas para aquellos con una esperanza de vida más larga. [16] Aunque los inhibidores de la 5α-reductasa parecen disminuir el riesgo de cáncer de grado bajo, no afectan el riesgo de cáncer de grado alto y no se recomiendan para la prevención. [3] La suplementación con vitaminas o minerales no parece afectar el riesgo. [3][17]
Muchos casos se tratan con vigilancia activa o espera vigilante . [2] Otros tratamientos pueden incluir una combinación de cirugía , radioterapia , terapia hormonal o quimioterapia . [2] Los tumores limitados a la próstata pueden ser curables. [1] Los analgésicos , los bisfosfonatos y la terapia dirigida , [18] entre otros, pueden ser útiles. [2] Los resultados dependen de la edad, el estado de salud y la agresividad y extensión del cáncer. [2] La mayoría de los hombres con cáncer de próstata no mueren a causa de él.[2] La tasa de supervivencia a cinco años de Estados Unidos es del 98%. [4]
A nivel mundial, es el segundo cáncer más común. Es la quinta causa principal de muerte relacionada con el cáncer en los hombres. [19] En 2018, se diagnosticó en 1,2 millones y causó 359.000 muertes. [5] Fue el cáncer más común en hombres en 84 países, [3] ocurriendo con mayor frecuencia en el mundo desarrollado . [20] Las tasas han ido aumentando en el mundo en desarrollo . [20] La detección aumentó significativamente en las décadas de 1980 y 1990 en muchas áreas debido al aumento de las pruebas de PSA. [3] Un estudio informó cáncer de próstata en 30% a 70% de los hombres rusos y japoneses mayores de 60 años que habían muerto por causas no relacionadas. [1]
Signos y síntomas [ editar ]
El cáncer de próstata temprano generalmente no presenta síntomas claros. Cuando aparecen, suelen ser similares a los de la hiperplasia prostática benigna . Estos incluyen micción frecuente, nicturia (aumento de la micción por la noche), dificultad para iniciar y mantener un flujo constante de orina, hematuria (sangre en la orina), disuria (dolor al orinar), así como fatiga debido a la anemia y dolor de huesos. [21] Un estudio encontró que alrededor de un tercio de los pacientes diagnosticados tenían uno o más de estos síntomas. [22]
El cáncer de próstata se asocia con disfunción urinaria ya que la glándula prostática rodea la uretra prostática . Los cambios dentro de la glándula afectan directamente la función urinaria. Debido a que los conductos deferentes depositan líquido seminal en la uretra prostática y las secreciones de la próstata están incluidas en el contenido del semen, el cáncer de próstata también puede causar problemas con la función y el desempeño sexual, como dificultad para lograr la erección o eyaculación dolorosa . [22]
El cáncer de próstata metastásico puede causar síntomas adicionales. El síntoma más común es el dolor de huesos , a menudo en las vértebras (huesos de la columna vertebral), la pelvis o las costillas . La diseminación del cáncer a otros huesos, como el fémur, suele ocurrir en la parte del hueso más cercana a la próstata . El cáncer de próstata en la columna puede comprimir la médula espinal , causando hormigueo, debilidad en las piernas e incontinencia urinaria y fecal . [23]
Factores de riesgo [ editar ]
Los principales factores de riesgo son la obesidad , [24] la edad y los antecedentes familiares. Se ha descubierto que los hombres obesos tienen un 34% más de mortalidad por cáncer de próstata que los que tienen un peso normal. [24] El cáncer de próstata es poco común en hombres menores de 45 años, pero se vuelve más común a medida que avanza la edad. La edad promedio en el momento del diagnóstico es de 70 años. [25] Los estudios de autopsia de hombres chinos, alemanes, israelíes, jamaicanos, suecos y ugandeses que murieron por otras causas encontraron cáncer de próstata en el 30% de los hombres de 50 años y en 80 % de hombres de 70 años. [26] [27] [28]
Los hombres con presión arterial alta tienen más probabilidades de desarrollar cáncer de próstata. [29] Un pequeño aumento en el riesgo se asocia con la falta de ejercicio. [30] Los niveles elevados de testosterona en sangre [31] pueden aumentar el riesgo.
Genética [ editar ]
La genética puede afectar el riesgo, como lo sugieren las asociaciones con la raza, la familia y variantes genéticas específicas . [32] Los hombres que tienen un pariente de primer grado (padre o hermano) con cáncer de próstata tienen el doble de riesgo de desarrollar cáncer de próstata, y aquellos con dos parientes de primer grado afectados tienen un riesgo cinco veces mayor en comparación con los hombres sin familia historia. [33] [34] Este riesgo parece ser mayor para los hombres con un hermano afectado que para aquellos con un padre afectado. En los Estados Unidos, el cáncer de próstata afecta con más frecuencia a los hombres negros que a los blancos o hispanos, y también es más mortal en los hombres negros. [35] [36]En contraste, las tasas de incidencia y mortalidad de los hombres hispanos son un tercio más bajas que las de los blancos no hispanos. Los estudios de gemelos en Escandinavia sugieren que el 40% del riesgo de cáncer de próstata puede explicarse por factores hereditarios . [37]
Muchos genes están involucrados en el cáncer de próstata. Se han implicado mutaciones en BRCA1 y BRCA2 (importantes factores de riesgo de cáncer de ovario y cáncer de mama en mujeres). [38] Otros genes relacionados incluyen hereditaria gen del cáncer de próstata 1 ( HPC1 ), el receptor de andrógenos , y el receptor de la vitamina D . [35] La fusión de la familia de genes TMPRSS2 - ETS , específicamente TMPRSS2- ERG o TMPRSS2- ETV1 / 4 promueve el crecimiento de células cancerosas. [39]Estas fusiones pueden surgir a través de complejas cadenas de reordenamiento llamadas cromoplexia . [40]
Dos grandes estudios de asociación de todo el genoma vincularon los polimorfismos de un solo nucleótido (SNP) con el cáncer de próstata en 2008. [41] [42] Estos estudios identificaron varios SNP relevantes. Por ejemplo, se informó que los individuos con el par de alelos TT en el SNP rs10993994 tenían un riesgo 1,6 veces mayor que aquellos con el par de alelos CC. Este SNP explica parte del mayor riesgo que enfrentan los afroamericanos. El alelo C es mucho más frecuente en este último; este SNP se encuentra en la región promotora del gen MSMB , por lo que afecta la cantidad de proteína MSMB sintetizada y secretada por las células epiteliales de la próstata. [43]
Si bien se han realizado menos estudios para evaluar el riesgo de ser diagnosticado con cáncer de próstata agresivo, un estudio de asociación de todo el genoma (GWAS) de 12,518 casos de cáncer de próstata identificó dos loci asociados con una puntuación de suma de Gleason alta , el SNP rs78943174 más cercano al gen NAALADL2 y SNP rs35148638 más cercano a RASA1 . [44]
Dietético [ editar ]
Se ha descubierto que el consumo de frutas y verduras tiene pocos beneficios preventivos. [45] Algunos estudios informan que un mayor consumo de carne se asoció con un mayor riesgo. [46]
El consumo de leche puede estar relacionado con el cáncer de próstata. [47] [48] Una revisión sistemática de 2020 encontró que los resultados sobre el consumo de leche y el cáncer de próstata no eran concluyentes, pero afirmó que las personas con mayor riesgo pueden reducir o eliminar la leche. [49] Un resumen de 2019 indicó que la evidencia que vinculaba la leche con tasas más altas de cáncer de próstata era inconsistente y no concluyente. [50]
Los niveles sanguíneos más bajos de vitamina D pueden aumentar los riesgos. [51] Un estudio no encontró efecto de ácido fólico suplementos en el riesgo. [52]
Exposición a medicamentos [ editar ]
Se han establecido algunos vínculos entre el cáncer de próstata y los medicamentos, los procedimientos médicos y las afecciones médicas. [53] Las estatinas también pueden reducir el riesgo. [54]
Infección [ editar ]
La prostatitis ( infección o inflamación ) puede aumentar el riesgo. En particular, la infección por las infecciones de transmisión sexual clamidia , gonorrea o sífilis parece aumentar el riesgo. [9] [55]
Se ha propuesto que el virus del papiloma tiene un papel potencial, pero a partir de 2015, la evidencia no era concluyente; [56] a partir de 2018, se debatió el aumento del riesgo. [57]
Medio ambiente [ editar ]
Los veteranos de guerra estadounidenses que habían estado expuestos al Agente Naranja tenían un 48% más de riesgo de recurrencia del cáncer de próstata después de la cirugía. [ cita médica necesaria ]
Sexo [ editar ]
Aunque algunas pruebas de estudios de cohortes prospectivos indican que la eyaculación frecuente puede reducir el riesgo de cáncer de próstata, [58] ningún ensayo controlado aleatorio informó este beneficio. [59] Se encontró una asociación entre la vasectomía y el cáncer de próstata, pero no se ha establecido la causalidad. [60]
Fisiopatología [ editar ]
La próstata es parte del sistema reproductor masculino que ayuda a producir y almacenar el líquido seminal . En los hombres adultos, una próstata típica mide unos 3 cm de largo y pesa unos 20 g. [61] Está ubicado en la pelvis , debajo de la vejiga urinaria y frente al recto . La próstata rodea parte de la uretra , el conducto que transporta la orina desde la vejiga durante la micción y el semen durante la eyaculación . [62] La próstata contiene muchas glándulas pequeñas , que producen aproximadamente el 20% del líquido que constituye el semen.. [63]
Superiormente, la base de la próstata está contigua a la salida de la vejiga. En la parte inferior, el vértice de la próstata se dirige en dirección al diafragma urogenital, que apunta hacia arriba y hacia abajo. La próstata se puede dividir en cuatro espacios anatómicos: estroma fibromuscular periférico, central, transicional y anterior . [64]El espacio periférico contiene las porciones posterior y lateral de la próstata, así como las porciones inferiores de la próstata. El espacio central contiene la porción superior de la próstata, incluidos los aspectos más proximales de la uretra y el cuello de la vejiga. El espacio de transición está ubicado justo anterior al espacio central e incluye la uretra distal a la uretra de la glándula central. Los haces neurovasculares recorren la superficie posterolateral de la próstata y penetran allí también en la cápsula prostática.
La mayor parte del tejido glandular se encuentra en las zonas periférica y central (zona periférica: 70-80% del tejido glandular; zona central: 20% del tejido glandular). [65] Algunos se encuentran en el espacio de transición (5% del tejido glandular). Por tanto, la mayoría de los cánceres que se desarrollan a partir del tejido glandular se encuentran en los espacios periférico y central, [66] mientras que alrededor del 5% se encuentra en el espacio de transición. No se encuentra ninguno en el estroma fibromuscular anterior ya que no hay glándulas en ese espacio anatómico.
Las glándulas prostáticas requieren hormonas masculinas , conocidas como andrógenos , para funcionar correctamente. Los andrógenos incluyen la testosterona , que se produce en los testículos ; dehidroepiandrosterona , producida en las glándulas suprarrenales ; y dihidrotestosterona , que se convierte a partir de testosterona dentro de la propia próstata. Los andrógenos también son responsables de las características sexuales secundarias , como el vello facial y el aumento de la masa muscular.
Debido a la ubicación de la próstata, las enfermedades de la próstata a menudo afectan la micción, la eyaculación y rara vez la defecación . En el cáncer de próstata, las células de estas glándulas se transforman en células cancerosas.
La mayoría de los cánceres de próstata se clasifican como adenocarcinomas o cánceres glandulares, que comienzan cuando las células de las glándulas secretoras de semen mutan en células cancerosas. La región de la glándula prostática donde el adenocarcinoma es más común es la zona periférica. Inicialmente, pequeños grupos de células cancerosas permanecen dentro de las glándulas prostáticas normales, una condición conocida como carcinoma in situ o neoplasia intraepitelial prostática (PIN). Aunque no hay pruebas que establezcan que el PIN sea un precursor del cáncer, está estrechamente asociado con el cáncer. Con el tiempo, estas células se multiplican y se diseminan al tejido prostático circundante (el estroma ) formando un tumor .
Con el tiempo, el tumor puede crecer lo suficiente como para invadir órganos cercanos, como las vesículas seminales o el recto, o las células tumorales pueden desarrollar la capacidad de viajar por el torrente sanguíneo y el sistema linfático .
El cáncer de próstata se considera un tumor maligno porque puede invadir otras áreas del cuerpo. Esta invasión se llama metástasis . El cáncer de próstata suele hacer metástasis en los huesos y los ganglios linfáticos y puede invadir el recto, la vejiga y los uréteres inferiores después de la progresión local. Se cree que la vía de metástasis al hueso es venosa , ya que el plexo venoso prostático que drena la próstata se conecta con las venas vertebrales. [67]
La próstata es un órgano productor de citrato que acumula zinc . La proteína de transporte ZIP1 es responsable del transporte de zinc a las células de la próstata. Una de las funciones importantes del zinc es cambiar el metabolismo de las células para producir citrato, un componente importante del semen. El proceso de acumulación de zinc, alteración del metabolismo y producción de citrato es energéticamente ineficiente, y las células de la próstata requieren enormes cantidades de energía ( ATP ) para realizar esta tarea. Las células de cáncer de próstata generalmente carecen de zinc. Las células del cáncer de próstata ahorran energía al no producir citrato y utilizan la energía conservada para crecer, reproducirse y diseminarse.
Se cree que la ausencia de zinc ocurre mediante el silenciamiento del gen que produce ZIP1. Se llama producto del gen supresor de tumores para el gen SLC39A1 . Se desconoce la causa del silenciamiento epigenético . Las estrategias que transportan zinc a las células prostáticas transformadas eliminan eficazmente estas células en los animales. El zinc inhibe las vías de NF-κB , es antiproliferativo e induce la apoptosis en células anormales. Desafortunadamente, la ingestión oral de zinc es ineficaz ya que no es posible obtener altas concentraciones de zinc en las células de la próstata sin ZIP1. [68]
La pérdida de genes supresores de cáncer, al inicio de la carcinogénesis prostática, se ha localizado en los cromosomas 8p , 10q , 13q y 16q . Las mutaciones de P53 en el cáncer de próstata primario son relativamente bajas y se observan con mayor frecuencia en entornos metastásicos, por lo que las mutaciones de p53 son un evento tardío en la patología. Otros genes supresores de tumores que se cree que juegan un papel incluyen PTEN y KAI1 . "Hasta el 70 por ciento de los hombres con cáncer de próstata han perdido una copia del gen PTEN en el momento del diagnóstico". [69] Frecuencia relativa de pérdida de E-cadherina y CD44también se ha observado. La pérdida de la proteína del retinoblastoma (RB) induce la desregulación del receptor de andrógenos en el cáncer de próstata resistente a la castración al desregular la expresión de ' E2F1 . [70]
RUNX2 es un factor de transcripción que evita que las células cancerosas sufran apoptosis, contribuyendo así al desarrollo del cáncer. [71]
La cascada de señalización PI3k / Akt trabaja con la cascada de señalización del factor de crecimiento transformante beta / SMAD para asegurar la supervivencia de las células cancerosas y proteger contra la apoptosis. [72] Pim-1 se regula al alza en el cáncer de próstata. [18] Se plantea la hipótesis de que el inhibidor de la apoptosis ligado al cromosoma X ( XIAP ) promueve la supervivencia y el crecimiento de las células cancerosas. [73] La citocina 1 inhibidora de macrófagos (MIC-1) estimula la vía de señalización de la quinasa de adhesión focal (FAK) que conduce al crecimiento y supervivencia de las células cancerosas. [74]
El receptor de andrógenos ayuda a las células cancerosas a sobrevivir. [75] El antígeno de membrana específico de la próstata (PSMA) estimula el desarrollo del cáncer al aumentar los niveles de folato, lo que ayuda a las células cancerosas a sobrevivir y crecer; aumenta los folatos disponibles para su uso hidrolizando folatos glutamados. [76]
Diagnóstico [ editar ]
La posición de la Sociedad Estadounidense del Cáncer con respecto a la detección temprana mediante pruebas de PSA es:
La investigación aún no ha demostrado que los beneficios potenciales de las pruebas superen los daños de las pruebas y el tratamiento. La Sociedad Estadounidense del Cáncer cree que los hombres no deben hacerse la prueba sin conocer lo que sabemos y lo que no sabemos sobre los riesgos y los posibles beneficios de las pruebas y el tratamiento. A partir de los 50 años, (45 si es afroamericano o hermano o padre padeció una afección antes de los 65 años) hable con su médico sobre los pros y los contras de las pruebas para que pueda decidir si las pruebas son la opción correcta para usted " [77].
Se pueden usar varias otras pruebas para recopilar información sobre la próstata y el tracto urinario. El tacto rectal puede permitir al médico detectar anomalías en la próstata. La cistoscopia muestra el tracto urinario desde el interior de la vejiga, utilizando un tubo de cámara delgado y flexible que se inserta en la uretra . La ecografía transrectal crea una imagen de la próstata usando ondas sonoras de una sonda en el recto, pero la única prueba que puede confirmar completamente el diagnóstico de cáncer de próstata es una biopsia , la extracción de pequeñas partes de la próstata para un examen microscópico.
Imágenes [ editar ]
Esta sección necesita más referencias médicas para su verificación o se basa demasiado en fuentes primarias . ( marzo de 2020 ) |
La ecografía y la resonancia magnética (IRM) son los dos principales métodos de obtención de imágenes utilizados para la detección del cáncer de próstata.
Resonancia magnética [ editar ]
Aspecto de la próstata en la resonancia magnética [ editar ]
En la resonancia magnética, las zonas central y de transición tienen una señal T2 más baja que la zona periférica. Dado que las zonas central y de transición no se pueden distinguir entre sí, se pueden describir mejor como la glándula central en la resonancia magnética. Por tanto, la glándula periférica tiene una señal más alta en T2WI que la glándula central. En la glándula periférica, el cáncer de próstata aparece como una lesión de baja intensidad.. Sin embargo, en la glándula central, las lesiones de baja intensidad no se pueden distinguir de la glándula central de baja intensidad. La restricción de la difusión es fundamental para identificar y caracterizar las lesiones de las glándulas centrales. Se pueden utilizar imágenes combinadas de difusión ponderada (DW) y resonancia magnética dinámica con contraste para distinguir las lesiones de próstata malignas de las benignas. Las imágenes fusionadas, de DW y MRI con realce dinámico de contraste, pueden visualizar áreas con baja intensidad de señal y efecto de lavado rápido, característico de los carcinomas. [78] Linfadenopatíase puede ver mejor con T1WI con supresión de grasa poscontraste. Otras regiones se pueden describir en MRI. El estroma fibromuscular anterior y la cápsula prostática a lo largo de la próstata posterior y lateral tienen una señal de T2WI baja, en contraste con la señal brillante de la zona periférica. Puede observarse extensión extraprostática con alteración de la integridad de la cápsula.
Resonancia magnética para la detección del cáncer de próstata [ editar ]
A partir de 2011, la resonancia magnética se utilizó para identificar los objetivos para la biopsia de próstata utilizando la resonancia magnética de fusión con ecografía (EE. UU.) O la guía de resonancia magnética solo. Una resonancia magnética por sí sola identificará correctamente al 91% de los hombres con cáncer de próstata clínicamente significativo, pero clasificará erróneamente al 63% de los hombres con riesgo de cáncer de próstata como pacientes con cáncer de próstata clínicamente significativo. [79] Una biopsia dirigida por resonancia magnética identificará correctamente al 80% de los hombres con cáncer de próstata. Sin embargo, clasificará al 6% de los hombres con riesgo de cáncer de próstata como pacientes con cáncer de próstata clínicamente significativo. [79]
Después de una resonancia magnética, las regiones de interés dentro de la exploración que pueden ser cancerosas a menudo se clasifican en una escala de probabilidad entre 1 y 5. Una de esas escalas es la escala del sistema de datos e informes de imágenes de próstata (PI-RADS) que define los estándares del servicio clínico. para resonancia magnética multiparamétrica (mpMRI), incluida la creación y generación de informes de imágenes. La puntuación de PI-RADS versión 2 ha mostrado una especificidad y sensibilidad de 73% y 95%, respectivamente, para la detección de cáncer de próstata. [80]
Cuando se utiliza una resonancia magnética para decidir si se debe realizar una biopsia en hombres que han tenido una biopsia previa, es un 5% más probable que haga un diagnóstico correcto que una biopsia estándar y es un 12% más probable que sea correcta para los hombres que pueden o puede no haber tenido una biopsia previa. [79] En los hombres que han tenido una biopsia negativa, esta combinación tiene un 44% más de probabilidades de conducir a un diagnóstico correcto. [79]
Otros usos de la resonancia magnética [ editar ]
La resonancia magnética de próstata también se utiliza para la planificación quirúrgica de la prostatectomía robótica . Ayuda a los cirujanos a decidir si resecar o preservar el paquete neurovascular, determinar el retorno a la continencia urinaria y ayudar a evaluar la dificultad quirúrgica. [81] La resonancia magnética se utiliza en otros tipos de planificación del tratamiento, tanto para la terapia focal [82] como para la radioterapia. [83] La resonancia magnética también se puede utilizar para seleccionar áreas para el muestreo de investigación en biobancos. [84] [85]
Base biológica de la visibilidad del cáncer de próstata en la resonancia magnética [ editar ]
Las propiedades biológicas que determinan si un tumor es visible o no en la resonancia magnética son poco conocidas. Una teoría es que las células tumorales sufren varios cambios genéticos durante la transformación que alteran la tasa de crecimiento celular y la formación de nuevos vasos sanguíneos, dando lugar a tumores con patrones histológicos más agresivos , regiones hipóxicas y aumento de la densidad celular, entre otras características. [86] Tener tumores más grandes y densos con cambios en la distribución de los vasos sanguíneos puede alterar la señal en la resonancia magnética mediante la restricción del agua y / o el movimiento de líquidos. [86]
Algunos estudios han relacionado la presencia de patrones histológicos raros dentro del tumor, como el patrón cribiforme. [87] Aunque investigaciones recientes sugieren que hay una serie de características histopatológicas que pueden influir en la detección de tumores por resonancia magnética. [88] A nivel genético , la visibilidad del cáncer de próstata en la resonancia magnética parece estar relacionada con características genéticas de una enfermedad agresiva, incluidos procesos como la proliferación celular , la hipoxia tumoral y el daño del ADN . [89] Los cambios genéticos que se observan de manera constante en los tumores visibles por resonancia magnética incluyen la pérdida del supresor de tumores PTEN , una mayor expresión de genes asociados a la proliferaciónCENPF , AGR2 y factor de crecimiento GDF15 , así como varios otros genes. [89] Los cambios en estas vías y genes pueden facilitar un mayor crecimiento tumoral, cambios en la vasculatura y la densidad que, en última instancia, cambian la señal en la resonancia magnética. [86]
Ultrasonido [ editar ]
Las imágenes por ultrasonido se pueden obtener por vía transrectal y se utilizan durante las biopsias de próstata. El cáncer de próstata puede verse como una lesión hipoecoica en el 60% de los casos. El otro 40% de las lesiones cancerosas son hiperecoicas o isoecoicas. En el Doppler color, las lesiones aparecen hipervasculares.
Biopsia [ editar ]
Si se sospecha cáncer, se ofrece una biopsia oportunamente. Durante una biopsia, un urólogo o radiólogo obtiene muestras de tejido de la próstata a través del recto o el perineo. [ verificación fallida ] Una pistola de biopsia inserta y retira agujas especiales de núcleo hueco (generalmente de tres a seis a cada lado de la próstata) en menos de un segundo. Las biopsias de próstata se realizan de forma rutinaria de forma ambulatoria y rara vez requieren hospitalización. Las biopsias sistemáticas identifican correctamente al 63% de los hombres con cáncer de próstata clínicamente significativo, pero se perderán el resto. [79] Para los hombres en riesgo de cáncer de próstata, la biopsia no clasificará erróneamente a ninguno de los hombres como pacientes con cáncer de próstata clínicamente significativo. [79]
Se deben utilizar antibióticos para prevenir complicaciones como fiebre , infecciones del tracto urinario y sepsis [90], incluso si no se ha definido el curso o la dosis más adecuados. [91] Aproximadamente el 55% de los hombres informan malestar durante la biopsia de próstata. [92]
Diagnóstico histopatológico [ editar ]
Un diagnóstico histopatológico incluye principalmente la evaluación de si existe un cáncer, así como cualquier subdiagnóstico, si es posible. El subdiagnóstico histopatológico tiene implicaciones para la posibilidad y metodología de la puntuación de Gleason . [94] El subdiagnóstico histopatológico más común es el adenocarcinoma acinar , que constituye el 93% de los diagnósticos. [95] La forma más común de adenocarcinoma acinar, a su vez, es el "adenocarcinoma, no especificado de otra manera", también denominado adenocarcinoma acinar convencional o habitual. [96]
Diagnóstico bioquímico [ editar ]
La fosfatasa alcalina está más elevada en las células metastásicas que en las no metastásicas. [97] Los niveles altos de fosfatasa alcalina se relacionan con una disminución significativa en la supervivencia. [97]
Puntuación de Gleason [ editar ]
El sistema de clasificación de Gleason se utiliza para ayudar a evaluar el pronóstico y ayuda a guiar la terapia. Una puntuación de Gleason se basa en la apariencia del tumor. [98] Los cánceres con una puntuación de Gleason más alta son más agresivos y tienen un pronóstico peor. Los puntajes patológicos varían de 2 a 10, y un número más alto indica mayores riesgos y mayor mortalidad.
Marcadores tumorales [ editar ]
Las muestras de tejido se pueden teñir para detectar la presencia de PSA y otros marcadores tumorales para determinar el origen de las células malignas que han hecho metástasis. [99]
El carcinoma de células pequeñas es un tipo raro (1% [100] ) que no se puede diagnosticar con PSA. [100] [101] A partir de 2009, los [actualizar]investigadores estaban investigando formas de detectar este tipo, porque es rápido para hacer metástasis. [101]
La oncoproteína BCL-2 se asocia con el desarrollo de cáncer de próstata independiente de andrógenos, debido a sus altos niveles de expresión en tumores independientes de andrógenos en estadios avanzados. La regulación positiva de BCL-2 después de la ablación de andrógenos en líneas celulares de carcinoma de próstata y en un modelo de rata macho castrada estableció además una conexión entre la expresión de BCL-2 y la progresión del cáncer de próstata. [102]
Puesta en escena [ editar ]
Una parte importante de la evaluación del cáncer de próstata es determinar el estadio o el grado de diseminación. Conocer el estadio ayuda a definir el pronóstico y es útil a la hora de seleccionar terapias. El sistema más común es el sistema TNM de cuatro etapas (abreviado de tumor / ganglios / metástasis). Sus componentes incluyen el tamaño del tumor, el número de ganglios linfáticos afectados y la presencia de cualquier otra metástasis . [103]
La distinción más importante que hace cualquier sistema de estadificación es si el cáncer se limita a la próstata. En el sistema TNM, los cánceres clínicos T1 y T2 se encuentran solo en la próstata, mientras que los cánceres T3 y T4 han hecho metástasis. Se pueden usar varias pruebas para buscar evidencia de propagación. Las organizaciones profesionales de especialidades médicas no recomiendan el uso de tomografías por emisión de positrones , tomografías computarizadas o gammagrafías óseas cuando un médico estadifica el cáncer de próstata temprano con bajo riesgo de metástasis. [104] Esas pruebas serían apropiadas en casos como cuando una tomografía computarizada evalúa la diseminación dentro de la pelvis, una gammagrafía ósea busca diseminación a los huesos y una resonancia magnética de bobina endorrectal.evalúa la cápsula prostática y las vesículas seminales . Las gammagrafías óseas deben revelar un aspecto osteoblástico debido al aumento de la densidad ósea en las áreas de metástasis ósea , lo contrario de lo que se encuentra en muchos otros cánceres metastásicos.
Después de una biopsia, un patólogo examina las muestras con un microscopio. Si hay cáncer, el patólogo informa el grado del tumor. El grado indica cuánto difiere el tejido tumoral del tejido prostático normal y sugiere qué tan rápido es probable que crezca el tumor. El patólogo asigna un número de Gleason del 1 al 5 para el patrón más común observado bajo el microscopio, luego hace lo mismo para el segundo patrón más común. La suma de estos dos números es la puntuación de Gleason. La etapa de Whitmore-Jewett es otro método.
En hombres con cáncer de próstata localizado de alto riesgo, la estadificación con PSMA PET / CT puede ser apropiada para detectar diseminación nodal o metastásica a distancia. En 2020, un ensayo aleatorizado de fase 3 comparó la PET / TC con PSMA de galio-68 con las imágenes estándar (TC y gammagrafía ósea). Informó una precisión superior de la PET / TC con Galio-68 PSMA-11 (92% frente a 65%), un mayor cambio significativo en el manejo (28% frente a 15%), hallazgos de imágenes menos ambiguos / inciertos (7% frente a 23%) y menor exposición a la radiación (10 msV frente a 19 mSv). El estudio concluyó que PSMA PET / CT es un reemplazo adecuado para las imágenes convencionales. [105]
Esclerosis de los huesos de la columna torácica debido a metástasis de cáncer de próstata (imagen de TC)
Esclerosis de los huesos de la columna torácica debido a metástasis de cáncer de próstata (imagen de TC)
Esclerosis de los huesos de la pelvis debido a metástasis de cáncer de próstata
Prevención [ editar ]
Dieta y estilo de vida [ editar ]
Los datos sobre la relación entre la dieta y el cáncer de próstata son escasos. [106] Sin embargo, la tasa de cáncer de próstata está relacionada con el consumo de la dieta occidental. [106] Pocas o ninguna evidencia asocia la ingesta de grasas trans , grasas saturadas y carbohidratos con el cáncer de próstata. [106] [107] La evidencia no ofrece un papel para los ácidos grasos omega-3 en la prevención del cáncer de próstata. [106] [108] Los suplementos vitamínicos parecen no tener ningún efecto y algunos pueden aumentar el riesgo. [17] [106] La ingesta alta de calcio suplementario se ha relacionado con el cáncer de próstata avanzado. [109]
El pescado puede reducir las muertes por cáncer de próstata, pero no parece afectar la ocurrencia. [110] Alguna evidencia apoya tasas más bajas de cáncer de próstata con una dieta vegetariana /, [111] licopeno , selenio [112] [113] verduras crucíferas , soja, frijoles y / u otras legumbres . [114]
El ejercicio regular puede reducir ligeramente el riesgo, especialmente la actividad vigorosa. [114]
Medicamentos [ editar ]
En aquellos que se someten a exámenes de detección con regularidad, los inhibidores de la 5-alfa-reductasa ( finasterida y dutasterida ) reducen el riesgo general de cáncer de próstata. Los datos son insuficientes para determinar si afectan el riesgo de muerte y pueden aumentar la posibilidad de casos más graves. [115]
Proyección [ editar ]
Las pruebas de detección del cáncer de próstata buscan cánceres en personas que no presentan síntomas. Las opciones incluyen el examen rectal digital y el análisis de sangre PSA. [116] Tal detección es controvertida, [117] y para muchos, puede conducir a interrupciones innecesarias y posiblemente a consecuencias dañinas. [118] Los daños de los exámenes de detección basados en la población, principalmente debido al sobrediagnóstico (la detección de cánceres latentes que de otro modo no se habrían descubierto) pueden superar los beneficios. [116] Otros recomiendan la toma de decisiones compartida, un enfoque en el que la detección puede ocurrir después de una consulta médica. [119]
El Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF) sugiere que la decisión de hacerse una prueba de detección de PSA se base en una consulta con un médico para hombres de 55 a 69 años. [12] USPSTF recomienda no realizar pruebas de detección de PSA después de los 70 años. [14] Los Centros para el Control y la Prevención de Enfermedades respaldaron la conclusión de USPSTF. [120] La Sociedad Estadounidense de Oncología Clínica y el Colegio Estadounidense de Médicos desalientan el cribado para quienes se espera que vivan menos de 10 a 15 años, mientras que quienes tienen una mayor esperanza de vida deben tomar una decisión individualmente para equilibrar los riesgos y beneficios potenciales.[121] En general, concluyeron, "es incierto si los beneficios asociados con las pruebas de PSA para la detección del cáncer de próstata valen los daños asociados con la detección y el tratamiento innecesario posterior". [122]
Las pautas de la American Urological Association (AUA 2013) exigen sopesar los beneficios inciertos de la detección con los daños conocidos asociados con las pruebas de diagnóstico y el tratamiento. La AUA recomienda que la toma de decisiones compartida debe controlar las pruebas de detección para las personas de 55 a 69 años, y que las pruebas de detección no deben realizarse con más frecuencia que cada dos años. [123] En el Reino Unido , en 2015, no existía ningún programa para detectar el cáncer de próstata. [13]
Gestión [ editar ]
La primera decisión es si se necesita tratamiento. Las formas de bajo grado que se encuentran en los hombres mayores a menudo crecen tan lentamente que no se requiere tratamiento. [124] El tratamiento también puede ser inapropiado si una persona tiene otros problemas de salud graves o no se espera que viva lo suficiente para que aparezcan los síntomas. Los enfoques en los que se pospone el tratamiento se denominan "manejo expectante". [124] El manejo expectante se divide en dos enfoques: espera vigilante , que tiene una intención paliativa (tiene como objetivo tratar los síntomas solamente) y vigilancia activa , que tiene una intención curativa (tiene como objetivo evitar que el cáncer avance). [124]
La mejor opción depende del estadio de la enfermedad, la puntuación de Gleason y el nivel de PSA. Otros factores importantes son la edad, la salud general y las opiniones de una persona sobre los posibles tratamientos y sus posibles efectos secundarios. Debido a que la mayoría de los tratamientos pueden tener efectos secundarios importantes , como disfunción eréctil e incontinencia urinaria , las discusiones sobre el tratamiento a menudo se centran en equilibrar los objetivos de la terapia con los riesgos de alteraciones del estilo de vida. Una revisión de 2017 encontró que se necesita más investigación centrada en los resultados centrados en la persona para guiar a los pacientes. [125] A menudo se recomienda una combinación de opciones de tratamiento. [126] [127] [128]
Aunque el uso generalizado de la prueba de detección del PSA en los EE. UU. Ha dado como resultado un diagnóstico a una edad más temprana y en la etapa del cáncer, casi todos los casos se siguen diagnosticando después de los 65 años, mientras que alrededor del 25% se diagnostica después de los 75 años. [129] Aunque la Red Nacional Integral del Cáncer de EE. UU. Las directrices recomiendan utilizar la esperanza de vida para ayudar a tomar decisiones sobre el tratamiento; en la práctica, a muchos pacientes de edad avanzada no se les ofrecen opciones de tratamiento curativo como la prostatectomía radical o la radioterapia y, en cambio, se tratan con hormonoterapia o espera vigilante. [130]
Las pautas para situaciones clínicas específicas requieren una estimación de la esperanza de vida. [131] A medida que aumenta la esperanza de vida promedio debido a los avances en el tratamiento de otras enfermedades, más pacientes vivirán lo suficiente para que el cáncer de próstata exprese síntomas. Por lo tanto, creció el interés en modalidades de tratamiento agresivas como la cirugía o la radiación incluso para enfermedades localizadas.
Alternativamente, se propuso un cuestionario de 18 ítems para saber si los pacientes tienen el conocimiento y la comprensión adecuados de sus opciones de tratamiento. En un estudio de 2015, la mayoría de los recién diagnosticados respondieron correctamente menos de la mitad de las preguntas. [131]
Vigilancia [ editar ]
Muchos hombres diagnosticados con cáncer de próstata de bajo riesgo son elegibles para la vigilancia activa. El tumor se observa cuidadosamente a lo largo del tiempo, con la intención de iniciar el tratamiento si aparecen signos de progresión. La vigilancia activa no es sinónimo de espera vigilante , término que no implica ningún tratamiento o programa específico de seguimiento, con el supuesto de que sólo se utilizaría tratamiento paliativo si se desarrolla una enfermedad sintomática avanzada. [124]
La vigilancia activa implica monitorear el crecimiento del tumor o los síntomas que desencadenan el tratamiento. El proceso de monitoreo puede incluir pruebas de PSA, tacto rectal y / o biopsias repetidas cada pocos meses. [132] El objetivo de la vigilancia activa es posponer el tratamiento y evitar el sobretratamiento y sus efectos secundarios, dado un tumor de crecimiento lento o autolimitado que en la mayoría de las personas es poco probable que cause problemas. Este enfoque no se usa para cánceres agresivos y puede causar ansiedad a las personas que creen erróneamente que todos los cánceres son mortales o que su condición es potencialmente mortal. Del 50 al 75% de los pacientes mueren por otras causas sin experimentar síntomas prostáticos. [133] En la enfermedad localizada, según el seguimiento a largo plazo,La prostatectomía radical da como resultado resultados oncológicos significativamente mejores en comparación con la espera vigilante. [134] Sin embargo, también hay aumentos marcados en las tasas de incontinencia urinaria y disfunción eréctil . [134] Dado que estos resultados se basan principalmente en hombres diagnosticados antes de la detección generalizada de PSA , los resultados no pueden ser muy generalizados. [134] En comparación con el monitoreo / vigilancia activa , en el seguimiento a los diez años, la prostatectomía radical probablemente tenga resultados similares para la supervivencia específica de la enfermedad y probablemente reduzca el riesgo de progresión y diseminación de la enfermedad. [134] Aún así, la función urinaria y sexual probablemente esté disminuida en pacientes tratados con prostatectomía radical. [134]
Tratamiento activo [ editar ]
Se encuentran disponibles tratamientos quirúrgicos y no quirúrgicos, pero el tratamiento puede ser difícil y se pueden utilizar combinaciones. [135] El tratamiento con radioterapia de haz externo , braquiterapia , criocirugía , ultrasonido focalizado de alta intensidad y prostatectomía se ofrece, en general, a los hombres cuyo cáncer permanece dentro de la próstata. La terapia hormonal y la quimioterapia a menudo se reservan para la enfermedad metastásica. Las excepciones incluyen la terapia local o dirigida por metástasis con radiación que se puede usar para tumores avanzados con metástasis limitada. [136] La terapia hormonal se usa para algunos tumores en estadio temprano. Crioterapia(el proceso de congelación del tumor), se puede ofrecer terapia hormonal y quimioterapia si el tratamiento inicial falla y el cáncer progresa. Se informó que Sipuleucel-T , una vacuna contra el cáncer , ofrece un aumento de cuatro meses en la supervivencia en el cáncer de próstata metastásico, [137] pero la autorización de comercialización se retiró el 19 de mayo de 2015.
Si la radioterapia falla, la prostatectomía radical puede ser una opción, [138] aunque es una cirugía técnicamente desafiante. [ cita requerida ] Sin embargo, la radioterapia después del fracaso quirúrgico puede tener muchas complicaciones. [139] Se relaciona con un pequeño aumento de cáncer de vejiga y colon. [140] La radioterapia y la cirugía parecen producir resultados similares con respecto a la función intestinal, eréctil y urinaria después de cinco años. [141]
Tratamiento no quirúrgico [ editar ]
El tratamiento no quirúrgico puede incluir radioterapia, quimioterapia, terapia hormonal, radioterapia de haz externo y terapia de partículas , ultrasonido focalizado de alta intensidad o alguna combinación. [142] [143]
El cáncer de próstata que persiste cuando los niveles de testosterona se reducen mediante la terapia hormonal se denomina cáncer de próstata resistente a la castración (CRPC). [144] [145] Muchos cánceres en etapa temprana necesitan niveles normales de testosterona para crecer, pero el CRPC no. Anteriormente considerado "cáncer de próstata resistente a hormonas" o "cáncer de próstata independiente de andrógenos", el término CRPC surgió porque estos cánceres muestran dependencia de hormonas, particularmente testosterona, para la activación del receptor de andrógenos . [146]
El docetaxel quimioterapéutico contra el cáncer se ha utilizado como tratamiento para el CRPC con una mediana de beneficio de supervivencia de 2 a 3 meses. [147] [148] Un tratamiento de quimioterapia de segunda línea es el cabazitaxel . [149] Una combinación de bevacizumab , docetaxel , talidomida y prednisona parece ser eficaz en el tratamiento del CRPC. [150]
El tratamiento de inmunoterapia con sipuleucel-T en CRPC pareció aumentar la supervivencia en cuatro meses. [151] Sin embargo, la autorización de comercialización de sipuleucel-T se retiró el 19 de mayo de 2015. La terapia hormonal de segunda línea con abiraterona aumenta la supervivencia en 4,6 meses. [152] La enzalutamida es otro agente hormonal de segunda línea con una ventaja de supervivencia de cinco meses. Tanto la abiraterona como la enzalutamida se encuentran actualmente en ensayos clínicos en personas con CRPC que no han recibido previamente quimioterapia. [153] [154]
No todos los pacientes responden a los fármacos bloqueadores de la señalización de andrógenos. Ciertas células con características que se asemejan a las células madre no se ven afectadas. [155] [156] Por lo tanto, el deseo de mejorar los resultados de CRPC resultó en dosis crecientes o terapia de combinación con agentes bloqueadores de la señalización de andrógenos sinérgicos. [157] Pero incluso estas combinaciones no afectarán a las células madre que no exhiben señalización de andrógenos. [158]
Para los pacientes con cáncer de próstata metastásico que se ha extendido a los huesos, los médicos usan una variedad de agentes modificadores de los huesos para prevenir complicaciones esqueléticas y apoyar la formación de nueva masa ósea. [159] El ácido zoledrónico (un bisfosfonato ) y el denosumab (un inhibidor del ligando RANK ) parecen ser agentes eficaces, pero se relacionan con eventos adversos más frecuentes y graves. [159]
Cirugía [ editar ]
La prostatectomía radical se considera el pilar del tratamiento quirúrgico del cáncer de próstata, donde el cirujano extirpa la próstata, las vesículas seminales y los ganglios linfáticos circundantes . Puede realizarse mediante una técnica abierta (una incisión en la piel en la parte inferior del abdomen) o por vía laparoscópica . La prostatectomía radical retropúbica es la técnica quirúrgica abierta más utilizada. [ cita requerida ] La prostatectomía asistida por robot se ha vuelto común. [160] Hombres con cáncer de próstata localizado, sometidos a prostatectomía radical laparoscópicao prostatectomía radical asistida por robot, pueden tener estadías más breves en el hospital y recibir menos transfusiones de sangre que los hombres que se someten a prostatectomía radical abierta. [161] Se desconoce cómo se comparan estos tratamientos con respecto a la supervivencia general o la supervivencia sin recidiva. [161]
La resección transuretral de la próstata es el tratamiento quirúrgico estándar para el agrandamiento benigno de la próstata . [160] En el cáncer de próstata, este procedimiento se puede usar para aliviar los síntomas de retención urinaria causados por un tumor de próstata grande, pero no se usa para tratar el cáncer en sí. El procedimiento se realiza bajo anestesia espinal, se inserta un resectoscopio dentro del pene y se corta el tejido prostático adicional para despejar el paso de la orina.
Complicaciones [ editar ]
Las dos principales complicaciones encontradas después de la prostatectomía y la radioterapia prostática son la disfunción eréctil y la incontinencia urinaria , principalmente de tipo estrés . La mayoría de los hombres recuperan la continencia entre 6 y 12 meses después de la operación, por lo que los médicos suelen esperar al menos un año antes de recurrir a tratamientos invasivos. [162]
La incontinencia urinaria de esfuerzo generalmente ocurre después de una cirugía de próstata o radioterapia debido a factores que incluyen daño al esfínter uretral o al tejido y los nervios circundantes. La próstata rodea la uretra, un tubo muscular que cierra la vejiga urinaria. Cualquiera de las razones mencionadas puede provocar un cierre incompetente de la uretra y, por tanto, incontinencia. [163] La terapia inicial incluye entrenamiento de la vejiga , cambios en el estilo de vida, ejercicios de Kegel y el uso de compresas para la incontinencia . El tratamiento quirúrgico más invasivo puede incluir la inserción de un cabestrillo uretral o un esfínter urinario artificial, que es un dispositivo mecánico que imita la función del esfínter uretral, y es activado manualmente por el paciente a través de un interruptor implantado en el escroto . Este último se considera el estándar de oro en pacientes con incontinencia urinaria de esfuerzo moderada o grave. [164]
La disfunción eréctil ocurre en diferentes grados en casi todos los hombres que se someten a un tratamiento para el cáncer de próstata, incluida la radioterapia o la cirugía; sin embargo, dentro de un año, la mayoría notará una mejora. Si los nervios se dañaron, es posible que este progreso no se lleve a cabo. El tratamiento farmacológico incluye inhibidores de la PDE-5 como viagra o cialis , o fármacos intracavernosos inyectables que se inyectan directamente en el pene ( prostaglandina E1 y mezclas de fármacos vasoactivos). Otra terapia no farmacológica incluye dispositivos de constricción por vacío e implantes de pene . [165]
Pronóstico [ editar ]
Muchos cánceres de próstata no están destinados a ser letales y, en última instancia, la mayoría de los hombres no morirán como resultado de la enfermedad. La mortalidad varía ampliamente según la geografía y otros elementos. En los Estados Unidos, las tasas de supervivencia a cinco años oscilan entre el 29% (metástasis a distancia) y el 100% (tumores locales o regionales). [166] En Japón, la tasa de letalidad se elevó a 8,6 / 100.000 en 2000. [167] En la India en la década de 1990, la mitad de los diagnosticados con cáncer local murieron dentro de los 19 años. [168] Un estudio informó que los afroamericanos tienen entre 50 y 60 veces más muertes que las encontradas en Shanghai, China. [169] En Nigeria , el 2% de los hombres desarrollan cáncer de próstata y el 64% de ellos muere después de 2 años. [170]La mayoría de los hombres nigerianos presentan enfermedad metastásica con una supervivencia típica de 40 meses. [171]
En los pacientes que se someten a tratamiento, los indicadores de pronóstico clínico más importantes del resultado de la enfermedad son el estadio, el nivel de PSA previo al tratamiento y la puntuación de Gleason. Cuanto mayor sea el grado y el estadio, peor será el pronóstico. Se pueden utilizar nomogramas para calcular el riesgo estimado de un paciente individual. Las predicciones se basan en la experiencia de grandes grupos de pacientes. [172] Un factor de complicación es que la mayoría de los pacientes tienen múltiples focos tumorales independientes al momento del diagnóstico, y estos focos tienen cambios genéticos y características moleculares independientes. [173] Debido a esta amplia heterogeneidad inter-focal, existe el riesgo de que el pronóstico se establezca en función del foco del tumor incorrecto.
La terapia de ablación de andrógenos causa remisión en 80 a 90% de los pacientes sometidos a terapia, lo que resulta en una mediana de supervivencia libre de progresión de 12 a 33 meses. Después de la remisión, generalmente surge un fenotipo independiente de andrógenos, en el que la mediana de supervivencia general es de 23 a 37 meses desde el momento del inicio de la terapia de ablación con andrógenos. [174] No está claro cómo se establece la independencia de los andrógenos y cómo se restablece la progresión. [175]
Sistemas de clasificación [ editar ]
Hay varias herramientas disponibles para ayudar a predecir los resultados, como el estadio patológico y la recurrencia después de la cirugía o la radioterapia. La mayoría combina el estadio, el grado y el nivel de PSA, y algunos incluyen el número o porcentaje de núcleos de biopsia positivos, la edad y / u otra información.
- La clasificación de D'Amico estratifica a los hombres en riesgo bajo, intermedio o alto según el estadio, el grado y el PSA. Se utiliza ampliamente en la práctica clínica y en entornos de investigación. La principal desventaja del sistema de tres niveles es que no tiene en cuenta múltiples parámetros adversos (p. Ej., Puntuación de Gleason alta y PSA alto) en la estratificación de los pacientes.
- La tabla de Partin] [176] predice resultados patológicos (estado de los márgenes, extensión extraprostática e invasión de vesículas seminales) basándose en las mismas tres variables y se publican como tablas de búsqueda.
- Los nomogramas de Kattan predicen la recurrencia después de la cirugía y / o la radioterapia, según los datos disponibles en el momento del diagnóstico o después de la cirugía. La puntuación de Kattan representa la probabilidad de permanecer libre de enfermedad en un intervalo de tiempo determinado después del tratamiento.
- La puntuación de la UCSF Cancer of the Prostate Risk Assessment (CAPRA) predice tanto el estado patológico como la recurrencia después de la cirugía. Ofrece una precisión comparable al nomograma preoperatorio de Kattan y se puede calcular sin tablas ni calculadora. Los puntos se asignan según el PSA, el grado, la etapa, la edad y el porcentaje de núcleos positivos; la suma arroja una puntuación de 0 a 10, y cada dos puntos representa aproximadamente el doble del riesgo de recurrencia. La puntuación CAPRA se obtuvo a partir de datos comunitarios en la base de datos CaPSURE. [177] Se ha validado entre más de 10,000 pacientes de prostatectomía, incluidos los pacientes de CaPSURE; [178] el registro SEARCH, que representa datos de varios centros médicos militares y de la Administración de Salud de los Veteranos ; [179]una cohorte multiinstitucional en Alemania; [180] y la cohorte de prostatectomía en la Universidad Johns Hopkins. [181] Más recientemente, se ha demostrado que predice la metástasis y la mortalidad después de la prostatectomía, la radioterapia, la conducta expectante o la terapia de privación de andrógenos. [182]
Esperanza de vida [ editar ]
Las proyecciones de esperanza de vida son promedios para toda la población masculina, y muchos factores médicos y de estilo de vida modifican estos números. Por ejemplo, los estudios han demostrado que un hombre de 40 años perderá 3,1 años de vida si tiene sobrepeso (IMC 25-29) y 5,8 años de vida si es obeso (IMC 30 o más), en comparación con los hombres de peso normal. Si tiene sobrepeso y fuma, perderá 6,7 años, y si es obeso y fuma, perderá 13,7 años. [183]
No hay evidencia que demuestre que la cirugía o la radiación de haz tengan una ventaja sobre la otra en este sentido. Las tasas de mortalidad más bajas informadas con la cirugía parecen ocurrir porque es más probable que la cirugía se ofrezca a hombres más jóvenes con cánceres menos graves. No se dispone de suficiente información para determinar si la radiación de las semillas prolonga la vida más fácilmente que los otros tratamientos, pero los datos hasta ahora no sugieren que así sea. [184]
Es poco probable que los hombres con enfermedad de bajo grado (Gleason 2-4) mueran de cáncer de próstata dentro de los 15 años posteriores al diagnóstico. Los hombres mayores (70 a 75 años) con enfermedad de bajo grado tuvieron una supervivencia general de aproximadamente 20% a los 15 años debido a muertes por causas concurrentes. Los hombres con enfermedad de alto grado (Gleason 8-10) experimentaron una alta mortalidad dentro de los 15 años posteriores al diagnóstico, independientemente de su edad. [185]
Epidemiología [ editar ]
En 2012, el cáncer de próstata es el segundo cáncer diagnosticado con mayor frecuencia (con un 15% de todos los cánceres masculinos) [187] y la sexta causa principal de muerte por cáncer en hombres en todo el mundo. [188] En 2010, el cáncer de próstata provocó 256 000 muertes, frente a las 156 000 muertes en 1990. [189] Las tasas de cáncer de próstata varían ampliamente. Las tarifas varían ampliamente entre países. Es menos común en el sur y este de Asia, y más común en Europa, América del Norte, Australia y Nueva Zelanda. [190] El cáncer de próstata es menos común entre los hombres asiáticos y más común entre los hombres negros, con hombres blancos en el medio. [191] [192]
La tasa de incidencia anual promedio de cáncer de próstata entre 1988 y 1992 entre los hombres chinos en los Estados Unidos fue 15 veces mayor que la de sus contrapartes que viven en Shanghai y Tianjin, [191] [192] [193] pero estas altas tasas pueden verse afectadas por mayores tasas de detección. [194] Muchos sugieren que el cáncer de próstata puede no estar informado, pero la incidencia de hiperplasia prostática benigna en China y Japón es similar a las tasas en los países occidentales. [195] [196]
Más del 80% de los hombres desarrollan cáncer de próstata a los 80 años. [197]
Estados Unidos [ editar ]
Esta sección necesita citas adicionales para su verificación . ( Agosto de 2020 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
El cáncer de próstata es la tercera causa principal de muerte por cáncer en los hombres, superado por el cáncer de pulmón y el cáncer colorrectal. Representa el 19% de todos los cánceres masculinos y el 9% de las muertes relacionadas con el cáncer masculinos.
Los casos oscilaron entre unos 230.000 en 2005 [198] y unos 164.690 en 2018.
Las muertes se mantuvieron estables en torno a 30.000 en 2005 [198] y 29.430 en 2018.
Las tasas de incidencia ajustadas por edad aumentaron de manera constante desde 1975 hasta 1992, con aumentos particularmente dramáticos asociados con la propagación de la detección del PSA a fines de la década de 1980, seguidos más tarde por una disminución en la incidencia. Una disminución en las tasas de incidencia en etapa temprana de 2011 a 2012 (19%) en hombres de 50 años o más persistió hasta 2013 (6%).
La disminución de las tasas de mortalidad en determinadas jurisdicciones puede reflejar la interacción de la detección del PSA y la mejora del tratamiento. El riesgo de por vida estimado es de aproximadamente el 14% y el riesgo de mortalidad de por vida es del 2,6%.
Entre 2005 y 2011, la proporción de enfermedades diagnosticadas en una etapa locorregional fue del 93% para los blancos y del 92% para los afroamericanos; la proporción de enfermedades diagnosticadas en una etapa tardía fue del 4% para los blancos y del 5% para los afroamericanos.
El cáncer de próstata es más común en la población afroamericana que en la población blanca estadounidense . [3] Un estudio de autopsia de hombres blancos y asiáticos también encontró un aumento en el cáncer de próstata oculto con la edad, alcanzando casi el 60% en hombres mayores de 80 años. Más del 50% de los cánceres en los hombres asiáticos y el 25% de los cánceres en los hombres blancos tenían una puntuación de Gleason de 7 o más, lo que sugiere que la puntuación de Gleason puede ser un indicador impreciso de casos clínicamente insignificantes. [199]
Canadá [ editar ]
El cáncer de próstata es el tercer tipo de cáncer entre los hombres canadienses. En 2016, alrededor de 4.000 murieron y se diagnosticó cáncer de próstata a 21.600 hombres. [117]
Europa [ editar ]
En Europa en 2012, fue el tercer cáncer más diagnosticado después de los cánceres de mama y colorrectal con 417.000 casos. [200]
En el Reino Unido, es la segunda causa más común de muerte por cáncer después del cáncer de pulmón, donde se diagnostican alrededor de 35.000 casos cada año, de los cuales alrededor de 10.000 son mortales. [201]
Historia [ editar ]
La próstata fue descrita por primera vez por el anatomista veneciano Niccolò Massa en 1536, e ilustrada por el anatomista flamenco Andreas Vesalius en 1538. [202] El cáncer de próstata se identificó en 1853. [203] [204] Inicialmente se consideró una enfermedad rara, probablemente debido a esperanzas de vida más cortas y métodos de detección más deficientes en el siglo XIX. Los primeros tratamientos fueron cirugías para aliviar la obstrucción urinaria. [205]
La extirpación de la glándula se describió por primera vez en 1851, [206] y la prostatectomía perineal radical fue realizada por primera vez en 1904 por Hugh H. Young en el Hospital Johns Hopkins . [207] [203]
La extirpación quirúrgica de los testículos ( orquiectomía ) para tratar el cáncer de próstata se realizó por primera vez en la década de 1890, con un éxito limitado. La resección transuretral de la próstata (RTUP) reemplazó la prostatectomía radical para el alivio sintomático de la obstrucción a mediados del siglo XX porque podría preservar mejor la función eréctil del pene. La prostatectomía radical retropúbica fue desarrollada en 1983 por Patrick Walsh. [208] Este abordaje quirúrgico permitió la extirpación de la próstata y los ganglios linfáticos con el mantenimiento de la función del pene.
En 1941, Charles B. Huggins publicó estudios en los que utilizó estrógeno para oponerse a la producción de testosterona en hombres con cáncer de próstata metastásico. Este descubrimiento de la " castración química " le valió a Huggins el Premio Nobel de Fisiología o Medicina de 1966 . [209] El papel de la hormona liberadora de gonadotropina (GnRH) en la reproducción fue determinado por Andrzej W. Schally y Roger Guillemin , quienes compartieron el Premio Nobel de Fisiología o Medicina de 1977 por este trabajo. Los agonistas del receptor de GnRH, como la leuprorelina y la goserelina , se desarrollaron y utilizaron posteriormente para tratar el cáncer de próstata.[210] [211]
La radioterapia para el cáncer de próstata se desarrolló por primera vez a principios del siglo XX e inicialmente consistía en implantes de radio intraprostático . La radioterapia de haz externo se hizo más popular a medida que se dispuso de fuentes de radiación [rayos X] más potentes a mediados del siglo XX. La braquiterapia con semillas implantadas (para el cáncer de próstata) se describió por primera vez en 1983. [212]
La quimioterapia sistémica para el cáncer de próstata se estudió por primera vez en la década de 1970. El régimen inicial de ciclofosfamida y 5-fluorouracilo se unió rápidamente a regímenes que utilizaban otros fármacos de quimioterapia sistémica. [213]
La enzalutamida obtuvo la aprobación de la FDA en 2012 para el tratamiento del cáncer de próstata resistente a la castración (CRPC). [153] [154] Alpharadin obtuvo la aprobación de la FDA en 2013, en el marco del programa de revisión prioritaria. [214]
En 2006, un retrovirus previamente desconocido, el virus Xenotrópico relacionado con MuLV (XMRV), se asoció con tumores de próstata humanos, [215] pero PLOS Pathogens se retractó del artículo en 2012. [215]
Sociedad y cultura [ editar ]
Las personas con cáncer de próstata generalmente encuentran disparidades significativas en la conciencia, el financiamiento, la cobertura de los medios y la investigación y, por lo tanto, un tratamiento inferior y resultados más pobres, en comparación con otros cánceres de igual prevalencia. [216] En 2001, The Guardian señaló que Gran Bretaña tenía 3.000 enfermeras especializadas en cáncer de mama , en comparación con una sola enfermera para el cáncer de próstata. El tiempo de espera entre la derivación y el diagnóstico fue de dos semanas para el cáncer de mama y de tres meses para el cáncer de próstata. [217]
Un informe de 2007 de la Coalición Nacional contra el Cáncer de Próstata con sede en EE. UU. Indicó que los medicamentos contra el cáncer de mama superaron en número siete a uno a los medicamentos contra el cáncer de mama. El Times también señaló un "sesgo anti-masculino en la financiación del cáncer" con una discrepancia de cuatro a uno en el Reino Unido tanto por parte del gobierno como por organizaciones benéficas contra el cáncer como Cancer Research UK . [216] [218] Los críticos citan estas cifras cuando afirman que la salud de las mujeres se ve favorecida por la salud de los hombres. [219]
Las disparidades se extienden a la detección, ya que los gobiernos no financian o exigen la detección del cáncer de próstata al tiempo que apoyan plenamente los programas de cáncer de mama. Por ejemplo, un informe de 2007 encontró que 49 estados de EE. UU. Exigen cobertura de seguro para la detección de cáncer de mama de rutina, en comparación con 28 para el cáncer de próstata. [220]
El cáncer de próstata experimenta una cobertura de los medios significativamente menor que otros cánceres igualmente prevalentes, superados en 2,6: 1 por el cáncer de mama. [216]
El Mes de Concientización sobre el Cáncer de Próstata tiene lugar en septiembre en varios países. Se usa una cinta azul claro para promover la causa. [221] [222]
Investigación [ editar ]
Cáncer de próstata resistente a la castración [ editar ]
La enzalutamida es un antiandrógeno no esteroideo (NSAA). [153] [154]
Alpharadin utiliza isótopos de radio 223 dirigidos a los huesos para destruir las células cancerosas mediante radiación alfa . [223] [ fuente médica no confiable? ]
PARP inhibidor olaparib es un fármaco aprobado para el cáncer de mama / ovario que está siendo sometido a ensayos clínicos. [224] También en ensayos para CRPC están: inhibidor de punto de control ipilimumab , inhibidor de CYP17 galeterona (TOK-001) e inmunoterapia PROSTVAC . [224]
Todos los medicamentos para el CRPC bloquean la señalización del receptor de andrógenos (AR) mediante el direccionamiento directo o indirecto del dominio de unión al ligando AR (LBD). AR pertenece a la familia de receptores nucleares de esteroides . El desarrollo de la próstata depende de la señalización de andrógenos mediada a través de la AR, y la AR también es importante para la progresión de la enfermedad. Han surgido moléculas que podrían apuntar con éxito a dominios alternativos. [225] Tales terapias podrían proporcionar una ventaja; particularmente en el tratamiento de cánceres de próstata que son resistentes a las terapias actuales. [225]
Preclínico [ editar ]
Se ha identificado que la araquidonato 5-lipoxigenasa juega un papel importante en la supervivencia de las células del cáncer de próstata. [226] [227] [228] Se están desarrollando medicamentos que se dirigen a esta enzima. [226] [227] [228] En particular, los inhibidores de la araquidonato 5-lipoxigenasa producen una muerte celular programada rápida y masiva en las células del cáncer de próstata. [226] [227] [228]
La galectina-3 es otro objetivo potencial. [229] Se han descrito perfiles de glucanos aberrantes en el cáncer de próstata, [230] [231] y los estudios han encontrado vínculos específicos entre la firma de galectina y el cáncer de próstata. [232] [233]
La familia de quinasas PIM es otro objetivo potencial para la inhibición selectiva. Se están desarrollando varios fármacos relacionados. Se ha sugerido que el enfoque más prometedor puede ser co-dirigirse a esta familia con otras vías, incluida PI3K . [18]
Modelos de cáncer [ editar ]
Los científicos han establecido líneas celulares de cáncer de próstata para investigar la progresión de la enfermedad. LNCaP , PC-3 ( PC3 ) y DU-145 ( DU145 ) son líneas celulares de cáncer de próstata de uso común. La línea celular de cáncer LNCaP se estableció a partir de una lesión metastásica de ganglio linfático humano de adenocarcinoma de próstata. Las células PC-3 y DU-145 se establecieron a partir de adenocarcinoma de próstata humano metastásico al hueso y al cerebro, respectivamente. Las células LNCaP expresan AR, pero las células PC-3 y DU-145 expresan muy poca o ninguna AR.
La proliferación de células LNCaP depende de los andrógenos, pero la proliferación de las células PC-3 y DU-145 es insensible a los andrógenos . La elevación de la expresión de AR se observa a menudo en pacientes con tumores de próstata avanzados . [234] [235] Se han desarrollado algunas sublíneas de LNCaP independientes de andrógenos a partir de las células LNCaP dependientes de andrógenos de la ATCC después de la privación de andrógenos para el estudio de la progresión del cáncer de próstata. Estas células LNCaP independientes de andrógenos tienen una expresión de AR elevada y expresan antígeno prostático específico tras el tratamiento con andrógenos. Paradójicamente, los andrógenos inhiben la proliferación de estos cánceres de próstata independientes de los andrógenos.células. [236] [237] [238]
Diagnóstico [ editar ]
Un área de investigación activa y las investigaciones no aplicadas clínicamente son los métodos no invasivos de detección de tumores. Se está investigando una prueba molecular que detecta la presencia de ARNm de PCA3 asociado a células en el líquido obtenido de la próstata y la muestra de orina del primer vaciado. El ARNm de PCA3 se expresa casi exclusivamente en las células de próstata y se ha demostrado que se sobreexpresa en gran medida en las células de cáncer de próstata. El resultado de la prueba se informa actualmente como una proporción de muestras de ARNm de PCA3 a ARNm de PSA.
La prueba de PCA3 intenta ayudar a decidir si, en hombres con sospecha de cáncer de próstata (especialmente si una biopsia inicial no explica el PSA sérico elevado), es necesaria una biopsia / rebiopsia. Cuanto mayor sea la expresión de PCA3 en la muestra, mayor será la probabilidad de una biopsia positiva. [239] El Grupo de Trabajo de Evaluación de Aplicaciones Genómicas en la Práctica y la Prevención de los CDC desalienta el uso clínico. [240]
Ver también [ editar ]
- Fundación de cáncer de próstata
- Cancer testicular
Referencias [ editar ]
- ^ a b c d e f g h "Tratamiento del cáncer de próstata (PDQ) - Versión para profesionales de salud" . Instituto Nacional del Cáncer. 2014-04-11. Archivado desde el original el 5 de julio de 2014 . Consultado el 1 de julio de 2014 .
- ^ a b c d e f g h i j k "Tratamiento del cáncer de próstata (PDQ) - Versión para pacientes" . Instituto Nacional del Cáncer. 2014-04-08. Archivado desde el original el 5 de julio de 2014 . Consultado el 1 de julio de 2014 .
- ^ a b c d e f g h i j k l m "Capítulo 5.11". Informe mundial sobre el cáncer . Organización Mundial de la Salud. 2014. ISBN 978-9283204299.
- ^ a b "Hojas de datos de estadísticas de SEER: cáncer de próstata" . NCI . Archivado desde el original el 6 de julio de 2014 . Consultado el 18 de junio de 2014 .
- ^ a b c Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A (noviembre de 2018). "Estadísticas mundiales de cáncer 2018: estimaciones de GLOBOCAN de incidencia y mortalidad en todo el mundo para 36 cánceres en 185 países" . CA: Una revista sobre el cáncer para médicos . 68 (6): 394–424. doi : 10.3322 / caac.21492 . PMID 30207593 . S2CID 52188256 .
- ^ "Cáncer de próstata" . Instituto Nacional del Cáncer . Enero de 1980. Archivado desde el original el 12 de octubre de 2014 . Consultado el 12 de octubre de 2014 .
- ^ Ruddon RW (2007). Biología del cáncer (4ª ed.). Oxford: Prensa de la Universidad de Oxford. pag. 223. ISBN 978-0195175431. Archivado desde el original el 15 de septiembre de 2015.
- ^ Koh KA, Sesso HD, Paffenbarger RS, Lee IM (diciembre de 2006). "Productos lácteos, calcio y riesgo de cáncer de próstata" . Revista británica de cáncer . 95 (11): 1582–5. doi : 10.1038 / sj.bjc.6603475 . PMC 2360740 . PMID 17106437 .
- ↑ a b Caini S, Gandini S, Dudas M, Bremer V, Severi E, Gherasim A (agosto de 2014). "Infecciones de transmisión sexual y riesgo de cáncer de próstata: una revisión sistemática y un metanálisis". Epidemiología del cáncer . 38 (4): 329–38. doi : 10.1016 / j.canep.2014.06.002 . PMID 24986642 .
- ^ Lee MV, Katabathina VS, Bowerson ML, Mityul MI, Shetty AS, Elsayes KM, et al. (2016). "Cánceres asociados a BRCA: papel de la imagen en el cribado, diagnóstico y tratamiento" . Radiografía . 37 (4): 1005–1023. doi : 10.1148 / rg.2017160144 . PMID 28548905 .
- ^ "Tratamiento del cáncer de próstata" . Instituto Nacional del Cáncer . 6 de febrero de 2018 . Consultado el 1 de marzo de 2018 .
Existe controversia con respecto al valor de las pruebas de detección ... no se informaron pruebas claras de que las pruebas de detección del cáncer de próstata reduzcan el riesgo de muerte por cáncer de próstata
- ^ a b Catalona WJ (marzo de 2018). "Detección de cáncer de próstata" . Las Clínicas Médicas de América del Norte . 102 (2): 199–214. doi : 10.1016 / j.mcna.2017.11.001 . PMC 5935113 . PMID 29406053 .
- ^ a b "Prueba de PSA" . nhs.uk . 3 de enero de 2015 . Consultado el 5 de marzo de 2018 .
- ^ a b "Declaración de recomendación final: cáncer de próstata: detección" . www.uspreventiveservicestaskforce.org . Grupo de Trabajo de Servicios Preventivos de EE. UU. (USPSTF) . Consultado el 30 de agosto de 2018 .
- ^ Grossman DC, Curry SJ, Owens DK, Bibbins-Domingo K, Caughey AB, Davidson KW, et al. (Mayo de 2018). "Detección de cáncer de próstata: declaración de recomendación del grupo de trabajo de servicios preventivos de Estados Unidos" . JAMA . 319 (18): 1901-1913. doi : 10.1001 / jama.2018.3710 . PMID 29801017 .
- ^ Cabarkapa S, Perera M, McGrath S, Lawrentschuk N (diciembre de 2016). "Detección de cáncer de próstata con antígeno prostático específico: una guía de las directrices" . Prostate International . 4 (4): 125-129. doi : 10.1016 / j.prnil.2016.09.002 . PMC 5153437 . PMID 27995110 .
- ↑ a b Stratton J, Godwin M (junio de 2011). "El efecto de los suplementos de vitaminas y minerales en el desarrollo del cáncer de próstata: una revisión sistemática y un metanálisis" . Práctica familiar . 28 (3): 243–52. doi : 10.1093 / fampra / cmq115 . PMID 21273283 .
- ↑ a b c Luszczak S, Kumar C, Sathyadevan VK, Simpson BS, Gately KA, Whitaker HC, Heavey S (2020). "Inhibición de la quinasa PIM: enfoques terapéuticos co-dirigidos en el cáncer de próstata" . Transducción de señales y terapia dirigida . 5 (1): 7. doi : 10.1038 / s41392-020-0109-y . PMC 6992635 . PMID 32296034 .
- ^ "Capítulo 1.1". Informe mundial sobre el cáncer . Organización Mundial de la Salud. 2014. ISBN 978-9283204299.
- ^ a b Baade PD, Youlden DR, Krnjacki LJ (febrero de 2009). "Epidemiología internacional del cáncer de próstata: distribución geográfica y tendencias seculares". Nutrición molecular e investigación alimentaria . 53 (2): 171–84. doi : 10.1002 / mnfr.200700511 . PMID 19101947 .
- ^ Leslie SW, Soon-Sutton TL, Sajjad H, Siref LE. Cancer de prostata. 2020 28 de octubre. En: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; PMID 29261872 .
- ^ a b Miller DC, Hafez KS, Stewart A, Montie JE, Wei JT (septiembre de 2003). "Presentación, diagnóstico y estadificación del carcinoma de próstata: una actualización de la base de datos nacional del cáncer" (PDF) . Cáncer . 98 (6): 1169–78. doi : 10.1002 / cncr.11635 . hdl : 2027,42 / 34379 . PMID 12973840 . S2CID 22077473 .
- ^ van der Cruijsen-Koeter IW, Vis AN, Roobol MJ, Wildhagen MF, de Koning HJ, van der Kwast TH, Schröder FH (julio de 2005). "Comparación de cáncer de próstata detectado y clínicamente diagnosticado en el estudio aleatorizado europeo de detección del cáncer de próstata, sección rotterdam". La Revista de Urología . 174 (1): 121–5. doi : 10.1097 / 01.ju.0000162061.40533.0f . PMID 15947595 .
- ↑ a b Calle EE, Rodríguez C, Walker-Thurmond K, Thun MJ (abril de 2003). "Sobrepeso, obesidad y mortalidad por cáncer en una cohorte estudiada prospectivamente de adultos estadounidenses" . La Revista de Medicina de Nueva Inglaterra . 348 (17): 1625–38. doi : 10.1056 / NEJMoa021423 . PMID 12711737 . S2CID 22714795 .
- ^ Hankey BF, Feuer EJ, Clegg LX, Hayes RB, Legler JM, Prorok PC, et al. (Junio de 1999). "Serie de vigilancia del cáncer: interpretación de las tendencias en el cáncer de próstata - parte I: evidencia de los efectos del cribado en las tasas recientes de incidencia, mortalidad y supervivencia del cáncer de próstata" . Revista del Instituto Nacional del Cáncer . 91 (12): 1017–24. doi : 10.1093 / jnci / 91.12.1017 . PMID 10379964 .
- ^ Breslow N, Chan CW, Dhom G, Drury RA, Franks LM, Gellei B, et al. (Noviembre de 1977). "Carcinoma latente de próstata en la autopsia en siete áreas. La Agencia Internacional para la Investigación del Cáncer, Lyon, Francia". Revista Internacional de Cáncer . 20 (5): 680–8. doi : 10.1002 / ijc.2910200506 . PMID 924691 . S2CID 42501757 .
- ^ Bell KJ, Del Mar C, Wright G, Dickinson J, Glasziou P (octubre de 2015). "Prevalencia de cáncer de próstata incidental: una revisión sistemática de estudios de autopsias" . Revista Internacional de Cáncer . 137 (7): 1749–57. doi : 10.1002 / ijc.29538 . PMC 4682465 . PMID 25821151 .
- ^ Jahn JL, Giovannucci EL, Stampfer MJ (diciembre de 2015). "La alta prevalencia de cáncer de próstata no diagnosticado en la autopsia: implicaciones para la epidemiología y el tratamiento del cáncer de próstata en la era del antígeno prostático específico" . Revista Internacional de Cáncer . 137 (12): 2795–802. doi : 10.1002 / ijc.29408 . PMC 4485977 . PMID 25557753 .
- ^ Martin RM, Vatten L, Gunnell D, Romundstad P (marzo de 2010). "Presión arterial y riesgo de cáncer de próstata: cohorte Noruega (CONOR)". Causas y control del cáncer . 21 (3): 463–72. doi : 10.1007 / s10552-009-9477-x . PMID 19949849 . S2CID 30484327 .
- ^ Friedenreich CM, Neilson HK, Lynch BM (septiembre de 2010). "Estado de la evidencia epidemiológica sobre actividad física y prevención del cáncer". Revista europea del cáncer . 46 (14): 2593–604. doi : 10.1016 / j.ejca.2010.07.028 . PMID 20843488 .
- ^ Gann PH, Hennekens CH, Ma J, Longcope C, Stampfer MJ (agosto de 1996). "Estudio prospectivo de niveles de hormonas sexuales y riesgo de cáncer de próstata" . Revista del Instituto Nacional del Cáncer . 88 (16): 1118–26. doi : 10.1093 / jnci / 88.16.1118 . PMID 8757191 .
- ^ "Cáncer de próstata" . Referencia casera de la genética . Consultado el 1 de mayo de 2020 .
- ^ Steinberg GD, Carter BS, Beaty TH, Childs B, Walsh PC (1990). "Antecedentes familiares y riesgo de cáncer de próstata". La próstata . 17 (4): 337–47. doi : 10.1002 / pros.2990170409 . PMID 2251225 . S2CID 44925478 .
- ^ Zeegers MP, Jellema A, Ostrer H (abril de 2003). "Riesgo empírico de carcinoma de próstata para familiares de pacientes con carcinoma de próstata: un metanálisis" . Cáncer . 97 (8): 1894–903. doi : 10.1002 / cncr.11262 . PMID 12673715 . S2CID 12607885 .
- ↑ a b Gallagher RP, Fleshner N (octubre de 1998). "Cáncer de próstata: 3. factores de riesgo individuales" (PDF) . CMAJ . 159 (7): 807-13. PMC 1232741 . PMID 9805030 . Archivado (PDF) desde el original el 29 de diciembre de 2009.
- ^ Hoffman RM, Gilliland FD, Eley JW, Harlan LC, Stephenson RA, Stanford JL, et al. (Marzo de 2001). "Diferencias raciales y étnicas en el cáncer de próstata en estadio avanzado: el estudio de resultados del cáncer de próstata" . Revista del Instituto Nacional del Cáncer . 93 (5): 388–95. doi : 10.1093 / jnci / 93.5.388 . PMID 11238701 .
- ^ Lichtenstein P, Holm NV, Verkasalo PK, Iliadou A, Kaprio J, Koskenvuo M, et al. (Julio de 2000). "Factores ambientales y hereditarios en la causa del cáncer: análisis de cohortes de gemelos de Suecia, Dinamarca y Finlandia". La Revista de Medicina de Nueva Inglaterra . 343 (2): 78–85. doi : 10.1056 / NEJM200007133430201 . PMID 10891514 .
- ^ Struewing JP, Hartge P, Wacholder S, Baker SM, Berlín M, McAdams M, et al. (Mayo de 1997). "El riesgo de cáncer asociado con mutaciones específicas de BRCA1 y BRCA2 entre judíos Ashkenazi". La Revista de Medicina de Nueva Inglaterra . 336 (20): 1401–8. doi : 10.1056 / NEJM199705153362001 . PMID 9145676 .
- ^ Beuzeboc P, Soulié M, Richaud P, Salomon L, Staerman F, Peyromaure M, et al. (Diciembre de 2009). "[Fusión de genes y cáncer de próstata. Del descubrimiento al pronóstico y perspectivas terapéuticas]". Progres en Urologie (en francés). 19 (11): 819–24. doi : 10.1016 / j.purol.2009.06.002 . PMID 19945666 .
- ^ Baca SC, Prandi D, Lawrence MS, Mosquera JM, Romanel A, Drier Y, et al. (Abril 2013). "Evolución puntuada de los genomas del cáncer de próstata" . Celular . 153 (3): 666–77. doi : 10.1016 / j.cell.2013.03.021 . PMC 3690918 . PMID 23622249 .
- ^ Eeles RA, Kote-Jarai Z, Giles GG, Olama AA, Guy M, Jugurnauth SK, et al. (Marzo de 2008). "Varios loci recientemente identificados asociados con la susceptibilidad al cáncer de próstata". Genética de la naturaleza . 40 (3): 316-21. doi : 10.1038 / ng.90 . PMID 18264097 . S2CID 30968525 .
- ^ Thomas G, Jacobs KB, Yeager M, Kraft P, Wacholder S, Orr N, et al. (Marzo de 2008). "Múltiples loci identificados en un estudio de asociación de todo el genoma del cáncer de próstata" . Genética de la naturaleza . 40 (3): 310–5. doi : 10.1038 / ng.91 . PMID 18264096 . S2CID 22978381 .
- ^ Whitaker HC, Kote-Jarai Z, Ross-Adams H, Warren AY, Burge J, George A, et al. (Octubre de 2010). Vickers A (ed.). "El alelo de riesgo rs10993994 para el cáncer de próstata da como resultado cambios clínicamente relevantes en la expresión de microseminoproteína beta en tejido y orina" . PLOS ONE . 5 (10): e13363. Código Bibliográfico : 2010PLoSO ... 513363W . doi : 10.1371 / journal.pone.0013363 . PMC 2954177 . PMID 20967219 .
- ^ Berndt SI, Wang Z, Yeager M, Alavanja MC, Albanes D, Amundadottir L, et al. (Mayo de 2015). "Dos loci de susceptibilidad identificados para la agresividad del cáncer de próstata" . Comunicaciones de la naturaleza . 6 : 6889. Bibcode : 2015NatCo ... 6.6889. . doi : 10.1038 / ncomms7889 . PMC 4422072 . PMID 25939597 .
- ^ Venkateswaran V, Klotz LH (agosto de 2010). "Dieta y cáncer de próstata: mecanismos de acción e implicaciones para la quimioprevención". Reseñas de la naturaleza. Urología . 7 (8): 442–53. doi : 10.1038 / nrurol.2010.102 . PMID 20647991 . S2CID 10602814 .
- ^ "Productos químicos en la carne cocida a altas temperaturas y riesgo de cáncer" . Instituto Nacional del Cáncer . 2018-04-02. Archivado desde el original el 6 de noviembre de 2011.
- ^ "Leche y salud" . Colegio Americano de Cardiología . Consultado el 21 de febrero de 2021 .
- ^ Willett WC, Ludwig DS (febrero de 2020). "Leche y Salud" . La Revista de Medicina de Nueva Inglaterra . 382 (7): 644–654. doi : 10.1056 / NEJMra1903547 . PMID 32053300 .
- ^ Sargsyan A, Dubasi HB (julio de 2020). "Consumo de leche y cáncer de próstata: una revisión sistemática" . The World Journal of Men's Health . 38 . doi : 10.5534 / wjmh.200051 . PMID 32777868 .
- ^ López-Plaza B, Bermejo LM, Santurino C, Cavero-Redondo I, Álvarez-Bueno C, Gómez-Candela C (mayo de 2019). "Consumo de leche y productos lácteos y riesgo y mortalidad del cáncer de próstata: una descripción general de revisiones sistemáticas y metanálisis" . Adv Nutr . 10 (supl_2): S212 – S223. doi : 10.1093 / avances / nmz014 . PMC 6518142 . PMID 31089741 .
- ^ Wigle DT, Turner MC, Gomes J, Parent ME (marzo de 2008). "Papel de factores hormonales y otros en el cáncer de próstata humano" . Revista de Toxicología y Salud Ambiental Parte B: Revisiones críticas . 11 (3–4): 242–59. doi : 10.1080 / 10937400701873548 . PMID 18368555 . S2CID 24489849 .
- ^ Qin X, Cui Y, Shen L, Sun N, Zhang Y, Li J, et al. (Septiembre 2013). "Suplementación con ácido fólico y riesgo de cáncer: un metanálisis de ensayos controlados aleatorios". Revista Internacional de Cáncer . 133 (5): 1033–41. doi : 10.1002 / ijc.28038 . PMID 23338728 . S2CID 19830376 .
- ^ Jacobs EJ, Rodríguez C, Mondul AM, Connell CJ, Henley SJ, Calle EE, Thun MJ (julio de 2005). "Un gran estudio de cohorte de aspirina y otros fármacos antiinflamatorios no esteroides y la incidencia del cáncer de próstata" . Revista del Instituto Nacional del Cáncer . 97 (13): 975–80. doi : 10.1093 / jnci / dji173 . PMID 15998950 .
- ^ Shannon J, Tewoderos S, Garzotto M, Beer TM, Derenick R, Palma A, Farris PE (agosto de 2005). "Riesgo de cáncer de próstata y estatinas: un estudio de casos y controles" . Revista Estadounidense de Epidemiología . 162 (4): 318-25. doi : 10.1093 / aje / kwi203 . PMID 16014776 .
- ^ Dennis LK, Lynch CF, Torner JC (julio de 2002). "Asociación epidemiológica entre prostatitis y cáncer de próstata". Urología . 60 (1): 78–83. doi : 10.1016 / S0090-4295 (02) 01637-0 . PMID 12100928 .
- ^ Heidegger I, Borena W, Pichler R (mayo de 2015). "El papel del virus del papiloma humano en neoplasias urológicas". Investigación contra el cáncer . 35 (5): 2513–9. PMID 25964524 .
- ^ Cai T, Di Vico T, Durante J, Tognarelli A, Bartoletti R (diciembre de 2018). "Virus del papiloma humano y cánceres genitourinarios: una revisión narrativa". Minerva Urologica e Nefrologica . 70 (6): 579–587. doi : 10.23736 / S0393-2249.18.03141-7 . PMID 30160386 .
- ^ Rider JR, Wilson KM, Sinnott JA, Kelly RS, Mucci LA, Giovannucci EL (diciembre de 2016). "Frecuencia de eyaculación y riesgo de cáncer de próstata: resultados actualizados con una década adicional de seguimiento" . Urología europea . 70 (6): 974–982. doi : 10.1016 / j.eururo.2016.03.027 . PMC 5040619 . PMID 27033442 .
- ^ Aboul-Enein BH, Bernstein J, Ross MW (julio de 2016). "Evidencia de la masturbación y el riesgo de cáncer de próstata: ¿tenemos un veredicto?". Reseñas de medicina sexual . 4 (3): 229–234. doi : 10.1016 / j.sxmr.2016.02.006 . PMID 27871956 .
- ^ "Un programa integral de control del cáncer para BC" . Archivado desde el original el 27 de septiembre de 2006 . Consultado el 9 de agosto de 2010 .
- ^ Aumüller G (1979). Glándula prostática y vesículas seminales . Berlín-Heidelberg: Springer-Verlag.
- ^ Moore KL, Chubb D (1999). Anatomía de orientación clínica . Baltimore, Maryland: Lippincott Williams y Wilkins. ISBN 978-0-683-06132-1.
- ^ Steive H (1930). "Männliche Genitalorgane".Handbuch der mikroskopischen Anatomie des Menschen. Vol. VII Parte 2 . Berlín: Springer. págs. 1-399.
- ^ McNeal JE (1984). "Anatomía de la próstata y morfogénesis de la HPB". Avances en la investigación clínica y biológica . 145 : 27–53. PMID 6201879 .
- ^ Oh WK, Hurwitz M, D'Amico AV, Richie JP, Kantoff PW (2003). "Biología del cáncer de próstata" . Medicina del cáncer de Holland-Frei (6ª ed.).
- ^ Reissigl A, Pointner J, Strasser H, Ennemoser O, Klocker H, Bartsch G (febrero de 1997). "Frecuencia y significado clínico del cáncer de zona de transición en el cribado del cáncer de próstata". La próstata . 30 (2): 130–5. doi : 10.1002 / (SICI) 1097-0045 (19970201) 30: 2 <130 :: AID-PROS8> 3.0.CO; 2-S . PMID 9051151 .
- ^ "Genitales masculinos - neoplasias de próstata" . Imágenes del estudio de patología . Facultad de Medicina de la Universidad de Virginia. Archivado desde el original el 20 de julio de 2011 . Consultado el 28 de abril de 2011 .
Existen muchas conexiones entre el plexo venoso prostático y las venas vertebrales. Las venas que forman el plexo prostático no contienen válvulas y se cree que esforzarse para orinar hace que la sangre venosa prostática fluya en dirección inversa y entre en las venas vertebrales que transportan células malignas a la columna vertebral.
- ^ Costello LC, Franklin RB (mayo de 2006). "La relevancia clínica del metabolismo del cáncer de próstata; zinc y supresión de tumores: conectando los puntos" . Cáncer molecular . 5 : 17. doi : 10.1186 / 1476-4598-5-17 . PMC 1481516 . PMID 16700911 .
- ^ "Los científicos descubren el mecanismo contra el cáncer que detiene el cáncer de próstata temprano" . 4 de agosto de 2005. Archivado desde el original el 19 de mayo de 2008.
- ^ Sharma A, Yeow WS, Ertel A, Coleman I, Clegg N, Thangavel C, et al. (Diciembre de 2010). "El supresor de tumores de retinoblastoma controla la señalización de andrógenos y la progresión del cáncer de próstata humano" . La Revista de Investigación Clínica . 120 (12): 4478–92. doi : 10.1172 / JCI44239 . PMC 2993601 . PMID 21099110 .
- ^ Leav I, Plescia J, Goel HL, Li J, Jiang Z, Cohen RJ, et al. (Enero de 2010). "Chaperona mitocondrial citoprotectora TRAP-1 como una nueva diana molecular en cáncer de próstata localizado y metastásico" . La Revista Estadounidense de Patología . 176 (1): 393–401. doi : 10.2353 / ajpath.2010.090521 . PMC 2797899 . PMID 19948822 .
- ^ Zha J, Huang YF (septiembre de 2009). "[TGF-beta / Smad en cáncer de próstata: una actualización]". Zhonghua Nan Ke Xue = Revista Nacional de Andrología (en chino). 15 (9): 840–3. PMID 19947572 .
- ^ Watanabe S, Miyata Y, Kanda S, Iwata T, Hayashi T, Kanetake H, Sakai H (mayo de 2010). "Expresión de inhibidor de la proteína de apoptosis ligado al cromosoma X en muestras de cáncer de próstata humano con y sin terapia hormonal neoadyuvante". Revista de investigación del cáncer y oncología clínica . 136 (5): 787–93. doi : 10.1007 / s00432-009-0718-x . PMID 19946707 . S2CID 34855148 .
- ^ Senapati S, Rachagani S, Chaudhary K, Johansson SL, Singh RK, Batra SK (marzo de 2010). "La sobreexpresión de citoquina-1 inhibidora de macrófagos induce metástasis de células de cáncer de próstata humano a través de la vía de señalización FAK-RhoA" . Oncogén . 29 (9): 1293–302. doi : 10.1038 / onc.2009.420 . PMC 2896817 . PMID 19946339 .
- ^ Narizhneva NV, Tararova ND, Ryabokon P, Shyshynova I, Prokvolit A, Komarov PG, et al. (Diciembre de 2009). "La detección de moléculas pequeñas revela una función de pro-supervivencia independiente de la transcripción del receptor de andrógenos en el cáncer de próstata resistente a la castración" . Ciclo celular . 8 (24): 4155–67. doi : 10.4161 / cc.8.24.10316 . PMC 2896895 . PMID 19946220 .
- ^ Yao V, Berkman CE, Choi JK, O'Keefe DS, Bacich DJ (febrero de 2010). "La expresión del antígeno de membrana específico de la próstata (PSMA) aumenta la captación y proliferación de folato celular y sugiere un papel novedoso para el PSMA en la captación del ácido fólico no poliglutamato, ácido fólico". La próstata . 70 (3): 305–16. doi : 10.1002 / pros.21065 . PMID 19830782 . S2CID 21518526 .
- ^ "Pautas para la detección del cáncer | Detección temprana del cáncer" . Archivado desde el original el 13 de junio de 2011 . Consultado el 16 de junio de 2011 . Sociedad Estadounidense del Cáncer Directrices de la Sociedad Estadounidense del Cáncer para la detección temprana del cáncer.
- ↑ Georgiev, A. (2016). Caso de cáncer de próstata con localización anterior - Estudio de resonancia magnética multiparamétrica. Rentgenologiya i Radiologiya, 55 (4), 285–87.
- ^ a b c d e f Drost FH, Osses DF, Nieboer D, Steyerberg EW, Bangma CH, Roobol MJ, Schoots IG, et al. (Grupo Cochrane de Urología) (abril de 2019). "Resonancia magnética de próstata, con o sin biopsia dirigida a resonancia magnética y biopsia sistemática para detectar cáncer de próstata" . La base de datos Cochrane de revisiones sistemáticas . 4 : CD012663. doi : 10.1002 / 14651858.CD012663.pub2 . PMC 6483565 . PMID 31022301 .
- ^ Wang X, Bao J, Ping X, Hu C, Hou J, Dong F, Guo L (septiembre de 2018). "El valor diagnóstico de PI-RADS V1 y V2 mediante resonancia magnética multiparamétrica en cáncer clínico de próstata en zona de transición" . Cartas de Oncología . 16 (3): 3201–3206. doi : 10.3892 / ol.2018.9038 . PMC 6096261 . PMID 30127915 .
- ^ Tan N, Margolis DJ, McClure TD, Thomas A, Finley DS, Reiter RE, et al. (Agosto 2012). "Prostatectomía radical: valor de la resonancia magnética de próstata en la planificación quirúrgica". Imagen abdominal . 37 (4): 664–74. doi : 10.1007 / s00261-011-9805-y . PMID 21993567 . S2CID 20471235 .
- ^ Scheltema MJ, Tay KJ, Postema AW, de Bruin DM, Feller J, Futterer JJ, et al. (Mayo de 2017). "Utilización de la resonancia magnética de próstata multiparamétrica en la práctica clínica y terapia focal: informe de un proyecto de consenso Delphi" . Revista mundial de urología . 35 (5): 695–701. doi : 10.1007 / s00345-016-1932-1 . OCLC 1188365278 . PMC 5397427 . PMID 27637908 .
- ^ Wang T, Zhou J, Tian S, Wang Y, Patel P, Jani AB, et al. (Marzo de 2020). "Un estudio de planificación de escaladas de dosis focales a lesiones intraprostáticas dominantes definidas por resonancia magnética multiparamétrica en la radioterapia de protones de próstata" . La Revista Británica de Radiología . 93 (1107): 20190845. doi : 10.1259 / bjr.20190845 . PMC 7066949 . PMID 31904261 .
- ^ Heavey S, Haider A, Sridhar A, Pye H, Shaw G, Freeman A, Whitaker H (octubre de 2019). "Uso de imágenes de resonancia magnética y datos de biopsia para guiar los procedimientos de muestreo para biobancos de cáncer de próstata" . Revista de experimentos visualizados (152). doi : 10.3791 / 60216 . PMID 31657791 .
- ^ Heavey S, Costa H, Pye H, Burt EC, Jenkinson S, Lewis GR, et al. (Mayo de 2019). "PERSONAS: MUESTRAS DE PRESTATOS PACIENTES PARA INVESTIGACIÓN, UNA VÍA DE RECOGIDA DE TEJIDOS QUE UTILIZA DATOS DE IMAGEN DE RESONANCIA MAGNÉTICA PARA OBTENER EL TUMOR Y EL TEJIDO BENIGNO EN MUESTRAS DE Prostatectomía radical fresca" . La próstata . 79 (7): 768–777. doi : 10.1002 / pros.23782 . PMC 6618051 . PMID 30807665 .
- ^ a b c Norris JM, Simpson BS, Freeman A, Kirkham A, Whitaker HC, Emberton M (noviembre de 2020). "Visibilidad del cáncer de próstata en la resonancia magnética multiparamétrica: una hipótesis traslacional interdisciplinaria" . Revista FASEB . 34 (11): 14150-14159. doi : 10.1096 / fj.202001466R . PMID 32920937 . S2CID 221675029 .
- ^ Truong M, Hollenberg G, Weinberg E, Messing EM, Miyamoto H, Frye TP (agosto de 2017). "Impacto del subtipo de Gleason en la detección del cáncer de próstata mediante resonancia magnética multiparamétrica: correlación con histopatología final". La Revista de Urología . 198 (2): 316–321. doi : 10.1016 / j.juro.2017.01.077 . PMID 28163032 . S2CID 45430609 .
- ^ Norris JM, Carmona Echeverria LM, Simpson BS, Allen C, Ball R, Freeman A, et al. (Agosto de 2020). "Visibilidad del cáncer de próstata en la resonancia magnética multiparamétrica: alto grado de Gleason y mayor volumen tumoral no son las únicas características histopatológicas importantes" . BJU International . 126 (2): 237–239. doi : 10.1111 / bju.15085 . PMID 32319152 .
- ^ a b Norris JM, Simpson BS, Parry MA, Allen C, Ball R, Freeman A, et al. (Julio de 2020). "Paisaje genético de la visibilidad del cáncer de próstata en la resonancia magnética multiparamétrica: una revisión sistemática y análisis bioinformático" . Ciencia Abierta Europea de Urología . 20 : 37–47. doi : 10.1016 / j.euros.2020.06.006 . PMC 7497895 . PMID 33000006 .
- ^ Yaghi MD, Kehinde EO (2015). "Antibióticos orales en biopsia de próstata transrectal y su eficacia para reducir las complicaciones infecciosas: revisión sistemática" . Anales de Urología . 7 (4): 417–27. doi : 10.4103 / 0974-7796.164860 . PMC 4660689 . PMID 26538868 .
- ^ Zani EL, Clark OA, Rodrigues Netto N (mayo de 2011). "Profilaxis antibiótica para biopsia de próstata transrectal". La base de datos Cochrane de revisiones sistemáticas (5): CD006576. doi : 10.1002 / 14651858.CD006576.pub2 . PMID 21563156 .
- ^ Essink-Bot ML, de Koning HJ, Nijs HG, Kirkels WJ, van der Maas PJ, Schröder FH (junio de 1998). "Efectos a corto plazo del cribado poblacional del cáncer de próstata en la calidad de vida relacionada con la salud" . Revista del Instituto Nacional del Cáncer . 90 (12): 925–31. doi : 10.1093 / jnci / 90.12.925 . PMID 9637143 .
- ^ Las referencias para el gráfico circular se encuentran en la tabla del artículo Diagnóstico histopatológico de cáncer de próstata : las incidencias generalmente incluyen casos en los que el patrón se encuentra mezclado con el adenocarcinoma acinar habitual.
- ^ Li J, Wang Z (febrero de 2016). "La patología de subtipos inusuales de cáncer de próstata" . Revista china de investigación del cáncer = Chung-Kuo Yen Cheng Yen Chiu . 28 (1): 130–43. doi : 10.3978 / j.issn.1000-9604.2016.01.06 . PMC 4779761 . PMID 27041935 .
- ^ Baig FA, Hamid A, Mirza T, Syed S (mayo de 2015). "Adenocarcinoma ductal y acinar de próstata: caracterización morfológica e inmunohistoquímica" . Revista médica de Omán . 30 (3): 162–6. doi : 10.5001 / omj.2015.36 . PMC 4459157 . PMID 26171121 .
- ^ "Adenocarcinoma de próstata" . Facultad de Medicina de la Universidad de Stanford . Consultado el 30 de octubre de 2019 .
- ^ a b Rao SR, Snaith AE, Marino D, Cheng X, Lwin ST, Orriss IR, et al. (Enero de 2017). "La fosfatasa alcalina derivada de tumores regula el crecimiento tumoral, la plasticidad epitelial y la supervivencia libre de enfermedad en el cáncer de próstata metastásico" . Revista británica de cáncer . 116 (2): 227–236. doi : 10.1038 / bjc.2016.402 . PMC 5243990 . PMID 28006818 .
- ^ "Patología genital masculina" . Consultado el 13 de mayo de 2009 .
- ^ Chuang AY, DeMarzo AM, Veltri RW, Sharma RB, Bieberich CJ, Epstein JI (agosto de 2007). "Diferenciación inmunohistoquímica del carcinoma de próstata de alto grado del carcinoma urotelial". La Revista Estadounidense de Patología Quirúrgica . 31 (8): 1246–55. doi : 10.1097 / PAS.0b013e31802f5d33 . PMID 17667550 . S2CID 11535862 .
- ↑ a b Nutting C, Horwich A, Fisher C, Parsons C, Dearnaley DP (junio de 1997). "Carcinoma microcítico de próstata" . Revista de la Real Sociedad de Medicina . 90 (6): 340–1. doi : 10.1177 / 014107689709000615 . PMC 1296316 . PMID 9227387 .
- ^ a b Wei ZF, Xu H, Wang H, Wei W, Cheng W, Zhou WQ, et al. (Septiembre de 2009). "[Caracterización clínico-patológica del carcinoma prostático de células pequeñas: reporte de un caso y revisión de la literatura]". Zhonghua Nan Ke Xue = Revista Nacional de Andrología (en chino). 15 (9): 829–32. PMID 19947569 .
- ^ Catz SD, Johnson JL (enero de 2003). "BCL-2 en cáncer de próstata: un minireview". Apoptosis . 8 (1): 29–37. doi : 10.1023 / A: 1021692801278 . PMID 12510149 . S2CID 21948907 .
- ^ BMJ Group (8 de diciembre de 2009). "Cáncer de próstata: ¿Hasta dónde se ha extendido su cáncer? El sistema TNM" . Guardian.co.uk . Londres. Archivado desde el original el 4 de abril de 2009 . Consultado el 9 de agosto de 2010 .
- ^ Sociedad Estadounidense de Oncología Clínica (abril de 2013). "Cinco cosas que los médicos y los pacientes deben cuestionar" (PDF) . Revista de la Asociación Médica del Estado de Oklahoma . 106 (4): 150-1. PMID 23795527 . Archivado desde el original (PDF) el 31 de julio de 2012.
- Makarov DV, Desai RA, Yu JB, Sharma R, Abraham N, Albertsen PC, et al. (Enero de 2012). "La prevalencia del nivel de población y los correlatos de imágenes apropiadas e inapropiadas para estadificar el cáncer de próstata incidente en la población de Medicare". La Revista de Urología . 187 (1): 97–102. doi : 10.1016 / j.juro.2011.09.042 . PMID 22088337 .
- Red Nacional Integral del Cáncer - Próstata (2012). "Pautas de práctica clínica de la NCCN en oncología" . nccn.org . Archivado desde el original el 9 de noviembre de 2012 . Consultado el 15 de noviembre de 2012 .
- Thompson I, Thrasher JB, Aus G, Burnett AL, Canby-Hagino ED, Cookson MS, et al. (Junio de 2007). "Guía para el tratamiento del cáncer de próstata clínicamente localizado: actualización de 2007". La Revista de Urología . 177 (6): 2106–31. doi : 10.1016 / j.juro.2007.03.003 . PMID 17509297 .
- ^ Hofman MS, Lawrentschuk N, Francis RJ, Tang C, Vela I, Thomas P, et al. (Abril de 2020). "PET-CT de antígeno de membrana específico de la próstata en pacientes con cáncer de próstata de alto riesgo antes de la cirugía o radioterapia con intención curativa (proPSMA): un estudio prospectivo, aleatorizado y multicéntrico" (PDF) . Lancet . 395 (10231): 1208–1216. doi : 10.1016 / S0140-6736 (20) 30314-7 . PMID 32209449 . S2CID 214609500 .
- ↑ a b c d e Masko EM, Allott EH, Freedland SJ (mayo de 2013). "La relación entre la nutrición y el cáncer de próstata: ¿más siempre es mejor?" . Urología europea . 63 (5): 810-20. doi : 10.1016 / j.eururo.2012.11.012 . PMC 3597758 . PMID 23219353 .
- ^ Thompson AK, Shaw DI, Minihane AM, Williams CM (diciembre de 2008). "Ácidos grasos trans y cáncer: la evidencia revisada" . Reseñas de investigaciones sobre nutrición . 21 (2): 174–88. doi : 10.1017 / S0954422408110964 . PMID 19087370 .
- ^ Heinze VM, Actis AB (febrero de 2012). "Ácido linoleico conjugado dietético y ácidos grasos n-3 de cadena larga en la protección del cáncer de mama y próstata: una revisión" . Revista Internacional de Ciencias de la Alimentación y Nutrición . 63 (1): 66–78. doi : 10.3109 / 09637486.2011.598849 . PMID 21762028 . S2CID 21614046 .
- ^ Datta M, Schwartz GG (2012). "Suplementación de calcio y vitamina D durante la terapia de privación de andrógenos para el cáncer de próstata: una revisión crítica" . El oncólogo . 17 (9): 1171–9. doi : 10.1634 / theoncologist.2012-0051 . PMC 3448410 . PMID 22836449 .
- ^ Szymanski KM, Wheeler DC, Mucci LA (noviembre de 2010). "El consumo de pescado y el riesgo de cáncer de próstata: una revisión y un metanálisis" . La Revista Estadounidense de Nutrición Clínica . 92 (5): 1223–33. doi : 10.3945 / ajcn.2010.29530 . PMID 20844069 .
- ^ Asociación Dietética Americana (junio de 2003). "Posición de la Asociación Dietética Americana y dietistas de Canadá: dietas vegetarianas" . Revista de la Asociación Dietética Estadounidense . 103 (6): 748–65. doi : 10.1053 / jada.2003.50142 . PMID 12778049 .
- ^ Fondo mundial de investigación del cáncer; Instituto Americano del Cáncer (2007). Alimentación, nutrición, actividad física y prevención del cáncer desde una perspectiva global (PDF) . Washington, DC: Instituto Americano de Investigación del Cáncer. pag. 76. ISBN 978-0-9722522-2-5. Archivado desde el original (PDF) el 23 de mayo de 2013.CS1 maint: varios nombres: lista de autores ( enlace )
- ^ Rowles JL, Ranard KM, Applegate CC, Jeon S, An R, Erdman JW (septiembre de 2018). "Consumo de tomate procesado y crudo y riesgo de cáncer de próstata: una revisión sistemática y metanálisis de dosis-respuesta". Cáncer de próstata y enfermedades prostáticas . 21 (3): 319–336. doi : 10.1038 / s41391-017-0005-x . PMID 29317772 . S2CID 3306182 .
- ^ a b "Directrices de la sociedad americana contra el cáncer sobre nutrición y actividad física para la prevención del cáncer" (PDF) . Sociedad Americana del Cáncer . Archivado (PDF) desde el original el 25 de junio de 2012.
- ^ Wilt TJ, MacDonald R, Hagerty K, Schellhammer P, Kramer BS (abril de 2008). Wilt TJ (ed.). "Inhibidores de la cinco-alfa-reductasa para la prevención del cáncer de próstata". La base de datos Cochrane de revisiones sistemáticas (2): CD007091. doi : 10.1002 / 14651858.CD007091 . PMID 18425978 .
- ^ a b Alberts AR, Schoots IG, Roobol MJ (junio de 2015). "Cribado de cáncer de próstata basado en antígenos específicos de próstata: pasado y futuro" . Revista Internacional de Urología . 22 (6): 524–32. doi : 10.1111 / iju.12750 . PMID 25847604 . S2CID 7525080 .
- ^ a b Rendon RA, Mason RJ, Marzouk K, Finelli A, Saad F, So A, et al. (Octubre de 2017). "Recomendaciones de la Asociación Canadiense de Urología sobre detección y diagnóstico precoz del cáncer de próstata" . Revista de la Asociación Canadiense de Urología = Revista de la Asociación de Urólogos de Canadá . 11 (10): 298-309. doi : 10.5489 / cuaj.4888 . PMC 5659858 . PMID 29381452 .
- ^ "Página de inicio - Proyecto de recomendaciones de detección de próstata de USPSTF" . Recomendaciones preliminares de detección de próstata de la USPSTF . Archivado desde el original el 2 de marzo de 2018 . Consultado el 2 de marzo de 2018 .
- ^ Mulhem E, Fulbright N, Duncan N (octubre de 2015). "Detección de cáncer de próstata". Médico de familia estadounidense . 92 (8): 683–8. PMID 26554408 .
- ^ Prueba de detección de cáncer de próstata Archivado el 7 de septiembre de 2017 en losCDC Wayback Machine , actualizado el 6 de abril de 2010
- ^ Qaseem A, Barry MJ, Denberg TD, Owens DK, Shekelle P (mayo de 2013). "Detección de cáncer de próstata: una declaración de orientación del Comité de Directrices Clínicas del Colegio Americano de Médicos" . Annals of Internal Medicine . 158 (10): 761–769. doi : 10.7326 / 0003-4819-158-10-201305210-00633 . PMID 23567643 . [ enlace muerto permanente ]
- ^ Basch E, Oliver TK, Vickers A, Thompson I, Kantoff P, Parnes H, et al. (Agosto 2012). "Detección de cáncer de próstata con pruebas de antígeno prostático específico: opinión clínica provisional de la Sociedad Americana de Oncología Clínica" . Revista de Oncología Clínica . 30 (24): 3020–5. doi : 10.1200 / JCO.2012.43.3441 . PMC 3776923 . PMID 22802323 .
- ^ "Detección temprana del cáncer de próstata: pautas de la AUA" . Asociación Americana de Urología . 2013. Archivado desde el original el 7 de mayo de 2013 . Consultado el 10 de mayo de 2013 .
- ↑ a b c d Filson CP, Marks LS, Litwin MS (8 de mayo de 2015). "Manejo expectante para hombres con cáncer de próstata en etapa temprana". Ca . 65 (4): 265–82. doi : 10.3322 / caac.21278 . PMID 25958817 . S2CID 36057004 .
- ^ Jayadevappa R, Chhatre S, Wong YN, Wittink MN, Cook R, Morales KH, et al. (Mayo de 2017). "Eficacia comparativa de los tratamientos del cáncer de próstata para los resultados centrados en el paciente: una revisión sistemática y un metanálisis (compatible con PRISMA)" . Medicina . 96 (18): e6790. doi : 10.1097 / MD.0000000000006790 . PMC 5419922 . PMID 28471976 .
- ^ Lu-Yao GL, Albertsen PC, Moore DF, Shih W, Lin Y, DiPaola RS, et al. (Septiembre de 2009). "Resultados del cáncer de próstata localizado después de un tratamiento conservador" . JAMA . 302 (11): 1202–9. doi : 10.1001 / jama.2009.1348 . PMC 2822438 . PMID 19755699 .
- ^ Mongiat-Artus P, Peyromaure M, Richaud P, Droz JP, Rainfray M, Jeandel C, et al. (Diciembre de 2009). "[Recomendaciones para el tratamiento del cáncer de próstata en el anciano: un estudio del comité de oncología de la asociación francesa de urología]". Progres en Urologie (en francés). 19 (11): 810–7. doi : 10.1016 / j.purol.2009.02.008 . PMID 19945664 .
- ^ Picard JC, Golshayan AR, Marshall DT, Opfermann KJ, Keane TE (noviembre de 2009). "El manejo multidisciplinario del cáncer de próstata de alto riesgo". Oncología Urológica . 30 (1): 3–15. doi : 10.1016 / j.urolonc.2009.09.002 . PMID 19945310 .
- ^ Fitzpatrick JM (marzo de 2008). "Manejo del cáncer de próstata localizado en adultos mayores: el papel crucial de la comorbilidad" . BJU International . 101 Suppl 2 (Suppl 2): 16–22. doi : 10.1111 / j.1464-410X.2007.07487.x . PMID 18307688 . S2CID 205538470 .
- ^ "Directrices sobre el cáncer basadas en la evidencia, Compendio de fármacos de oncología, Educación médica continua en oncología" . NCCN . Consultado el 29 de agosto de 2011 .
- ↑ a b Mohan R, Schellhammer PF (agosto de 2011). "Opciones de tratamiento para el cáncer de próstata localizado". Médico de familia estadounidense . 84 (4): 413-20. PMID 21842788 .
- ^ "Vigilancia activa para el tratamiento del cáncer de próstata localizado" . Cancer Care Ontario . Archivado desde el original el 10 de abril de 2020.
- ^ "La vigilancia activa puede ser la opción preferida en algunos hombres con cáncer de próstata" . Cancer.gov. 2011-04-19. Archivado desde el original el 3 de mayo de 2011 . Consultado el 29 de agosto de 2011 .
- ↑ a b c d e Vernooij, Robin Wm; Lancee, Michelle; Cleves, Anne; Dahm, Philipp; Bangma, Chris H .; Aben, Katja Kh (4 de junio de 2020). "Prostatectomía radical versus tratamiento diferido para el cáncer de próstata localizado" . La base de datos Cochrane de revisiones sistemáticas . 6 : CD006590. doi : 10.1002 / 14651858.CD006590.pub3 . ISSN 1469-493X . PMC 7270852. PMID 32495338 .
- ^ Sartor O, de Bono JS (febrero de 2018). "Cáncer de próstata metastásico". La Revista de Medicina de Nueva Inglaterra . 378 (7): 645–657. doi : 10.1056 / NEJMra1701695 . PMID 29412780 .
- ^ Dhondt B, De Bleser E, Claeys T, Buelens S, Lumen N, Vandesompele J, et al. (Diciembre de 2019). "Descubrimiento y validación de una firma de microARN en suero para caracterizar el cáncer de próstata oligo y polimetastásico: no está listo para el horario de máxima audiencia". Revista mundial de urología . 37 (12): 2557-2564. doi : 10.1007 / s00345-018-2609-8 . PMID 30578441 . S2CID 58594673 .
- ^ Hammerstrom AE, Cauley DH, Atkinson BJ, Sharma P (agosto de 2011). "Inmunoterapia contra el cáncer: sipuleucel-T y más allá" . Farmacoterapia . 31 (8): 813-28. doi : 10.1592 / phco.31.8.813 . PMC 4159742 . PMID 21923608 .
- ^ "Cáncer de próstata: prostatectomía radical" . WebMD . Consultado el 10 de mayo de 2020 .
- ^ Mouraviev V, Evans B, Polascik TJ (2006). "Crioablación de próstata de rescate después del fracaso de la braquiterapia intersticial primaria: un enfoque factible" . Cáncer de próstata y enfermedades prostáticas . 9 (1): 99–101. doi : 10.1038 / sj.pcan.4500853 . PMID 16314889 .
- ^ Wallis CJ, Mahar AL, Choo R, Herschorn S, Kodama RT, Shah PS, et al. (Marzo de 2016). "Segundas neoplasias después de la radioterapia para el cáncer de próstata: revisión sistemática y metanálisis" . BMJ . 352 : i851. doi : 10.1136 / bmj.i851 . PMC 4775870 . PMID 26936410 .
- ^ Wallis CJ, Glaser A, Hu JC, Huland H, Lawrentschuk N, Moon D, et al. (Enero de 2018). "Supervivencia y complicaciones después de la cirugía y la radiación para el cáncer de próstata localizado: una revisión colaborativa internacional" (PDF) . Urología europea . 73 (1): 11-20. doi : 10.1016 / j.eururo.2017.05.055 . PMID 28610779 .
- ^ Hong H, Zhang Y, Sun J, Cai W (junio de 2010). "Imagen de tomografía por emisión de positrones del cáncer de próstata" . Aminoácidos . 39 (1): 11-27. doi : 10.1007 / s00726-009-0394-9 . PMC 2883014 . PMID 19946787 .
- ^ Peyromaure M, Valéri A, Rebillard X, Beuzeboc P, Richaud P, Soulié M, Salomon L (diciembre de 2009). "[Características del cáncer de próstata en hombres menores de 50 años]". Progres en Urologie (en francés). 19 (11): 803–9. doi : 10.1016 / j.purol.2009.04.010 . PMID 19945663 .
- ^ "Cáncer de próstata resistente a la castración: en el Diccionario de términos de cáncer del NCI" . Instituto Nacional del Cáncer, Institutos Nacionales de Salud de EE. UU. 2019 . Consultado el 17 de septiembre de 2019 .
- ^ "Tratamientos para el cáncer de próstata resistente a la castración" . Sociedad Canadiense del Cáncer. 2019 . Consultado el 17 de septiembre de 2019 .
- ^ Seruga B, Ocana A, Tannock IF (enero de 2011). "Resistencia a fármacos en cáncer de próstata metastásico resistente a la castración". Reseñas de la naturaleza. Oncología clínica . 8 (1): 12-23. doi : 10.1038 / nrclinonc.2010.136 . PMID 20859283 . S2CID 24512148 .
- ^ Clarke NW (2005). "Docetaxel para el tratamiento del cáncer de próstata resistente a hormonas" (PDF) . Archivado desde el original (PDF) el 12 de julio de 2012.
- ^ "Cáncer de próstata (refractario a hormonas) - docetaxel" . Instituto Nacional de Salud y Excelencia Clínica. 2010-12-10. Archivado desde el original el 2 de febrero de 2012 . Consultado el 4 de julio de 2011 .
- ↑ de Bono JS, Oudard S, Ozguroglu M, Hansen S, Machiels JP, Kocak I, et al. (Octubre de 2010). "Prednisona más cabazitaxel o mitoxantrona para el cáncer de próstata metastásico resistente a la castración que progresa después del tratamiento con docetaxel: un ensayo aleatorizado de etiqueta abierta". Lancet . 376 (9747): 1147–54. doi : 10.1016 / S0140-6736 (10) 61389-X . PMID 20888992 . S2CID 4791847 .
- ^ "Avastin, Thalomid, Taxotere y prednisona eficaz para hombres con cáncer de próstata resistente a hormonas" . Marzo de 2010. Archivado desde el original el 15 de junio de 2010 . Consultado el 10 de mayo de 2010 .
- ^ Kantoff PW, Higano CS, Shore ND, Berger ER, Small EJ, Penson DF, et al. (Julio de 2010). "Inmunoterapia con Sipuleucel-T para el cáncer de próstata resistente a la castración" . La Revista de Medicina de Nueva Inglaterra . 363 (5): 411–22. doi : 10.1056 / NEJMoa1001294 . PMID 20818862 . S2CID 12168204 .
- ^ "La FDA aprueba Zytiga para el cáncer de próstata en etapa tardía" . Administración de Drogas y Alimentos de los Estados Unidos. 2011-04-28. Archivado desde el original el 22 de septiembre de 2013.
- ^ a b c "La FDA aprueba un nuevo tratamiento para un tipo de cáncer de próstata en etapa tardía" (Comunicado de prensa). Administración de Alimentos y Medicamentos. 2012-08-31. Archivado desde el original el 2 de octubre de 2013.
- ↑ a b c Azvolinsky A (4 de septiembre de 2012). "La FDA aprueba la enzalutamida (Xtandi) para el cáncer de próstata en etapa tardía" . CancerNetwork. Archivado desde el original el 13 de septiembre de 2012.
- ^ Qin J, Liu X, Laffin B, Chen X, Choy G, Jeter CR, et al. (Mayo de 2012). "La población de células de cáncer de próstata PSA (- / lo) alberga células de propagación tumoral a largo plazo autorrenovables que resisten la castración" . Célula madre celular . 10 (5): 556–69. doi : 10.1016 / j.stem.2012.03.009 . PMC 3348510 . PMID 22560078 .
- ^ Maitland NJ, Collins AT (junio de 2008). "Células madre del cáncer de próstata: un nuevo objetivo para la terapia". Revista de Oncología Clínica . 26 (17): 2862–70. doi : 10.1200 / JCO.2007.15.1472 . PMID 18539965 .
- ^ Attard G, Richards J, de Bono JS (abril de 2011). "Nuevas estrategias en el cáncer de próstata metastásico: dirigidas a la vía de señalización del receptor de andrógenos" . Investigación clínica del cáncer . 17 (7): 1649–57. doi : 10.1158 / 1078-0432.CCR-10-0567 . PMC 3513706 . PMID 21372223 .
- ^ Rane JK, Pellacani D, Maitland NJ (octubre de 2012). "Cáncer de próstata avanzado: un caso para la terapia de diferenciación adyuvante". Reseñas de la naturaleza. Urología . 9 (10): 595–602. doi : 10.1038 / nrurol.2012.157 . PMID 22890299 . S2CID 43634798 .
- ^ a b Jakob T, Tesfamariam YM, Macherey S, Kuhr K, Adams A, Monsef I, et al. (Grupo Cochrane de Urología) (diciembre de 2020). "Bifosfonatos o inhibidores de ligando de RANK para hombres con cáncer de próstata y metástasis óseas: un metanálisis de red". La base de datos Cochrane de revisiones sistemáticas . 12 : CD013020. doi : 10.1002 / 14651858.CD013020.pub2 . PMID 33270906 .
- ^ a b "Cirugía para el cáncer de próstata" . www.cancer.org . Consultado el 30 de marzo de 2020 .
- ^ a b Ilic D, Evans SM, Allan CA, Jung JH, Murphy D, Frydenberg M (septiembre de 2017). "Prostatectomía radical laparoscópica y asistida por robot versus abierta para el tratamiento del cáncer de próstata localizado" . La base de datos Cochrane de revisiones sistemáticas . 9 : CD009625. doi : 10.1002 / 14651858.cd009625.pub2 . PMC 6486168 . PMID 28895658 .
- ^ "Manejo de continencia después de cirugía de próstata" . Fundación Continencia de Australia . Archivado desde el original el 10 de abril de 2020.
- ^ Singla N, Singla AK (marzo de 2014). "Incontinencia pos prostatectomía: etiología, evaluación y manejo" . Revista Turca de Urología . 40 (1): 1–8. doi : 10.5152 / tud.2014.222014 . PMC 4548645 . PMID 26328137 .
- ^ "Directrices de la EAU sobre incontinencia urinaria en adultos" (PDF) . Asociación Europea de Urología . 2018.
- ^ "Disfunción eréctil después del cáncer de próstata" . www.hopkinsmedicine.org . Consultado el 1 de abril de 2020 .
- ^ "Cáncer de próstata - datos de estadísticas de cáncer" . seer.cancer.gov . Archivado desde el original el 18 de marzo de 2017 . Consultado el 11 de abril de 2017 .
- ^ Wakai K (febrero de 2005). "[Epidemiología descriptiva del cáncer de próstata en Japón y países occidentales]". Nihon Rinsho. Revista japonesa de medicina clínica (en japonés). 63 (2): 207–12. PMID 15714967 .
- ^ Jaubert de Beaujeu M, Chavrier Y (enero de 1976). "[Deformaciones de la pared torácica anterior (traducción del autor)]". Annales de Chirurgie Thoracique et Cardio-Vasculaire (en francés). 15 (1): 1–6. PMID 1259345 .
- ^ Hsing AW, Tsao L, Devesa SS (enero de 2000). "Tendencias y patrones internacionales de incidencia y mortalidad por cáncer de próstata". Revista Internacional de Cáncer . 85 (1): 60–7. doi : 10.1002 / (SICI) 1097-0215 (20000101) 85: 1 <60 :: AID-IJC11> 3.0.CO; 2-B . PMID 10585584 .
- ^ Osegbe DN (abril de 1997). "El cáncer de próstata en los nigerianos: hechos y no hechos". La Revista de Urología . 157 (4): 1340–3. doi : 10.1016 / S0022-5347 (01) 64966-8 . PMID 9120935 .
- ^ Bello JO (mayo de 2017). "Predictores de resultados de supervivencia en hombres negros subsaharianos nativos recién diagnosticados con cáncer de próstata metastásico" . Urología BMC . 17 (1): 39. doi : 10.1186 / s12894-017-0228-0 . PMC 5450414 . PMID 28558685 .
- ^ Di Blasio CJ, Rhee AC, Cho D, Scardino PT, Kattan MW (octubre de 2003). "Predicción de puntos finales clínicos: nomogramas de tratamiento en cáncer de próstata". Seminarios de Oncología . 30 (5): 567–86. doi : 10.1016 / S0093-7754 (03) 00351-8 . PMID 14571407 .
- ^ Løvf M, Zhao S, Axcrona U, Johannessen B, Bakken AC, Carm KT, et al. (Marzo de 2019). "El cáncer de próstata primario multifocal presenta un alto grado de heterogeneidad genómica". Urología europea . 75 (3): 498–505. doi : 10.1016 / j.eururo.2018.08.009 . PMID 30181068 .
- ^ Hellerstedt BA, Pienta KJ (2002). "El estado actual de la terapia hormonal para el cáncer de próstata" . Ca . 52 (3): 154–79. doi : 10.3322 / canjclin.52.3.154 . PMID 12018929 . S2CID 25311034 .
- ^ Feldman BJ, Feldman D (octubre de 2001). "El desarrollo del cáncer de próstata independiente de los andrógenos". Reseñas de la naturaleza. Cáncer . 1 (1): 34–45. doi : 10.1038 / 35094009 . PMID 11900250 . S2CID 205020623 .
- ^ Eifler JB, Feng Z, Lin BM, Partin MT, Humphreys EB, Han M, et al. (Enero 2013). "Un nomograma de estadificación del cáncer de próstata actualizado (tablas de Partin) basado en los casos de 2006 a 2011" . BJU International . 111 (1): 22–9. doi : 10.1111 / j.1464-410X.2012.11324.x . PMC 3876476 . PMID 22834909 .
- ^ "Página de inicio de CaPSURE.net" . 2006-09-27. Archivado desde el original el 27 de septiembre de 2006 . Consultado el 8 de agosto de 2020 .
- ^ Cooperberg MR, Pasta DJ, Elkin EP, Litwin MS, Latini DM, Du Chane J, Carroll PR (junio de 2005). "La puntuación de la Evaluación de Riesgo de Próstata de la Universidad de California, San Francisco: un predictor preoperatorio sencillo y confiable de la recurrencia de la enfermedad después de la prostatectomía radical" . La Revista de Urología . 173 (6): 1938–42. doi : 10.1097 / 01.ju.0000158155.33890.e7 . PMC 2948569 . PMID 15879786 .
- ^ Cooperberg MR, Freedland SJ, Pasta DJ, Elkin EP, Presti JC, Amling CL, et al. (Noviembre de 2006). "Validación multiinstitucional del cáncer UCSF de la evaluación del riesgo de próstata para la predicción de recurrencia después de prostatectomía radical" . Cáncer . 107 (10): 2384–91. doi : 10.1002 / cncr.22262 . PMID 17039503 . S2CID 17420454 .
- ↑ May M, Knoll N, Siegsmund M, Fahlenkamp D, Vogler H, Hoschke B, Gralla O (noviembre de 2007). "Validez de la puntuación CAPRA para predecir la supervivencia libre de recurrencia bioquímica después de la prostatectomía radical. Resultados de una encuesta multicéntrica europea de 1.296 pacientes". La Revista de Urología . 178 (5): 1957–62, discusión 1962. doi : 10.1016 / j.juro.2007.07.043 . PMID 17868719 .
- ^ Zhao KH, Hernandez DJ, Han M, Humphreys EB, Mangold LA, Partin AW (agosto de 2008). "Validación externa de la Universidad de California, San Francisco, puntaje de evaluación de riesgo de cáncer de próstata". Urología . 72 (2): 396–400. doi : 10.1016 / j.urology.2007.11.165 . PMID 18372031 .
- ^ Cooperberg MR, Broering JM, Carroll PR (junio de 2009). "Evaluación de riesgo de metástasis y mortalidad por cáncer de próstata en el momento del diagnóstico" . Revista del Instituto Nacional del Cáncer . 101 (12): 878–87. doi : 10.1093 / jnci / djp122 . PMC 2697208 . PMID 19509351 .
- ^ "CDC FastStats" . Centros para el Control de Enfermedades . Archivado desde el original el 28 de julio de 2017.
- ^ "Opciones de tratamiento para hombres con cáncer de próstata en etapa temprana" . Instituto Nacional del Cáncer. 2014-10-17. Archivado desde el original el 4 de abril de 2015.
- ^ Eggener SE, Badani K, Barocas DA, Barrisford GW, Cheng JS, Chin AI, et al. (Septiembre de 2015). "Cáncer de próstata de Gleason 6: traducción de la biología en salud de la población" . La Revista de Urología . 194 (3): 626–34. doi : 10.1016 / j.juro.2015.01.126 . PMC 4551510 . PMID 25849602 .
- ^ "Estimaciones del país de enfermedades y lesiones de la OMS" . Organización Mundial de la Salud . 2009. Archivado desde el original el 11 de noviembre de 2009 . Consultado el 11 de noviembre de 2009 .
- ^ Informe mundial sobre el cáncer 2014 . Agencia Internacional de Investigaciones sobre el Cáncer, Organización Mundial de la Salud. ISBN 978-92-832-0432-9.
- ^ Jemal A, Bray F, Centro MM, Ferlay J, Ward E, Forman D (2011). "Estadísticas mundiales de cáncer" . Ca . 61 (2): 69–90. doi : 10.3322 / caac.20107 . PMID 21296855 . S2CID 30500384 .
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al. (Diciembre 2012). "Mortalidad mundial y regional de 235 causas de muerte para 20 grupos de edad en 1990 y 2010: un análisis sistemático para el estudio de carga mundial de enfermedad 2010" . Lancet . 380 (9859): 2095–128. doi : 10.1016 / S0140-6736 (12) 61728-0 . hdl : 10536 / DRO / DU: 30050819 . PMID 23245604 . S2CID 1541253 .
- ^ "Estadísticas del cáncer de próstata" . Urología laparoscópica. Archivado desde el original el 24 de junio de 2016 . Consultado el 19 de junio de 2016 .
- ^ a b Descripción general: cáncer de próstata: ¿qué causa el cáncer de próstata? Archivado el 4 de abril de 2006 en la Wayback Machine American Cancer Society (2 de mayo de 2006). Consultado el 5 de abril de 2007.
- ^ a b Preguntas frecuentes sobre el cáncer de próstata. Archivado el 29 de mayo de 2006 en el Departamento de Urología de la Facultad de Medicina de la Universidad Estatal Wayback Machine de Nueva York (31 de agosto de 2006). Consultado el 5 de abril de 2007.
- ^ Lee MM, Gomez SL, Chang JS, Wey M, Wang RT, Hsing AW (julio de 2003). "Consumo de soja e isoflavonas en relación con el riesgo de cáncer de próstata en China". Epidemiología, biomarcadores y prevención del cáncer . 12 (7): 665–8. PMID 12869409 .
- ^ Potosky AL, Miller BA, Albertsen PC, Kramer BS (febrero de 1995). "El papel de la creciente detección en la creciente incidencia de cáncer de próstata". JAMA . 273 (7): 548–52. doi : 10.1001 / jama.273.7.548 . PMID 7530782 .
- ^ Hanno PM, Malcowicz SB, Wein AJ, "Manual clínico de urología" McGraw Hill 2001
- ^ Homma Y, Kawabe K, Tsukamoto T, Yamanaka H, Okada K, Okajima E, et al. (Enero de 1997). "Encuesta epidemiológica de los síntomas del tracto urinario inferior en Asia y Australia utilizando la puntuación internacional de síntomas de la próstata". Revista Internacional de Urología . 4 (1): 40–6. doi : 10.1111 / j.1442-2042.1997.tb00138.x . PMID 9179665 . S2CID 19636484 .
- ^ Bostwick DG, Eble JN (2007). Patología quirúrgica urológica . San Luis: Mosby. pag. 468 . ISBN 978-0-323-01970-5.
- ^ a b Jemal A, Murray T, Ward E, Samuels A, Tiwari RC, Ghafoor A, et al. (2005). "Estadísticas de cáncer, 2005" . Ca . 55 (1): 10–30. doi : 10.3322 / canjclin.55.1.10 . PMID 15661684 . S2CID 22356919 .
- ^ Comité editorial de detección y prevención del PDQ (2002). "Examen de detección de cáncer de próstata (PDQ®): versión para profesionales de la salud" . Resúmenes de información sobre el cáncer del PDQ . Bethesda (MD): Instituto Nacional del Cáncer (EE. UU.). PMID 26389383 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ Ferlay J, Steliarova-Foucher E, Lortet-Tieulent J, Rosso S, Coebergh JW, Comber H, et al. (Abril 2013). "Patrones de incidencia y mortalidad por cáncer en Europa: estimaciones para 40 países en 2012" . Revista europea del cáncer . 49 (6): 1374–403. doi : 10.1016 / j.ejca.2012.12.027 . PMID 23485231 .
- ^ "Estadísticas del cáncer de próstata" . Cancer Research Reino Unido . Archivado desde el original el 6 de octubre de 2014 . Consultado el 3 de octubre de 2014 .
- ^ Ghabili K, Tosoian JJ, Schaeffer EM, Pavlovich CP, Golzari SE, Khajir G, et al. (Noviembre de 2016). "La historia del cáncer de próstata desde la antigüedad: revisión de estudios paleopatológicos". Urología . 97 : 8-12. doi : 10.1016 / j.urology.2016.08.032 . PMID 27591810 .
- ↑ a b Nahon I, Waddington G, Dorey G, Adams R (2011). "La historia de la cirugía urológica: de las cañas a la robótica". Enfermería Urológica . 31 (3): 173–80. doi : 10.7257 / 1053-816X.2011.31.3.173 . PMID 21805756 .
- ↑ Adams J (1853). "El caso de escirro de la glándula prostática con la correspondiente aflicción de los ganglios linfáticos en la región lumbar y en la pelvis". Lancet . 1 (1547): 393–94. doi : 10.1016 / S0140-6736 (02) 68759-8 .
- ^ Lytton B (junio de 2001). "Cáncer de próstata: una breve historia y el descubrimiento del tratamiento de ablación hormonal". La Revista de Urología . 165 (6 Pt 1): 1859–62. doi : 10.1016 / S0022-5347 (05) 66228-3 . PMID 11371867 .
- ^ Samuel David Gross (1851). Un tratado práctico sobre las enfermedades y lesiones de la vejiga urinaria, la próstata y la uretra . Filadelfia: Blanchard y Lea.
- ^ Joven HH (1905). "Cuatro casos de prostatectomía radical". Toro de Johns Hopkins . 16 .
- ^ Walsh PC, Lepor H, Eggleston JC (1983). "Prostatectomía radical con preservación de la función sexual: consideraciones anatómicas y patológicas". La próstata . 4 (5): 473–85. doi : 10.1002 / pros.2990040506 . PMID 6889192 . S2CID 30740301 .
- ^ Huggins CB, Hodges CV (1941). "Estudios sobre cáncer de próstata: 1. Los efectos de la castración, de la inyección de estrógenos y andrógenos sobre las fosfatasas séricas en el carcinoma metastásico de próstata" . Cancer Res . 1 (4): 293. Archivado desde el original el 30 de junio de 2017 . Consultado el 2 de septiembre de 2015 .
- ^ Schally AV, Kastin AJ, Arimura A (noviembre de 1971). "Hormona estimulante del folículo hipotalámico (FSH) y hormona reguladora de la hormona luteinizante (LH): estructura, fisiología y estudios clínicos". Fertilidad y esterilidad . 22 (11): 703-21. doi : 10.1016 / S0015-0282 (16) 38580-6 . PMID 4941683 .
- ^ Tolis G, Ackman D, Stellos A, Mehta A, Labrie F, Fazekas AT, et al. (Marzo de 1982). "Inhibición del crecimiento tumoral en pacientes con carcinoma de próstata tratados con agonistas de la hormona liberadora de hormona luteinizante" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 79 (5): 1658–62. Código Bibliográfico : 1982PNAS ... 79.1658T . doi : 10.1073 / pnas.79.5.1658 . PMC 346035 . PMID 6461861 .
- ^ Denmeade SR, Isaacs JT (mayo de 2002). "Una historia de tratamiento del cáncer de próstata" . Reseñas de la naturaleza. Cáncer . 2 (5): 389–96. doi : 10.1038 / nrc801 . PMC 4124639 . PMID 12044015 .
- ^ Scott WW, Johnson DE, Schmidt JE, Gibbons RP, Prout GR, Joiner JR, et al. (Diciembre de 1975). "Quimioterapia del carcinoma de próstata avanzado con ciclofosfamida o 5-fluorouracilo: resultados del primer estudio aleatorizado nacional". La Revista de Urología . 114 (6): 909-11. doi : 10.1016 / S0022-5347 (17) 67172-6 . PMID 1104900 .
- ^ "La FDA aprueba un nuevo fármaco para el cáncer de próstata avanzado" (Comunicado de prensa). Administración de Alimentos y Medicamentos. 15 de mayo de 2013. Archivado desde el original el 4 de junio de 2013.
- ^ a b Urisman A, Molinaro RJ, Fischer N, Plummer SJ, Casey G, Klein EA, et al. (Marzo de 2006). "Identificación de un nuevo Gammaretrovirus en tumores de próstata de pacientes homocigotos para la variante R462Q RNASEL" . PLOS Patógenos . 2 (3): e25. doi : 10.1371 / journal.ppat.0020025 . PMC 1434790 . PMID 16609730 . (Retirado, ver doi : 10.1371 / annotation / 7e2efc01-2e9b-4e9b-aef0-87ab0e4e4732 )
- ↑ a b c Arnst C (13 de junio de 2007). "Una brecha de género en el cáncer" . Businessweek.com. Archivado desde el original el 6 de agosto de 2011 . Consultado el 29 de agosto de 2011 .
- ↑ Browne A (7 de octubre de 2001). "El sesgo del cáncer pone los senos primero" . The Guardian . Londres. Archivado desde el original el 26 de diciembre de 2016.
- ↑ Templeton S (16 de octubre de 2005). "Los hombres pierden en la batalla por el dinero en efectivo contra el cáncer" . Sunday Times . Archivado desde el original el 24 de mayo de 2011.
- ^ Farrell W, Sterba JP (2008). ¿El feminismo discrimina a los hombres? : un debate . ISBN 978-0-19-531283-6. Consultado el 29 de agosto de 2011 .
- ^ Coalición nacional contra el cáncer de próstata. La brecha del cáncer de próstata. Una crisis en la salud de los hombres . Coalición Nacional de Cáncer de Próstata; 2007 Webcite
- ^ "Hombres, no esperen hasta que haya un problema para ver a un médico" . Tampa Bay Times . 7 de julio de 2016 . Consultado el 27 de agosto de 2019 .
- ^ Minium, Harry. "Los hombres necesitan escuchar la historia de la recuperación del cáncer de próstata del entrenador de ODU, Jeff Jones" . El piloto de Virginia . Consultado el 27 de agosto de 2019 .
- ^ "Resultado positivo del análisis intermedio del estudio fundamental de Alpharadin: criterio de valoración principal cumplido en el estudio de fase III ALSYMPCA" (Comunicado de prensa). Algeta ASA. 2011-06-06. Archivado desde el original el 11 de agosto de 2011 . Consultado el 4 de julio de 2011 .CS1 maint: unfit URL (link)
- ↑ a b Geethakumari PR, Cookson MS, Kelly WK (febrero de 2016). "La evolución de la biología del cáncer de próstata resistente a la castración: revisión de las recomendaciones del grupo de trabajo de ensayos clínicos de cáncer de próstata 3" . Oncología . 30 (2): 187–95, 199. PMID 26888794 . Archivado desde el original el 22 de febrero de 2016.
- ^ a b Elshan NG, Rettig MB, Jung ME (mayo de 2019). "Moléculas que se dirigen al eje de señalización del receptor de andrógenos (AR) más allá del dominio de unión AR-Ligand" . Revisiones de investigaciones medicinales . 39 (3): 910–960. doi : 10.1002 / med.21548 . PMC 6608750 . PMID 30565725 .
- ↑ a b c Ghosh J, Myers CE (octubre de 1998). "La inhibición de la araquidonato 5-lipoxigenasa desencadena la apoptosis masiva en las células de cáncer de próstata humano" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 95 (22): 13182–7. Código bibliográfico : 1998PNAS ... 9513182G . doi : 10.1073 / pnas.95.22.13182 . PMC 23752 . PMID 9789062 .
La inhibición de la 5-lipoxigenasa por MK886 bloquea completamente la producción de 5-HETE e induce una apoptosis masiva en las células de cáncer de próstata humano que responden a hormonas (LNCaP) y no responden (PC3). Esta muerte celular es muy rápida
- ↑ a b c Greene ER, Huang S, Serhan CN, Panigrahy D (noviembre de 2011). "Regulación de la inflamación en el cáncer por eicosanoides" . Prostaglandinas y otros mediadores lipídicos . 96 (1–4): 27–36. doi : 10.1016 / j.prostaglandins.2011.08.004 . PMC 4051344 . PMID 21864702 .
La vía de la 5-lipoxigenasa (5-LOX) está implicada en el desarrollo y progresión de los cánceres humanos. La 5-LOX, cuya estructura cristalina se identificó recientemente (118), es una enzima clave en la metabolización del ácido araquidónico a leucotrienos. La 5-LOX puede ser inducida por estímulos proinflamatorios y se expresa en cánceres epiteliales que incluyen pulmón, próstata, mama y colon (113). Por lo tanto, los inhibidores de la 5-LOX han sido seleccionados por sus efectos quimiopreventivos. Se ha demostrado que la inhibición de la actividad 5-LOX bloquea la proliferación de células de cáncer de próstata, así como la tumorigénesis pulmonar inducida por carcinógenos (119, 120). ... Tanto el 5-HETE como el 12-HETE también son productos de la lipoxigenasa y están involucrados en la progresión del tumor (12). El 5-HETE exógeno puede estimular la proliferación de células de cáncer de próstata y actuar como factor de supervivencia (137, 138).Estos resultados requieren concentraciones relativamente altas (a una concentración de 10 µM). El bloqueo de la formación de 5-HETE, mediante la inhibición de la 5-lipoxigenasa, da como resultado una apoptosis masiva de las células de cáncer de próstata humano (139).
- ↑ a b c Bishayee K, Khuda-Bukhsh AR (septiembre de 2013). "Terapia con antagonista de la 5-lipoxigenasa: un nuevo enfoque hacia la quimioterapia contra el cáncer dirigida" . Acta Biochimica et Biophysica Sinica . 45 (9): 709-19. doi : 10.1093 / abbs / gmt064 . PMID 23752617 .
Estudios recientes demostraron la participación de factores de crecimiento, como el factor de crecimiento epidérmico (EGF) y la neurotensina en la progresión tumoral mediada por 5-LOX en el cáncer de próstata [22,23]. Estudios recientes con ARNip 5-LOX [10] y bloqueador específico de 5-LOX [24] revelaron la relación de este gen con la proliferación de células tumorales. ... El meclofenamato sódico (MS) es conocido por su actividad antiinflamatoria y, aparte de esto, Boctor et al. [37] informó que cuando se usa, provoca una reducción en la formación de 5-HETE en leucocitos humanos. Por tanto, la EM puede considerarse un inhibidor dual de las rutas 5-LOX y COX de la cascada del ácido araquidónico. Una investigación más a fondo con esta sustancia reveló que podría interferir con los receptores de LT en el carcinoma de pulmón [38]. En un estudio reciente,un grupo de científicos ha demostrado el efecto de la EM en las células del cáncer de próstata tanto in vitro como in vivo [39], y su resultado sugiere una profunda reducción del crecimiento tumoral y la metástasis del cáncer. ... Si bien los inhibidores de uso común produjeron una fuerte citotoxicidad, en particular, el zileuton, el único inhibidor de 5-LOX comercializado, no logró inducir una respuesta antiproliferativa o citotóxica en todos los demás tipos de células tumorales donde la 5-LOX estaba en estado inactivo ( por ejemplo, células HeLa). Pero donde la 5-LOX estaba en estado activo, el zileuton podría inhibir eficazmente la progresión, como en el caso del cáncer de próstata.no pudo inducir una respuesta antiproliferativa o citotóxica en todos los demás tipos de células tumorales en las que la 5-LOX estaba en estado inactivo (por ejemplo, células HeLa). Pero donde la 5-LOX estaba en estado activo, el zileuton podría inhibir eficazmente la progresión, como en el caso del cáncer de próstata.no pudo inducir una respuesta antiproliferativa o citotóxica en todos los demás tipos de células tumorales en las que la 5-LOX estaba en estado inactivo (por ejemplo, células HeLa). Pero donde la 5-LOX estaba en estado activo, el zileuton podría inhibir eficazmente la progresión, como en el caso del cáncer de próstata.
- ^ Martínez-Bosch N, Rodriguez-Vida A, Juanpere N, Lloreta J, Rovira A, Albanell J, et al. (Julio de 2019). "Galectinas en cáncer de próstata y vejiga: roles tumorigénicos y oportunidades clínicas". Reseñas de la naturaleza. Urología . 16 (7): 433–445. doi : 10.1038 / s41585-019-0183-5 . hdl : 10261/201560 . PMID 31015643 . S2CID 128360958 .
- ^ Munkley J, Mills IG, Elliott DJ (junio de 2016). "El papel de los glicanos en el desarrollo y progresión del cáncer de próstata" . Reseñas de la naturaleza. Urología . 13 (6): 324–33. doi : 10.1038 / nrurol.2016.65 . PMID 27091662 . S2CID 25916024 .
- ^ Drake RR, Jones EE, Powers TW, Nyalwidhe JO (2015). "Glucosilación alterada en cáncer de próstata". En Drake RR, Ball LE (eds.). Glicosilación y cáncer . Avances en la investigación del cáncer vol. 126. 126 . págs. 345–82. doi : 10.1016 / bs.acr.2014.12.001 . ISBN 9780128013816. PMID 25727153 .
- ^ Laderach DJ, Gentilini LD, Giribaldi L, Delgado VC, Nugnes L, Croci DO, et al. (Enero 2013). "Una firma de galectina única en la progresión del cáncer de próstata humano sugiere que la galectina-1 es un objetivo clave para el tratamiento de la enfermedad avanzada" . Investigación del cáncer . 73 (1): 86–96. doi : 10.1158 / 0008-5472.CAN-12-1260 . PMID 23108139 .
- ^ Compagno D, Gentilini LD, Jaworski FM, Pérez IG, Contrufo G, Laderach DJ (octubre de 2014). "Glicanos y galectinas en biología, angiogénesis y metástasis del cáncer de próstata" . Glicobiología . 24 (10): 899–906. doi : 10.1093 / glycob / cwu055 . PMID 24939371 .
- ^ Linja MJ, Savinainen KJ, Saramäki OR, Tammela TL, Vessella RL, Visakorpi T (mayo de 2001). "Amplificación y sobreexpresión del gen del receptor de andrógenos en el cáncer de próstata refractario a hormonas" . Investigación del cáncer . 61 (9): 3550–5. PMID 11325816 .
- ^ Ford OH, Gregory CW, Kim D, Smitherman AB, Mohler JL (noviembre de 2003). "Amplificación del gen del receptor de andrógenos y expresión de proteínas en el cáncer de próstata recurrente". La Revista de Urología . 170 (5): 1817–21. doi : 10.1097 / 01.ju.0000091873.09677.f4 . PMID 14532783 .
- ^ Kokontis J, Takakura K, Hay N, Liao S (marzo de 1994). "Aumento de la actividad del receptor de andrógenos y expresión alterada de c-myc en células de cáncer de próstata después de la privación de andrógenos a largo plazo" . Investigación del cáncer . 54 (6): 1566–73. PMID 7511045 .
- ^ Umekita Y, Hiipakka RA, Kokontis JM, Liao S (octubre de 1996). "Crecimiento del tumor de próstata humana en ratones atímicos: inhibición por andrógenos y estimulación por finasterida" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 93 (21): 11802–7. Código Bibliográfico : 1996PNAS ... 9311802U . doi : 10.1073 / pnas.93.21.11802 . PMC 38139 . PMID 8876218 .
- ^ Kokontis JM, Hsu S, Chuu CP, Dang M, Fukuchi J, Hiipakka RA, Liao S (diciembre de 2005). "Papel del receptor de andrógenos en la progresión de las células tumorales de próstata humana a la independencia e insensibilidad de los andrógenos". La próstata . 65 (4): 287–98. doi : 10.1002 / pros.20285 . PMID 16015608 . S2CID 22349673 .
- ^ Bourdoumis A, Papatsoris AG, Chrisofos M, Efstathiou E, Skolarikos A, Deliveliotis C (2010). "El nuevo biomarcador del antígeno 3 del cáncer de próstata (PCA3)" . Internacional Braz J Urol . 36 (6): 665–8, discusión 669. doi : 10.1590 / S1677-55382010000600003 . PMID 21176272 .
- ^ "Pruebas de PCA3 para el diagnóstico y tratamiento del cáncer de próstata mejoran los resultados de salud del paciente" . www.cdc.gov . 2018-11-19 . Consultado el 9 de agosto de 2020 .
Enlaces externos [ editar ]
| Clasificación | D
|
|---|---|
| Recursos externos |
|
- Cáncer de próstata en Curlie
- Información centrada en el paciente de la Asociación Urológica Europea
- "Diagnóstico y tratamiento del cáncer de próstata (video)" . Mayo Clinic . Febrero de 2020.