Retina
Este artículo necesita la atención de un experto en medicina . ( Mayo de 2018 ) |
| Retina | |
|---|---|
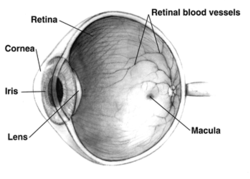 Vista en sección transversal del ojo humano derecho ; los ojos varían significativamente entre los animales. | |
| Detalles | |
| Pronunciación | Reino Unido : / r ɛ t ɪ n ə / , Estados Unidos : / r ɛ t ən ə / , pl. retinae / - n i / |
| Parte de | Ojo |
| Sistema | Sistema visual |
| Artería | Arteria central de la retina |
| Identificadores | |
| latín | Rēte |
| Malla | D012160 |
| TA98 | A15.2.04.002 |
| TA2 | 6776 |
| FMA | 58301 |
| Terminología anatómica | |
La retina (del latín : rete "net") es la capa de tejido más interna y sensible a la luz del ojo de la mayoría de los vertebrados y algunos moluscos . La óptica del ojo crea una imagen bidimensional enfocada del mundo visual en la retina, que traduce esa imagen en impulsos neuronales eléctricos al cerebro para crear percepción visual . La retina cumple una función análoga a la de la película o el sensor de imagen en una cámara .
La retina neural consta de varias capas de neuronas interconectadas por sinapsis y está sostenida por una capa externa de células epiteliales pigmentadas. Las células sensibles a la luz primarias en la retina son las células fotorreceptoras , que son de dos tipos: bastones y conos . Las varillas funcionan principalmente con poca luz y proporcionan una visión en blanco y negro. Los conos funcionan en condiciones de buena iluminación y son responsables de la percepción del color, así como de la visión de alta agudeza utilizada para tareas como la lectura. Un tercer tipo de célula fotosensible , la célula ganglionar fotosensible , es importante para el arrastre de los ritmos circadianos y las respuestas reflejas como lareflejo pupilar a la luz .
La luz que golpea la retina inicia una cascada de eventos químicos y eléctricos que finalmente desencadenan impulsos nerviosos que se envían a varios centros visuales del cerebro a través de las fibras del nervio óptico . Las señales neurales de los conos y bastones son procesadas por otras neuronas, cuya salida toma la forma de potenciales de acción en las células ganglionares de la retina cuyos axones forman el nervio óptico. [1] Varias características importantes de la percepción visual se pueden rastrear hasta la codificación retiniana y el procesamiento de la luz.
En el desarrollo embrionario de vertebrados , la retina y el nervio óptico se originan como excrecencias del cerebro en desarrollo, específicamente el diencéfalo embrionario ; por lo tanto, la retina se considera parte del sistema nervioso central (SNC) y en realidad es tejido cerebral. [2] [3] Es la única parte del SNC que se puede visualizar de forma no invasiva .
Estructura
Retina invertida versus no invertida
La retina de los vertebrados está invertida en el sentido de que las células sensibles a la luz están en la parte posterior de la retina, de modo que la luz tiene que atravesar capas de neuronas y capilares antes de llegar a los conos y bastones. [4] Las células ganglionares, cuyos axones forman el nervio óptico, se encuentran en la parte frontal de la retina; por lo tanto, el nervio óptico debe atravesar la retina de camino al cerebro. En esta región no hay fotorreceptores, lo que da lugar al punto ciego . [5] En contraste, en la retina de los cefalópodos los fotorreceptores están al frente, con las neuronas de procesamiento y los capilares detrás de ellos. Debido a esto, los cefalópodos no tienen un punto ciego.
Aunque el tejido neural suprayacente es parcialmente transparente, y se ha demostrado que las células gliales que lo acompañan actúan como canales de fibra óptica para transportar fotones directamente a los fotorreceptores, [6] [7] sí se produce dispersión de luz. [8] Algunos vertebrados, incluidos los humanos, tienen un área de la retina central adaptada para una visión de alta agudeza. Esta área, denominada fovea centralis , es avascular (no tiene vasos sanguíneos) y tiene un tejido neural mínimo frente a los fotorreceptores, lo que minimiza la dispersión de la luz. [8]
Los cefalópodos tienen una retina no invertida que es comparable en poder de resolución a los ojos de muchos vertebrados. Los ojos de calamar no tienen un análogo del epitelio pigmentario de la retina (EPR) de los vertebrados . Aunque sus fotorreceptores contienen una proteína, retinocromo, que recicla la retina y replica una de las funciones del EPR de vertebrados, se podría argumentar que los fotorreceptores de cefalópodos no se mantienen tan bien como en los vertebrados y que, como resultado, la vida útil de los fotorreceptores en Los invertebrados son mucho más cortos que los vertebrados. [9] El tener ojos de tallo fácilmente reemplazados (algunas langostas) o retinae (algunas arañas, como Deinopis [10] ) ocurre raramente.
La retina de los cefalópodos no se origina como una excrecencia del cerebro, como lo hace la de los vertebrados. Es discutible que esta diferencia muestre que los ojos de los vertebrados y los cefalópodos no son homólogos sino que han evolucionado por separado. Desde una perspectiva evolutiva, una estructura más compleja, como la retina invertida, generalmente puede surgir como consecuencia de dos procesos alternativos: (a) un compromiso "bueno" ventajoso entre limitaciones funcionales en competencia, o (b) como una reliquia histórica desadaptativa de el enrevesado camino de la evolución y transformación de los órganos. La visión es una adaptación importante en los vertebrados superiores.
Una tercera visión del ojo de vertebrado "invertido" es que combina dos beneficios: el mantenimiento de los fotorreceptores mencionados anteriormente, y la reducción de la intensidad de la luz necesaria para evitar cegar los fotorreceptores, que se basan en los ojos extremadamente sensibles de los antepasados de Hagfishes modernos (un pez que vive en aguas muy profundas y oscuras). [11]
Capas de retina
La retina de los vertebrados tiene diez capas distintas. [13] Desde el más cercano al más lejano del cuerpo vítreo:
- Membrana limitante interna - membrana basal elaborada por células de Müller .
- Capa de fibras nerviosas : axones de los cuerpos de las células ganglionares (tenga en cuenta que existe una capa delgada de placas base de células de Müller entre esta capa y la membrana limitante interna).
- Capa de células ganglionares: contiene núcleos de células ganglionares, cuyos axones se convierten en fibras del nervio óptico y algunas células amacrinas desplazadas . [2]
- Capa plexiforme interna : contiene la sinapsis entre los axones de las células bipolares y las dendritas del ganglio y las células amacrinas. [2]
- Capa nuclear interna : contiene los núcleos y los cuerpos celulares circundantes (perikarya) de las células amacrinas , las células bipolares y las células horizontales . [2]
- Capa plexiforme externa : proyecciones de bastones y conos que terminan en la esférula del bastón y el pedículo del cono, respectivamente. Estos forman sinapsis con dendritas de células bipolares y células horizontales. [2] En la región macular , esto se conoce como la capa de fibra de Henle .
- Capa nuclear externa : cuerpos celulares de bastones y conos.
- Membrana limitante externa : capa que separa las porciones del segmento interno de los fotorreceptores de sus núcleos celulares.
- Capa de segmento interno / segmento externo: segmentos internos y segmentos externos de varillas y conos. Los segmentos exteriores contienen un aparato sensor de luz altamente especializado. [14] [15]
- Epitelio pigmentario de la retina : capa única de células epiteliales cuboidales (con extrusiones que no se muestran en el diagrama). Esta capa es la más cercana a la coroides y proporciona nutrición y funciones de apoyo a la retina neural. El pigmento negro melanina en la capa de pigmento evita el reflejo de la luz en todo el globo ocular; esto es extremadamente importante para una visión clara. [16] [17] [18]
Estas capas se pueden agrupar en 4 etapas principales de procesamiento: fotorrecepción; transmisión a células bipolares ; transmisión a las células ganglionares , que también contienen fotorreceptores, las células ganglionares fotosensibles ; y transmisión a lo largo del nervio óptico. En cada etapa sináptica también hay células horizontales y amacrinas conectadas lateralmente .
El nervio óptico es un tracto central de muchos axones de células ganglionares que se conectan principalmente al cuerpo geniculado lateral , una estación de retransmisión visual en el diencéfalo (la parte posterior del prosencéfalo). También se proyecta hacia el colículo superior , el núcleo supraquiasmático y el núcleo del tracto óptico . Pasa a través de las otras capas, creando el disco óptico en los primates. [19]
Estructuras adicionales, no directamente asociadas con la visión, se encuentran como excrecencias de la retina en algunos grupos de vertebrados. En las aves , el pecten es una estructura vascular de forma compleja que se proyecta desde la retina hacia el humor vítreo ; suministra oxígeno y nutrientes al ojo y también puede ayudar en la visión. Los reptiles tienen una estructura similar, pero mucho más simple. [20]
En los seres humanos adultos, toda la retina es aproximadamente el 72% de una esfera de unos 22 mm de diámetro. Toda la retina contiene alrededor de 7 millones de conos y de 75 a 150 millones de bastones. El disco óptico, una parte de la retina a veces llamada "el punto ciego" porque carece de fotorreceptores, se encuentra en la papila óptica , donde las fibras del nervio óptico salen del ojo. Aparece como un área blanca ovalada de 3 mm². Temporal (en la dirección de las sienes) a este disco es la mácula , en cuyo centro está la fóvea , un hoyo que es responsable de nuestra visión central aguda pero en realidad es menos sensible a la luz debido a su falta de bastones. Humanos y no humanos primatesposeen una fóvea, a diferencia de ciertas especies de aves, como los halcones, que son bifoviados, y los perros y gatos, que no poseen fóvea sino una banda central conocida como raya visual. [ cita requerida ] Alrededor de la fóvea se extiende la retina central unos 6 mm y luego la retina periférica. El borde más lejano de la retina está definido por la ora serrata . La distancia de una ora a otra (o mácula), el área más sensible a lo largo del meridiano horizontal es de unos 32 mm. [ aclaración necesaria ]
En la sección, la retina no tiene más de 0,5 mm de grosor. Tiene tres capas de células nerviosas y dos de sinapsis , incluida la única sinapsis de cinta . El nervio óptico transporta los axones de las células ganglionares al cerebro y los vasos sanguíneos que irrigan la retina. Las células ganglionares se encuentran en la parte más interna del ojo, mientras que las células fotorreceptoras se encuentran más allá. Debido a esta disposición contraria a la intuición, la luz debe pasar primero a través y alrededor de las células ganglionares y a través del grosor de la retina (incluidos sus vasos capilares, no mostrados) antes de llegar a los conos y bastones. La luz es absorbida por el epitelio pigmentario de la retina o la coroides (ambos opacos).
Los glóbulos blancos en los capilares frente a los fotorreceptores pueden percibirse como pequeños puntos brillantes en movimiento cuando se mira a la luz azul. Esto se conoce como fenómeno entóptico de campo azul (o fenómeno de Scheerer).
Entre la capa de células ganglionares y los bastones y conos hay dos capas de neuropilos donde se establecen los contactos sinápticos. Las capas de neuropilo son la capa plexiforme externa y la capa plexiforme interna . En la capa externa de neurópilos, los bastones y los conos se conectan a las células bipolares que corren verticalmente , y las células horizontales orientadas horizontalmente se conectan a las células ganglionares.
La retina central contiene predominantemente conos, mientras que la retina periférica contiene predominantemente bastones. En total, hay alrededor de siete millones de conos y cien millones de barras. En el centro de la mácula está el hoyo foveal donde los conos son estrechos y largos, y dispuestos en mosaico hexagonal , el más denso, en contraposición a los conos mucho más gordos ubicados más periféricamente en la retina. [21] En la fosa foveal, las otras capas retinianas se desplazan, antes de acumularse a lo largo de la pendiente foveal hasta el borde de la fóvea o parafovea., se alcanza, que es la porción más gruesa de la retina. La mácula tiene una pigmentación amarilla, debido a los pigmentos de cribado, y se la conoce como mácula lútea. El área que rodea directamente la fóvea tiene la mayor densidad de bastones que convergen en células bipolares individuales. Dado que sus conos tienen una convergencia de señales mucho menor, la fóvea permite la visión más nítida que puede alcanzar el ojo. [2]
Aunque el bastón y los conos son una especie de mosaico , la transmisión de los receptores a los bipolares y a las células ganglionares no es directa. Dado que hay alrededor de 150 millones de receptores y solo 1 millón de fibras del nervio óptico, debe haber convergencia y, por lo tanto, mezcla de señales. Además, la acción horizontal de las células horizontales y amacrinas puede permitir que un área de la retina controle a otra (por ejemplo, un estímulo inhibiendo a otro). Esta inhibición es clave para disminuir la suma de mensajes enviados a las regiones superiores del cerebro. En algunos vertebrados inferiores (por ejemplo, la paloma), hay un control "centrífugo" de los mensajes, es decir, una capa puede controlar a otra, o regiones superiores del cerebro pueden impulsar las células nerviosas de la retina, pero en los primates esto no ocurre. [2]
Imágenes de capas con tomografía de coherencia óptica
Utilizando la tomografía de coherencia óptica (OCT) hay 18 capas que se pueden identificar en la retina. Las capas y la correlación anatómica son las siguientes: [22] [23] [24]
Desde la más interna a la más externa, las capas identificables por OCT son las siguientes:
| # | Capa OCT / Etiqueta convencional | Correlación anatómica | Reflectividad en OCT | Específico anatómico ¿límites? | Adicional referencias |
|---|---|---|---|---|---|
| 1 | Vítreo cortical posterior | Vítreo cortical posterior | Hiperreflectante | sí | [23] |
| 2 | Espacio prerretiniano | En los ojos donde el vítreo se ha desprendido total o parcialmente de la retina, este es el espacio creado entre la cara vítrea cortical posterior y la membrana limitante interna de la retina. | Hiporeflectante | [23] | |
| 3 | Membrana limitante interna (ILM) | Formado por pies terminales de celda de Müller (no está claro si se puede observar en OCT) | Hiperreflectante | No | [23] |
| Capa de fibras nerviosas (NFL) | Las células ganglionares de axones que viajan hacia el nervio óptico | ||||
| 4 | Capa de células ganglionares (GCL) | Cuerpos de células ganglionares (y algunas células amacrinas desplazadas ) | Hiporeflectante | [23] | |
| 5 | Capa plexiforme interna (IPL) | Sinapsis entre células bipolares , amacrinas y ganglionares | Hiperreflectante | [23] | |
| 6 | Capa nuclear interna (INL) | a) Cuerpos celulares horizontales , bipolares y amacrinos b) Núcleos de células de Müller | Hiporeflectante | [23] | |
| 7 | Capa plexiforme externa (OPL) | Sinapsis entre fotorreceptores , células bipolares y horizontales | Hiperreflectante | [23] | |
| 8 | (Mitad interior) Capa de fibras nerviosas de Henle (HL) | fotorreceptoras axones (fibras orientadas oblicuamente; no presentes en la retina periférica media o periférica) | Hiporeflectante | No | [23] |
| (Mitad exterior) Capa nuclear exterior (ONL) | Los cuerpos celulares de los fotorreceptores | ||||
| 9 | Membrana limitadora externa (ELM) | Hecho de zonulae adherentes entre las células de Müller y los segmentos internos de los fotorreceptores | Hiperreflectante | [23] | |
| 10 | Zona mioide (MZ) | La porción más interna del segmento interno del fotorreceptor (IS) que contiene:
| Hiporeflectante | No | [25] [26] |
| 11 | Zona elipsoide (EZ) | La porción más externa del segmento interno del fotorreceptor (IS) llena de mitocondrias | Muy hiperreflectante | No | [22] [27] [25] [23] [28] [29] |
| Unión IS / OS o línea de integridad del fotorreceptor (PIL) | El fotorreceptor que conecta los cilios que unen los segmentos internos y externos de las células fotorreceptoras. | ||||
| 12 | Segmentos externos del fotorreceptor (OS) | Los segmentos externos del fotorreceptor (OS) que contienen discos llenos de opsina , la molécula que absorbe los fotones. | Hiporeflectante | [30] [23] | |
| 13 | Zona de interdigitación (IZ) | Ápices de las células del RPE que encierran parte de los OS del cono. Poco distinguible del RPE. Anteriormente: "línea de puntas del segmento exterior del cono" (COST) | Hiperreflectante | No | |
| 14 | RPE / complejo de Bruch | Zona del fagosoma RPE | Muy hiperreflectante | No | [22] [23] |
| Zona de melanosoma del EPR | Hiporeflectante | ||||
| Zona de mitocondrias del RPE + Unión entre el RPE y la membrana de Bruch | Muy hiperreflectante | ||||
| 15 | Coriocapillaris | Capa delgada de reflectividad moderada en la coroides interna. | No | [23] | |
| dieciséis | Capa de Sattler | Capa gruesa de perfiles hiperreflectantes redondos u ovalados, con núcleos hiporeflectantes en la mitad de la coroides | [23] | ||
| 17 | Capa de Haller | Capa gruesa de perfiles hiperreflectantes de forma ovalada, con núcleos hiporeflectantes en la coroides exterior | [23] | ||
| 18 | Coyuntura coroidea-escleral | Zona en la coroides exterior con un marcado cambio de textura, en la que grandes perfiles circulares u ovoides colindan con un región homogénea de reflectividad variable | [23] | ||
Desarrollo
El desarrollo de la retina comienza con el establecimiento de los campos oculares mediados por las proteínas SHH y SIX3 , con el desarrollo posterior de las vesículas ópticas reguladas por las proteínas PAX6 y LHX2 . [31] El papel de Pax6 en el desarrollo del ojo fue elegantemente demostrado por Walter Gehring y sus colegas, quienes demostraron que la expresión ectópica de Pax6 puede conducir a la formación de ojos en las antenas, alas y patas de Drosophila . [32]La vesícula óptica da lugar a tres estructuras: la retina neural, el epitelio pigmentado retiniano y el tallo óptico. La retina neural contiene las células progenitoras de la retina (RPC) que dan lugar a los siete tipos de células de la retina. La diferenciación comienza con las células ganglionares de la retina y concluye con la producción de la glía de Muller. [33] Aunque cada tipo de célula se diferencia de los RPC en un orden secuencial, existe una superposición considerable en el momento en que se diferencian los tipos de células individuales. [31] Las señales que determinan el destino de una célula hija de RPC están codificadas por múltiples familias de factores de transcripción, incluidos los factores de homeodominio y bHLH . [34] [35]
Además de guiar la determinación del destino celular, existen señales en la retina para determinar los ejes dorsal-ventral (DV) y nasal-temporal (NT). El eje DV se establece mediante un gradiente ventral a dorsal de VAX2 , mientras que el eje NT está coordinado por la expresión de los factores de transcripción en horquilla FOXD1 y FOXG1 . Se forman gradientes adicionales dentro de la retina. [35] Esta distribución espacial puede ayudar en la orientación adecuada de los axones RGC que funcionan para establecer el mapa retinotópico. [31]
Suministro de sangre
Este artículo tiene varios problemas. Ayude a mejorarlo o discuta estos problemas en la página de discusión . ( Obtenga información sobre cómo y cuándo eliminar estos mensajes de plantilla )
|
La retina se estratifica en capas distintas, cada una de las cuales contiene tipos de células o compartimentos celulares específicos [36] que tienen metabolismos con diferentes requisitos nutricionales. [37] Para satisfacer estos requisitos, la arteria oftálmica se bifurca e irriga la retina a través de dos redes vasculares distintas: la red coroidea, que irriga la coroides y la retina externa, y la red retiniana, que irriga la capa interna de la retina. [38]
Mecanismos circulatorios
A primera vista, uno puede pensar que la retina de los vertebrados está "mal conectada" o "mal diseñada"; pero de hecho, la retina no podría funcionar si no estuviera invertida. La capa de fotorreceptores debe estar incrustada en el epitelio pigmentario de la retina (EPR), que realiza al menos siete funciones vitales, [39]uno de los más obvios es el suministro de oxígeno y otros nutrientes necesarios para el funcionamiento de los fotorreceptores. Estos nutrientes incluyen glucosa, ácidos grasos y retina. El proceso de amplificación de fotorreceptores de mamíferos utiliza grandes cantidades de energía para la visión en condiciones fotópicas (que requieren menos en condiciones escotópicas) y, por lo tanto, requiere el gran suministro de nutrientes suministrados por los vasos sanguíneos en la coroides, que se encuentra más allá del RPE. La coroides suministra aproximadamente el 75% de estos nutrientes a la retina y la vasculatura retiniana solo el 25%. [4]
Cuando la luz incide sobre el 11-cis-retinal (en los discos de los bastones y los conos), el 11-cis-retinal cambia a todo-trans-retinal, lo que desencadena cambios en las opsinas. Ahora, los segmentos externos no regeneran la retina de nuevo a la forma cis- una vez que ha sido cambiada por la luz. En cambio, la retina se bombea hacia el EPR circundante, donde se regenera y se transporta de regreso a los segmentos externos de los fotorreceptores. Esta función de reciclaje del RPE protege a los fotorreceptores contra el daño fotooxidativo [40] [41] y permite que las células fotorreceptoras tengan una vida útil de décadas.
En aves
La retina del pájaro carece de vasos sanguíneos, tal vez para permitir un paso de luz sin obstrucciones para formar imágenes, dando así una mejor resolución. Por lo tanto, es una opinión considerada que la retina del ave depende para la nutrición y el suministro de oxígeno de un órgano especializado, llamado "pecten" o pecten oculi , ubicado en el punto ciego o disco óptico. Este órgano es extremadamente rico en vasos sanguíneos y se cree que suministra nutrición y oxígeno a la retina de las aves por difusión a través del cuerpo vítreo. El pecten es muy rico en actividad de fosfatasa alcalina y células polarizadas en su porción de puente, ambos acordes con su función secretora. [42]Las células de pecten están repletas de gránulos de melanina oscura, que se ha teorizado para mantener este órgano caliente con la absorción de la luz parásita que cae sobre el pecten. Se considera que esto mejora la tasa metabólica del pecten, exportando así más moléculas nutritivas para cumplir con los estrictos requisitos de energía de la retina durante largos períodos de exposición a la luz. [43]
Identificación biométrica y diagnóstico de enfermedades.
Se sabe que las bifurcaciones y otras características físicas de la red vascular interna de la retina varían entre los individuos, [44] y estas variaciones individuales se han utilizado para la identificación biométrica y para la detección temprana del inicio de la enfermedad. El mapeo de bifurcaciones vasculares es uno de los pasos básicos en la identificación biométrica. [45] Los resultados de tales análisis de la estructura de los vasos sanguíneos de la retina pueden evaluarse contra los datos reales [46] de las bifurcaciones vasculares de las imágenes del fondo de ojo de la retina que se obtienen del conjunto de datos DRIVE. [47] Además, también se han identificado las clases de buques del conjunto de datos DRIVE, [48]y también está disponible un método automatizado para la extracción precisa de estas bifurcaciones. [49] Los cambios en la circulación sanguínea de la retina se observan con el envejecimiento [50] y la exposición a la contaminación del aire, [51] y pueden indicar enfermedades cardiovasculares como hipertensión y aterosclerosis. [52] [53] [54] La determinación del ancho equivalente de las arteriolas y vénulas cerca del disco óptico también es una técnica ampliamente utilizada para identificar los riesgos cardiovasculares. [55]
Función
La retina traduce una imagen óptica en impulsos neuronales que comienzan con la excitación modelada de los pigmentos sensibles al color de sus conos y bastones, las células fotorreceptoras de la retina . La excitación es procesada por el sistema neural y varias partes del cerebro que trabajan en paralelo para formar una representación del entorno externo en el cerebro.
Los conos responden a la luz brillante y median la visión de color de alta resolución durante la iluminación diurna (también llamada visión fotópica ). Las respuestas de los bastones están saturadas a los niveles de luz diurna y no contribuyen a la visión del patrón. Sin embargo, los bastones responden a la luz tenue y median la visión monocromática de baja resolución bajo niveles muy bajos de iluminación (llamada visión escotópica ). La iluminación en la mayoría de los entornos de oficina se encuentra entre estos dos niveles y se denomina visión mesópica . A niveles de luz mesópicos, tanto los bastones como los conos contribuyen activamente a la información del patrón. No está claro qué contribución hace la información de la varilla a la visión del patrón en estas circunstancias.
La respuesta de los conos a varias longitudes de onda de luz se denomina sensibilidad espectral. En la visión humana normal, la sensibilidad espectral de un cono cae en uno de los tres subtipos, a menudo llamados azul, verde y rojo, pero más exactamente conocidos como subtipos de conos sensibles a la longitud de onda corta, media y larga. Es la falta de uno o más de los subtipos de conos lo que hace que las personas tengan deficiencias en la visión del color o varios tipos de daltonismo . Estas personas no son ciegas a los objetos de un color en particular, pero no pueden distinguir entre los colores que pueden distinguir las personas con visión normal. Los humanos tenemos esta visión tricromática, mientras que la mayoría de los demás mamíferos carecen de conos con pigmento sensible al rojo y, por lo tanto, tienen una visión del color dicromática más pobre. Sin embargo, algunos animales tienen cuatro subtipos espectrales, por ejemplo, la trucha agrega un subgrupo ultravioleta a los subtipos corto, medio y largo que son similares a los humanos. Algunos peces también son sensibles a la polarización de la luz.
En los fotorreceptores, la exposición a la luz hiperpolariza la membrana en una serie de cambios graduales. El segmento de la celda exterior contiene un fotopigmento . Dentro de la célula, los niveles normales de monofosfato de guanosina cíclico (cGMP) mantienen abierto el canal de Na + y, por lo tanto, en el estado de reposo, la célula se despolariza. El fotón hace que la retina unida a la proteína receptora se isomerice a transretiniana . Esto hace que el receptor para activar múltiples proteínas G . Esto, a su vez, hace que la subunidad Ga de la proteína active una fosfodiesterasa (PDE6), que degrada cGMP, lo que resulta en el cierre de los canales iónicos activados por nucleótidos cíclicos de Na +.(GNC). Por tanto, la célula está hiperpolarizada. La cantidad de neurotransmisor liberado se reduce con luz brillante y aumenta a medida que caen los niveles de luz. El fotopigmento real se decolora con luz brillante y solo se reemplaza como un proceso químico, por lo que en una transición de luz brillante a oscuridad, el ojo puede tardar hasta treinta minutos en alcanzar la sensibilidad completa.
Cuando es así excitado por la luz, el fotoceptor envía una respuesta proporcional sinápticamente a las células bipolares que a su vez señalan a las células ganglionares de la retina . Los fotorreceptores también están entrecruzados por células horizontales y células amacrinas , que modifican la señal sináptica antes de que llegue a las células ganglionares, las señales neurales se entremezclan y combinan. De las células nerviosas de la retina, solo las células ganglionares de la retina y algunas células amacrinas crean potenciales de acción .
En las células ganglionares de la retina existen dos tipos de respuesta, dependiendo del campo receptivo de la célula. Los campos receptivos de las células ganglionares de la retina comprenden un área central, aproximadamente circular, donde la luz tiene un efecto sobre el disparo de la célula, y un entorno anular, donde la luz tiene el efecto opuesto. En las células ON, un incremento en la intensidad de la luz en el centro del campo receptivo hace que aumente la velocidad de disparo. En las celdas OFF, lo hace disminuir. En un modelo lineal, este perfil de respuesta está bien descrito por una diferencia de gaussianos y es la base para la detección de bordes.algoritmos. Más allá de esta simple diferencia, las células ganglionares también se diferencian por la sensibilidad cromática y el tipo de suma espacial. Las células que muestran una suma espacial lineal se denominan células X (también llamadas células ganglionares parvocelulares, P o enanas), y las que muestran una suma no lineal son células Y (también llamadas células ganglionares retinianas magnocelulares, M o parasol), aunque la correspondencia entre Las células X e Y (en la retina del gato) y las células P y M (en la retina de los primates) no es tan simple como parecía.
En la transferencia de señales visuales al cerebro, la vía visual , la retina se divide verticalmente en dos, una mitad temporal (más cercana a la sien) y una mitad nasal (más cercana a la nariz). Los axones de la mitad nasal cruzan el cerebro en el quiasma óptico para unirse con los axones de la mitad temporal del otro ojo antes de pasar al cuerpo geniculado lateral .
Aunque hay más de 130 millones de receptores retinianos, solo hay aproximadamente 1,2 millones de fibras (axones) en el nervio óptico. Por lo tanto, se realiza una gran cantidad de preprocesamiento dentro de la retina. La fóvea produce la información más precisa. A pesar de ocupar aproximadamente el 0,01% del campo visual (menos de 2 ° del ángulo visual ), aproximadamente el 10% de los axones del nervio óptico se dedican a la fóvea. Se ha determinado que el límite de resolución de la fóvea ronda los 10.000 puntos. La capacidad de información se estima en 500.000 bits por segundo (para obtener más información sobre bits, consulte la teoría de la información ) sin color o alrededor de 600.000 bits por segundo, incluido el color. [56]
Codificación espacial
Cuando la retina envía impulsos neuronales que representan una imagen al cerebro, codifica espacialmente (comprime) esos impulsos para que se ajusten a la capacidad limitada del nervio óptico. La compresión es necesario porque hay 100 veces más células fotorreceptoras que las células ganglionares . Esto se hace mediante la " descorrelación ", que se lleva a cabo mediante las "estructuras centro-circundantes", que son implementadas por las células bipolares y ganglionares.
Hay dos tipos de estructuras que rodean el centro de la retina: dentro y fuera del centro. Los centros tienen un centro ponderado positivamente y un entorno ponderado negativamente. Los fuera de los centros son todo lo contrario. La ponderación positiva se conoce más comúnmente como excitadora y la ponderación negativa como inhibitoria .
Estas estructuras que rodean el centro no son aparentes desde el punto de vista físico, en el sentido de que no se pueden ver al teñir muestras de tejido y examinar la anatomía de la retina. Las estructuras centro-circundantes son lógicas (es decir, matemáticamente abstractas) en el sentido de que dependen de las fuerzas de conexión entre las células bipolares y ganglionares. Se cree que la fuerza de la conexión entre las células es causada por el número y los tipos de canales iónicos incrustados en las sinapsis entre las células bipolares y ganglionares.
Las estructuras del centro y el entorno son matemáticamente equivalentes a los algoritmos de detección de bordes utilizados por los programadores de computadoras para extraer o mejorar los bordes en una fotografía digital. Por lo tanto, la retina realiza operaciones sobre los impulsos que representan la imagen para mejorar los bordes de los objetos dentro de su campo visual. Por ejemplo, en una imagen de un perro, un gato y un automóvil, son los bordes de estos objetos los que contienen más información. Para que las funciones superiores en el cerebro (o en una computadora para el caso) extraigan y clasifiquen objetos como un perro y un gato, la retina es el primer paso para separar los diversos objetos dentro de la escena.
Como ejemplo, la siguiente matriz está en el corazón de un algoritmo informático que implementa la detección de bordes. Esta matriz es la computadora equivalente a la estructura central-envolvente. En este ejemplo, cada caja (elemento) dentro de esta matriz estaría conectada a un fotorreceptor. El fotorreceptor del centro es el receptor actual que se está procesando. El fotorreceptor central se multiplica por el factor de peso +1. Los fotorreceptores circundantes son los "vecinos más cercanos" al centro y se multiplican por el valor -1/8. Finalmente, se calcula la suma de los nueve elementos. Esta suma se repite para cada fotorreceptor de la imagen desplazándose hacia la izquierda hasta el final de una fila y luego hacia la siguiente línea.
| -1/8 | -1/8 | -1/8 |
| -1/8 | +1 | -1/8 |
| -1/8 | -1/8 | -1/8 |
La suma total de esta matriz es cero, si todas las entradas de los nueve fotorreceptores tienen el mismo valor. El resultado cero indica que la imagen era uniforme (sin cambios) dentro de este pequeño parche. Las sumas negativas o positivas significan que la imagen estaba variando (cambiando) dentro de este pequeño parche de nueve fotorreceptores.
La matriz anterior es solo una aproximación de lo que realmente sucede dentro de la retina. Las diferencias son:
- El ejemplo anterior se llama "equilibrado". El término equilibrado significa que la suma de las ponderaciones negativas es igual a la suma de las ponderaciones positivas, de modo que se cancelan perfectamente. Las células ganglionares de la retina casi nunca están perfectamente equilibradas.
- La mesa es cuadrada, mientras que las estructuras que rodean el centro de la retina son circulares.
- Las neuronas operan en trenes de picos que viajan por los axones de las células nerviosas . Las computadoras operan en un solo número de punto flotante que es esencialmente constante desde cada píxel de entrada . (El píxel de la computadora es básicamente el equivalente a un fotorreceptor biológico).
- La retina realiza todos estos cálculos en paralelo mientras la computadora opera en cada píxel de uno en uno. La retina no realiza sumas ni cambios repetidos como lo haría una computadora.
- Finalmente, las células horizontales y amacrinas juegan un papel importante en este proceso, pero eso no está representado aquí.
A continuación, se muestra un ejemplo de una imagen de entrada y cómo la modificaría la detección de bordes.
Una vez que la imagen está codificada espacialmente por las estructuras centrales circundantes, la señal se envía a lo largo del nervio óptico (a través de los axones de las células ganglionares) a través del quiasma óptico hasta el LGN ( núcleo geniculado lateral ). La función exacta del LGN se desconoce en este momento. La salida del LGN luego se envía a la parte posterior del cerebro. Específicamente, la salida del LGN "irradia" hacia la corteza visual primaria V1 .
Flujo de señal simplificado: Fotorreceptores → Bipolar → Ganglio → Quiasma → LGN → Corteza V1
Significación clínica
Hay muchas enfermedades o trastornos heredados y adquiridos que pueden afectar la retina. Algunos de ellos incluyen:
- La retinosis pigmentaria es un grupo de enfermedades genéticas que afectan la retina y provocan la pérdida de la visión nocturna y la visión periférica.
- La degeneración macular describe un grupo de enfermedades caracterizadas por la pérdida de la visión central debido a la muerte o deterioro de las células de la mácula .
- La distrofia cono-bastón (CORD) describe una serie de enfermedades en las que la pérdida de la visión es causada por el deterioro de los conos y / o bastones de la retina.
- En la separación de la retina, la retina se desprende de la parte posterior del globo ocular. Ignipuntura es un método de tratamiento obsoleto. El término desprendimiento de retina se utiliza para describir una separación de la retina neurosensorial del epitelio pigmentario de la retina . [57] Existen varios métodos de tratamiento modernos para reparar un desprendimiento de retina: retinopexia neumática , hebilla escleral , crioterapia , fotocoagulación con láser y vitrectomía pars plana .
- Tanto la hipertensión como la diabetes mellitus pueden dañar los diminutos vasos sanguíneos que irrigan la retina, provocando retinopatía hipertensiva y retinopatía diabética .
- El retinoblastoma es un cáncer de retina.
- Enfermedades de la retina en perros incluyen displasia de la retina , atrofia progresiva de retina , y la degeneración retiniana adquirida súbita .
- La lipemia retinal es una apariencia blanca de la retina y puede ocurrir por depósito de lípidos en la deficiencia de lipoproteína lipasa .
- Desprendimiento de retina . En ocasiones, la retina neural se desprende del epitelio pigmentario. En algunos casos, la causa de tal desprendimiento es una lesión en el globo ocular que permite que se acumule líquido o sangre entre la retina neural y el epitelio pigmentario. En ocasiones, el desprendimiento es causado por la contractura de finas fibrillas de colágeno en el humor vítreo, que tiran de áreas de la retina hacia el interior del globo. [21]
- Ceguera nocturna : La ceguera nocturna ocurre en cualquier persona con deficiencia severa de vitamina A. La razón de esto es que sin vitamina A, las cantidades de retina y rodopsina que se pueden formar se reducen gravemente. Esta condición se llama ceguera nocturna porque la cantidad de luz disponible durante la noche es demasiado pequeña para permitir una visión adecuada en personas con deficiencia de vitamina A. [dieciséis]
Además, la retina se ha descrito como una "ventana" al cerebro y al cuerpo, dado que las anomalías detectadas a través de un examen de la retina pueden descubrir enfermedades tanto neurológicas como sistémicas. [58]
Diagnóstico
Se encuentran disponibles varios instrumentos diferentes para el diagnóstico de enfermedades y trastornos que afectan a la retina. La oftalmoscopia y la fotografía del fondo de ojo se han utilizado durante mucho tiempo para examinar la retina. Recientemente, se ha utilizado la óptica adaptativa para obtener imágenes de bastones y conos individuales en la retina humana viva, y una empresa con sede en Escocia ha diseñado una tecnología que permite a los médicos observar la retina completa sin ninguna molestia para los pacientes. [59]
El electrorretinograma se utiliza para medir de forma no invasiva la actividad eléctrica de la retina, que se ve afectada por determinadas enfermedades. Una tecnología relativamente nueva, que ahora está ampliamente disponible, es la tomografía de coherencia óptica (OCT). Esta técnica no invasiva permite obtener un tomograma tridimensional volumétrico o de corte transversal de alta resolución de las estructuras finas de la retina, con calidad histológica . El análisis de los vasos retinianos es un método no invasivo para examinar las pequeñas arterias y venas de la retina que permite sacar conclusiones sobre la morfología y la función de los pequeños vasos en otras partes del cuerpo humano. Se ha establecido como un predictor deenfermedad cardiovascular [60] y parece tener, según un estudio publicado en 2019, potencial en la detección temprana de la enfermedad de Alzheimer. [61]
Tratamiento
El tratamiento depende de la naturaleza de la enfermedad o trastorno.
Modalidades de tratamiento habituales
Las siguientes son modalidades habituales de tratamiento para la enfermedad de la retina:
- Intravítrea medicación, tales como anti-VEGF o corticosteroides agentes
- Cirugía vitreorretiniana
- Uso de complementos nutricionales
- Modificación de los factores de riesgo sistémicos de enfermedad de la retina.
Modalidades de tratamiento poco frecuentes
Métodos de tratamiento raros o poco comunes para la enfermedad de la retina. |
|---|
Terapia génica retiniana La terapia genética es prometedora como una vía potencial para curar una amplia gama de enfermedades de la retina. Esto implica el uso de un virus no infeccioso para transportar un gen a una parte de la retina. Los vectores de virus adenoasociados recombinantes (rAAV) poseen una serie de características que los hacen ideales para la terapia génica retiniana, incluida la falta de patogenicidad, inmunogenicidad mínima y la capacidad de transducir células postmitóticas de manera estable y eficiente. [62] Los vectores rAAV se utilizan cada vez más por su capacidad para mediar en la transducción eficiente del epitelio pigmentario de la retina (EPR), las células fotorreceptoras y las células ganglionares de la retina.. Cada tipo de célula puede ser dirigido específicamente eligiendo la combinación apropiada de serotipo AAV , promotor y sitio de inyección intraocular. Varios ensayos clínicos ya han informado resultados positivos con el uso de rAAV para tratar la amaurosis congénita de Leber , lo que demuestra que la terapia era segura y eficaz. [63] [64] No hubo eventos adversos graves y los pacientes de los tres estudios mostraron una mejoría en su función visual medida por varios métodos. Los métodos utilizados variaron entre los tres ensayos, pero incluyeron tanto métodos funcionales como la agudeza visual [64] [65] [66] y la movilidad funcional [65] [66] [67] , así como medidas objetivas que son menos susceptibles al sesgo , como la capacidad de la pupila para responder a la luz [63] [68] y mejoras en la resonancia magnética funcional.[69] Las mejoras se mantuvieron a largo plazo, y los pacientes continuaron mejorando después de más de 1,5 años. [63] [64] La arquitectura única de la retina y su entorno relativamente privilegiado para el sistema inmunológico ayudan en este proceso. [70] Las uniones estrechas que forman la barrera hemato-retiniana separan el espacio subretiniano del suministro de sangre, protegiéndolo así de los microbios y la mayoría de los daños inmunomediados, y mejorando su potencial para responder a las terapias mediadas por vectores. La anatomía altamente compartimentada del ojo facilita la administración precisa de suspensiones de vectores terapéuticos a tejidos específicos bajo visualización directa utilizando técnicas microquirúrgicas. [71] En el entorno protegido de la retina, los vectores AAV pueden mantener altos niveles de transgénexpresión en el epitelio pigmentado de la retina (EPR), fotorreceptores o células ganglionares durante largos períodos de tiempo después de un único tratamiento. Además, el ojo y el sistema visual se pueden monitorizar de forma rutinaria y fácilmente para la función visual y los cambios estructurales de la retina después de las inyecciones con tecnología avanzada no invasivo, tales como agudeza visual, sensibilidad al contraste , fundus auto-fluorescencia (FAF), oscuro-adaptado umbrales visuales , diámetros vasculares, pupilometría, electrorretinografía (ERG), ERG multifocal y tomografía de coherencia óptica (OCT). [72] Esta estrategia es eficaz contra una serie de enfermedades de la retina que se han estudiado, incluidas las enfermedades neovasculares que son características de la degeneración macular relacionada con la edad , la retinopatía diabética y la retinopatía del prematuro . Dado que la regulación de la vascularización en la retina madura implica un equilibrio entre factores de crecimiento positivos endógenos , como el factor de crecimiento endotelial vascular (VEGF) e inhibidores de la angiogénesis , como el factor derivado del epitelio pigmentario ( PEDF)), se ha demostrado que la expresión mediada por rAAV de PEDF, angiostatina y el receptor soluble de VEGF sFlt-1, que son proteínas antiangiogénicas, reducen la formación de vasos aberrantes en modelos animales. [73] Dado que las terapias génicas específicas no pueden usarse fácilmente para tratar una fracción significativa de pacientes con distrofia retiniana, existe un gran interés en desarrollar una terapia de factor de supervivencia de aplicación más general. Los factores neurotróficos tienen la capacidad de modular el crecimiento neuronal durante el desarrollo para mantener las células existentes y permitir la recuperación de poblaciones neuronales dañadas en el ojo. AAV que codifica factores neurotróficos como los miembros de la familia del factor de crecimiento de fibroblastos (FGF) y GDNF protegieron a los fotorreceptores de la apoptosis o ralentizaron la muerte celular. [73] Trasplante de órganos Se ha intentado el trasplante de retinas, pero sin mucho éxito. En el MIT , la Universidad del Sur de California, la Universidad RWTH Aachen y la Universidad de Nueva Gales del Sur , se está desarrollando una "retina artificial": un implante que evitará los fotorreceptores de la retina y estimulará las células nerviosas adheridas directamente, con señales. desde una cámara digital. |
Historia
Alrededor del 300 a. C. , Herophilos identificó la retina a partir de disecciones de ojos de cadáveres. Lo llamó capa aracnoidea , por su parecido con una telaraña, y retiforme , por su parecido con una red de lanzamiento. El término aracnoides pasó a referirse a una capa alrededor del cerebro; el término retiforme pasó a referirse a la retina . [74]
Entre 1011 y 1021 d.C., Ibn Al-Haytham publicó numerosos experimentos que demostraban que la vista se produce a partir de la luz que se refleja de los objetos en el ojo. Esto es consistente con la teoría de la intromisión y contra la teoría de la emisión , la teoría de que la vista se produce a partir de los rayos emitidos por los ojos. Sin embargo, Ibn Al-Haytham decidió que la retina no podía ser responsable de los inicios de la visión porque la imagen formada en ella estaba invertida. En su lugar, decidió que debía comenzar en la superficie de la lente. [75]
En 1604, Johannes Kepler elaboró la óptica del ojo y decidió que la retina debía estar donde comienza la vista. Dejó en manos de otros científicos reconciliar la imagen retiniana invertida con nuestra percepción del mundo como vertical. [76]
En 1894, Santiago Ramón y Cajal publicó la primera gran caracterización de las neuronas de la retina en Retina der Wirbelthiere ( La retina de los vertebrados ). [77]
George Wald , Haldan Keffer Hartline y Ragnar Granit ganaron el Premio Nobel de Fisiología o Medicina en 1967 por su investigación científica sobre la retina. [78]
Un estudio reciente de la Universidad de Pensilvania calculó que el ancho de banda aproximado de las retinas humanas es de 8,75 megabits por segundo, mientras que la tasa de transferencia retiniana de un conejillo de indias es de 875 kilobits por segundo. [79]
MacLaren & Pearson y sus colegas del University College London y el Moorfields Eye Hospital en Londres, en 2006, demostraron que las células fotorreceptoras podrían trasplantarse con éxito en la retina del ratón si las células del donante se encontraran en una etapa crítica de desarrollo. [80] Recientemente, Ader y sus colegas en Dublín demostraron, utilizando el microscopio electrónico, que los fotorreceptores trasplantados formaban conexiones sinápticas. [81]
En 2012, Sebastian Seung y su laboratorio en el MIT lanzaron EyeWire , un juego de ciencia ciudadana en línea donde los jugadores rastrean neuronas en la retina. [82] Los objetivos del proyecto EyeWire son identificar tipos de células específicas dentro de las amplias clases conocidas de células de la retina y trazar un mapa de las conexiones entre las neuronas de la retina, lo que ayudará a determinar cómo funciona la visión. [83] [84]
Imágenes Adicionales
Las estructuras del ojo etiquetadas
Otra vista del ojo y las estructuras del ojo etiquetadas
Ilustración de la imagen "vista" por la retina independientemente del procesamiento del nervio óptico y la corteza estriada.
Ver también
- Virus adeno asociado y terapia génica de la retina humana
- Charles Schepens : "el padre de la cirugía de retina moderna"
- Evolución del ojo
- Retina dúplex
- Escaneo de retina
- Lista de variantes de xantoma asociadas con subtipos de hiperlipoproteinemia
- Rodopsina
Referencias
- ^ J, Krause William (2005). Histología humana esencial de Krause para estudiantes de medicina . Boca Raton, FL: Universal Publishers. ISBN 978-1-58112-468-2.
- ^ a b c d e f g "Recepción sensorial: Visión humana: estructura y función del ojo humano" vol. 27, Encyclopædia Britannica, 1987
- ^ "Copia archivada" . Archivado desde el original el 11 de marzo de 2013 . Consultado el 11 de febrero de 2013 .Mantenimiento de CS1: copia archivada como título ( enlace )
- ↑ a b Kolb, Helga (1995). "Anatomía simple de la retina" . Webvision . PMID 21413391 . Consultado el 1 de enero de 2018 .
- ^ Kolb, Helga. "Fotorreceptores" . Webvision . Consultado el 11 de enero de 2018 .
- ^ Franze K, Grosche J, Skatchkov SN, Schinkinger S, Foja C, Schild D, Uckermann O, Travis K, Reichenbach A, Guck J (2007). "Las células de Muller son fibras ópticas vivas en la retina de los vertebrados" . Proc. Natl. Acad. Sci. USA . 104 (20): 8287–8292. Código Bibliográfico : 2007PNAS..104.8287F . doi : 10.1073 / pnas.0611180104 . PMC 1895942 . PMID 17485670 .
- ^ Baker, Oliver (23 de abril de 2010). "Enfoque: células oculares como tubos de luz". Enfoque de revisión física . Vol. 25 no. 15. doi : 10.1103 / physrevfocus.25.15 .
- ↑ a b Bringmann A, Syrbe S, Görner K, Kacza J, Francke M, Wiedemann P, Reichenbach A (2018). "La fóvea de los primates: estructura, función y desarrollo". Prog Retin Eye Res . 66 : 49–84. doi : 10.1016 / j.preteyeres.2018.03.006 . PMID 29609042 . S2CID 5045660 .
- ^ Sperling, L .; Hubbard, R. (1 de febrero de 1975). "Retinocromo de calamar" . La Revista de Fisiología General . 65 (2): 235–251. doi : 10.1085 / jgp.65.2.235 . ISSN 0022-1295 . PMC 2214869 . PMID 235007 .
- ^ "Cómo ven el mundo las arañas - Museo Australiano" . www.australian.museum . Archivado desde el original el 12 de septiembre de 2017 . Consultado el 5 de diciembre de 2017 .
- ^ Drazen, JC; Yeh, J .; Friedman, J .; Condon, N. (junio de 2011). "Metabolismo y actividades enzimáticas del hagfish de aguas poco profundas y profundas del Océano Pacífico". Bioquímica y fisiología comparada Parte A: Fisiología molecular e integrativa . 159 (2): 182–187. doi : 10.1016 / j.cbpa.2011.02.018 . PMID 21356325 .
- ^ Fundamentos de la visión Archivado el 3 de diciembre de 2013 en Wayback Machine , Brian A. Wandell
- ^ La túnica retiniana. Archivado el 18 de mayo de 2007 en la Wayback Machine Virginia – Maryland Regional College of Veterinary Medicine
- ^ Goldberg AF, Moritz OL, Williams DS (2016). "Base molecular para la arquitectura del segmento exterior del fotorreceptor" . Prog Retin Eye Res . 55 : 52–81. doi : 10.1016 / j.preteyeres.2016.05.003 . PMC 5112118 . PMID 27260426 .
- ↑ Arshavsky VY, Burns ME (2012). "Señalización de fotorreceptores: apoyo a la visión en una amplia gama de intensidades de luz" . J Biol Chem . 287 (3): 1620–1626. doi : 10.1074 / jbc.R111.305243 . PMC 3265842 . PMID 22074925 .
- ^ a b Fisiología de Guyton y Hall . pag. 612.
- ^ Gorrión JR, Hicks D, Hamel CP (2010). "El epitelio pigmentario de la retina en salud y enfermedad" . Curr Mol Med . 10 (9): 802–823. doi : 10.2174 / 156652410793937813 . PMC 4120883 . PMID 21091424 .
- ^ Letelier J, Bovolenta P, Martínez-Morales JR (2017). "El epitelio pigmentado, un socio brillante contra la degeneración de los fotorreceptores". J Neurogenet . 31 (4): 203–215. doi : 10.1080 / 01677063.2017.1395876 . PMID 29113536 . S2CID 1351539 .
- ^ Pastor, Gordon (2004). La organización sináptica del cerebro . Nueva York: Oxford University Press. págs. 217 –225. ISBN 978-0-19-515956-1.
- ^ Romer, Alfred Sherwood; Parsons, Thomas S. (1977). El cuerpo de los vertebrados . Filadelfia, PA: Holt-Saunders International. pag. 465. ISBN 978-0-03-910284-5.
- ^ a b Fisiología de Guyton y Hall . pag. 609.
- ^ a b c Cuenca, Nicolás; Ortuño-Lizarán, Isabel; Pinilla, Isabel (marzo de 2018). "Caracterización celular de OCT y bandas retinianas externas mediante marcadores de inmunohistoquímica específicos e implicaciones clínicas" (PDF) . Oftalmología . 125 (3): 407–422. doi : 10.1016 / j.ophtha.2017.09.016 . hdl : 10045/74474 . PMID 29037595 .
- ^ a b c d e f g h i j k l m n o p q Staurenghi, Giovanni; Sadda, Srinivas; Chakravarthy, Usha; Spaide, Richard F. (2014). "Léxico propuesto para hitos anatómicos en la tomografía de coherencia óptica de dominio espectral del segmento posterior normal". Oftalmología . 121 (8): 1572-1578. doi : 10.1016 / j.ophtha.2014.02.023 . PMID 24755005 .
- ^ Tomografía de coherencia óptica de dominio espectral en enfermedades maculares . Meyer, Carsten H .; Saxena, Sandeep; Sadda, SriniVas R. Nueva Delhi: Springer. 2017. ISBN 978-8132236108. OCLC 964379175 .CS1 maint: otros ( enlace )
- ↑ a b Hildebrand, Göran Darius; Fielder, Alistair R. (2011). Retina pediátrica . Springer, Berlín, Heidelberg. págs. 39–65. doi : 10.1007 / 978-3-642-12041-1_2 . ISBN 978-3642120404.
- ^ Turgut, Burak; Universidad, Fırat; Medicina, Facultad de; Oftalmología, Departamento de; Elazig; Turquía (2017). "Terminología pasada y presente de las estructuras retinianas y coroideas en la tomografía de coherencia óptica" . Revista oftálmica europea . 11 (1): 59. doi : 10.17925 / eor.2017.11.01.59 .
- ^ "Capas de la retina externa como predictores de la pérdida de visión" . Revisión de Oftalmología .
- ^ "El ABC de OCT" . Revisión de Optometría .
- ^ Sherman, J (junio de 2009). "La línea de integridad del fotorreceptor se une a la capa de fibras nerviosas como clave para el diagnóstico clínico". Optometría . 80 (6): 277–278. doi : 10.1016 / j.optm.2008.12.006 . PMID 19465337 .
- ^ Boston, Marco A. Bonini Filho, MD y Andre J. Witkin, MD. "Capas de la retina externa como predictores de la pérdida de visión" . Consultado el 7 de abril de 2018 .
- ^ a b c Heavner, W; Pevny, L (1 de diciembre de 2012). "Desarrollo ocular y retinogénesis" . Perspectivas de Cold Spring Harbor en biología . 4 (12): a008391. doi : 10.1101 / cshperspect.a008391 . PMC 3504437 . PMID 23071378 .
- ^ Halder, G; Callaerts, P; Gehring, WJ (24 de marzo de 1995). "Inducción de ojos ectópicos por expresión dirigida del gen sin ojos en Drosophila". Ciencia . 267 (5205): 1788–1792. Código Bibliográfico : 1995Sci ... 267.1788H . doi : 10.1126 / science.7892602 . PMID 7892602 .
- ^ Cepko, Connie (septiembre de 2014). "Las células progenitoras de la retina intrínsecamente diferentes producen tipos específicos de progenie". Nature Reviews Neurociencia . 15 (9): 615–627. doi : 10.1038 / nrn3767 . ISSN 1471-003X . PMID 25096185 . S2CID 15038502 .
- ^ Hatakeyama, J; Kageyama, R (febrero de 2004). "Determinación del destino de las células retinianas y factores bHLH". Seminarios en Biología Celular y del Desarrollo . 15 (1): 83–89. doi : 10.1016 / j.semcdb.2003.09.005 . PMID 15036211 .
- ^ a b Lo Giudice, Quentin; Leleu, Marion; La Manno, Gioele; Fabre, Pierre J. (1 de septiembre de 2019). "Lógica transcripcional unicelular de la especificación del destino celular y la guía del axón en las neuronas retinianas de nacimiento temprano" . Desarrollo . 146 (17): dev178103. doi : 10.1242 / dev.178103 . ISSN 0950-1991 . PMID 31399471 .
- ^ Remington, Lee Ann (2012). Anatomía clínica y fisiología del sistema visual (3ª ed.). San Luis: Elsevier / Butterworth-Heinemann. ISBN 978-1-4377-1926-0. OCLC 745905738 .
- ^ Yu, DY; Yu, PK; Cringle, SJ; Kang, MH; Su, EN (mayo de 2014). "Características funcionales y morfológicas de la vasculatura retiniana y coroidea". Progresos en la investigación de la retina y los ojos . 40 : 53–93. doi : 10.1016 / j.preteyeres.2014.02.001 . PMID 24583621 . S2CID 21312546 .
- ^ Kiel, Jeffrey W. Anatomía . Morgan & Claypool Life Sciences. Archivado desde el original el 5 de diciembre de 2017 . Consultado el 17 de abril de 2017 .
- ^ Strauss, Olaf. "El epitelio pigmentario de la retina" . Webvision . Consultado el 1 de enero de 2018 .
- ^ Fotobiología de la retina "Daño de la retina inducido por la luz" . Archivado desde el original el 9 de agosto de 2012 . Consultado el 27 de julio de 2012 .
- ^ Representación esquemática del desprendimiento del disco y la recuperación del fagosoma en la célula epitelial del pigmento "Copia archivada" . Archivado desde el original el 21 de septiembre de 2012 . Consultado el 27 de julio de 2012 .Mantenimiento de CS1: copia archivada como título ( enlace )
- ^ Bawa SR; YashRoy RC (1972). "Efecto de la adaptación a la luz y la oscuridad sobre la retina y el pecten de pollo" . Investigación ocular experimental . 13 (1): 92–97. doi : 10.1016 / 0014-4835 (72) 90129-7 . PMID 5060117 . Archivado desde el original el 9 de octubre de 2014.
- ^ Bawa, SR; YashRoy, RC (1974). "Estructura y función del buitre pecten" . Órganos de tejidos de células . 89 (3): 473–480. doi : 10.1159 / 000144308 . PMID 4428954 . Archivado desde el original el 14 de julio de 2015.
- ^ Sherman, T (1981). "Sobre la conexión de vasos grandes a pequeños - el significado de la ley de Murray" . Revista de fisiología general . 78 (4): 431–453. doi : 10.1085 / jgp.78.4.431 . PMC 2228620 . PMID 7288393 .
- ^ Azzopardi G .; Petkov N. (2011). Detección de bifurcaciones vasculares retinianas mediante filtros entrenables tipo V4, en Análisis informático de imágenes y patrones (CAIP), Sevilla (PDF) . Apuntes de conferencias en Ciencias de la Computación. 6854 . págs. 451–459. doi : 10.1007 / 978-3-642-23672-3_55 . ISBN 978-3-642-23671-6. Archivado (PDF) desde el original el 9 de agosto de 2017.
- ^ "Imágenes del fondo de ojo de la retina - verdad de tierra de bifurcaciones vasculares y cruces" . Universidad de Groningen . Consultado el 20 de abril de 2018 .
- ^ "DRIVE: Imágenes digitales de retina para extracción de vasos" . Instituto de Ciencias de la Imagen, Universidad de Utrecht . Consultado el 20 de abril de 2018 .
- ^ Qureshi, TA; Habib, M .; Hunter, A .; Al-Diri, B. (junio de 2013). Un punto de referencia clasificado de arterias / venas etiquetado manualmente para el conjunto de datos DRIVE . Actas del 26º Simposio internacional de IEEE sobre sistemas médicos basados en computadora . págs. 485–488. doi : 10.1109 / cbms.2013.6627847 . ISBN 978-1-4799-1053-3. S2CID 7705121 .
- ^ Qureshi, TA; Hunter, A .; Al-Diri, B. (junio de 2014). Un marco bayesiano para la configuración local de las uniones retinianas . 2014 IEEE Conference on Computer Vision and Pattern Recognition . págs. 3105–3110. CiteSeerX 10.1.1.1026.949 . doi : 10.1109 / cvpr.2014.397 . ISBN 978-1-4799-5118-5. S2CID 14654500 .
- ^ Adar SD, Klein R, Klein BE, Szpiro AA, Cotch MF, Wong TY, et al. (2010). "Contaminación del aire y la microvasculatura: una evaluación transversal de imágenes retinianas in vivo en el estudio multiétnico poblacional de aterosclerosis (MESA)" . PLOS Med . 7 (11): e1000372. doi : 10.1371 / journal.pmed.1000372 . PMC 2994677 . PMID 21152417 .
- ^ Louwies, Tijs; Panis, Luc Int; Kicinski, Michal; Boever, Patrick De; Nawrot, Tim S. (2013). "Respuestas microvasculares de la retina a cambios a corto plazo en la contaminación del aire por partículas en adultos sanos" . Perspectivas de salud ambiental . 121 (9): 1011–1016. doi : 10.1289 / ehp.1205721 . PMC 3764070 . PMID 23777785 .
- ^ Tso, Mark OM; Jampol, Lee M. (1982). "Fisiopatología de la retinopatía hipertensiva". Oftalmología . 89 (10): 1132-1145. doi : 10.1016 / s0161-6420 (82) 34663-1 . PMID 7155524 .
- ↑ Chapman, N .; Dell'omo, G .; Sartini, MS; Witt, N .; Hughes, A .; Thom, S .; Pedrinelli, R. (1 de agosto de 2002). "La enfermedad vascular periférica se asocia con relaciones anormales de diámetro arteriolar en bifurcaciones en la retina humana". Ciencia Clínica . 103 (2): 111-116. doi : 10.1042 / cs1030111 . ISSN 0143-5221 . PMID 12149100 .
- ^ Patton, N .; Aslam, T .; MacGillivray, T .; Deary, I .; Dhillon, B .; Eikelboom, R .; Yogesan, K .; Constable, I. (2006). "Análisis de imágenes retinianas: conceptos, aplicaciones y potencialidades". Progresos en la investigación de la retina y los ojos . 25 (1): 99-127. doi : 10.1016 / j.preteyeres.2005.07.001 . PMID 16154379 . S2CID 7434103 .
- ^ Wong TY, Knudtson MD, Klein R, Klein BE, Meuer SM, Hubbard LD (2004). "Medición asistida por computadora de los diámetros de los vasos retinianos en el estudio Beaver Dam Eye: metodología, correlación entre los ojos y efecto de los errores de refracción". Oftalmología . 111 (6): 1183-1190. doi : 10.1016 / j.ophtha.2003.09.039 . PMID 15177969 .
- ^ Manual de tecnología de visualización visual . Chen, Janglin., Cranton, Wayne., Fihn, Mark. (2ª ed.). Cham, Suiza: Springer. 2016. ISBN 9783319143460. OCLC 962009228 .CS1 maint: otros ( enlace )
- ^ Retina (4ª ed.). Filadelfia: Elsevier / Mosby. 2006. págs. 2013-2015. ISBN 978-0-323-02598-0. OCLC 62034580 .
- ^ Frith, Peggy; Mehta, Arpan R (noviembre de 2021). "La retina como ventana al cerebro" . The Lancet Neurology . 20 (11): 892. doi : 10.1016 / S1474-4422 (21) 00332-X .
- ^ Mirando hacia el futuro Ingenia , marzo de 2007
- ^ Seidelmann, SB; et al. (1 de noviembre de 2016). "Calibres de vasos retinianos en la predicción de resultados cardiovasculares a largo plazo" . Circulación . 134 (18): 1328-1338. doi : 10.1161 / CIRCULATIONAHA.116.023425 . PMC 5219936 . PMID 27682886 .
- ^ Querques, G; et al. (11 de enero de 2019). "Cambios funcionales y morfológicos de los vasos retinianos en la enfermedad de Alzheimer y deterioro cognitivo leve" . Informes científicos . 9 (63): 63. Bibcode : 2019NatSR ... 9 ... 63Q . doi : 10.1038 / s41598-018-37271-6 . PMC 6329813 . PMID 30635610 .
- ^ Dinculescu Astra; Glushakova Lyudmyla; Seok-Hong Min; Hauswirth William W. (2005). "Terapia génica vectorizada por virus adenoasociados para la enfermedad de la retina". Terapia de genes humanos . 16 (6): 649–663. doi : 10.1089 / hum.2005.16.649 . PMID 15960597 .
- ^ a b c Cideciyan AV; Hauswirth WW; Aleman TS; Kaushal S .; Schwartz SB; Boye SL; Windsor EAM; et al. (2009). "Terapia génica humana RPE65 para amaurosis congénita de Leber: persistencia de mejoras visuales tempranas y seguridad en 1 año" . Terapia de genes humanos . 20 (9): 999–1004. doi : 10.1089 / hum.2009.086 . PMC 2829287 . PMID 19583479 .
- ^ a b c Simonelli F .; Maguire AM; Testa F .; Pierce EA; Mingozzi F .; Bennicelli JL; Rossi S .; et al. (2010). "La terapia génica para la amaurosis congénita de Leber es segura y eficaz hasta 1,5 años después de la administración del vector" . Terapia molecular . 18 (3): 643–650. doi : 10.1038 / mt.2009.277 . PMC 2839440 . PMID 19953081 .
- ^ a b Maguire AM; Simonelli F .; Pierce EA; Pugh EN; Mingozzi F .; Bennicelli J .; Banfi S .; et al. (2008). "Seguridad y eficacia de la transferencia de genes para la amaurosis congénita de Leber" . La Revista de Medicina de Nueva Inglaterra . 358 (21): 2240–2248. doi : 10.1056 / NEJMoa0802315 . PMC 2829748 . PMID 18441370 .
- ^ a b Maguire AM; Alto KA; Auricchio A .; Wright JF; Pierce EA; Testa F .; Mingozzi F .; et al. (2009). "Efectos dependientes de la edad de la terapia génica RPE65 para la amaurosis congénita de Leber: un ensayo de escalada de dosis de fase 1" . Lancet . 374 (9701): 1597–1605. doi : 10.1016 / S0140-6736 (09) 61836-5 . PMC 4492302 . PMID 19854499 .
- ^ Bainbridge JWB; Smith AJ; Barker SS; Robbie S .; Henderson R .; Balaggan K .; Viswanathan A .; et al. (2008). "Efecto de la terapia génica sobre la función visual en la amaurosis congénita de Leber" (PDF) . La Revista de Medicina de Nueva Inglaterra . 358 (21): 2231–2239. CiteSeerX 10.1.1.574.4003 . doi : 10.1056 / NEJMoa0802268 . PMID 18441371 . Archivado (PDF) desde el original el 11 de agosto de 2017.
- ^ Hauswirth WW; Aleman TS; Kaushal S .; Cideciyan AV; Schwartz SB; Wang L .; Conlon TJ; et al. (2008). "Tratamiento de la amaurosis congénita de Leber debido a mutaciones de RPE65 por inyección subretiniana ocular de vector genético del virus adenoasociado: resultados a corto plazo de un ensayo de fase I" . Terapia de genes humanos . 19 (10): 979–990. doi : 10.1089 / hum.2008.107 . PMC 2940541 . PMID 18774912 .
- ^ Ashtari M .; Cyckowski LL; Monroe JF; Marshall KA; Chung DC; Auricchio A .; Simonelli F .; et al. (2011). "La corteza visual humana responde a la recuperación de la función de la retina mediada por la terapia génica" . La Revista de Investigación Clínica . 121 (6): 2160–2168. doi : 10.1172 / JCI57377 . PMC 3104779 . PMID 21606598 .
- ^ Bennett J (2003). "Respuesta inmune después de la administración intraocular de vectores virales recombinantes" . Terapia génica . 10 (11): 977–982. doi : 10.1038 / sj.gt.3302030 . PMID 12756418 .
- ^ Curace Enrico M .; Auricchio Alberto (2008). "Versatilidad de los vectores AAV para la transferencia de genes retinianos" . Investigación de la visión . 48 (3): 353–359. doi : 10.1016 / j.visres.2007.07.027 . PMID 17923143 . S2CID 9926758 .
- ^ den Hollander, Anneke I .; Roepman, Ronald; Koenekoop, Robert K .; Cremers, Frans PM (2008). "Amaurosis congénita de Leber: genes, proteínas y mecanismos de la enfermedad". Progresos en la investigación de la retina y los ojos . 27 (4): 391–419. doi : 10.1016 / j.preteyeres.2008.05.003 . PMID 18632300 . S2CID 30202286 .
- ↑ a b Rolling, F. (2004). "Transferencia génica recombinante mediada por AAV a la retina: perspectivas de la terapia génica" . Terapia génica . 11 (S1): S26 – S32. doi : 10.1038 / sj.gt.3302366 . ISSN 0969-7128 . PMID 15454954 .
- ^ Dobson, JF (1925). Herophilus de Alejandría. Actas de la Royal Society of Medicine, 18, 19-32. https://doi.org/10.1177/003591572501801704
- ^ Sabra, AI (Ed.). (1011-1021 / 1989). La óptica de Ibn Al-Haytham: Libros I-III: Sobre visión directa (AI Sabra, Trad.). El Instituto Warburg.
- ^ Fishman, RS (1973). Descubrimiento de Kepler de la imagen retiniana. Archivos de Oftalmología, 89 (1), 59-61. https://doi.org/10.1001/archopht.1973.01000040061014
- ^ "Santiago Ramón y Cajal - Biográfico" . www.nobelprize.org . Archivado desde el original el 6 de octubre de 2015 . Consultado el 20 de octubre de 2015 .
- ^ "Nobelprize.org" . nobelprize.org . Archivado desde el original el 30 de junio de 2017 . Consultado el 5 de diciembre de 2017 .
- ^ "Cálculo de la velocidad de la vista" . newscientist.com . Archivado desde el original el 31 de mayo de 2015 . Consultado el 5 de diciembre de 2017 .
- ^ MacLaren, RE; Pearson, RA; MacNeil, A; et al. (Noviembre de 2006). "Reparación de retina por trasplante de precursores de fotorreceptores" (PDF) . Naturaleza . 444 (7116): 203–7. Código Bibliográfico : 2006Natur.444..203M . doi : 10.1038 / nature05161 . hdl : 2027,42 / 62596 . PMID 17093405 . S2CID 4415311 .
- ^ Bartsch, U .; Oriyakhel, W .; Kenna, PF; Linke, S .; Richard, G .; Petrowitz, B .; Humphries, P .; Farrar, GJ; Ader, M. (2008). "Las células de la retina se integran en la capa nuclear externa y se diferencian en fotorreceptores maduros después del trasplante subretiniano en ratones adultos". Investigación ocular experimental . 86 (4): 691–700. doi : 10.1016 / j.exer.2008.01.018 . PMID 18329018 .
- ^ "Acerca de: EyeWire" . Archivado desde el original el 13 de febrero de 2012 . Consultado el 26 de marzo de 2012 .
- ^ "Retina << EyeWire" . Archivado desde el original el 24 de marzo de 2012 . Consultado el 27 de marzo de 2012 .
- ^ "EyeWire" . Archivado desde el original el 24 de abril de 2012 . Consultado el 27 de marzo de 2012 .
Otras lecturas
- S. Ramón y Cajal , Histologie du Système Nerveux de l'Homme et des Vertébrés , Maloine, París, 1911.
- Rodieck RW (1965). "Análisis cuantitativo de la respuesta de las células ganglionares de la retina del gato a los estímulos visuales". Vision Res . 5 (11): 583–601. doi : 10.1016 / 0042-6989 (65) 90033-7 . PMID 5862581 .
- Wandell, Brian A. (1995). Fundamentos de la visión . Sunderland, Mass: Sinauer Associates. ISBN 978-0-87893-853-7.
- Wässle H, Boicot BB (1991). "Arquitectura funcional de la retina de mamíferos". Physiol. Rev . 71 (2): 447–480. doi : 10.1152 / physrev.1991.71.2.447 . PMID 2006220 .
- Schulz HL, Goetz T, Kaschkoetoe J, Weber BH (2004). "El retinoma - Definición de un transcriptoma de referencia del epitelio pigmentario de retina / retina de mamíferos adultos" . BMC Genomics (sobre un transcriptoma para el color de ojos). 5 (1): 50. doi : 10.1186 / 1471-2164-5-50 . PMC 512282 . PMID 15283859 .
- Dowling, John (2007). "Retina" . Scholarpedia . 2 (12): 3487. Bibcode : 2007SchpJ ... 2.3487D . doi : 10.4249 / scholarpedia.3487 .
enlaces externos
- Histología del ojo , editado por William Krause, Departamento de Patología y Ciencias Anatómicas, Facultad de Medicina de la Universidad de Missouri
- Eye, Brain, and Vision - libro en línea - por David Hubel
- Kolb, H., Fernandez, E. y Nelson, R. (2003). Webvision: la organización neuronal de la retina de vertebrados . Salt Lake City, Utah: John Moran Eye Center, Universidad de Utah . Consultado el 22 de julio de 2014.
- Demostración: Retina artificial , MIT Technology Review, septiembre de 2004. Informes sobre la investigación de implantes en Technology Review
- Trasplante exitoso de fotorreceptores , MIT Technology Review, noviembre de 2006. Cómo las células madre pueden restaurar la vista Technology Review
- Grupo Australiano de Prótesis de Visión , Escuela de Graduados de Ingeniería Biomédica, Universidad de Nueva Gales del Sur
- RetinaCentral , Genética y enfermedades de la retina humana en la Universidad de Würzburg
- Imagen de capas de retina. NeuroScience 2nd Ed en la Biblioteca Nacional de Medicina de los Estados Unidos
- Seminarios de Jeremy Nathans: "La retina de vertebrados: estructura, función y evolución"
- Retina - Base de datos centrada en células
- Imagen de histología: 07901loa - Sistema de aprendizaje de histología en la Universidad de Boston
- Enciclopedia MedlinePlus : 002291
- Sistema visual
- Anatomía del ojo humano