 | |
| Datos clinicos | |
|---|---|
| Otros nombres | GSK-221149-A |
| Código ATC |
|
| Estatus legal | |
| Estatus legal |
|
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Tablero CompTox ( EPA ) | |
| Datos químicos y físicos | |
| Fórmula | C 27 H 34 N 4 O 5 |
| Masa molar | 494,592 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
Retosiban, también conocido como GSK-221,149-A [1] [2], es un fármaco oral que actúa como antagonista del receptor de oxitocina . GlaxoSmithKline lo está desarrollando para el tratamiento del trabajo de parto prematuro . [3] [4] Retosiban tiene alta afinidad por el receptor de oxitocina (K i = 0,65 nM) y tiene mayor que 1400 veces selectividad [5] sobre los relacionados vasopresina receptores
Mecanismo de acción [ editar ]
Retosiban es un antagonista competitivo del receptor de oxitocina que bloquea la contracción mediada por oxitocina del músculo liso uterino en el útero femenino que ocurre durante el inicio del trabajo de parto prematuro. Esto se ha utilizado para prevenir el parto prematuro y el nacimiento prematuro .
Farmacología [ editar ]
Se ha demostrado que retosiban es un tocolítico eficaz . Por administración intravenosa y oral, produce una disminución dependiente de la dosis en las contracciones uterinas inducidas por oxitocina en ratas hembras no preñadas. En ratas gestantes tardías, reduce significativamente las contracciones uterinas espontáneas de una manera dependiente de la dosis por administración intravenosa. [5]En el ser humano, retosiban prolonga el embarazo y reduce el parto prematuro. La administración intravenosa de retosiban en mujeres con trabajo de parto prematuro espontáneo se asoció con un aumento de más de 1 semana en el tiempo hasta el parto en comparación con placebo, una reducción significativa de los partos prematuros, un aumento no significativo de la inactividad uterina y un perfil de seguridad favorable. Los resultados demuestran una prueba de concepto en el tratamiento de la amenaza de trabajo de parto prematuro espontáneo [6]
Farmacocinética [ editar ]
La biodisponibilidad oral de retosiban es del orden del 100% en la rata con una vida media de 1,4 horas. Tiene un aclaramiento intrínseco bajo a moderado en microsomas de tres especies preclínicas (rata, perro, mono cynomolgus) y un aclaramiento intrínseco bajo en microsomas humanos. Tiene un buen perfil de citocromo P450 (Cyp450) sin inhibición significativa, con IC50> 100μM, baja unión a proteínas (<80%) y baja penetración prevista en el SNC. [4]
Propiedades físicas y químicas [ editar ]
A pH fisiológico , retosiban existe sin carga. Tiene buena solubilidad (> 0,22 mg / ml), con un logd de 2,2. [4]
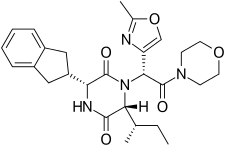
Retosiban consiste en un anillo central de 2,5 dicetopiperazina con un grupo R - indanilo en la posición 3 y un R ( S -secButilo) en la posición 6, ambos cis entre sí y con un anillo R -2-metil oxazol en la posición 6. la posición 7 en la amida acíclica unida a la posición N1. Retosiban es el isómero (3 R , 6 R , 7 R ) y es un antagonista del receptor de oxitocina sub-nanomolar (Ki = 0,65 nM) , mientras que el (3 R , 6 R , 7 S) -isómero donde la estereoquímica en la cadena lateral de amida en C-7 está invertida, es 10 veces menos potente. Normalmente, en esta serie de antagonistas de 2,5 dicetopiperazina oxitocina, el isómero (3 S , 6 S , 7 S ) es> 500 menos activo que el isómero (3 R , 6 R , 7 R ). Además del núcleo esencial de 2,5 dicetopiperazina, retosiban también contiene varias características estructurales que mejoran su eficacia y seguridad. Un indaniloEl grupo en la posición 3 es la mejor opción en términos de potencia antagonista del receptor de oxitocina, su reemplazo por grupos fenetilo y bencilo condujo a un debilitamiento progresivo de la actividad. En C-3, se demostró que se prefiere un alquilo ramificado de 4 carbonos, siendo R ( S -secButilo) el mejor; los grupos alquilo más pequeños dan como resultado una actividad antagonista reducida. [4] El anillo de 2-metil oxazol en la posición 7 proporciona buena solubilidad acuosa, baja unión a proteínas y mínima interacción Cyp450. Esta relación estructura-actividad (SAR) está respaldada por la estructura cristalina del receptor de oxitocina humano en el complejo con retosiban, [7]donde el sustituyente indanilo lipófilo penetra en una hendidura profunda, principalmente hidrófoba en la parte inferior de la bolsa de unión, mientras que el resto de amida de oxazol-morfolina está más cerca de la superficie extracelular. El anillo de oxazol es el sustituyente más expuesto al disolvente y el anillo de morfolina no tiene interacciones directas con el receptor. El núcleo de 2,5-dicetopiperazina interactúa específicamente con el receptor a través de una interfaz de interacción polar.
Síntesis [ editar ]
Retosiban es un dipéptido cíclico o 2,5-dicetopiperazina y estos se forman ciclando el dipéptido lineal correspondiente. En el corto a escala de laboratorio y altamente síntesis estereoselectiva de Retosiban 8 el péptido lineal 5 está formado por la de cuatro componentes de reacción Ugi de la carboxibencilo (Cbz) protegido R-indanylglycine 1 , D-aloisoleucina metil éster clorhidrato de 2 , 2-methyloxazole- 4-carboxaldehído 3 y 2-benciloxifenilisonitrilo 4 . La hidrogenación para eliminar los grupos protectores Cbz y bencilo permitió la ciclación del péptido lineal 5que ocurra para dar el dipéptido cíclico fenólico 6 . La hidrólisis de la amida fenólica, por reacción con carbonildiimidazol (CDI), seguida de la adición de ácido clorhídrico acuoso dio el ácido 7 que se convirtió en la amida Retosiban 8 activando el ácido con el reactivo de acoplamiento peptídico PyBOP (benzotriazol-1-iloxitripirrolidinofosfonio hexafluorofosfato ) seguido de la adición de morfolina . [4] Aunque el péptido lineal 5 y el dipéptido cíclico 6 son una mezcla de diastereoisómeros (7 RS) A la amida exocíclico, la hidrólisis de ácido clorhídrico de la amida causado fenólico activado epimerización en la posición exocíclico y dio el ácido 7 con la requerida (7 R estereoquímica) como el producto principal.
Ver también [ editar ]
- Atosiban
- Barusiban
- Epelsiban
- L-368,899
- L-371,257
Referencias [ editar ]
- ^ Liddle J, Allen MJ, Borthwick AD, Brooks DP, Davies DE, Edwards RM, et al. (Enero de 2008). "El descubrimiento de GSK221149A: un antagonista de oxitocina potente y selectivo". Cartas de Química Bioorgánica y Medicinal . 18 (1): 90–4. doi : 10.1016 / j.bmcl.2007.11.008 . PMID 18032036 .
- ^ Borthwick AD, Liddle J (enero de 2013). "Retosiban y Epelsiban: antagonistas de oxitocina disponibles por vía oral potentes y selectivos". En Domling A (ed.). Métodos y principios en química medicinal: interacciones proteína-proteína en el descubrimiento de fármacos . Weinheim: Wiley-VCH. págs. 225-256. doi : 10.1002 / 9783527648207.ch10 . ISBN 978-3-527-33107-9.
- ^ Consejo de USAN (2007). "Declaración sobre una denominación común adoptada por el Consejo de USAN" (PDF) .
- ↑ a b c d e f Borthwick AD, Liddle J (julio de 2011). "El diseño de antagonistas de oxitocina de 2,5-Diketopiperazine oralmente biodisponibles: del concepto al candidato clínico para el parto prematuro". Revisiones de investigaciones medicinales . 31 (4): 576–604. doi : 10.1002 / med.20193 . PMID 20027670 .
- ^ a b McCafferty GP, Pullen MA, Wu C, Edwards RM, Allen MJ, Woollard PM, Borthwick AD, Liddle J, Hickey DM, Brooks DP, Westfall TD (2007). "Uso de un antagonista del receptor de oxitocina novedoso y altamente selectivo para caracterizar las contracciones uterinas en la rata". Revista estadounidense de fisiología. Fisiología reguladora, integradora y comparada . 293 (1): R299-305. doi : 10.1152 / ajpregu.00057.2007 . PMID 17395790 .
- ^ Thornton S, Miller H, Valenzuela G, Snidow J, Stier B, Fossler MJ, Montague TH, Powell M, Beach KJ (octubre de 2015). "Tratamiento del trabajo de parto prematuro espontáneo con retosiban: un estudio de prueba de concepto de fase 2" . Revista británica de farmacología clínica . 80 (4): 740–749. doi : 10.1111 / bcp.12646 . PMC 4594710 . PMID 25819462 .
- ^ Waltenspühl Y, Schöppe J, Ehrenmann J, Kummer L, Plückthun A (julio de 2020). "Estructura cristalina del receptor de oxitocina humana" . Avances científicos . 6 (29): 1–11. doi : 10.1126 / sciadv.abb5419 . PMID 32832646 .