 | |
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC sulfuro de silicio (IV) | |
| Otros nombres disulfuro de silicio | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| ChemSpider | |
| Tarjeta de información ECHA | 100.033.935 |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| SiS 2 | |
| Masa molar | 92,218 g / mol |
| Apariencia | Agujas blancas (las muestras son a veces grises o marrones). Olor a huevo podrido en el aire húmedo. |
| Densidad | 1,853 g / cm 3 |
| Punto de fusion | 1.090 ° C (1.990 ° F; 1.360 K) sublima |
| Se descompone | |
| Estructura | |
| Ortorrómbico , OI12 | |
| Ibam, Nº 72 [1] | |
| Tetraédrico | |
| Peligros | |
| NFPA 704 (diamante de fuego) | |
| Compuestos relacionados | |
Otros aniones | dióxido de silicio |
Otros cationes | disulfuro de carbono disulfuro de germanio sulfuro de estaño (IV) sulfuro de plomo (IV) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
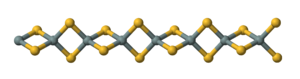
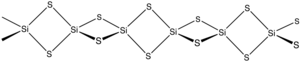
El sulfuro de silicio es el compuesto inorgánico de fórmula Si S 2 . Al igual que el dióxido de silicio , este material es polimérico , pero adopta una estructura unidimensional bastante diferente de las formas habituales de SiO 2 .
Síntesis, estructura y propiedades [ editar ]
El material se forma calentando silicio y azufre o mediante la reacción de intercambio entre SiO 2 y Al 2 S 3 . El material consta de cadenas de tetraedros con bordes compartidos , Si (μ-S) 2 Si (μS) 2 , etc. [2]
Al igual que otros compuestos de azufre de silicio (p. Ej., Bis (trimetilsilil) sulfuro ), el SiS 2 se hidroliza fácilmente para liberar H 2 S. En el amoníaco líquido se informa que forma la imida Si (NH) 2 y NH 4 SH, [3] pero una un informe reciente ha identificado (NH 4 ) 2 [SiS 3 (NH 3 )] · 2NH 3 cristalino como un producto que contiene el anión tiosilicato tetraédrico, SiS 3 (NH 3 ). [4]
La reacción con etanol da el alcóxido de ortosilicato de tetraetilo y H 2 S. [3] Con voluminoso terc-butanol, alcoholisis da tris (terc-butoxi) silanethiol : [5]
- 3 (CH 3 ) 3 COH + SiS 2 → [(CH 3 ) 3 CO] 3 SiSH + H 2 S
La reacción con sulfuro de sodio , sulfuro de magnesio y aluminio sulfuro de dar thiosilicates . [3]
Se afirma que SiS 2 ocurre en ciertos objetos interestelares. [6]
Referencias [ editar ]
- ^ Weiss, A .; Weiss, A. (1954). "Über Siliciumchalkogenide. VI. Zur Kenntnis der faserigen Siliciumdioxyd-Modifikation". Zeitschrift für Anorganische und Allgemeine Chemie . 276 (1–2): 95–112. doi : 10.1002 / zaac.19542760110 .
- ^ Holleman, AF; Wiberg, E. (2001). Química inorgánica . San Diego: Prensa académica. ISBN 0-12-352651-5.Un error de impresión en este libro indica que r SiSi es 214 picómetros , cuando en realidad esa distancia describe r SiS .
- ↑ a b c Greenwood, Norman N .; Earnshaw, Alan (1984). Química de los elementos . Oxford: Pergamon Press . pag. 359. ISBN 978-0-08-022057-4.
- ^ Meier, Martin; Korber, Nikolaus (2009). "El primer tiosilicato de la solución: síntesis y estructura cristalina de (NH4) 2 [SiS3 (NH3)] · 2NH3". Dalton Transactions (9): 1506. doi : 10.1039 / b818856d . ISSN 1477-9226 .
- ^ R. Piękoś, W. Wojnowski (1962). "Untersuchungen über die Alkoholyse des SiS2. II. Darstellung von Trialkoxysilanthiolen und Tetraalkoxycyclodisilthianen aus den tertiären Alkoholen". Z. anorg. allg. Chem . 318 : 212-216. doi : 10.1002 / zaac.19623180310 .
- ^ Goebel, JH (1993). "SiS 2 en conchas circunestelares" (PDF) . Astronomía y Astrofísica . 278 (1): 226–230. Bibcode : 1993A y A ... 278..226G .
