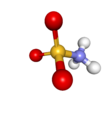
Ácido sulfámico
 | |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC Ácido sulfámico | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.023.835 | ||
| Número CE |
| ||
PubChem CID | |||
| Número RTECS |
| ||
| UNII | |||
| un numero | 2967 | ||
Tablero CompTox ( EPA ) | |||
| |||
| Propiedades | |||
| H 3 NSO 3 | |||
| Masa molar | 97,10 g / mol | ||
| Apariencia | cristales blancos | ||
| Densidad | 2,15 g / cm 3 | ||
| Punto de fusion | 205 ° C (401 ° F; 478 K) se descompone | ||
| Moderado, con hidrólisis lenta | |||
| Solubilidad | |||
| Acidez (p K a ) | 1.0 [1] | ||
| Riesgos | |||
| Ficha de datos de seguridad | ICSC 0328 | ||
Clasificación de la UE (DSD) (desactualizada) | Irritante ( Xi ) | ||
| Frases R (desactualizadas) | R36 / 38 R52 / 53 | ||
| Frases S (desactualizadas) | (S2) S26 S28 S61 | ||
| Compuestos relacionados | |||
Otros cationes | Sulfamato de amonio | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
Ácido sulfámico , también conocido como ácido amidosulfónico , ácido amidosulfónico , ácido aminosulfónico , y ácido sulfamıdico , es un compuesto molecular con la fórmula H 3 NSO 3 . Este compuesto incoloro soluble en agua encuentra muchas aplicaciones. El ácido sulfámico se derrite a 205 ° C antes de descomponerse a temperaturas más altas en agua , trióxido de azufre , dióxido de azufre y nitrógeno . [2]
El ácido sulfámico (H 3 NSO 3 ) puede considerarse un compuesto intermedio entre el ácido sulfúrico (H 2 SO 4 ) y la sulfamida (H 4 N 2 SO 2 ), reemplazando efectivamente un grupo hidroxilo (–OH) con una amina (–NH 2 ) agrupar en cada paso. Este patrón no puede extenderse más en ninguna dirección sin descomponer el resto sulfonilo (–SO 2 -). Los sulfamatos son derivados del ácido sulfámico.
Producción
El ácido sulfámico se produce industrialmente tratando la urea con una mezcla de trióxido de azufre y ácido sulfúrico (u oleum ). La conversión se realiza en dos etapas:
- OC (NH 2 ) 2 + SO 3 → OC (NH 2 ) (NHSO 3 H)
- OC (NH 2 ) (NHSO 3 H) + H 2 SO 4 → CO 2 + 2 H 3 NSO 3
De esta forma, se produjeron aproximadamente 96.000 toneladas en 1995. [3]
Estructura y reactividad
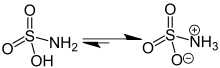
El compuesto está bien descrito por la fórmula H 3 NSO 3 , no por el tautómero H 2 NSO 2 (OH). Las distancias de enlace relevantes son 1,44 Å para S = O y 1,77 Å para S – N. La mayor longitud de S – N es consistente con un enlace simple. [5] Además, un estudio de difracción de neutrones localizó los átomos de hidrógeno, los tres están a 1,03 Å de distancia del nitrógeno. [4] En estado sólido, la molécula de ácido sulfámico está bien descrita por una forma zwiteriónica .
Las soluciones acuosas de ácido sulfámico son inestables y se hidrolizan lentamente a bisulfato de amonio , pero el sólido cristalino es indefinidamente estable en condiciones normales de almacenamiento. Su comportamiento se asemeja al de la urea , (H 2 N) 2 CO. Ambos presentan grupos amino ligados a centros sustractores de electrones que pueden participar en enlaces deslocalizados . Ambos liberan amoniaco al calentarlos en agua; sin embargo, el ácido sulfámico vuelve a convertirse en ácido sulfúrico , en lugar del CO 2 que liberaría la urea, de acuerdo con la siguiente reacción:
- H 3 NSO 3 + H 2 O → H 2 SO 4 + NH 3
Reacciones ácido-base
El ácido sulfámico es un ácido moderadamente fuerte, K a = 0,101 (p K a = 0,995). Debido a que el sólido no es higroscópico , se utiliza como estándar en acidimetría (ensayos cuantitativos de contenido de ácido).
- H 3 NSO 3 + NaOH → NaH 2 NSO 3 + H 2 O
Se puede realizar una doble desprotonación en una solución de amoníaco para dar el anión HNSO2−
3. [6]
- H 3 NSO 3 + 2 NH 3 → HNSO2−
3+ 2 NH+
4
Reacción con ácidos nítrico y nitroso.
Con ácido nitroso , el ácido sulfámico reacciona para dar nitrógeno :
- HNO 2 + H 3 NSO 3 → H 2 SO 4 + N 2 + H 2 O
mientras que con ácido nítrico , produce óxido nitroso : [7]
- HNO 3 + H 3 NSO 3 → H 2 SO 4 + N 2 O + H 2 O
Reacción con hipoclorito
La reacción del exceso de iones hipoclorito con ácido sulfámico o una sal sulfamato da lugar de forma reversible tanto a iones N -clorosulfamato como a N , N- diclorosulfamato. [8] [9] [10]
- HClO + H 2 NSO 3 H → ClNHSO 3 H + H 2 O
- HClO + ClNHSO 3 H ⇌ Cl 2 NSO 3 H + H 2 O
En consecuencia, el ácido sulfámico se utiliza como depurador de hipoclorito en la oxidación de aldehídos con clorito como la oxidación de Pinnick .
Reacción con alcohol
Al calentar, el ácido sulfámico reaccionará con los alcoholes para formar los correspondientes organosulfatos . Es más caro que otros reactivos para hacer esto, como el ácido clorosulfónico u oleum , pero también es significativamente más suave y no sulfona los anillos aromáticos. Los productos se producen como sus sales de amonio . Tales reacciones pueden catalizarse por la presencia de urea . [10]
- ROH + H 2 NSO 3 H → ROS (O) 2 O - + NH+
4
Sin la presencia de catalizadores, el ácido sulfámico no reaccionará con el etanol a temperaturas inferiores a 100 ° C.
Aplicaciones
El ácido sulfámico es principalmente un precursor de compuestos de sabor dulce. La reacción con ciclohexilamina seguida de la adición de NaOH da C _ { 6} H _ { 11} NHSO _ { 3} Na, ciclamato de sodio . Los compuestos relacionados también son edulcorantes , como el acesulfamo de potasio .
Los sulfamatos se han utilizado en el diseño de muchos tipos de agentes terapéuticos, como antibióticos , inhibidores de la transcriptasa inversa nucleósidos / nucleótidos del virus de la inmunodeficiencia humana (VIH) , inhibidores de la proteasa (IP) del VIH , medicamentos contra el cáncer ( esteroides sulfatasa e inhibidores de la anhidrasa carbónica ), antiepilépticos. medicamentos y medicamentos para bajar de peso . [11]
Agente de limpieza
El ácido sulfámico se utiliza como agente de limpieza ácido , a veces puro o como componente de mezclas patentadas, típicamente para metales y cerámicas . Se utiliza con frecuencia para eliminar óxido y cal , reemplazando el ácido clorhídrico más volátil e irritante , que es más económico. A menudo es un componente de los agentes descalcificadores domésticos , por ejemplo, el gel espeso Lime-A-Way contiene hasta un 8% de ácido sulfámico y tiene un pH de 2,0 a 2,2, [12] o detergentes utilizados para eliminar la cal.. Cuando se compara con la mayoría de los ácidos minerales fuertes comunes, el ácido sulfámico tiene propiedades deseables para desincrustar el agua, baja volatilidad y baja toxicidad. Forma sales solubles en agua de calcio y hierro férrico.
El ácido sulfámico es preferible al ácido clorhídrico en el uso doméstico, debido a su seguridad intrínseca. Si se mezcla erróneamente con productos a base de hipoclorito como lejía , no forma cloro gaseoso, mientras que los ácidos más comunes lo harían; la reacción ( neutralización ) con amoniaco produce una sal, como se muestra en la sección anterior.
También encuentra aplicaciones en la limpieza industrial de equipos lácteos y cerveceros. Aunque se considera menos corrosivo que el ácido clorhídrico , los inhibidores de corrosión a menudo se agregan a los limpiadores comerciales de los que es un componente. Se puede utilizar para descalcificar cafeteras y espresso en el hogar y en limpiadores de dentaduras postizas.
Otros usos
- Catalizador para proceso de esterificación
- Fabricación de tintes y pigmentos
- Herbicida
- Coagulador para resinas de urea-formaldehído
- Ingrediente en los medios de extinción de incendios . El ácido sulfámico es la principal materia prima del sulfamato de amonio, que es un herbicida y un material retardante del fuego ampliamente utilizado para productos domésticos.
- Industria de la pulpa y el papel como estabilizador de cloruros
- Síntesis de óxido nitroso por reacción con ácido nítrico.
- La forma desprotonada (sulfamato) es un contraión común para el níquel (II) en galvanoplastia .
- Se utiliza para separar los iones de nitrito de la mezcla de iones de nitrito y nitrato (NO 3 - + NO 2 - ) durante el análisis cualitativo de nitrato mediante la prueba del anillo marrón.
Pulido de plata
Según la etiqueta del producto de consumo, el producto de limpieza de plata líquida TarnX contiene tiourea , un detergente y ácido sulfámico.
Referencias
- ^ Candlin, JP; Wilkins, RG (1960). "828. Compuestos de azufre-nitrógeno. Parte I. La hidrólisis del ion sulfamato en ácido perclórico". Revista de la Sociedad Química ( reanudación ) : 4236–4241. doi : 10.1039 / JR9600004236 .
- ^ Yoshikubo, K .; Suzuki, M. (2000). "Ácido sulfámico y sulfamatos". Enciclopedia Kirk-Othmer de tecnología química . doi : 10.1002 / 0471238961.1921120625151908.a01 . ISBN 0471238961.
- ^ Metzger, A. "Ácido sulfámico". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a25_439 .
- ↑ a b Sass, RL (1960). "Un estudio de difracción de neutrones sobre la estructura cristalina del ácido sulfámico" . Acta Crystallographica . 13 (4): 320–324. doi : 10.1107 / S0365110X60000789 .
- ^ Murciélagos, JW; Coppens, P .; Koetzle, TF (1977). "La densidad de carga experimental en moléculas que contienen azufre. Un estudio de la densidad de electrones de deformación en ácido sulfámico a 78 K por difracción de rayos X y neutrones" . Acta Crystallographica Sección B . 33 : 37–45. doi : 10.1107 / S0567740877002568 .
- ^ Clapp, LB (1943). "Ácido sulfámico y sus usos". Revista de educación química . 20 (4): 189–346. doi : 10.1021 / ed020p189 .
- ^ Dzelzkalns, Laila; Bonner, Francis (1978). "Reacción entre los ácidos nítrico y sulfámico en solución acuosa". Química inorgánica . 17 (12): 3710–3711. doi : 10.1021 / ic50190a080 .
- ^ US 3328294
- ^ FR 2087248
- ↑ a b Benson, G. Anthony; Spillane, William J. (1980). "Ácido sulfámico y sus derivados N- sustituidos". Revisiones químicas . 80 (2): 151–186. doi : 10.1021 / cr60324a002 . ISSN 0009-2665 .
- ^ Winum, JY; Scozzafava, A .; Montero, JL; Supuran, CT (2005). "Sulfamatos y su potencial terapéutico". Revisiones de investigaciones medicinales . 25 (2): 186–228. doi : 10.1002 / med.20021 . PMID 15478125 .
- ^ Benckiser, Reckitt. "Hoja de datos de seguridad del material - Limpiador de cal, calcio y óxido Lime-A-Way (spray de gatillo)" (PDF) . hardwarestore.com . Archivado desde el original (PDF) el 17 de julio de 2011 . Consultado el 17 de noviembre de 2011 .
Otras lecturas
- "Información de muestreo químico - ácido sulfámico" . Administración de Seguridad y Salud Ocupacional. 6 de mayo de 1997 . Consultado el 17 de noviembre de 2011 .
- Cremlyn, RJ (1996). Introducción a la química del azufre orgánico . Chichester: John Wiley and Sons. ISBN 978-0-471-95512-2.
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
| Wikimedia Commons tiene medios relacionados con el ácido sulfámico . |
- Compuestos de hidrógeno
- Oxoácidos de azufre
- Productos químicos para el hogar
- Componentes del producto de limpieza
- Sulfamatos