 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / T ɔr ə m ɪ f i n / |
| Nombres comerciales | Fareston, otros |
| Otros nombres | ( Z ) -toremifeno; 4-clorotamoxifeno; 4-CT; Acapodene; CCRIS-8745; FC-1157; FC-1157a; GTx-006; NK-622; NSC-613680 |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a608003 |
| Datos de licencia | |
| Vías de administración | Oral |
| Clase de droga | Modulador selectivo del receptor de estrógenos |
| Código ATC | |
| Datos farmacocinéticos | |
| Biodisponibilidad | Bueno / ~ 100% [1] [2] |
| Enlace proteico | 99,7% [1] |
| Metabolismo | Hígado ( CYP3A4 ) [5] [2] |
| Metabolitos | N-desmetiltoremifeno; 4-hidroxitoremifeno; Ospemifeno [3] [4] |
| Vida media de eliminación | Toremifeno: 3 a 7 días [1] Metabolitos: 4 a 21 días [2] [4] [1] |
| Excreción | Heces : 70% (como metabolitos) [2] |
| Identificadores | |
| |
| Número CAS |
|
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Ligando PDB | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.125.139 |
| Datos químicos y físicos | |
| Fórmula | C 26 H 28 Cl N O |
| Masa molar | 405,97 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
| (verificar) | |
El toremifeno , vendido bajo la marca Fareston entre otros, es un medicamento que se utiliza en el tratamiento del cáncer de mama avanzado en mujeres posmenopáusicas . [4] [6] [3] Se toma por vía oral . [4]
Los efectos secundarios del toremifeno incluyen sofocos , sudoración , náuseas , vómitos , mareos , flujo vaginal y sangrado vaginal . [5] [7] También puede causar coágulos de sangre , latidos cardíacos irregulares , cataratas , alteraciones visuales , enzimas hepáticas elevadas , hiperplasia endometrial y cáncer de endometrio . [5] Los niveles altos de calcio en sangre pueden ocurrir en mujeres con metástasis óseas .[5]
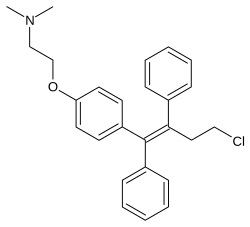
El medicamento es un modulador selectivo del receptor de estrógeno (SERM) y, por lo tanto, es un agonista - antagonista mixto del receptor de estrógeno (ER), el objetivo biológico de los estrógenos como el estradiol . [5] [7] Tiene efectos estrogénicos en los huesos , el hígado y el útero y efectos antiestrogénicos en los senos . [6] [8] [9] [5] Es un derivado de trifeniletileno y está estrechamente relacionado con el tamoxifeno . [10]
El toremifeno se introdujo para uso médico en 1997. [11] [12] Fue el primer antiestrógeno que se introdujo desde el tamoxifeno en 1978. [13] Está disponible como medicamento genérico en los Estados Unidos . [14]
Usos médicos [ editar ]
El toremifeno está aprobado para el tratamiento del cáncer de mama metastásico en mujeres posmenopáusicas con tumores con receptor de estrógeno positivo o de estado desconocido . [4] [6] Este es su único uso aprobado en los Estados Unidos . [4] Muestra una eficacia equivalente al tamoxifeno para esta indicación. [6] [15] Se ha descubierto que el toremifeno es eficaz en el tratamiento del dolor de mama y puede ser un medicamento más eficaz que el tamoxifeno para esta indicación. [16] También tiene efectos superiores sobre la densidad mineral ósea y el perfil lipídico , incluidos los niveles decolesterol y triglicéridos , en comparación con el tamoxifeno. [15] Se ha informado que el toremifeno mejora significativamente los síntomas de la ginecomastia en los hombres. [17]
Formas disponibles [ editar ]
El toremifeno se proporciona en la forma de 60 mg orales tabletas . [18] [19]
Efectos secundarios [ editar ]
Los efectos secundarios del toremifeno son similares a los del tamoxifeno. [5] El efecto secundario más común son los sofocos . [5] Otros efectos secundarios incluyen sudoración , náuseas , vómitos , mareos , flujo vaginal y sangrado vaginal . [5] [7] En mujeres con metástasis óseas , puede ocurrir hipercalcemia . [5] El toremifeno tiene un pequeño riesgo de eventos tromboembólicos . [5] Cataratas , cambios en la visión ySe ha informado elevación de las enzimas hepáticas . [5] [7] El fármaco prolonga el intervalo QT y, por lo tanto, tiene un riesgo de arritmias potencialmente mortales . [5] El riesgo de arritmias se puede reducir evitando su uso en pacientes con hipopotasemia , hipomagnesemia , prolongación del QT preexistente y en aquellos que toman otros fármacos que prolongan el intervalo QT. [5] Debido a que el toremifeno tiene acciones estrogénicas en el útero , puede aumentar el riesgo de hiperplasia endometrial y cáncer endometrial . [5]
El toremifeno parece ser más seguro que el tamoxifeno. [15] Tiene un riesgo menor de tromboembolismo venoso (TEV) (p. Ej., Embolia pulmonar ), accidente cerebrovascular y cataratas . [15] El menor riesgo de TEV puede estar relacionado con el hecho de que el tamoxifeno disminuye los niveles de antitrombina III en un grado significativamente mayor que 60 o 200 mg / día de toremifeno. [15]
Interacciones [ editar ]
El toremifeno es un sustrato de CYP3A4 , una enzima del citocromo P450 y, por lo tanto, los fármacos que inducen o inhiben esta enzima pueden disminuir o aumentar respectivamente los niveles de toremifeno en el cuerpo. [5]
Farmacología [ editar ]
Farmacodinámica [ editar ]
El toremifeno es un modulador selectivo del receptor de estrógeno (SERM). [5] [7] [20] Es decir, es un agonista-antagonista selectivo mixto de los receptores de estrógenos (RE), con acciones estrogénicas en algunos tejidos y acciones antiestrogénicas en otros tejidos. [5] [7] El medicamento tiene efectos estrogénicos en los huesos , efectos estrogénicos parciales en el útero y el hígado y efectos antiestrogénicos en los senos . [6] [8] [9][5]
| Medicamento | Seno | Hueso | Hígado | Útero | Vagina | Cerebro | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Lípidos | Coagulación | SHBG | IGF-1 | Sofocos | Gonadotropinas | |||||||||
| Estradiol | + | + | + | + | + | + | + | + | + | + | ||||
| "SERM ideal" | - | + | + | ± | ± | ± | - | + | + | ± | ||||
| Bazedoxifeno | - | + | + | + | + | ? | - | ± | - | ? | ||||
| Clomifeno | - | + | + | ? | + | + | - | ? | - | ± | ||||
| Lasofoxifeno | - | + | + | + | ? | ? | ± | ± | - | ? | ||||
| Ospemifeno | - | + | + | + | + | + | ± | ± | - | ± | ||||
| Raloxifeno | - | + | + | + | + | + | ± | - | - | ± | ||||
| Tamoxifeno | - | + | + | + | + | + | + | - | - | ± | ||||
| Toremifeno | - | + | + | + | + | + | + | - | - | ± | ||||
| Efecto: + = Estrógeno / agonista . ± = Mixto o neutro. - = Antiestrogénico / antagonista . Nota: Los SERM generalmente aumentan los niveles de gonadotropina en hombres hipogonadales y eugonadales, así como en mujeres premenopáusicas (antiestrogénico), pero disminuyen los niveles de gonadotropina en mujeres posmenopáusicas (estrogénico). Fuentes: Ver plantilla. | ||||||||||||||
La afinidad del toremifeno por el RE es similar a la del tamoxifeno. [6] [21] [22] En estudios que utilizaron ER de ratas, el toremifeno tenía aproximadamente un 1,4% y el tamoxifeno tenía aproximadamente un 1,6% de la afinidad del estradiol por el ER. [23] [24] [25] [26] [27] [22] Las afinidades (K i ) del toremifeno en el RE humanos se han reportado como 20,3 ± 0,1 nM para el ER y 15,4 ± 3,1 nM para el ERβ . [20] En otros estudios de RE en ratas, el toremifeno tenía entre el 3 y el 9% de la afinidad del estradiol por el RE, mientras que sus metabolitos N-desmetiltoremifeno y 4-hidroxitoremifeno tenían 3-5% y 64-158% de la afinidad del estradiol por el RE, respectivamente. [28] [29] [30] No se evaluó la afinidad de otro metabolito, 4-hidroxi- N -desmetiltoremifeno. [29] El 4-hidroxitoremifeno mostró una potencia antiestrogénica aproximadamente 100 veces mayor que el toremifeno in vitro en un estudio, [29] pero no en otro. [28] También se ha descubierto que el 4-hidroxi- N -desmetiltoremifeno es fuertemente antiestrogénico in vitro . [28]Los metabolitos del toremifeno, particularmente el 4-hidroxitoremifeno, pueden contribuir de manera importante a la actividad clínica del medicamento. [1] [29] [28] Por otro lado, algunas autoridades consideran que el toremifeno no es un profármaco . [31]
El toremifeno es muy similar al tamoxifeno y comparte la mayoría de sus propiedades. [6] [8] [9] [5] Existen algunas indicaciones de que el toremifeno puede ser más seguro que el tamoxifeno, ya que no es un hepatocarcinógeno en animales y puede tener menos potencial de genotoxicidad . [6] [3] Sin embargo, los estudios clínicos no han encontrado diferencias significativas entre el toremifeno y el tamoxifeno, incluso en términos de efectividad , tolerabilidad y seguridad , y por lo tanto, el uso clínico del toremifeno ha sido algo limitado. [6] [3] Se cree que el toremifeno tiene aproximadamente un tercio delpotencia del tamoxifeno; es decir, 60 mg de toremifeno equivalen aproximadamente a 20 mg de tamoxifeno en el tratamiento del cáncer de mama. [32]
Se ha encontrado que el toremifeno tiene efectos antigonadotrópicos en mujeres posmenopáusicas, [33] efectos progonadotrópicos en los hombres, [34] para aumentar los niveles de globulina transportadora de hormonas sexuales , [33] y para disminuir los niveles del factor de crecimiento similar a la insulina 1 en aproximadamente un 20% en mujeres y hombres posmenopáusicos. [35]
Además de su actividad como SERM, el 4-hidroxitoremifeno es un antagonista del receptor γ relacionado con los estrógenos (ERRγ). [36]
Farmacocinética [ editar ]
Absorción [ editar ]
La biodisponibilidad del toremifeno no se ha determinado con precisión, pero se sabe que es buena y se ha estimado en aproximadamente el 100%. [1] [2] Los niveles de toremifeno en estado estable con una dosis de 60 mg / día son de 800 a 879 ng / ml. [1] Los niveles de N -desmetiltoremifeno en estado estacionario con toremifeno fueron 3058 ng / ml a 60 mg / día, 5942 ng / ml a 200 mg / día y 11,913 ng / ml a 400 mg / día. [1] Los niveles de 4-hidroxitoremifeno en estado estable con toremifeno fueron 438 ng / ml a 200 mg / día y 889 ng / ml a 400 mg / día. [1] Las concentraciones de toremifeno aumentan linealmente en un rango de dosis de 10 a 680 mg. [37] [38]
Distribución [ editar ]
El toremifeno se une en 99,7% a las proteínas plasmáticas , 92% se une específicamente a la albúmina , aproximadamente 6% a la fracción de globulina β 1 y aproximadamente 2% a una fracción entre la albúmina y las globulinas α 1 . [37] [1] El volumen aparente de distribución del toremifeno osciló entre 457 y 958 L. [37]
Metabolismo [ editar ]
El toremifeno se metaboliza en el hígado principalmente por el CYP3A4 y luego sufre una hidroxilación secundaria . [2] Los metabolitos del toremifeno incluyen N -desmetiltoremifeno, 4-hidroxitoremifeno y 4-hidroxi- N -desmetiltoremifeno, entre otros. [1] [29] [2] [39] El ospemifeno (deaminohidroxitoremifeno) también es un metabolito principal de toremifeno. [1] [4]
Eliminación [ editar ]
La vida media de eliminación del toremifeno es de 3 a 7 días en individuos sanos. [1] En personas con insuficiencia hepática , la vida media es de 11 días. [1] Las semividas de eliminación de los metabolitos del toremifeno son de 5 a 21 días para el N -desmetiltoremifeno, 5 días para el 4-hidroxitoremifeno y 4 días para el ospemifeno. [1] [2] [4] Se cree que las largas semividas de eliminación del toremifeno y sus metabolitos se deben a la recirculación enterohepática y la alta unión a proteínas plasmáticas. [1] [5] El toremifeno se elimina en un 70% en las heces , como metabolitos.[2]
Química [ editar ]
El toremifeno, también conocido como 4-clorotamoxifeno , es un derivado del trifeniletileno y un análogo cercano del tamoxifeno . [10] También está estrechamente relacionado con el afimoxifeno (4-hidroxitamoxifeno) y el ospemifeno (deaminohidroxitoremifeno). [40] [41]
Historia [ editar ]
El toremifeno se introdujo en los Estados Unidos en 1997. [11] [12] Fue el primer antiestrógeno que se introdujo en este país desde el tamoxifeno en 1978. [13]
Sociedad y cultura [ editar ]
Nombres genéricos [ editar ]
Toremifeno es el nombre genérico del fármaco y su DCI y BAN , mientras que el citrato de toremifeno es su USAN y JAN y torémifène es su DCF . [42] [43] [44] [45]
Nombres de marca [ editar ]
El toremifeno se comercializa casi exclusivamente bajo la marca Fareston. [43] [45]
Disponibilidad [ editar ]
El toremifeno se comercializa ampliamente en todo el mundo y está disponible en los Estados Unidos , el Reino Unido , Irlanda , muchos otros países europeos , Sudáfrica , Australia , Nueva Zelanda y en otras partes del mundo. [43] [45]
Investigación [ editar ]
Esta sección debe actualizarse . ( Abril de 2017 ) |
El toremifeno también se evaluó para la prevención del cáncer de próstata y tenía el nombre comercial provisional Acapodene. [46]
En 2007, la compañía farmacéutica GTx, Inc estaba llevando a cabo dos ensayos clínicos de fase 3 diferentes ; Primero, un ensayo clínico de fase fundamental para el tratamiento de los efectos secundarios graves de la terapia de privación de andrógenos (ADT) (especialmente fracturas vertebrales / de la columna y sofocos , perfil de lípidos y ginecomastia ) para el cáncer de próstata avanzado, y segundo, un ensayo clínico fundamental de fase III ensayo para la prevención del cáncer de próstata en hombres de alto riesgo con neoplasia intraepitelial prostática de alto grado o PIN. Los resultados de estos ensayos se esperan para el primer trimestre de 2008 [47].
En febrero de 2009 se presentó una NDA para la primera aplicación (alivio de los efectos secundarios de ADT en el cáncer de próstata), [48] y en octubre de 2009 la FDA dijo que necesitarían más datos clínicos, por ejemplo, otro ensayo de fase III. [49]
En última instancia, el desarrollo se interrumpió y el toremifeno nunca se comercializó para las complicaciones asociadas con la ADT o el tratamiento o la prevención del cáncer de próstata. [50]
El toremifeno puede ser útil en la prevención de la ginecomastia inducida por bicalutamida . [15]
Resultados del ensayo de fase III [ editar ]
Se realizó un ensayo clínico de 3 años, doble ciego, controlado con placebo y aleatorizado de toremifeno con una muestra de 1260 hombres. Los sujetos tenían una edad promedio de 64 años y fueron diagnosticados con neoplasia intraepitelial prostática de alto grado (HGPIN), que se considera premaligna, aunque Thompson y Leach creen que un PIN de bajo grado también podría considerarse premaligno. [51]
El patrocinador, GTx, que diseñó y dirigió el estudio, encontró que el 34,7% de los grupos de placebo y el 32,3% de los grupos de toremifeno tenían eventos de cáncer. No se encontró distinción en las puntuaciones de Gleason de ninguno de los grupos. [52]
Estudios murinos previos que utilizaron adenocarcinoma transgénico de próstata de ratón (TRAMP) mostraron que el toremifeno previno los tumores palpables en el 60% de los animales. Este estudio utilizó toremifeno como profiláctico temprano, lo que lo diferencia de los estudios en humanos de fase III. [53]
Referencias [ editar ]
- ^ a b c d e f g h i j k l m n o p Taras TL, Wurz GT, Linares GR, DeGregorio MW (noviembre de 2000). "Farmacocinética clínica del toremifeno". Clin Pharmacokinet . 39 (5): 327–34. doi : 10.2165 / 00003088-200039050-00002 . PMID 11108432 .
- ^ a b c d e f g h i Vincent T. DeVita Jr .; Theodore S. Lawrence; Steven A. Rosenberg (7 de enero de 2015). Cáncer de DeVita, Hellman y Rosenberg: Principios y práctica de la oncología . Salud de Wolters Kluwer. págs. 1126–. ISBN 978-1-4698-9455-3.
- ↑ a b c d Bruce A. Chabner; Dan L. Longo (7 de diciembre de 2011). Quimioterapia y bioterapia del cáncer: principios y práctica . Lippincott Williams y Wilkins. págs. 659–. ISBN 978-1-4511-4820-6.
- ^ a b c d e f g h https://www.accessdata.fda.gov/drugsatfda_docs/label/2011/020497s006lbl.pdf
- ^ a b c d e f g h i j k l m n o p q r s t u Laura Rosenthal; Jacqueline Burchum (17 de febrero de 2017). Farmacoterapéutica de Lehne para proveedores de práctica avanzada - Libro electrónico . Ciencias de la salud de Elsevier. págs. 931–. ISBN 978-0-323-44779-9.
- ^ a b c d e f g h i William R. Miller; James N. Ingle (8 de marzo de 2002). Terapia endocrina en el cáncer de mama . Prensa CRC. págs. 55–57. ISBN 978-0-203-90983-6.
- ^ a b c d e f David Schiff; Isabel Arrillaga; Patrick Y. Wen (16 de septiembre de 2017). Neurología del cáncer en la práctica clínica: complicaciones neurológicas del cáncer y su tratamiento . Prensa Humana. págs. 296–. ISBN 978-3-319-57901-6.
- ^ a b c Monica Morrow; Virgil Craig Jordan (2003). Manejo del riesgo de cáncer de mama . PMPH-USA. págs. 192–. ISBN 978-1-55009-260-8.
- ^ a b c Moduladores selectivos del receptor de estrógeno: avances en investigación y aplicación: Edición de 2013: ScholarlyBrief . ScholarlyEditions. 1 de mayo de 2013. págs. 51–. ISBN 978-1-4901-0447-8.
- ^ a b Antonio Cano; Joacquim Calaf i Alsina; Jose Luis Duenas-Diez (22 de septiembre de 2006). Moduladores selectivos del receptor de estrógeno: una nueva marca de fármacos multidireccionales . Springer Science & Business Media. págs. 52–. ISBN 978-3-540-34742-2.
- ↑ a b Orlando E. Silva; Stefano Zurrida (2005). Cáncer de mama: una guía práctica . Ciencias de la salud de Elsevier. págs. 355–. ISBN 0-7020-2744-8.
- ^ a b Wayne R. Bidlack; Stanley T. Omaye; Mark S. Meskin; Debra KW Topham (16 de marzo de 2000). Fitoquímicos como agentes bioactivos . Prensa CRC. págs. 26–. ISBN 978-1-56676-788-0.
- ↑ a b Philip J. DiSaia; William T. Creasman; Robert S Mannel; D. Scott McMeekin, David G Mutch (4 de febrero de 2017). Libro electrónico de oncología ginecológica clínica . Ciencias de la salud de Elsevier. págs. 124–. ISBN 978-0-323-44316-6.
- ^ "Disponibilidad genérica de Fareston - Drugs.com" . Drugs.com . Consultado el 19 de abril de 2019 .
- ↑ a b c d e f Sieber PR (diciembre de 2007). "Tratamiento de eventos de mama inducidos por bicalutamida". Expert Rev Anticancer Ther . 7 (12): 1773–9. doi : 10.1586 / 14737140.7.12.1773 . PMID 18062751 . S2CID 40410461 .
- ^ Kirby I. Bland; Edward M. Copeland; V. Suzanne Klimberg; William J Gradishar (29 de junio de 2017). The Breast E-Book: Manejo integral de enfermedades benignas y malignas . Ciencias de la salud de Elsevier. págs. 86–. ISBN 978-0-323-51187-2.
- ↑ Tabbal, Mahmoud; Fuleihan, Ghada El-Hajj (2010). "Terapias futuras". Osteoporosis en hombres . págs. 713–732. doi : 10.1016 / B978-0-12-374602-3.00057-2 . ISBN 9780123746023.
- ^ Mari J. Wirfs, PhD, MN, APRN, ANP-BC, FNP-BC, CNE (9 de mayo de 2019). La guía completa de APRN y PA para prescribir farmacoterapia 2020 . Springer Publishing Company. págs. 60–. ISBN 978-0-8261-7934-0.CS1 maint: multiple names: authors list (link)
- ^ Casciato; Mary C. Territo (2012). Manual de Oncología Clínica . Lippincott Williams y Wilkins. págs. 122–. ISBN 978-1-4511-1560-4.
- ^ a b Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (marzo de 2006). "Toremifeno: una terapia prometedora para la prevención del cáncer de próstata y las complicaciones de la terapia de privación de andrógenos". Opinión de Expertos Investigar Drogas . 15 (3): 293-305. doi : 10.1517 / 13543784.15.3.293 . PMID 16503765 . S2CID 29510508 .
- ^ Paul Workman (6 de diciembre de 2012). Nuevos enfoques en farmacología del cáncer: diseño y desarrollo de fármacos . Springer Science & Business Media. págs. 104–. ISBN 978-3-642-77874-2.
- ↑ a b Kallio S, Kangas L, Blanco G, Johansson R, Karjalainen A, Perilä M, Pippo I, Sundquist H, Södervall M, Toivola R (1986). "Un nuevo compuesto de trifeniletileno, Fc-1157a. I. Efectos hormonales". Cancer Chemother Pharmacol . 17 (2): 103–8. doi : 10.1007 / BF00306736 . PMID 2941176 .
- ^ Wittliff, JL, Kerr II, DA y Andrés, SA (2005). "Estrógenos IV: productos farmacéuticos similares al estrógeno". En Wexler, P. (ed.). Enciclopedia de Toxicología, 2ª edición . Dib – L. págs. 254-258.CS1 maint: uses authors parameter (link)
- ^ Blair RM, Fang H, Branham WS, Hass BS, Dial SL, Moland CL, Tong W, Shi L, Perkins R, Sheehan DM (marzo de 2000). "Las afinidades de unión relativas del receptor de estrógeno de 188 naturales y xenoquímicos: diversidad estructural de ligandos" . Toxicol Sci . 54 (1): 138–53. doi : 10.1093 / toxsci / 54.1.138 . PMID 10746941 .
- ^ Fang H, Tong W, Shi LM, Blair R, Perkins R, Branham W, Hass BS, Xie Q, Dial SL, Moland CL, Sheehan DM (marzo de 2001). "Relaciones estructura-actividad para un gran conjunto diverso de estrógenos naturales, sintéticos y ambientales". Chem Res Toxicol . 14 (3): 280–94. doi : 10.1021 / tx000208y . PMID 11258977 .
- ^ Chander SK, Sahota SS, Evans TR, Luqmani YA (diciembre de 1993). "La evaluación biológica de nuevos antiestrógenos para el tratamiento del cáncer de mama". Crit Rev Oncol Hematol . 15 (3): 243–69. doi : 10.1016 / 1040-8428 (93) 90044-5 . PMID 8142059 .
- ^ Robert J. Kavlock; George P. Daston (6 de diciembre de 2012). Toxicidad farmacológica en el desarrollo embrionario II: avances en la comprensión de los mecanismos de los defectos de nacimiento: comprensión de los mecanismos de las sustancias tóxicas para el desarrollo humano . Springer Science & Business Media. págs. 437–. ISBN 978-3-642-60447-8.
- ↑ a b c d Kangas L (1990). "Efectos bioquímicos y farmacológicos de los metabolitos del toremifeno". Cancer Chemother Pharmacol . 27 (1): 8-12. doi : 10.1007 / BF00689269 . PMID 2147128 .
- ↑ a b c d e Robinson SP, Parker CJ, Jordan VC (agosto de 1990). "Estudios preclínicos con toremifeno como agente antitumoral". Tratamiento para el cáncer de mama . 16 Supl: S9-17. doi : 10.1007 / BF01807139 . PMID 2149286 .
- ^ C. Kent Osborne (6 de diciembre de 2012). Terapias endocrinas en cáncer de mama y próstata . Springer Science & Business Media. págs. 104–. ISBN 978-1-4613-1731-9.
- ^ Vogel CL, Johnston MA, Alcaparras C, Braccia D (febrero de 2014). "Toremifeno para el cáncer de mama: una revisión de 20 años de datos" . Clin Breast Cancer . 14 (1): 1–9. doi : 10.1016 / j.clbc.2013.10.014 . PMID 24439786 .
- ^ MacGregor JI, Jordan VC (junio de 1998). "Guía básica de los mecanismos de acción de los antiestrógenos" . Pharmacol. Rev . 50 (2): 151–96. PMID 9647865 .
- ↑ a b Ellmén J, Hakulinen P, Partanen A, Hayes DF (noviembre de 2003). "Efectos estrogénicos del toremifeno y el tamoxifeno en pacientes posmenopáusicas con cáncer de mama" (PDF) . Res. De cáncer de mama Tratar . 82 (2): 103-11. doi : 10.1023 / B: BREA.0000003957.54851.11 . hdl : 2027,42 / 44217 . PMID 14692654 . S2CID 207694212 .
- ^ Tsourdi E, Kourtis A, Farmakiotis D, Katsikis I, Salmas M, Panidis D (abril de 2009). "El efecto de la administración selectiva del modulador del receptor de estrógeno sobre el eje hipotalámico-pituitario-testicular en hombres con oligozoospermia idiopática". Fertil. Esteril . 91 (4 Suppl): 1427–30. doi : 10.1016 / j.fertnstert.2008.06.002 . PMID 18692782 .
- ^ Roelfsema F, Yang RJ, Takahashi PY, Erickson D, Bowers CY, Veldhuis JD (febrero de 2018). "Efectos del toremifeno, un modulador selectivo del receptor de estrógeno, sobre la secreción espontánea y estimulada de GH, IGF-I y proteínas de unión a IGF en sujetos ancianos sanos" . Revista de la Sociedad Endocrina . 2 (2): 154-165. doi : 10.1210 / js.2017-00457 . PMC 5789038 . PMID 29383334 .
- ^ Ariazi EA, Jordan VC (2006). "Receptores relacionados con el estrógeno como objetivos emergentes en el cáncer y los trastornos metabólicos". Curr Top Med Chem . 6 (3): 203–15. doi : 10.2174 / 1568026610606030203 . PMID 16515477 .
- ↑ a b c Gennari L, Merlotti D, Stolakis K, Nuti R (abril de 2012). "Evaluación farmacocinética del toremifeno y sus implicaciones clínicas para el tratamiento de la osteoporosis". Opinión del experto Droga Metab Toxicol . 8 (4): 505-13. doi : 10.1517 / 17425255.2012.665873 . PMID 22356442 .
- ^ Anttila M, Valavaara R, Kivinen S, Mäenpää J (junio de 1990). "Farmacocinética del toremifeno". J Steroid Biochem . 36 (3): 249–52. doi : 10.1016 / 0022-4731 (90) 90019-o . PMID 2142247 .
- ^ George M. Brenner; Craig Stevens (28 de septiembre de 2017). Libro electrónico de farmacología de Brenner y Stevens . Ciencias de la salud de Elsevier. págs. 394–. ISBN 978-0-323-39172-6.
- ^ Georg F. Weber (22 de julio de 2015). Terapias moleculares del cáncer . Saltador. págs. 304–. ISBN 978-3-319-13278-5.
- ↑ Philipp Y. Maximov; Russell E. McDaniel; V. Craig Jordan (23 de julio de 2013). Tamoxifeno: Medicina pionera en el cáncer de mama . Springer Science & Business Media. págs. 170–. ISBN 978-3-0348-0664-0.
- ^ J. Elks (14 de noviembre de 2014). El diccionario de drogas: datos químicos: datos químicos, estructuras y bibliografías . Saltador. págs. 1222–. ISBN 978-1-4757-2085-3.
- ^ a b c Índice Nominum 2000: Directorio internacional de medicamentos . Taylor y Francis. 2000. págs. 1048–. ISBN 978-3-88763-075-1.
- ^ IK Morton; Judith M. Hall (6 de diciembre de 2012). Diccionario conciso de agentes farmacológicos: propiedades y sinónimos . Springer Science & Business Media. págs. 277–. ISBN 978-94-011-4439-1.
- ^ a b c "Toremifeno - Drugs.com" . Drugs.com . Consultado el 8 de febrero de 2018 .
- ^ Precio N, Sartor O, Hutson T, Mariani S (2005). "Papel de los inhibidores de la 5a-reductasa y los moduladores selectivos del receptor de estrógeno como agentes quimiopreventivos potenciales para el cáncer de próstata". Cáncer de próstata de Clin . 3 (4): 211–4. doi : 10.1016 / s1540-0352 (11) 70089-0 . PMID 15882476 . CS1 maint: multiple names: authors list (link)
- ^ "Desarrollo clínico de fase III de GTx de ACAPODENE en curso siguiendo la revisión de seguridad planificada" (Comunicado de prensa). GTx Inc. 2007-07-12 . Consultado el 14 de julio de 2006 .
- ^ "GTx anuncia Toremifeno 80 mg NDA aceptado para revisión por la FDA" (Comunicado de prensa).
- ^ "GTx e Ipsen finalizan la colaboración del cáncer de próstata debido a los costos del estudio de fase III solicitado por la FDA" . 2 de marzo de 2011.
- ^ "Toremifeno - AdisInsight" . adisinsight.springer.com . Consultado el 8 de febrero de 2018 .
- ^ Thompson Jr, IM y Leach, R., Cáncer de próstata y neoplasia intraepitelial prostática: ¿verdadero, verdadero y no relacionado? J Clin Oncol, 2013; 31: 515-6. https://ascopubs.org/doi/full/10.1200/JCO.2012.46.6151= Consultado el 31 de julio de 2019
- ^ Taneja, SS, Morton, R., Barnette, G., Sieber, P., Hancock, ML y Steiner, M., Diagnóstico de cáncer de próstata entre hombres con neoplasia intraepitelial de alto grado aislada inscritos en una fase prospectiva de 3 años III ensayo clínico de toremifeno oral J Clin Oncol, 2013; 31: 523-9. https://ascopubs.org/doi/abs/10.1200/JCO.2012.41.7634= Consultado el 31 de julio de 2019
- ^ Raghow, S., Hooshdaran, MZ, Katiyar, S. y Steiner, MS, Toremifeno previene el cáncer de próstata en el modelo de adenocarcinoma transgénico de próstata de ratón. Cancer Research 2002; 62: 1370-6. http://cancerres.aacrjournals.org/content/62/5/1370= Consultado el 31 de julio de 2019
Lectura adicional [ editar ]
- Taras TL, Wurz GT, Linares GR, DeGregorio MW (2000). "Farmacocinética clínica del toremifeno". Clin Pharmacokinet . 39 (5): 327–34. doi : 10.2165 / 00003088-200039050-00002 . PMID 11108432 . S2CID 26647296 .
- Harvey HA, Kimura M, Hajba A (2006). "Toremifeno: una evaluación de su perfil de seguridad". De mama . 15 (2): 142–57. doi : 10.1016 / j.breast.2005.09.007 . PMID 16289904 .
- Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (2006). "Toremifeno: una terapia prometedora para la prevención del cáncer de próstata y las complicaciones de la terapia de privación de andrógenos". Opinión de Expertos Investigar Drogas . 15 (3): 293-305. doi : 10.1517 / 13543784.15.3.293 . PMID 16503765 . S2CID 29510508 .
- Zhou WB, Ding Q, Chen L, Liu XA, Wang S (2011). "El toremifeno es una alternativa eficaz y segura al tamoxifeno en la terapia endocrina adyuvante para el cáncer de mama: resultados de cuatro ensayos aleatorizados". Res. De cáncer de mama Tratar . 128 (3): 625–31. doi : 10.1007 / s10549-011-1556-5 . PMID 21553116 . S2CID 36985808 .
- Gennari L, Merlotti D, Stolakis K, Nuti R (2012). "Evaluación farmacocinética del toremifeno y sus implicaciones clínicas para el tratamiento de la osteoporosis". Opinión del experto Droga Metab Toxicol . 8 (4): 505-13. doi : 10.1517 / 17425255.2012.665873 . PMID 22356442 . S2CID 19547631 .
- Mao C, Yang ZY, He BF, Liu S, Zhou JH, Luo RC, Chen Q, Tang JL (2012). "Toremifeno versus tamoxifeno para el cáncer de mama avanzado". Cochrane Database Syst Rev (7): CD008926. doi : 10.1002 / 14651858.CD008926.pub2 . PMID 22786516 .
- Vogel CL, Johnston MA, Alcaparras C, Braccia D (2014). "Toremifeno para el cáncer de mama: una revisión de 20 años de datos" . Clin. Cáncer de mama . 14 (1): 1–9. doi : 10.1016 / j.clbc.2013.10.014 . PMID 24439786 .
- Mustonen MV, Pyrhönen S, Kellokumpu-Lehtinen PL (2014). "Toremifeno en el tratamiento del cáncer de mama" . Mundo J Clin Oncol . 5 (3): 393–405. doi : 10.5306 / wjco.v5.i3.393 . PMC 4127610 . PMID 25114854 .
Enlaces externos [ editar ]
- Toremifeno - AdisInsight