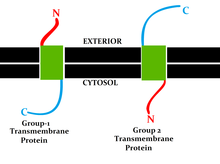
La topología de una proteína transmembrana se refiere a las ubicaciones de los extremos N y C de la cadena polipeptídica que atraviesa la membrana con respecto a los lados interno o externo de la membrana biológica ocupada por la proteína. [1]
Varias bases de datos proporcionan topologías determinadas experimentalmente de proteínas de membrana. Incluyen Uniprot , TOPDB, [3] [4] [5] OPM y ExTopoDB. [6] [7] También hay una base de datos de dominios ubicados de forma conservadora en un cierto lado de las membranas, TOPDOM. [8]
Se desarrollaron varios métodos computacionales, con un éxito limitado, para predecir hélices alfa transmembrana y su topología. Los métodos pioneros utilizaron el hecho de que las regiones que atraviesan la membrana contienen más residuos hidrófobos que otras partes de la proteína; sin embargo, la aplicación de diferentes escalas hidrófobas alteró los resultados de la predicción. Posteriormente, se desarrollaron varios métodos estadísticos para mejorar la predicción de la topografía y se introdujo un método de alineación especial. [9] Según la regla del interior positivo, [10]Los bucles citosólicos cerca de la bicapa lipídica contienen más aminoácidos cargados positivamente. La aplicación de esta regla dio como resultado los primeros métodos de predicción de topología. También existe una regla externa negativa en las hélices alfa transmembrana de proteínas de paso único, aunque los residuos cargados negativamente son más raros que los residuos cargados positivamente en los segmentos transmembrana de proteínas. [11] A medida que se determinaron más estructuras, aparecieron algoritmos de aprendizaje automático. Los métodos de aprendizaje supervisados se entrenan en un conjunto de estructuras determinadas experimentalmente; sin embargo, estos métodos dependen en gran medida del conjunto de entrenamiento. [12] [13] [14] [15] Aprendizaje no supervisadoLos métodos se basan en el principio de que la topología depende de la divergencia máxima de las distribuciones de aminoácidos en diferentes partes estructurales. [16] [17] También se demostró que bloquear la ubicación de un segmento basándose en el conocimiento previo sobre la estructura mejora la precisión de la predicción. [18] Esta característica se ha agregado a algunos de los métodos de predicción existentes. [19] [20] Los métodos más recientes utilizan la predicción por consenso (es decir, utilizan varios algoritmos para determinar la topología final) [21] e incorporan automáticamente información experimental previamente determinada. [22] Base de datos HTP [23] [24] proporciona una colección de topologías que se predicen computacionalmente para proteínas transmembrana humanas.
La discriminación de péptidos señal y segmentos transmembrana es un problema adicional en la predicción de topología tratada con un éxito limitado por diferentes métodos. [25] Tanto los péptidos señal como los segmentos transmembrana contienen regiones hidrófobas que forman hélices α. Esto provoca la predicción cruzada entre ellos, que es una debilidad de muchos predictores de topología transmembrana. Al predecir péptidos señal y hélices transmembrana simultáneamente (Phobius [26] ), los errores causados por la predicción cruzada se reducen y el rendimiento aumenta sustancialmente. Otra característica utilizada para aumentar la precisión de la predicción es la homología (PolyPhobius) ".
También es posible predecir la topología de las proteínas de membrana de barril beta. [27] [28]
Ver también
Referencias
- ^ von Heijne, Gunnar (diciembre de 2006). "Topología de proteínas de membrana". Nature Reviews Biología celular molecular . 7 (12): 909–918. doi : 10.1038 / nrm2063 . PMID 17139331 . S2CID 22218266 .
- ^ Goder, Veit; Spiess, Martin (31 de agosto de 2001). "Topogénesis de proteínas de membrana: determinantes y dinámica" . Cartas FEBS . 504 (3): 87–93. doi : 10.1016 / S0014-5793 (01) 02712-0 . PMID 11532438 .
- ^ Tusnády, Gábor E .; Kalmár, Lajos; Simon, István (1 de enero de 2008). "TOPDB: banco de datos de topología de proteínas transmembrana" . Investigación de ácidos nucleicos . 36 (supl_1): D234 – D239. doi : 10.1093 / nar / gkm751 . PMID 17921502 .
- ^ Dobson, László; Langó, Tamás; Reményi, István; Tusnády, Gábor E. (28 de enero de 2015). "Agilización de la recopilación de datos de topología para la base de datos TOPDB" . Investigación de ácidos nucleicos . 43 (D1): D283 – D289. doi : 10.1093 / nar / gku1119 . PMC 4383934 . PMID 25392424 .
- ^ Base de datos TOPDB
- ↑ Tsaousis, Georgios N .; Tsirigos, Konstantinos D .; Andrianou, Xanthi D .; Liakopoulos, Theodore D .; Bagos, Pantelis G .; Hamodrakas, Stavros J. (1 de octubre de 2010). "ExTopoDB: una base de datos de modelos topológicos derivados experimentalmente de proteínas transmembrana" . Bioinformática . 26 (19): 2490–2492. doi : 10.1093 / bioinformatics / btq362 . PMID 20601677 .
- ^ ExTopoDB
- ^ Base de datos TOPDOM
- ^ DAS
- ^ von Heijne, Gunnar (noviembre de 1986). "La distribución de residuos cargados positivamente en las proteínas de la membrana interna bacteriana se correlaciona con la topología transmembrana" . El diario EMBO . 5 (11): 3021-3027. doi : 10.1002 / j.1460-2075.1986.tb04601.x . PMC 1167256 . PMID 16453726 .
- ^ Baker, James Alexander; Wong, Wing-Cheong; Eisenhaber, Birgit; Warwicker, Jim; Eisenhaber, Frank (2017). "Residuos cargados junto a las regiones transmembrana revisadas: la" regla interior positivo "se complementa con la" regla de enriquecimiento exterior / agotamiento interior negativo " " . Biología BMC . 15 (1): 66. doi : 10.1186 / s12915-017-0404-4 . PMC 5525207 . PMID 28738801 .
- ^ Krogh, Anders; Larsson, Björn; von Heijne, Gunnar; Sonnhammer, Erik LL (enero de 2001). "Predicción de la topología de proteínas transmembrana con un modelo de Markov oculto: aplicación para completar genomas11Editado por F. Cohen" (PDF) . Revista de Biología Molecular . 305 (3): 567–580. doi : 10.1006 / jmbi.2000.4315 . PMID 11152613 . S2CID 15769874 . Archivado desde el original (PDF) el 4 de agosto de 2020.
- ^ Servidor TMHMM
- ^ Servidor Phobius
- ^ Servidor OCTOPUS
- ^ Tusnády, Gábor E .; Simon, István (octubre de 1998). "Principios que rigen la composición de aminoácidos de proteínas integrales de membrana: aplicación a la predicción de topología 1 1Editado por J. Thornton" (PDF) . Revista de Biología Molecular . 283 (2): 489–506. doi : 10.1006 / jmbi.1998.2107 . PMID 9769220 . S2CID 15027232 . Archivado desde el original (PDF) el 8 de febrero de 2020.
- ^ Servidor HMMTOP
- ^ Tusnady, GE; Simon, I. (1 de septiembre de 2001). "El servidor de predicción de topología transmembrana HMMTOP" . Bioinformática . 17 (9): 849–850. doi : 10.1093 / bioinformatics / 17.9.849 . PMID 11590105 .
- ^ Servidor HMMTOP
- ^ Servidor Phobius
- ^ Servidor TOPCONS
- ^ Servidor CCTOP
- ^ Dobson, László; Reményi, István; Tusnády, Gábor E. (28 de mayo de 2015). "El proteoma transmembrana humano" . Biology Direct . 10 (1): 31. doi : 10.1186 / s13062-015-0061-x . PMC 4445273 . PMID 26018427 .
- ^ La base de datos del proteoma transmembrana humano
- ^ E. Tusnady, Gabor; Simon, Istvan (1 de noviembre de 2010). "Predicción topológica de proteínas transmembrana helicoidales: ¿qué tan lejos hemos llegado?" (PDF) . Ciencia actual de proteínas y péptidos . 11 (7): 550–561. doi : 10.2174 / 138920310794109184 . PMID 20887261 . S2CID 6431228 . Archivado desde el original (PDF) el 7 de marzo de 2019.
- ^ http://phobius.sbc.su.se/
- ↑ Tsirigos, Konstantinos D .; Elofsson, Arne; Bagos, Pantelis G. (1 de septiembre de 2016). "PRED-TMBB2: predicción de topología mejorada y detección de proteínas de membrana externa de barril beta" . Bioinformática . 32 (17): i665 – i671. doi : 10.1093 / bioinformatics / btw444 . PMID 27587687 .
- ^ Savojardo, Castrense; Fariselli, Piero; Casadio, Rita (15 de febrero de 2013). "BETAWARE: una herramienta de aprendizaje automático para detectar y predecir proteínas de barril beta transmembrana en procariotas" . Bioinformática . 29 (4): 504–505. doi : 10.1093 / bioinformática / bts728 . PMID 23297037 .
- Proteínas integrales de membrana
- Biología de membranas
- Topología molecular