 | |
| Nombres | |
|---|---|
| Nombre IUPAC Diclorodioxouranio | |
| Otros nombres Uranio (VI), diclorodioxi | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| ChemSpider | |
| Tarjeta de información ECHA | 100.029.315 |
| Número CE |
|
PubChem CID | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| UO 2 Cl 2 | |
| Masa molar | 340,90 |
| Punto de fusion | Se descompone |
| Punto de ebullición | Se descompone |
| Solubilidad en otros disolventes. | 320 @ 18C |
| Riesgos | |
| Ficha de datos de seguridad | MSDS externa |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El cloruro de uranilo se refiere a compuestos inorgánicos con la fórmula UO 2 Cl 2 (H 2 O) n donde n = 0, 1 o 3. Estos son sólidos de color amarillo.
Síntesis y estructuras
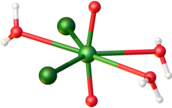
Los hidratos se obtienen disolviendo sulfato de uranilo o acetato de uranilo en ácido clorhídrico seguido de cristalización en soluciones concentradas. Dependiendo del método de secado, se obtiene el mono o el trihidrato. El monohidrato se describe como un polvo amarillo similar al azufre. Es muy higroscópico. [2] El trihidrato es de color amarillo verdoso. Ambos hidratos son sólidos fluorescentes que son altamente solubles en agua. [3]
El material anhidro se puede obtener mediante la reacción de oxígeno con tetracloruro de uranio :
- UCl 4 + O 2 → UO 2 Cl 2 + Cl 2
En términos de estructuras, estos tres compuestos presentan el centro de uranilo ( trans -UO 2 2+ ) unido a cinco ligandos adicionales, que pueden incluir cloruro (puente), agua u otro oxígeno de uranilo. [4] [5]
Reacciones
Los ligandos aquo se pueden reemplazar por una variedad de donantes, por ejemplo, THF. [6]
Importancia industrial
La empresa Indian Rare Earths Limited (IREL) ha desarrollado un proceso para extraer uranio de las arenas de dunas costeras occidentales y orientales de la India . Después del preprocesamiento con separadores magnéticos de alta intensidad y molienda fina, las arenas minerales (conocidas como monacita ) se digieren con sosa cáustica a aproximadamente 120 ° C (248 ° F) y agua. El concentrado de hidróxido se digiere adicionalmente con ácido clorhídrico concentrado para solubilizar todos los hidróxidos y formar una solución de alimentación compuesta de cloruros de uranio y otros elementos de tierras raras, incluido el torio . La solución se somete aextracción líquido-líquido con sistemas de doble disolvente para producir cloruro de uranilo y oxalato de torio . La solución de cloruro de uranilo en bruto se refina posteriormente a diuranato de amonio de grado nuclear mediante un proceso de purificación que implica precipitación y extracción con disolvente en un medio de nitrato.
Referencias
- ^ Debets, PC (1968). "Las estructuras del cloruro de uranilo y sus hidratos". Acta Crystallographica Sección B Cristalografía estructural y química cristalina . 24 (3): 400–402. doi : 10.1107 / S056774086800244X .
- ^ Hefley, Jack D .; Mathews, Daniel M .; Amis, Edward S. (1963). "Cloruro de uranilo 1-hidrato". Síntesis inorgánica . Síntesis inorgánica. 7 . págs. 146-148. doi : 10.1002 / 9780470132388.ch41 . ISBN 9780470132388.
- ^ F. Hein, S. Herzog (1963). "Cloruro de uranilo". En G. Brauer (ed.). Manual de Química Inorgánica Preparativa, 2ª Ed . 2 . Nueva York, Nueva York: Academic Press. pag. 1439.
- ^ Taylor, JC; Wilson, PW (1973). "La estructura del cloruro de uranilo anhidro por difracción de neutrones en polvo". Acta Crystallographica Sección B Cristalografía estructural y química cristalina . 29 (5): 1073–1076. doi : 10.1107 / S0567740873003882 .
- ^ Leary, Joseph A .; Suttle, John F. (1957). "Cloruro de uranilo". Síntesis inorgánica . Síntesis inorgánica. 5 . págs. 148–150. doi : 10.1002 / 9780470132364.ch41 . ISBN 9780470132364.
- ^ Wilkerson, Marianne P .; Burns, Carol J .; Paine, Robert T .; Scott, Brian L. (1999). "Síntesis y estructura cristalina de UO 2 Cl 2 (THF) 3 : una preparación simple de un reactivo de uranilo anhidro". Química inorgánica . 38 (18): 4156–4158. doi : 10.1021 / ic990159g .
- "Uranio". Encyclopædia Britannica . V27 . 1911. p. 788.
- Heyes, SJ (1998). "Lantánidos y actínidos" . Cuatro Conferencias de Química Inorgánica de 2º año . Consultado el 22 de noviembre de 2011 .
Enlaces externos
- Tranquilízate, Frank. "Química nuclear y comunidad" . www.chemcases.com: Casos de estudio de química general . Consultado el 22 de noviembre de 2011 .