
En química, un vanadato es un complejo de coordinación aniónico de vanadio . A menudo, el vanadato se refiere a oxoaniones de vanadio , la mayoría de los cuales existen en su estado de oxidación más alto de +5. Los complejos [V (CN) 6 ] 3- y [V 2 Cl 9 ] 3- se denominan hexacianovanadato y no clorodivanadato.
Un ion vanadato simple es el tetraédrico, ortovanadato, VO3−
4anión, que está presente, por ejemplo, en ortovanadato de sodio y en soluciones de V 2 O 5 en una base fuerte ( pH > 13 [1] ). Convencionalmente, este ion se representa con un enlace doble simple, sin embargo, esta es una forma de resonancia ya que el ion es un tetraedro regular con cuatro átomos de oxígeno equivalentes.
Además, existe una gama de iones polioxovanadato que incluyen iones discretos e iones poliméricos "infinitos". [2] También hay vanadatos, como el vanadato de rodio, RhVO 4 , que tiene una estructura estadística de rutilo donde los iones Rh 3+ y V 5+ ocupan aleatoriamente las posiciones de Ti 4+ en la red de rutilo, [3] que no contienen una red de cationes y aniones de vanadato equilibrantes, pero son óxidos mixtos .
En la nomenclatura química, cuando el vanadato forma parte del nombre, indica que el compuesto contiene un anión con un átomo de vanadio central, por ejemplo, hexafluorovanadato de amonio es un nombre común para el compuesto (NH 4 ) 3 VF 6 con el nombre IUPAC de hexafluoridovanadato de amonio ( III).
Ejemplos de iones oxovanadato
Algunos ejemplos de iones discretos son
- VO3−
4"ortovanadato", tetraédrico. [2] - V
2O4−
7"pirovanadato", VO 4 tetraedros compartidos en las esquinas , similar al ion dicromato [2] - V
3O3-
9, cíclico con tetraedros VO 4 compartidos en las esquinas [4] - V
4O4−
12, cíclico con tetraedros VO 4 compartidos en las esquinas [5] - V
5O3-
14, esquina compartida VO 4 tetraedros [6] - V
6O6-
18, anillo. [7] - V
10O6-
28"decavanadate", VO de 6 octaedros con bordes y esquinas compartidos [2] - V
12O4−
32 - V
13O3−
34, VO 6 octaedros fusionados [8] - V
18O12−
42[9]
Algunos ejemplos de iones poliméricos "infinitos" son
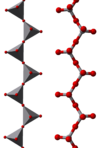 |  | 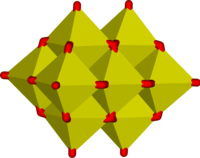 |
En estos iones, el vanadio exhibe coordinación tetraédrica, piramidal cuadrada y octaédrica. A este respecto, el vanadio muestra similitudes con el tungstato y el molibdato , mientras que el cromo, sin embargo, tiene una gama de iones más limitada.
Soluciones acuosas
La disolución de pentóxido de vanadio en una solución acuosa fuertemente básica da el VO incoloro3−
4ion. Con la acidificación, el color de esta solución se oscurece gradualmente de naranja a rojo a aproximadamente pH 7. El V 2 O 5 marrón hidratado precipita alrededor de pH 2, volviéndose a disolver para formar una solución de color amarillo claro que contiene el ión [VO 2 (H 2 O) 4 ] + . El número y la identidad de los oxianiones que existen entre pH 13 y 2 dependen del pH y de la concentración. Por ejemplo, la protonación de vanadato inicia una serie de condensaciones para producir iones polioxovanadato: [2]
- pH 9-12; HVO2−
4, V
2O4−
7 - pH 4-9; H
2VO-
4, V
4O4−
12, HV
10O5−
28 - pH 2-4; H 3 VO 4 , H
2V
10O4−
28
Propiedades farmacológicas
Vanadato es un potente inhibidor de ciertas ATPasas de la membrana plasmática , como Na + / K + -ATPasa y Ca 2+ -ATPasa ( PMCA ). Actuando como un análogo del fosfato en el estado de transición, el vanadato sufre un ataque nucleofílico por el agua durante la transferencia de fosforilo, esencialmente "atrapando" las ATPasas de tipo P en su estado E2 fosforilado.[11] [12] Sin embargo, no inhibe otras ATPasas, como SERCA (sarco / retículo endoplásmico Ca 2+ -ATPasa), actomiosina ATPasa y ATPasa mitocondrial. [13] [14] [15]
Referencias
- ^ Algodón, F. Albert ; Wilkinson, Geoffrey ; Murillo, Carlos A .; Bochmann, Manfred (1999), Química inorgánica avanzada (6.a ed.), Nueva York: Wiley-Interscience, ISBN 0-471-19957-5
- ^ a b c d e f Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Wells AF (1984) Química inorgánica estructural 5ta edición Publicaciones de ciencia de Oxford ISBN 0-19-855370-6
- ^ Hamilton EE; Fanwick PE; Wilker JJ (2002). "El escurridizo Vanadato (V 3 O 9 ) 3− : aislamiento, estructura cristalina y comportamiento de solución no acuosa" . Mermelada. Chem. Soc. 124 (1): 78–82. doi : 10.1021 / ja010820r . PMID 11772064 .
- ^ G.-Y. Yang, D.-W. Gao, Y. Chen, J.-Q. Xu, Q.-X. Zeng, H.-R. Sol, Z.-W. Pei, Q. Su, Y. Xing, Y.-H. Ling y H.-Q. Jia (1998). "[Ni (C 10 H 8 N 2 ) 3 ] 2 [V 4 O 12 ] · 11H 2 O". Acta Crystallographica C . 54 (5): 616–618. doi : 10.1107 / S0108270197018751 .CS1 maint: varios nombres: lista de autores ( enlace )
- ^ Día de VW; Walter G. Klemperer; OM Yaghi (1989). "Un nuevo tipo de estructura en la química de polioxoaniones: síntesis y estructura de la V
5O3-
14anión ". J. Am. Chem. Soc. 111 (12): 4518. doi : 10.1021 / ja00194a068 . - ^ Guang-Chuan Ou .; Long Jiang; Xiao-Long Feng; Tong-Bu Lu (2009). "Complejos metálicos macrocíclicos con puentes de polioxoanión de vanadio: de estructuras unidimensionales a tridimensionales" . Transacciones de Dalton . 1 (1): 71–76. doi : 10.1039 / B810802A . PMID 19081973 .
- ^ Hou D .; Hagen KD; Hill CL (1992). "Tridecavanadate, [V 13 O 34 ] 3− , un nuevo isopolvanadato de alto potencial". Mermelada. Chem. Soc. 114 (14): 5864. doi : 10.1021 / ja00040a061 .
- ^ Müller A .; Sessoli R .; Krickemeyer E .; Bögge H .; Meyer J .; Gatteschi D .; Pardi L .; Westphal J .; Hovemeier K .; Rohlfing R .; Döring J; Hellweg F .; Beugholt C .; Schmidtmann M. (1997). "Polioxovanadates: clústeres de espín de alta nuclearidad con interesantes sistemas huésped-invitado y diferentes poblaciones de electrones. Síntesis, organización de espín, magnetoquímica y estudios espectroscópicos". Inorg. Chem. 36 (23): 5239. doi : 10.1021 / ic9703641 .
- ^ Jouanneau, S .; Verbaere, A .; Guyomard, D. (2003). "Sobre un nuevo vanadato de calcio: síntesis, estructura y comportamiento de inserción de Li". Revista de química del estado sólido . 172 (1): 116-122. Código bibliográfico : 2003JSSCh.172..116J . doi : 10.1016 / S0022-4596 (02) 00164-0 .
- ^ Kühlbrandt, Werner (abril de 2004). "Biología, estructura y mecanismo de las ATPasas tipo P". Reseñas de la naturaleza. Biología celular molecular . 5 (4): 282–295. doi : 10.1038 / nrm1354 . ISSN 1471-0072 . PMID 15071553 .
- ^ Davies, Douglas R .; Hol, Wim GJ (19 de noviembre de 2004). "El poder del vanadato en las investigaciones cristalográficas de las enzimas de transferencia de fosforilo" . Cartas FEBS . 577 (3): 315–321. doi : 10.1016 / j.febslet.2004.10.022 . ISSN 0014-5793 . PMID 15556602 .
- ^ Luo D .; Nakazawa M .; Yoshida Y .; Cai J .; Imai S. (2000). "Efectos de tres inhibidores de ATPasa de bomba de Ca 2+ diferentes sobre las contracciones provocadas en la aorta de conejo y actividades de las ATPasas de bomba de Ca 2+ en la aorta porcina". Farmacología general: el sistema vascular . 34 (3): 211–220. doi : 10.1016 / S0306-3623 (00) 00064-1 . PMID 11120383 .
- ^ Bowman BJ; Slayman CW (1979). "Los efectos del vanadato sobre la ATPasa de membrana plasmática de Neurospora crassa". Revista de Química Biológica . 254 (8): 2928–2934. PMID 155060 .
- ↑ Aureliano, Manuel; Crans, Debbie C. (2009). "Decavanadate ( V10O6- 28) y oxovanadatos: oxometalatos con muchas actividades biológicas " . Journal of Inorganic Biochemistry . 103 (4): 536–546. doi : 10.1016 / j.jinorgbio.2008.11.010 . ISSN 0162-0134 .