 | |
| Datos clinicos | |
|---|---|
| Otros nombres | SKF-10047; WIN-19631; N- alinormetazocina; NANM; YAYA; ANMC; 2'-Hidroxi-5,9-dimetil-2-alil-6,7-benzomorfano |
| Código ATC |
|
| Identificadores | |
| |
| Número CAS |
|
| PubChem CID | |
| ChemSpider | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.162.264 |
| Datos químicos y físicos | |
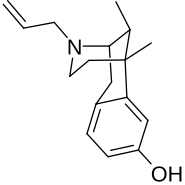
| Fórmula | C 17 H 23 N O |
| Masa molar | 257,377 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
| | |
La alazocina (nombre de código de desarrollo SKF -10047 ), también conocida más comúnmente como N- alinormetazocina ( NANM ), es un analgésico opioide sintético de la familia de los benzomorfanos relacionado con la metazocina , que nunca se comercializó. [1] [2] [3] Además de su actividad opioide, el fármaco es un agonista del receptor sigma y se ha utilizado ampliamente en investigaciones científicas en estudios de este receptor. [4] [5] La alazocina se describe como un analgésico potente , psicotomimético o alucinógeno y morfina o antagonista opioide . [2] Por otra parte, uno de sus enantiómeros fue el primer compuesto que se encontró que selectivamente etiquetar la σ 1 receptor , y condujo al descubrimiento y la caracterización del receptor. [4] [5]
Farmacología [ editar ]
Farmacodinámica [ editar ]
Alazocina muestra estereoselectividad en su farmacodinámica . [6] El (-) - enantiómero es un ligando no selectivo y de alta afinidad de los receptores opioides μ , κ y δ (K i = 3,0, 4,7 y 15 nM en las membranas cerebrales de cobayas ) con muy baja afinidad por el receptor sigma σ 1 (K i = 1.800–4.657 nM en membranas cerebrales de cobaya). [6] [7] Actúa como un agonista parcial de eficacia moderada del receptor de opioides κ (K i = 0,4 nM, CE 50 = 24 nM, y E max = 66% para (±) -alazocine contra el ratón receptor transfectado en HEK293 células) [8] y como un antagonista del receptor μ-opioide (K i = 1,15 nM para (±) -alazocina contra el receptor de ratón transfectado en células HEK293). [9] También es un agonista del receptor δ-opioide con una potencia mucho menor (K i = no informado, IC 50 = 184 nM e I max = 68% para (±) -alazocina contra el receptor de ratón transfectado en HEK293 células). [10]
A la inversa, la (+) - estereoisómero tiene poca afinidad por los receptores opioides (K i para 1900 nM, 1600 nM, y 19.000 nM para la μ-, κ-, los receptores delta opioide en membranas de cerebro de conejillo de indias) y en su lugar es una selectiva y de alta afinidad agonista de la σ 1 receptor (K i = 48-66 nM en las membranas de conejillo de indias cerebro). [6] [7] Sin embargo, la (+) - enantiómero también muestra moderada afinidad por la dizocilpina (MK-801) o fenciclidina (PCP) sitio del receptor de NMDA (K i = 587 nM en rata membranas de cerebro con relación a 45 nM para la σ1 ) y, por lo tanto, es un antagonista del receptor de NMDA no competitivo también a concentraciones más altas. [11] Como tal, la (+) - alazocina es sólo modestamente selectiva como ligando del receptor σ 1 . [11]
Ambos enantiómeros de alazocine tienen muy baja afinidad por el sigma sigma 2 receptor (K i = 13694 nM y 4581 nM para la (+) - y (-) - enantiómeros, respectivamente, en las membranas de cerebro de rata o de rata PC12 células). [11] [7] [5] Como tal, debido a su alta afinidad por el receptor σ 1 , (+) - alazocina se puede utilizar para distinguir entre los dos subtipos de receptores sigma en la investigación científica, por ejemplo, en ensayos de unión de radioligandos . [11] [5]
En conjunto, la (-) - alazocina es un agonista parcial selectivo del receptor opioide κ, antagonista del receptor opioide μ y, en mucho menor grado, agonista del receptor opioide δ [8] [9] [10] con muy baja afinidad por los receptores sigma, mientras que (+) - alazocina es un agonista selectivo del receptor sigma σ 1 y en menor grado (~ 10 veces) antagonista del receptor NMDA con baja afinidad por el opioide y sigma σ 2 receptores. [6] [7] [11] [5]
Historia [ editar ]
Alazocine fue uno de los primeros miembros de la familia benzomorfano de analgésicos opioides que se investigó. [1] Se describió por primera vez en la literatura científica en 1961. [12] Su desarrollo fue el resultado de la nalorfina (N-alilnormorfina), un potente antagonista analgésico y opioide con farmacología similar que se había introducido a mediados de la década de 1950. [1] Se encontró que la alazocina produce fuertes efectos psicotomiméticos en humanos, y no se desarrolló más para uso clínico. [13] [1] Posteriormente, otros benzomorfanos, como pentazocina (un N -dimetilalilbenzomorfano), ciclazocina(un N- ciclopropilmetilbenzomorfano) y fenazocina (un N- feniletilbenzomorfano), y algunos se han comercializado para su uso como analgésicos. [1]
El receptor sigma σ 1 se nombró en 1976 y (+) - alazocina se describió como su ligando prototípico. [13] [14] [15] Inicialmente se pensó que el receptor era un receptor opioide y luego se confundió con el receptor NMDA durante un tiempo, pero finalmente se distinguió de ambos. [13] [14] [5] Los efectos psicotomiméticos de la alazocina y los otros benzomorfanos se atribuyeron inicialmente de forma incorrecta al agonismo del receptor σ 1 ; investigaciones posteriores establecieron que los efectos son de hecho causados por el agonismo del receptor de opioides κ y / o antagonismo del receptor de NMDA. [13] [5] El sigma σ 2receptor fue descubierto y nombrado en 1990, y fue identificado en parte debido a la afinidad dramáticamente reducida de la alazocina por el receptor en relación con el receptor σ 1 (en contraste con ligandos no selectivos como haloperidol , ditolilguanidina y (+) - 3- PPP , que muestran una afinidad similar por ambos subtipos). [7]
Referencias [ editar ]
- ^ a b c d e A.F. Casy; RT Parfitt (29 de junio de 2013). Analgésicos opioides: química y receptores . Springer Science & Business Media. págs. 176–178, 420–421. ISBN 978-1-4899-0585-7.
- ↑ a b Keats, Arthur S .; Telford, Jane (1964). "Antagonistas narcóticos como analgésicos". Modificación molecular en el diseño de fármacos . Avances en Química. 45 . págs. 170-176. doi : 10.1021 / ba-1964-0045.ch014 . ISBN 0-8412-0046-7. ISSN 0065-2393 .
- ^ Iwamoto ET (febrero de 1981). "Efectos farmacológicos de la N-alilnormetazocina (SKF-10047)". Monografía de investigación del NIDA . 34 : 82–8. PMID 6783955 .
- ↑ a b Narayanan S, Bhat R, Mesangeau C, Poupaert JH, McCurdy CR (enero de 2011). "Desarrollo temprano de ligandos del receptor sigma". Futura química medicinal . 3 (1): 79–94. doi : 10.4155 / fmc.10.279 . PMID 21428827 .
- ↑ a b c d e f g Hayashi T, Su TP (2004). "Ligandos del receptor sigma-1: potencial en el tratamiento de trastornos neuropsiquiátricos". Medicamentos para el SNC . 18 (5): 269–84. doi : 10.2165 / 00023210-200418050-00001 . PMID 15089113 . S2CID 72726251 .
- ↑ a b c d Tam SW (febrero de 1985). "(+) - [3H] SKF 10.047, (+) - [3H] etilcetociclazocina, sitios de unión mu, kappa, delta y fenciclidina en membranas cerebrales de cobaya". Revista europea de farmacología . 109 (1): 33–41. doi : 10.1016 / 0014-2999 (85) 90536-9 . PMID 2986989 .
- ↑ a b c d e Hellewell SB, Bowen WD (septiembre de 1990). "Un sitio de unión similar a sigma en células de feocromocitoma de rata (PC12): la afinidad disminuida por (+) - benzomorfanos y el peso molecular más bajo sugieren una forma de receptor sigma diferente de la del cerebro de cobaya". Investigación del cerebro . 527 (2): 244–53. doi : 10.1016 / 0006-8993 (90) 91143-5 . PMID 2174717 . S2CID 24546226 .
- ↑ a b Gharagozlou P, Hashemi E, DeLorey TM, Clark JD, Lameh J (enero de 2006). "Perfiles farmacológicos de ligandos opioides en receptores opioides kappa" . Farmacología de BMC . 6 : 3. doi : 10.1186 / 1471-2210-6-3 . PMC 1403760 . PMID 16433932 .
- ↑ a b Gharagozlou P, Demirci H, David Clark J, Lameh J (enero de 2003). "Actividad de ligandos opioides en células que expresan receptores opioides mu clonados" . Farmacología de BMC . 3 : 1. doi : 10.1186 / 1471-2210-3-1 . PMC 140036 . PMID 12513698 .
- ↑ a b Gharagozlou P, Demirci H, Clark JD, Lameh J (noviembre de 2002). "Perfiles de activación de ligandos opioides en células HEK que expresan receptores opioides delta" . BMC Neuroscience . 3 : 19. doi : 10.1186 / 1471-2202-3-19 . PMC 137588 . PMID 12437765 .
- ^ a b c d e Chou YC, Liao JF, Chang WY, Lin MF, Chen CF (marzo de 1999). "Unión de dimemorfan al receptor sigma-1 y sus efectos anticonvulsivos y locomotores en ratones, en comparación con dextrometorfano y dextrorfano". Investigación del cerebro . 821 (2): 516–9. doi : 10.1016 / s0006-8993 (99) 01125-7 . PMID 10064839 . S2CID 22762264 .
- ^ Gordon M, Lafferty JJ, Tedeschi DH, Eddy NB, May EL (diciembre de 1961). "Un nuevo antagonista analgésico potente" . Naturaleza . 192 (4807): 1089. doi : 10.1038 / 1921089a0 . PMID 13900480 . S2CID 4212447 .
- ^ a b c d Osborne Almeida; Toni S. Shippenberg (6 de diciembre de 2012). Neurobiología de los opioides . Springer Science & Business Media. págs. 356–. ISBN 978-3-642-46660-1.
- ↑ a b Jürgen Schüttler; Helmut Schwilden (8 de enero de 2008). Anestésicos modernos . Springer Science & Business Media. págs. 97–. ISBN 978-3-540-74806-9.
- ^ Martin WR, Eades CG, Thompson JA, Huppler RE, Gilbert PE (junio de 1976). "Los efectos de los fármacos similares a la morfina y la nalorfina en el perro espinal crónico no dependiente y dependiente de la morfina". La Revista de Farmacología y Terapéutica Experimental . 197 (3): 517–32. PMID 945347 .