Amidina
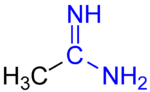
Las amidinas son compuestos orgánicos con el grupo funcional RC(NR)NR 2 , donde los grupos R pueden ser iguales o diferentes. Son los derivados imínicos de las amidas (RC(O)NR 2 ). La amidina más simple es la formamidina, HC(=NH)NH 2 .
Una ruta común a las amidinas primarias es la reacción de Pinner . La reacción del nitrilo con alcohol en presencia de ácido da un iminoéter . El tratamiento del compuesto resultante con amoníaco luego completa la conversión a la amidina. [1] En lugar de usar un ácido de Bronsted , los ácidos de Lewis como el tricloruro de aluminio promueven la aminación directa de los nitrilos . [2] También se generan por aminación de un cloruro de imidoilo . [3] También se preparan mediante la adición de reactivos de organolitio adiiminas , seguidas de protonación o alquilación .
Las amidinas son mucho más básicas que las amidas y se encuentran entre las bases sin carga/sindicadas más fuertes. [5] [6]
La protonación se produce en el nitrógeno hibridado sp 2 . Esto ocurre porque la carga positiva se puede deslocalizar en ambos átomos de nitrógeno. La especie catiónica resultante se conoce como ion amidinio [7] y posee longitudes de enlace CN idénticas.
Varios fármacos o candidatos a fármacos presentan sustituyentes de amidina. Los ejemplos incluyen el antiprotozoario Imidocarb , el insecticida amitraz , el antihelmíntico tribendimidina y xilamidina , un antagonista del receptor 5HT2A. [8]
El formamidinio (ver más abajo) se puede hacer reaccionar con un haluro metálico para formar el material semiconductor que absorbe la luz en las células solares de perovskita . Los cationes o haluros de formamidinio (FA) pueden reemplazar parcial o totalmente a los haluros de metilamonio en la formación de capas absorbentes de perovskita en dispositivos fotovoltaicos .