 | |
| Nombres | |
|---|---|
| Otros nombres Exolit AP 422, FR CROS 484, CS FR APP 231 | |
| Identificadores | |
| CHEBI | |
| Tarjeta de información ECHA | 100.063.425 |
| Número e | E452 (v) (espesantes, ...) |
Tablero CompTox ( EPA ) | |
| Propiedades | |
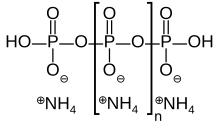
| [NH 4 PO 3 ] n (OH) 2 | |
| Masa molar | 97,01 g / mol |
| Apariencia | polvo blanco |
| Densidad | 1,9 g / cm 3 ; densidad aparente = 0,7 g / cm 3 |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El polifosfato de amonio es una sal inorgánica de ácido polifosfórico y amoníaco que contiene ambas cadenas y posiblemente ramificaciones. Su fórmula química es [NH 4 PO 3 ] n (OH) 2 mostrando que cada monómero consiste en un radical ortofosfato de un átomo de fósforo con tres oxígenos y una carga negativa neutralizada por un catión amonio dejando dos enlaces libres para polimerizar . En los casos ramificados, a algunos monómeros les falta el anión amonio y, en cambio, se unen a otros tres monómeros.
Las propiedades del polifosfato de amonio dependen del número de monómeros en cada molécula y hasta cierto punto de la frecuencia con la que se ramifica. Las cadenas más cortas (n <100) son más sensibles al agua y menos estables térmicamente que las cadenas más largas (n> 1000), [1] pero las cadenas de polímero cortas ( p. Ej., Piro-, tripoli- y tetrapoli-) son más solubles y muestran una solubilidad creciente con mayor longitud de cadena. [2]
El polifosfato de amonio se puede preparar haciendo reaccionar ácido fosfórico concentrado con amoníaco. Sin embargo, las impurezas de hierro y aluminio, solubles en ácido fosfórico concentrado, forman precipitados gelatinosos o "lodos" en polifosfato de amonio a pH entre 5 y 7. [3] Otras impurezas metálicas como cobre, cromo, magnesio y zinc forman precipitados granulares. [4] Sin embargo, dependiendo del grado de polimerización, el polifosfato de amonio puede actuar como un agente quelante para mantener ciertos iones metálicos disueltos en solución. [5]
El polifosfato de amonio se utiliza como aditivo alimentario, emulsionante ( número E : E545) y como fertilizante .
El polifosfato de amonio (APP) también se utiliza como retardante de llama en muchas aplicaciones como pinturas y recubrimientos, y en una variedad de polímeros: los más importantes son las poliolefinas , y en particular el polipropileno, donde APP forma parte de sistemas intumescentes. [6] La composición con retardantes de llama basados en APP en polipropileno se describe en. [7] Otras aplicaciones son los termoestables, donde APP se utiliza en poliésteres insaturados y gelcoats (APP se mezcla con sinergistas), epoxis y fundiciones de poliuretano (sistemas intumescentes). APP también se aplica a espumas de poliuretano retardantes de llama .
Los polifosfatos de amonio utilizados como retardadores de llama en polímeros tienen cadenas largas y una cristalinidad específica (Forma II). Comienzan a descomponerse a 240 ° C para formar amoníaco y ácido fosfórico. El ácido fosfórico actúa como catalizador ácido en la deshidratación de polialcoholes a base de carbono, como la celulosa en la madera. El ácido fosfórico reacciona con grupos alcohol para formar ésteres de fosfato inestables al calor . Los ésteres se descomponen para liberar dióxido de carbono y regenerar el catalizador de ácido fosfórico [ cita requerida ]. En la fase gaseosa, la liberación de dióxido de carbono no inflamable ayuda a diluir el oxígeno del aire y los productos de descomposición inflamables del material que se está quemando. En la fase condensada, el carbón carbonoso resultante ayuda a proteger el polímero subyacente del ataque del oxígeno y el calor radiante. [8] El uso como intumescente se logra cuando se combina con materiales a base de almidón como pentaeritritol y melamina como agentes de expansión. Los mecanismos de intumescencia y el modo de acción de la APP se describen en una serie de publicaciones. [9] [10]
Referencias [ editar ]
- ^ [1] Archivado el 22 de mayo de 2010 en la Wayback Machine.
- ^ US 4041133
- ^ US 4721519
- ^ US 3044851
- ^ Gowariker, Vasant; Krishnamurthy, VN; Gowariker, Sudha; Dhanorkar, Manik; Paranjape, Kalyani (8 de abril de 2009). "La enciclopedia de fertilizantes" . John Wiley e hijos . Consultado el 30 de junio de 2018 , a través de Google Books.
- ^ Weil, ED, Levchik, SV Retardantes de llama para plásticos y textiles, p. 16. Hanser Publishers, Munich, Alemania, 2009
- ^ "Como retardante de llama" . Mindfully.org . Archivado desde el original el 13 de septiembre de 2007 . Consultado el 30 de junio de 2018 .
- ^ US 4515632
- ^ Camino, G .; Luda, MP Estudio mecanicista de la intumescencia, p. 48 s, en Le Bras, M .; Camino, G .; Bourbigot, S .; Delobel, R. Eds., Retardancia al fuego de polímeros; El uso de la intumescencia, The Royal Society of Chemistry, Cambridge, Reino Unido, 1998
- ↑ Bourbigot, S .; Le Bras, M. Intumescencia retardadores de llama y formación de carbonilla, p. 139 y sigs., En Troitzsch, J. Ed. Manual de inflamabilidad de plásticos, 3.a edición, Hanser Publishers, Munich, 2004
Enlaces externos [ editar ]
- US 2950961
- US 4211546
- Specialchem4polymers.com