| Nombres | |||
|---|---|---|---|
| Nombre IUPAC Fluoruro de arsénico (III) | |||
| Otros nombres Trifluoruro de arsénico, trifluoroarsane | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.029.145 | ||
| Número CE |
| ||
PubChem CID | |||
| Número RTECS |
| ||
| UNII | |||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| AsF 3 | |||
| Masa molar | 131,9168 g / mol | ||
| Apariencia | líquido incoloro | ||
| Densidad | 2,666 g / cm 3 [1] | ||
| Punto de fusion | −8,5 ° C (16,7 ° F; 264,6 K) | ||
| Punto de ebullición | 60,4 ° C (140,7 ° F; 333,5 K) | ||
| se descompone | |||
| Solubilidad | soluble en solución de alcohol , éter , benceno y amoniaco | ||
| Peligros | |||
| Principales peligros | Tóxico, corrosivo | ||
| Pictogramas GHS |  | ||
| Palabra de señal GHS | Peligro | ||
| H301 , H311 , H331 | |||
| P261 , P264 , P270 , P271 , P280 , P301 + 310 , P302 + 352 , P304 + 340 , P311 , P312 , P321 , P322 , P330 , P361 , P363 , P403 + 233 , P405 , P501 | |||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
PEL (permitido) | [1910.1018] TWA 0.010 mg / m 3 [2] | ||
REL (recomendado) | Ca C 0,002 mg / m 3 [15 minutos] [2] | ||
IDLH (peligro inmediato) | Ca [5 mg / m 3 (como As)] [2] | ||
| Termoquímica | |||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | -821,3 kJ / mol | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
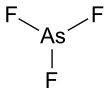
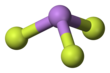
El trifluoruro de arsénico es un compuesto químico de arsénico y flúor con la fórmula química AsF 3 . Es un líquido incoloro que reacciona fácilmente con el agua. [3]
Preparación y propiedades [ editar ]
Puede prepararse haciendo reaccionar fluoruro de hidrógeno , HF, con trióxido de arsénico : [3]
- 6HF + Como 2 O 3 → 2AsF 3 + 3H 2 O
Tiene una estructura molecular piramidal en la fase gaseosa que también está presente en el sólido. [3] En la fase gaseosa, la longitud del enlace As-F es de 170,6 pm y el ángulo de enlace F-As-F de 96,2 °. [4]
El trifluoruro de arsénico se utiliza como agente fluorante para la conversión de cloruros no metálicos en fluoruros, por lo que es menos reactivo que el SbF 3 . [3]
Se pueden preparar sales que contienen anión AsF 4 -, por ejemplo CsAsF 4 . [5] la sal de potasio KAs 2 F 7 preparado a partir de KF y AsF 3 contiene AsF 4 - y ASF 3 moléculas con evidencia de interacción entre el AsF 3 molécula y el anión. [6]
AsF 3 reacciona con SbF 5 . El producto obtenido podría describirse como el compuesto iónico AsF 2 + SbF 6 - . Sin embargo, los autores concluyen que el producto formado no puede verse solo como un compuesto iónico ni completamente como el aducto neutro AsF 3 SbF 5 . La estructura cristalina muestra características tanto de un par iónico como de un aducto neutro, ocupando el término medio entre ambos modelos. [7]
Referencias [ editar ]
- ^ Pradyot Patnaik. Manual de productos químicos inorgánicos . McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ a b c Guía de bolsillo de NIOSH sobre peligros químicos. "# 0038" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ↑ a b c d Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Wells AF (1984) Química inorgánica estructural 5ta edición Publicaciones de ciencia de Oxford ISBN 0-19-855370-6
- ^ Nuevos tetrafluoroarsenatos de metales alcalinos y tetrametilamonio (III), sus espectros vibracionales y estructura cristalina de tetrafluoroarsenato de cesio (III) Klampfer P, Benkič P, Lesar A, Volavšek B, Ponikvar M, Jesih A., Collect. Checo. Chem. Comun. 2004, 69, 339-350 doi : 10.1135 / cccc20040339
- ^ Heptafluorodiarsenates de metales alcalinos (III): su preparación y la estructura cristalina de la sal de potasio, Edwards AJ, Patel SN, J. Chem. Soc., Dalton Trans., 1980, 1630-1632, doi : 10.1039 / DT9800001630
- ^ Estructuras cristalinas de fluoruro. Parte XV. Trifluoruro de arsénico-pentafluoruro de antimonio, Edwards AJ, Sills RJCJ Chem. Soc. A, 1971, 942 - 945, doi : 10.1039 / J19710000942