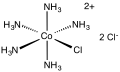
Cloruro de cloropentaminecobalto
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC Cloruro de pentaamminaclorocobalto (III) | |||
| Otros nombres Cloruro de pentaamminaclorocobalto (III) | |||
| Identificadores | |||
| |||
Modelo 3D ( JSmol ) | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.034.163 | ||
| Número CE |
| ||
PubChem CID | |||
| |||
| Propiedades | |||
| [Co (NH 3 ) 5 Cl] Cl 2 | |||
| Masa molar | 250,4 g / mol | ||
| Apariencia | cristal rojo violeta en forma de rombo | ||
| Densidad | 1,783 g / ml | ||
| Punto de ebullición | N / A | ||
| 0,4 g / 100 ml | |||
| Presión de vapor | 5990 mm Hg | ||
| Termoquímica | |||
| −1,0376E + 06 Jmol −1 ; Energía de formación molar de Gibbs = −606480 J / mol | |||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
El cloruro de cloropentamminecobalto es la sal dicloruro del complejo de coordinación [Co (NH 3 ) 5 Cl] 2+ . Es una sal de color rojo violeta, diamagnética, soluble en agua. El complejo ha sido de interés académico e histórico.
Síntesis y reacciones
La sal se prepara con un proceso de dos pasos que comienza con la oxidación de una solución de cloruro de cobalto y amoníaco. [1] [2]
- 2 CoCl 2 · 6H 2 O + 10 NH 3 + 2 HCl + H 2 O 2 → 2 [Co (NH 3 ) 5 (OH 2 )] Cl 3 + 12 H 2 O
Este intermedio luego se calienta para inducir la coordinación de uno de los ligandos de cloruro de la esfera externa:
- [Co (NH 3 ) 5 (OH 2 )] Cl 3 → [Co (NH 3 ) 5 Cl] Cl 2 + H 2 O
La indicación [Co (NH 3 ) 5 Cl] 2+ ha idealizado la simetría C 4v . [3] [4]
En una solución acuosa, el cloruro de cloropentaaminocobalto (III) reforma el complejo de aquopentamina. Con ácido sulfúrico concentrado , el cloruro de cloropentaaminocobalto (III) forma el complejo de sulfato de hidrógeno [Co (NH 3 ) 5 OSO 3 H] 2+ .
Historia
Los complejos de cobalto han sido de interés desde hace mucho tiempo en la química inorgánica porque son numerosos, fáciles de preparar y coloridos. Fue en parte sobre la base de su estudio de la química de coordinación del cobalto que Alfred Werner recibió el Premio Nobel de Química . Antes de Werner, los modelos de complejos de amina postulaban cadenas de centros de nitrógeno pentavalente. Este modelo de Jørgensen –Bloomstrand fue derrocado por Werner, quien introdujo la idea de que los complejos de coordinación presentan átomos metálicos de formas octaédricas y tetraédricas, con amoníaco y otros ligandos unidos individualmente al metal. El modelo de Werner tuvo en cuenta que los ligandos de la esfera interna eran menos reactivos. [5] En [Co (NH 3 ) 5Cl] Cl 2 , dos iones de cloruro son la esfera externa (contraiones) y uno está unido al centro de Co (III): la reacción con un exceso de nitrato de plata precipitaría inmediatamente los dos contraiones de cloruro, pero el ión de cloruro unido no precipitaría .
Ver también
Referencias
- ^ Gert G. Schlessinger (1967). "Cloruro de cloropentaamminecobalto (III)". Síntesis inorgánica . 9 : 160. doi : 10.1002 / 9780470132401.ch43 .
- ^ Williams, Gregory M; Olmsted, John, III; Preksa, Andrew P., III (1989). "Complejos de coordinación de cobalto: síntesis inorgánica en el laboratorio de química general". Revista de educación química . 66 : 1043–5. doi : 10.1021 / ed066p1043 .CS1 maint: varios nombres: lista de autores ( enlace )
- ^ GG Messmer; EL Amma (1968). "Redeterminación de la estructura cristalina del dicloruro de cloropentaamminecobalto (III)". Acta Crystallogr. B . 24 : 417–422. doi : 10.1107 / S0567740868002475 .
- ^ Hambley, Trevor W .; Lay, Peter A. (1986). "Comparaciones de enlaces π y enlaces de hidrógeno en compuestos isomorfos: [M (NH 3 ) 5 Cl] Cl 2 (M = Cr, Co, Rh, Ir, Ru, Os)". Química inorgánica . 25 : 4553–8. doi : 10.1021 / ic00245a020 .
- ^ Schwab, E. (8 de septiembre de 2003). "Cobalto". Noticias de Química e Ingeniería . 81 (36): 80. doi : 10.1021 / cen-v081n036.p080 .
- Complejos de cobalto
- Compuestos de cobalto (III)
- Complejos de ammina