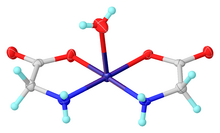
 Estructura de la forma cis monohidrato de bis (glicinato) cobre (II) | |
| Nombres | |
|---|---|
| Nombre IUPAC bis (glicinato) cobre (II) | |
| Otros nombres glicinato cúprico | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.033.425 |
| Número CE |
|
PubChem CID | |
| UNII |
|
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 4 H 10 Cu N 2 O 5 | |
| Masa molar | 229,679 g · mol −1 |
| Apariencia | cristales de color azul claro en forma de escamas ( forma cis ) |
| Densidad | 2,029 g / cm 3 |
| Punto de fusion | 212 ° C (414 ° F; 485 K) (descomp.) |
| 0,18 g / 100 g (0 ° C) 0,52 g / 100 g (25 ° C) | |
| Solubilidad | soluble en DMF , DMSO , piridina ; ligeramente soluble en etanol |
| Estructura [1] | |
| Ortorrómbico | |
| № 19 (P2 1 2 1 2 1 ) | |
| 222 | |
a = 5,21 Å, b = 10,81 Å, c = 13,49 Å | |
Unidades de fórmula ( Z ) | 4 |
| Riesgos | |
| Pictogramas GHS |   |
| Palabra de señal GHS | Advertencia |
| H302 , H315 , H319 , H400 | |
| P264 , P270 , P273 , P280 , P301 + 312 , P302 + 352 , P305 + 351 + 338 , P321 , P330 , P332 + 313 , P337 + 313 , P362 , P391 , P501 | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
Glicinato de cobre (II) ( nombre sugerido por la IUPAC : bis (glicinato) cobre (II)) se refiere al complejo de coordinación de cobre (II) con dos equivalentes de glicinato , con la fórmula [Cu (glicinato) 2 (H 2 O) x ] donde x = 1 ( monohidrato ) o 0 ( forma anhidra ). El complejo se informó por primera vez en 1841, y su química se ha revisado muchas veces, particularmente en relación con la reacción de isomerización entre las formas cis y trans que se informó por primera vez en 1890. [2] [3]
Todas las formas son sólidos azules, con diversos grados de solubilidad en agua . Una aplicación práctica del compuesto es como fuente de cobre dietético en alimentos para animales. [4]
Síntesis
El bis (glicinato) cobre (II) se prepara típicamente a partir de la reacción de acetato de cobre (II) en etanol acuoso con glicina: [2] [3]
- Cu (OAc) 2 + 2 H 2 NCH 2 COOH + x H 2 O → [Cu (H 2 NCH 2 COO) 2 (H 2 O) x ] + 2 AcOH, x = 0 o 1
La reacción procede a través de un mecanismo de sustitución disociativa no redox y normalmente produce el isómero cis . [2] [3]
Estructura
Como la mayoría de los complejos de aminoácidos , el glicinato forma un anillo quelato de 5 miembros, y el ligando glicinato actúa como una especie bidentada ( κ 2 Ο, Ν ). [2] [5] Los ligandos quelantes asumen una configuración plana cuadrada alrededor del átomo de cobre como es común para los complejos tetracoordinados d 9 , calculados para ser mucho más bajos en energía que la disposición tetraédrica alternativa. [3]
Cis y trans isomería
La naturaleza asimétrica del ligando y la coordinación plana cuadrada del mismo da lugar a dos posibles isómeros geométricos: una forma cis y una forma trans .
Existen múltiples formas de diferenciar los isómeros geométricos, una de las cuales es fácilmente accesible la espectroscopia IR con el número característico de C – N, C – O y Cu II –N que identifica la configuración del ligando. Apariencia cristalina también puede ser de algún valor para la indicación isómero, aunque la técnica de diagnóstico final es la cristalografía de rayos X . [1]
Todas las formas del complejo se han caracterizado cristalográficamente, siendo la más comúnmente aislada el cis monohidrato ( x = 1). [5] [1]
La isomerización de la forma cis a la trans se produce a altas temperaturas mediante un mecanismo de torsión de anillo. [2] [3]
Referencias
- ↑ a b c Köse, Dursun Ali; Toprak, Emre; Kaşarcı, Aliye; Avcı, Emre; Avcı, Gülçin Alp; Şahin, Onur; Büyükgüngör, Orhan (2 de julio de 2016). "Síntesis, estudios espectrales y térmicos de complejos de Co (II), Ni (II), Cu (II) y Zn (II) -glicinato e investigación de sus propiedades biológicas: estructura cristalina de [Cu (µ-gly) 2 (H2O)] n " . Síntesis y reactividad en química inorgánica, metal-orgánica y nano-metal . 46 (7): 1109-1118. doi : 10.1080 / 15533174.2013.801855 . ISSN 1553-3174 .
- ^ a b c d e Delf, BW; Gillard, RD; O'Brien, P. (1 de enero de 1979). "Los isómeros de α-aminoácidos con cobre (II). Parte 5. Los isómeros cis y trans del bis (glicinato) cobre (II), y su nueva isomerización térmica" . Revista de la Sociedad Química, Transacciones de Dalton (8): 1301-1305. doi : 10.1039 / DT9790001301 . ISSN 1364-5447 .
- ↑ a b c d e Tautermann, Christofer S .; Sabolović, Jasmina; Voegele, Andreas F .; Liedl, Klaus R. (1 de febrero de 2004). "Mecanismo de la isomerización cis-trans de bis (glicinato) cobre (II)" . El Journal of Physical Chemistry B . 108 (6): 2098–2102. doi : 10.1021 / jp0364497 . ISSN 1520-6106 .
- ^ Ward, JD; Spears, JW (1997). "Efectos a largo plazo del consumo de dietas bajas en cobre con o sin molibdeno suplementario sobre el estado del cobre, el rendimiento y las características de la canal del ganado" . Revista de ciencia animal . 75 (11): 3057–3065. doi : 10.2527 / 1997.75113057x . PMID 9374323 .
- ↑ a b Casari, BM; Mahmoudkhani, AH; Langer, V. (2004). "Una redeterminación de cis -Aquabis (glycinato-κ 2 N, O ) cobre (II)". Acta Crystallogr. E . 60 (12): m1949 – m1951. doi : 10.1107 / S1600536804030041 .