 | |
 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Prograf, Advagraf, Protopic, otros |
| Otros nombres | FK-506, fujimicina |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a601117 |
| Datos de licencia |
|
| Categoría de embarazo |
|
| Vías de administración | Tópico , por vía oral , intravenoso (IV) |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 24% (5-67%), menos después de ingerir alimentos ricos en grasas |
| Enlace proteico | ≥98,8% |
| Metabolismo | CYP3A4 , CYP3A5 de hígado |
| Vida media de eliminación | 11,3 h para pacientes trasplantados (rango 3,5 a 40,6 h) |
| Excreción | Mayormente fecal |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Ligando PDB | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.155.367 |
| Datos químicos y físicos | |
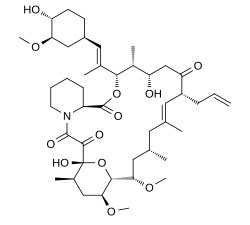
| Fórmula | C 44 H 69 N O 12 |
| Masa molar | 804.031 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
| | |
Tacrolimus , vendido bajo las marcas Protopic y Prograf entre otros, es un fármaco inmunosupresor . Después de un alotrasplante de órganos , el riesgo de rechazo de órganos es moderado. Para reducir el riesgo de rechazo de órganos, se administra tacrolimus. El fármaco también se puede vender como un medicamento tópico en el tratamiento de enfermedades mediadas por células T como el eccema y la psoriasis . Por ejemplo, se prescribe para uveítis refractaria grave después de un trasplante de médula ósea, exacerbaciones de la enfermedad de cambios mínimos , enfermedad de Kimura.y vitiligo . Puede utilizarse para tratar el síndrome del ojo seco en perros y gatos. [2] [3]
Tacrolimus inhibe la calcineurina , que participa en la producción de interleucina-2 , una molécula que promueve el desarrollo y la proliferación de las células T , como parte de la respuesta inmune aprendida (o adaptativa ) del cuerpo .
Químicamente, es una lactona macrólido [4] que se descubrió por primera vez en 1987, a partir del caldo de fermentación de una muestra de suelo japonés que contenía la bacteria Streptomyces tsukubaensis .
Usos médicos [ editar ]
Trasplante de órganos [ editar ]
Tiene propiedades inmunosupresoras similares a la ciclosporina , pero es mucho más potente. La inmunosupresión con tacrolimus se asoció con una tasa significativamente menor de rechazo agudo en comparación con la inmunosupresión basada en ciclosporina (30,7% frente a 46,4%) en un estudio. [5] El resultado clínico es mejor con tacrolimus que con ciclosporina durante el primer año de trasplante de hígado. [6] [7] El resultado a largo plazo no ha mejorado en la misma medida. El tacrolimus normalmente se prescribe como parte de un cóctel postrasplante que incluye esteroides , micofenolato e inhibidores del receptor de IL-2 como basiliximab.. Las dosis se titulan para alcanzar los niveles sanguíneos en momentos específicos después de la administración de la medicación. [8]
Colitis ulcerosa [ editar ]
En los últimos años, [ ¿cuándo? ] tacrolimus se ha utilizado para suprimir la inflamación asociada con la colitis ulcerosa (CU), una forma de enfermedad inflamatoria intestinal . Aunque se utiliza casi exclusivamente en casos de prueba, tacrolimus ha demostrado ser significativamente eficaz en la supresión de los brotes de CU. [9] [10]
Piel [ editar ]
Como ungüento , el tacrolimus se usa en el tratamiento del eccema , en particular la dermatitis atópica . Suprime la inflamación de forma similar a los esteroides y es tan eficaz como un esteroide de potencia media. Una ventaja importante del tacrolimus es que, a diferencia de los esteroides, no causa adelgazamiento de la piel ( atrofia ) ni otros efectos secundarios relacionados con los esteroides. [11]
Se aplica sobre las lesiones activas hasta que cicatrizan, pero también se puede utilizar de forma continua en dosis bajas (dos veces por semana), y se aplica sobre la piel más fina de la cara y los párpados. [ cita requerida ] Se han realizado ensayos clínicos de hasta un año. Recientemente también se ha utilizado para tratar el vitiligo segmentario en niños, especialmente en áreas de la cara. [12]
Nefritis lúpica [ editar ]
Se ha demostrado que tacrolimus reduce el riesgo de infecciones graves al mismo tiempo que aumenta la remisión de la función renal en la nefritis lúpica . [13] [14]
Contraindicaciones y precauciones [ editar ]
Las contraindicaciones y precauciones incluyen: [15]
- Amamantamiento
- Enfermedad hepática
- Inmunosupresión
- Infantes
- Infección
- Enfermedad neoplásica , como:
- Cáncer de piel
- Cáncer de pulmón
- Oliguria
- El embarazo
- Prolongación del intervalo QT
- Exposición a la luz solar ( UV )
- Zumo de pomelo [16]
Uso tópico [ editar ]
- Vendaje oclusivo
- Lesiones malignas conocidas o sospechadas
- Síndrome de Netherton o enfermedades cutáneas similares
- Ciertas infecciones de la piel [11]
Efectos secundarios [ editar ]
Por vía oral o intravenosa [ editar ]
Los efectos secundarios pueden ser graves e incluyen infección, daño cardíaco, hipertensión , visión borrosa, problemas hepáticos y renales ( nefrotoxicidad por tacrolimus ), [17] hiperpotasemia , hipomagnesemia , hiperglucemia , diabetes mellitus , picazón , daño pulmonar (el sirolimus también causa daño pulmonar), [18] y diversos problemas neuropsiquiátricos como pérdida de apetito, insomnio , síndrome de encefalopatía posterior reversible , confusión, debilidad, depresión, pesadillas vívidas, calambres, neuropatía, convulsiones ,temblores y catatonia . [19]
Además, puede aumentar potencialmente la gravedad de las enfermedades infecciosas o fúngicas existentes, como el herpes zóster o las infecciones virales por polioma . [15]
Carcinogénesis y mutagénesis [ editar ]
En las personas que reciben inmunosupresores para reducir el rechazo del injerto trasplantado, un mayor riesgo de malignidad (cáncer) es una complicación reconocida. [15] Los cánceres más comunes son el linfoma no Hodgkin [20] y los cánceres de piel. El riesgo parece estar relacionado con la intensidad y duración del tratamiento.
Uso tópico [ editar ]
Los eventos adversos más comunes asociados con el uso de ungüentos tópicos de tacrolimus, especialmente si se usan en un área amplia, incluyen una sensación de ardor o picazón en las aplicaciones iniciales, con una mayor sensibilidad a la luz solar y al calor en las áreas afectadas. Menos comunes son los síntomas similares a los de la gripe , dolor de cabeza, tos y ardor en los ojos. [21]
Riesgos de cáncer [ editar ]
Se sospechaba que el tacrolimus y un fármaco relacionado para el eccema ( pimecrolimus ) conllevaban un riesgo de cáncer, aunque el asunto sigue siendo objeto de controversia. La FDA emitió una advertencia sanitaria en marzo de 2005 para el medicamento, basada en modelos animales y en un pequeño número de pacientes. Hasta que nuevos estudios en humanos arrojen resultados más concluyentes, la FDA recomienda que se informe a los usuarios de los riesgos potenciales. Sin embargo, la práctica actual de los dermatólogos del Reino Unido no considera que esto sea una preocupación real significativa y recomiendan cada vez más el uso de estos nuevos fármacos. [22]
Interacciones [ editar ]
También como la ciclosporina, tiene una amplia gama de interacciones. El tacrolimus es metabolizado principalmente por el sistema de enzimas hepáticas del citocromo P450 , y hay muchas sustancias que interactúan con este sistema e inducen o inhiben la actividad metabólica del sistema. [15]
Las interacciones incluyen la de la toronja que aumenta las concentraciones plasmáticas de tacrolimus. Como las infecciones son una de las principales causas de morbilidad y mortalidad en el paciente postrasplante, las interacciones [ cita requerida ] informadas con mayor frecuencia incluyen interacciones con fármacos antimicrobianos. Los antibióticos macrólidos que incluyen eritromicina y claritromicina , así como varias de las clases más nuevas de antifúngicos, especialmente de la clase azoles ( fluconazol , voriconazol ), aumentan los niveles de tacrolimus al competir por las enzimas del citocromo. [15]
Farmacología [ editar ]
Mecanismo de acción [ editar ]
Tacrolimus es un inhibidor de la calcineurina macrólido . En las células T , la activación del receptor de las células T normalmente aumenta el calcio intracelular, que actúa a través de la calmodulina para activar la calcineurina . A continuación, la calcineurina desfosforila el factor nuclear del factor de transcripción de las células T activadas (NF-AT), que se desplaza al núcleo de la célula T y aumenta la actividad de los genes que codifican la IL-2 y las citocinas relacionadas. Tacrolimus previene la desfosforilación de NF-AT. [23]
En detalle, tacrolimus reduce la actividad de la peptidilprolil isomerasa al unirse a la inmunofilina FKBP12 (proteína de unión FK506), creando un nuevo complejo. Este complejo FKBP12-FK506 interactúa e inhibe la calcineurina, inhibiendo así tanto la transducción de señales de linfocitos T como la transcripción de IL-2. [24] Aunque esta actividad es similar a la de la ciclosporina, la incidencia de rechazo agudo se reduce con el uso de tacrolimus sobre el uso de ciclosporina. [5]Aunque la inmunosupresión a corto plazo con respecto a la supervivencia del paciente y del injerto es similar entre los dos fármacos, el tacrolimus da como resultado un perfil lipídico más favorable, y esto puede tener importantes implicaciones a largo plazo dada la influencia pronóstica del rechazo en la supervivencia del injerto. [25]
Farmacocinética [ editar ]
El tacrolimus oral se absorbe lentamente en el tracto gastrointestinal , con una biodisponibilidad total del 20 al 25% (pero con variaciones del 5 al 67%) y las concentraciones plasmáticas sanguíneas más altas (C max ) se alcanzan después de una a tres horas. La ingesta del fármaco junto con una comida, especialmente una rica en grasas, ralentiza la reabsorción y reduce la biodisponibilidad. En la sangre, tacrolimus se une principalmente a los eritrocitos ; sólo el 5% se encuentran en el plasma , de los cuales más del 98,8% se unen a las proteínas plasmáticas . [15] [26]
La sustancia se metaboliza en el hígado, principalmente a través de CYP3A , y en la pared intestinal. Todos los metabolitos que se encuentran en la circulación están inactivos. La vida media biológica varía ampliamente y parece ser más alta para las personas sanas (43 horas en promedio) que para los pacientes con trasplantes de hígado (12 horas) o trasplantes de riñón (16 horas), debido a las diferencias en el aclaramiento . Tacrolimus se elimina predominantemente a través de las heces en forma de sus metabolitos. [15] [26]
Cuando se aplica localmente sobre el eccema, el tacrolimus tiene poca o ninguna biodisponibilidad. [15]
Farmacogenética [ editar ]
La enzima predominante responsable del metabolismo de tacrolimus es CYP3A5 . Las variaciones genéticas dentro de CYP3A5 que dan como resultado cambios en la actividad de la proteína CYP3A5 pueden afectar las concentraciones de tacrolimus en el cuerpo. En particular, los individuos que son homocigotos para el alelo G en el polimorfismo de un solo nucleótido (SNP) rs776746 (también conocido como CYP3A5 * 3 / * 3) tienen una proteína CYP3A5 no funcional. La frecuencia del alelo G varía en todo el mundo, desde el 4% en algunas poblaciones africanas hasta el 80-90% en las poblaciones caucásicas. [27]En un gran número de estudios, se ha demostrado que los individuos homocigotos para el alelo G tienen concentraciones más altas de tacrolimus y requieren dosis más bajas del fármaco, en comparación con los individuos que no son homocigotos para el alelo G. Lograr las concentraciones objetivo de tacrolimus es importante: si los niveles son demasiado bajos, existe el riesgo de rechazo del trasplante , si los niveles son demasiado altos, existe el riesgo de toxicidad por fármacos. Existe evidencia que sugiere que la dosificación de pacientes basada en el genotipo rs776746puede resultar en un logro más rápido y frecuente de los niveles objetivo de tacrolimus. Sin embargo, hay una falta de evidencia consistente sobre si la dosificación basada en el genotipo rs776746 da como resultado mejores resultados clínicos (como un menor riesgo de rechazo del trasplante o toxicidad de los medicamentos), probablemente porque los pacientes que toman tacrolimus están sujetos a un control terapéutico de los medicamentos . [28] [29] [30] [31]
Los estudios han demostrado que los polimorfismos genéticos de genes distintos de CYP3A5, como NR1I2 [32] [33] (que codifica PXR ), también influyen significativamente en la farmacocinética de tacrolimus.
Historia [ editar ]
El tacrolimus se descubrió en 1987; [34] fue uno de los primeros inmunosupresores macrólidos descubiertos, precedido por el descubrimiento de rapamicina (sirolimus) en Rapa Nui (Isla de Pascua) en 1975. [35] Es producido por una bacteria del suelo, Streptomyces tsukubaensis . [36] El nombre tacrolimus se deriva de " inmunosupresor macrólido Tsukuba ". [37]
El tacrolimus fue aprobado por primera vez por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) en 1994, [38] [39] para su uso en el trasplante de hígado ; las indicaciones se ampliaron para incluir trasplantes de riñón, corazón, intestino delgado, páncreas, pulmón, tráquea, piel, córnea, médula ósea y extremidades. [ cita médica necesaria ] Las versiones genéricas de tacrolimus se aprobaron en los EE. UU. en 2017. [40]
El tacrolimus fue aprobado para uso médico en la Unión Europea en 2002, para el tratamiento de la dermatitis atópica moderada a grave. [41] En 2007, las indicaciones se ampliaron para incluir la profilaxis del rechazo de trasplantes en receptores de aloinjertos de hígado o riñón adultos y el tratamiento del rechazo de aloinjertos resistentes al tratamiento con otros medicamentos inmunosupresores en adultos. [42] En 2009, las indicaciones se ampliaron para incluir la profilaxis del rechazo de trasplantes en adultos y pediátricos, receptores de aloinjertos de riñón, hígado o corazón y el tratamiento del rechazo de aloinjertos resistentes al tratamiento con otros medicamentos inmunosupresores en adultos y niños. [43]
Formas disponibles [ editar ]
Una versión de marca del medicamento es propiedad de Astellas Pharma y se vende bajo la marca Prograf, administrada dos veces al día. Varios otros fabricantes tienen autorización de comercialización para marcas alternativas de la formulación de dos veces al día. [44]
Las formulaciones de una vez al día con autorización de comercialización incluyen Advagraf (Astellas Pharma) y Envarsus (comercializado como Envarsus XR en EE. UU. Por Veloxis Pharmaceuticals y comercializado en Europa por Chiesi ). [44] Estas formulaciones están destinadas a reducir la variación farmacocinética de los niveles en sangre y facilitar el cumplimiento de la dosificación. [ cita médica necesaria ]
La formulación tópica es comercializada por LEO Pharma con el nombre de Protopic. [44]
Biosíntesis [ editar ]
La biosíntesis de tacrolimus es la síntesis híbrida de policétido sintasas de tipo 1 (PKS 1) y péptido sintasas no ribosomales (NRPS). La investigación muestra que la síntesis híbrida consta de diez módulos de policétido sintasa tipo 1 y un módulo de péptido sintasa no ribosómico. Las enzimas sintéticas de tacrolimus se encuentran en 19 grupos de genes llamados fkb. Los 19 genes son fkbQ, fkbN, fkbM, fkbD, fkbA, fkbP, fkbO, fkbB, fkbC, fkbL, fkbK, fkbJ, fkbI, fkbH, fkbG, allD, allR, allK y allA. [45]
Hay varias formas posibles de biosíntesis de tacrolimus. Las unidades fundamentales para la biosíntesis son las siguientes: una molécula de ácido 4,5-dihidroxiciclohex-1-encarboxílico (DHCHC) como unidad inicial, cuatro moléculas de malonil-CoA, cinco moléculas de metilmalonil-CoA, una molécula de alilmalonil-CoA como unidades de alargamiento. Sin embargo, dos moléculas de malonil-CoA pueden ser reemplazadas por dos moléculas de metoximalonil CoA. Una vez que se reemplazan dos moléculas de malonil-CoA, los pasos de adaptación de la post-sintasa ya no son necesarios cuando se sustituyen dos moléculas de metoximalonil CoA. La biosíntesis de metoximalonil CoA a proteína portadora acilo se realiza mediante cinco enzimas (fkbG, fkbH, fkbI, fkbJ y fkbK). La alilmalonil-CoA también se puede reemplazar por propionilmalonil-CoA. [45]
La unidad de inicio, DHCHC del ácido corísmico, se forma mediante la enzima fkbO y se carga en el dominio CoA-ligasa (CoL). Luego, procede a la reducción dependiente de NADPH (ER). Tres enzimas, fkbA, B, C refuerzan los procesos desde el módulo de carga al módulo 10, el último paso de PKS 1. La enzima fkbB es responsable de la síntesis de alilmalonil-CoA o posiblemente propionilmalonil-CoA en C21, que es un paso inusual de PKS general 1. Como se mencionó, si dos moléculas de metoximalonil CoA se sustituyen por dos moléculas de malonil-CoA, tendrán lugar en los módulos 7 y 8 (C13 y C15), y la enzima fkbA reforzará este proceso. Después del último paso (módulo 10) de PKS 1, una molécula de ácido L - pipecólico formada a partir de L - lisinay catalizada a través de la enzima fkbL sintetiza con la molécula del módulo 10. El proceso de síntesis del ácido L- pipecólico es NRPS reforzado por la enzima fkbP. Después de sintetizar todas las subunidades, la molécula se cicla. Después de la ciclación, la molécula de pre-tacrolimus pasa por los pasos de adaptación de la post-sintasa, como la oxidación y la S -adenosil metionina . En particular, la enzima fkbM es responsable de la metilación del alcohol que se dirige al alcohol de la unidad de inicio DHCHC (número de carbono 31 representado en marrón), y la enzima fkbD es responsable de C9 (representado en verde). Después de estos pasos de adaptación, la molécula de tacrolimus se vuelve biológicamente activa. [45] [46] [47]
Referencias [ editar ]
- ^ a b "Uso de tacrolimus durante el embarazo" . Drugs.com . 3 de octubre de 2019 . Consultado el 29 de abril de 2020 .
- ^ Berdoulay A, RV inglés, Nadelstein B (2005). "Efecto de la suspensión acuosa tópica de tacrolimus al 0,02% sobre la producción de lágrimas en perros con queratoconjuntivitis seca". Oftalmología veterinaria . 8 (4): 225–32. doi : 10.1111 / j.1463-5224.2005.00390.x . PMID 16008701 .
- ^ "Tacrolimus para perros y gatos" .
- ^ Baldo A, Cafiero M, Di Caterino P, Di Costanzo L (enero de 2009). "Ungüento de tacrolimus en el tratamiento de la dermatitis atópica" . Clin Cosmet Investig Dermatol . 2 : 1–7. doi : 10.2147 / ccid.s3378 . PMC 3047924 . PMID 21436963 .
- ↑ a b McCauley, Jerry (19 de mayo de 2004). "Supervivencia a largo plazo del injerto en receptores de trasplante de riñón" . Serie de juegos de diapositivas sobre análisis de terapias inmunosupresoras . Medscape . Consultado el 6 de junio de 2006 .
- ^ Haddad EM, McAlister VC, Renouf E, Malthaner R, Kjaer MS, Gluud LL (octubre de 2006). McAlister V (ed.). "Ciclosporina versus tacrolimus para pacientes con trasplante de hígado" . La base de datos Cochrane de revisiones sistemáticas . 4 (4): CD005161. doi : 10.1002 / 14651858.CD005161.pub2 . PMID 17054241 .
- ^ O'Grady JG, Burroughs A, Hardy P, Elbourne D, Truesdale A (octubre de 2002). "Tacrolimus versus ciclosporina microemulsificada en el trasplante de hígado: el ensayo controlado aleatorizado de TMC". Lancet . 360 (9340): 1119–25. doi : 10.1016 / S0140-6736 (02) 11196-2 . PMID 12387959 . S2CID 10417106 .
- ^ Lee MN, Butani L (junio de 2007). "Mejor control farmacocinético de la exposición a tacrolimus después del trasplante renal pediátrico". Trasplante pediátrico . 22 (4): 388–93. doi : 10.1111 / j.1399-3046.2006.00618.x . PMID 17493218 .
- ^ Baumgart DC, Pintoffl JP, Sturm A, Wiedenmann B, Dignass AU (mayo de 2006). "El tacrolimus es seguro y eficaz en pacientes con enfermedad intestinal inflamatoria severa resistente a esteroides o dependiente de esteroides: un seguimiento a largo plazo". La Revista Estadounidense de Gastroenterología . 101 (5): 1048–56. PMID 16573777 .
- ^ Baumgart DC, Macdonald JK, Feagan B (julio de 2008). Baumgart DC (ed.). "Tacrolimus (FK506) para la inducción de la remisión en la colitis ulcerosa refractaria". La base de datos Cochrane de revisiones sistemáticas . 16 (3): CD007216. doi : 10.1002 / 14651858.CD007216 . PMID 18646177 .
- ↑ a b Haberfeld, H, ed. (2015). Austria-Codex (en alemán). Viena: Österreichischer Apothekerverlag. Protopic.
- ^ Silverberg NB, Lin P, Travis L, Farley-Li J, Mancini AJ, Wagner AM, Chamlin SL, Paller AS (noviembre de 2004). "La pomada de tacrolimus promueve la repigmentación del vitiligo en los niños: una revisión de 57 casos". Revista de la Academia Estadounidense de Dermatología . 51 (5): 760–6. doi : 10.1016 / j.jaad.2004.05.036 . PMID 15523355 .
- ^ Singh JA, Hossain A, Kotb A, Wells G (septiembre de 2016). "Riesgo de infecciones graves con fármacos inmunosupresores y glucocorticoides para la nefritis lúpica: una revisión sistemática y metanálisis de red" . Medicina BMC . 14 (1): 137. doi : 10.1186 / s12916-016-0673-8 . PMC 5022202 . PMID 27623861 .
- ^ Singh, Jasvinder A .; Hossain, Alomgir; Kotb, Ahmed; Wells, George A. (2016). "Eficacia comparativa de fármacos inmunosupresores y corticosteroides para la nefritis lúpica: una revisión sistemática y metanálisis de red" . Revisiones sistemáticas . 5 (1): 155. doi : 10.1186 / s13643-016-0328-z . ISSN 2046-4053 . PMC 5020478 . PMID 27619512 .
- ^ a b c d e f g h Haberfeld, H, ed. (2015). Austria-Codex (en alemán). Viena: Österreichischer Apothekerverlag. Prograf.
- ^ Fukatsu S, Fukudo M, Masuda S, Yano I, Katsura T, Ogura Y, Oike F, Takada Y, Inui K (abril de 2006). "Efecto retardado del jugo de toronja sobre la farmacocinética y la farmacodinámica de tacrolimus en un receptor de trasplante de hígado de donante vivo". Metabolismo y farmacocinética de fármacos . 21 (2): 122–5. doi : 10.2133 / dmpk.21.122 . PMID 16702731 .
- ^ Naesens M, Kuypers DR, Sarwal M (febrero de 2009). "Nefrotoxicidad del inhibidor de calcineurina" (PDF) . Revista clínica de la Sociedad Americana de Nefrología . 4 (2): 481–508. doi : 10.2215 / CJN.04800908 . PMID 19218475 .
- ^ Miwa Y, Isozaki T, Wakabayashi K, Odai T, Matsunawa M, Yajima N, Negishi M, Ide H, Kasama T, Adachi M, Hisayuki T, Takemura T (2008). "Lesión pulmonar inducida por tacrolimus en un paciente con artritis reumatoide con neumonitis intersticial". Reumatología moderna . 18 (2): 208-11. doi : 10.1007 / s10165-008-0034-3 . PMID 18306979 . S2CID 39537409 .
- ^ O'Donnell MM, Williams JP, Weinrieb R, Denysenko L (2007). "Mutismo catatónico después de un trasplante de hígado rápidamente revertido con lorazepam". Psiquiatría Hospitalaria General . 29 (3): 280–1. doi : 10.1016 / j.genhosppsych.2007.01.004 . PMID 17484951 .
- ^ "Estadísticas clave para el linfoma no Hodgkin" . www.cancer.org . Consultado el 19 de febrero de 2020 .
- ^ Hanifin JM, Paller AS, Eichenfield L, Clark RA, Korman N, Weinstein G, Caro I, Jaracz E, Rico MJ (agosto de 2005). "Eficacia y seguridad del tratamiento con pomada de tacrolimus hasta por 4 años en pacientes con dermatitis atópica". Revista de la Academia Estadounidense de Dermatología . 53 (2 Suppl 2): S186–94. doi : 10.1016 / j.jaad.2005.04.062 . PMID 16021174 .
- ^ NH Cox y Catherine H Smith (diciembre de 2002). "Consejos a los dermatólogos sobre tacrolimus tópico" (PDF) . Comité de Directrices de Terapia . Asociación Británica de Dermatólogos. Archivado desde el original (PDF) el 13 de diciembre de 2013.
- ^ William F. Ganong (8 de marzo de 2005). Revisión de fisiología médica (22ª ed.). Libros de medicina de Lange. pag. 530. ISBN 978-0-07-144040-0.
- ^ Liu J, Farmer JD, Lane WS, Friedman J, Weissman I, Schreiber SL (agosto de 1991). "La calcineurina es un objetivo común de los complejos ciclofilina-ciclosporina A y FKBP-FK506". Celular . 66 (4): 807-15. doi : 10.1016 / 0092-8674 (91) 90124-H . PMID 1715244 . S2CID 22094672 .
- ^ Abou-Jaoude MM, Najm R, Shaheen J, Nawfal N, Abboud S, Alhabash M, Darwish M, Mulhem A, Ojjeh A, Almawi WY (septiembre de 2005). "Tacrolimus (FK506) versus microemulsión de ciclosporina (neoral) como terapia de inmunosupresión de mantenimiento en receptores de trasplante de riñón". Procedimientos de trasplante . 37 (7): 3025–8. doi : 10.1016 / j.transproceed.2005.08.040 . PMID 16213293 .
- ↑ a b Dinnendahl, V; Fricke, U, eds. (2003). Arzneistoff-Profile (en alemán). 9 (18 ed.). Eschborn, Alemania: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ Bains, Ripudaman Kaur. "Estructura de la diversidad molecular y la población en el gen CYP3A5 en África" (PDF) . University College de Londres . Consultado el 13 de junio de 2016 .
- ^ Staatz CE, Tett SE (2004). "Farmacocinética clínica y farmacodinámica del tacrolimus en el trasplante de órganos sólidos". Farmacocinética clínica . 43 (10): 623–53. doi : 10.2165 / 00003088-200443100-00001 . PMID 15244495 . S2CID 33877550 .
- ^ Staatz CE, Goodman LK, Tett SE (marzo de 2010). "Efecto de los polimorfismos de un solo nucleótido CYP3A y ABCB1 sobre la farmacocinética y farmacodinamia de los inhibidores de calcineurina: Parte I". Farmacocinética clínica . 49 (3): 141–75. doi : 10.2165 / 11317350-000000000-00000 . PMID 20170205 . S2CID 28346861 .
- ^ Staatz CE, Goodman LK, Tett SE (abril de 2010). "Efecto de los polimorfismos de un solo nucleótido CYP3A y ABCB1 sobre la farmacocinética y farmacodinamia de los inhibidores de calcineurina: Parte II". Farmacocinética clínica . 49 (4): 207-21. doi : 10.2165 / 11317550-000000000-00000 . PMID 20214406 . S2CID 27047235 .
- ^ Barbarino JM, Staatz CE, Venkataramanan R, Klein TE, Altman RB (octubre de 2013). "Resumen de PharmGKB: vías de ciclosporina y tacrolimus" . Farmacogenética y Genómica . 23 (10): 563–85. doi : 10.1097 / fpc.0b013e328364db84 . PMC 4119065 . PMID 23922006 .
- ^ Benkali K, Prémaud A, Picard N, Rérolle JP, Toupance O, Hoizey G, Turcant A, Villemain F, Le Meur Y, Marquet P, Rousseau A (1 de enero de 2009). "Análisis farmacocinético-farmacogenético poblacional de tacrolimus y estimación bayesiana en receptores de trasplante renal". Farmacocinética clínica . 48 (12): 805–16. doi : 10.2165 / 11318080-000000000-00000 . PMID 19902988 . S2CID 19900291 .
- ^ Choi Y, Jiang F, An H, Park HJ, Choi JH, Lee H (enero de 2017). "Un estudio farmacogenómico sobre la farmacocinética de tacrolimus en sujetos sanos utilizando la plataforma DMETTM Plus" . The Pharmacogenomics Journal . 17 (1): 105–106. doi : 10.1038 / tpj.2016.85 . PMID 27958377 .
- ^ Hatanaka H, Iwami M, Kino T, Goto T, Okuhara M (noviembre de 1988). "FR-900520 y FR-900523, nuevos inmunosupresores aislados de un Streptomyces. I. Taxonomía de la cepa productora" . The Journal of Antibiotics . 41 (11): 1586–91. doi : 10.7164 / antibióticos.41.1586 . PMID 3198493 .
- ^ Kino T, Hatanaka H, Hashimoto M, Nishiyama M, Goto T, Okuhara M, Kohsaka M, Aoki H, Imanaka H (septiembre de 1987). "FK-506, un nuevo inmunosupresor aislado de un Streptomyces. I. Fermentación, aislamiento y características físico-químicas y biológicas" . The Journal of Antibiotics . 40 (9): 1249–55. doi : 10.7164 / antibióticos.40.1249 . PMID 2445721 .
- ^ Pritchard DI (mayo de 2005). "Obtención de una sucesión química de ciclosporina de parásitos y patógenos humanos". Descubrimiento de drogas hoy . 10 (10): 688–91. doi : 10.1016 / S1359-6446 (05) 03395-7 . PMID 15896681 . Admite el organismo de origen, pero no la información del equipo
- ^ Ponner, B, Cvach, B (Fujisawa Pharmaceutical Co.): Protopic Update 2005
- ^ "Prograf: medicamentos aprobados por la FDA" . EE.UU. Administración de Drogas y Alimentos (FDA) . Consultado el 29 de abril de 2020 .
- ^ "Prograf: medicamentos aprobados por la FDA" . EE.UU. Administración de Drogas y Alimentos (FDA) . Consultado el 29 de abril de 2020 .
- ^ "Tacrolimus: medicamentos aprobados por la FDA" . EE.UU. Administración de Drogas y Alimentos (FDA) . Consultado el 29 de abril de 2020 .
- ^ "EPAR Protopic" . Agencia Europea de Medicamentos (EMA) . Consultado el 29 de abril de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ "EPAR de Advagraf" . Agencia Europea de Medicamentos (EMA) . Consultado el 29 de abril de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ "Modigraf EPAR" . Agencia Europea de Medicamentos (EMA) . Consultado el 29 de abril de 2020 .
- ^ a b c Comité conjunto del formulario. "British National Formulary (en línea)" . Londres: BMJ Group y Pharmaceutical Press . Consultado el 24 de septiembre de 2015 .
- ^ a b c Ordóñez-Robles M, Santos-Beneit F, Martín JF (mayo de 2018). "Aproximaciones ómicas" . Antibióticos . 7 (2): 39. doi : 10.3390 / antibiotics7020039 . PMC 6022917 . PMID 29724001 .
- ^ Chen D, Zhang L, Pang B, Chen J, Xu Z, Abe I, Liu W (mayo de 2013). "La maduración de FK506 implica una oxidación de C-9 de cuatro electrones catalizada por la proteína del citocromo p450 en paralelo con una O-metilación de C-31" . Revista de bacteriología . 195 (9): 1931–9. doi : 10.1128 / JB.00033-13 . PMC 3624582 . PMID 23435975 .
- ^ Mo S, Ban YH, Park JW, Yoo YJ, Yoon YJ (diciembre de 2009). "Producción mejorada de FK506 en Streptomyces clavuligerus CKD1119 mediante la ingeniería del suministro de precursor de metilmalonil-CoA". Revista de Microbiología y Biotecnología Industrial . 36 (12): 1473–82. doi : 10.1007 / s10295-009-0635-7 . PMID 19756799 . S2CID 32967249 .
Lectura adicional [ editar ]
- Lv X, Qi J, Zhou M, et al. (Marzo de 2020). "Eficacia comparativa de 20 terapias de profilaxis de la enfermedad de injerto contra huésped para pacientes después del trasplante de células madre hematopoyéticas: un metanálisis de red de múltiples tratamientos". Crit. Rev. Oncol. Hematol . 150 : 102944. doi : 10.1016 / j.critrevonc.2020.102944 . PMID 32247246 .
Enlaces externos [ editar ]
- "Tacrolimus" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- "Inyección de tacrolimus" . MedlinePlus .
- "Tacrolimus tópico" . MedlinePlus .
- Tacrolimus en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .