 | |
 | |
| Nombres | |
|---|---|
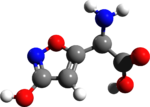
| Nombre IUPAC Ácido ( S ) -2-amino-2- (3-hidroxiisoxazol-5-il) acético | |
| Otros nombres Ácido iboténico | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.151.170 |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 5 H 6 N 2 O 4 | |
| Masa molar | 158,113 g · mol −1 |
| Punto de fusion | 151-152 ° C (anhidro) 144-146 ° C (monohidrato) |
| H 2 O: 1 mg / mL NaOH 0,1 M: 10,7 mg / mL HCl 0,1 M: 4,7 mg / mL | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El ácido iboténico o ácido ( S ) -2-amino-2- (3-hidroxiisoxazol-5-il) acético , también conocido como ibotenato , es un compuesto químico y fármaco psicoactivo que se encuentra naturalmente en Amanita muscaria y especies relacionadas de hongos típicamente encontrado en las regiones templadas y boreales del hemisferio norte. Es un análogo conformacionalmente restringido del neurotransmisor glutamato y, debido a su similitud estructural con este neurotransmisor, actúa como un agonista no selectivo del receptor de glutamato . [1]Debido a esto, el ácido iboténico puede ser una poderosa neurotoxina y se emplea como " agente lesionador del cerebro " a través de inyecciones craneales en la investigación científica . [2] [3]
Farmacología [ editar ]
El ácido iboténico actúa como un potente agonista del NMDA y de los receptores metabotrópicos de glutamato del grupo I ( mGluR1 y mGluR5 ) y II ( mGluR2 y mGluR3 ) . [1] [4] Está inactivo en los mGluR del grupo III . [5] El ácido iboténico también actúa como un agonista débil de los receptores AMPA y kainato . [1] [4] Además, debido a la descarboxilación in vivo en muscimol , actúa indirectamente como un potente Agonista del receptor GABA A y GABA A -ρ . [4] A diferencia del muscimol, el principal componente psicoactivo de Amanita muscaria que se cree que causa sedación y delirio , los efectos psicoactivos del ácido iboténico no se conocen independientemente de su función como profármaco del muscimol, sin embargo, se puede especular que actuaría como un estimulante. [6] [7]
Propiedades biológicas [ editar ]
Mecanismo de acción [ editar ]
El ácido iboténico es un agonista de los receptores de glutamato, específicamente en los sitios del receptor N-metil-D-aspartato o NMDA y trans-ACPD en múltiples sistemas del sistema nervioso central . La neurotoxicidad iboténica puede potenciarse con glicina y bloquearse con dizocilpina . La dizocilpina actúa como un antagonista no competitivo en los receptores NMDA . [8]
La toxicidad del ácido iboténico proviene de la activación de los receptores NMDA . Los receptores NMDA están relacionados con la plasticidad sináptica y trabajan con los receptores metabotrópicos de glutamato para establecer una potenciación a largo plazo o LTP. Se cree que el proceso de potenciación a largo plazo está relacionado con la adquisición de información. El receptor de NMDA funciona correctamente al permitir que los iones Ca 2+ pasen después de la activación en el sitio del receptor.
La unión del ácido iboténico permite que el exceso de Ca 2+ ingrese al sistema, lo que da como resultado la muerte de las células neuronales. Ca 2+ también activa CaM-KII o Ca 2+ / Calmodulin Kinasa que fosforila múltiples enzimas. Las enzimas activadas comienzan a producir especies reactivas de oxígeno que dañan el tejido circundante. El exceso de Ca 2+ da como resultado la mejora del sistema de transporte de electrones mitocondrial que aumentará aún más el número de especies reactivas de oxígeno. [9]
Efectos biológicos [ editar ]
El ácido iboténico afecta típicamente a los receptores NMDA y trans-ACPD en el sistema nervioso central. [8] Debido a que se dirigen a estos sistemas, los síntomas asociados con la intoxicación por ácido iboténico a menudo se relacionan con la percepción y el control.
La mayor parte del ácido iboténico ingerido probablemente se descarboxila en muscimol, por lo que los efectos de ingerir ácido iboténico son similares a los efectos del muscimol. [10] Los síntomas asociados con el ácido iboténico suelen aparecer en 30 a 60 minutos e incluyen una variedad de efectos sobre el sistema nervioso. Los síntomas más comunes incluyen náuseas, vómitos y somnolencia. Sin embargo, después de la primera hora los síntomas comienzan a incluir confusión, euforia , distorsiones visuales y auditivas, sensación de flotar y amnesia retrógrada . [11]
Los síntomas son levemente diferentes para los niños, por lo general comienzan después de 30 a 180 minutos. Los síntomas dominantes en los niños incluyen ataxia , obnubilación y letargo . Sin embargo, ocasionalmente se informan convulsiones, más comúnmente en niños. [11]
Tratamiento [ editar ]
El tratamiento de la intoxicación por ácido iboténico es limitado y varía, ya que la dosis tóxica del compuesto varía de persona a persona. Los pacientes ingresados en el hospital por intoxicación con ácido iboténico generalmente reciben carbón para detener la absorción del compuesto y prevenir una mayor intoxicación. Al recibir el tratamiento con carbón, se controlan los signos vitales del paciente y la toxicidad suele durar entre 6 y 8 horas; sin embargo, algunos síntomas pueden tardar unos días en desaparecer. Ocasionalmente, para reducir el malestar asociado con los síntomas, se administrarán benzodiazepinas para controlar los ataques de pánico y las alucinaciones.
Se debe prestar especial atención a la monitorización de la respiración, el control de las vías respiratorias y la circulación. Si el tratamiento se produce dentro de la primera hora de la ingestión, el lavado gástrico puede ser eficaz. Si los vómitos se vuelven demasiado intensos, se administran líquidos por vía intravenosa , también se puede proporcionar atención psiquiátrica.
En casos raros , se pueden necesitar medicamentos anticolinérgicos , como la atropina . [12]
Uso en investigación [ editar ]
El ácido iboténico utilizado para lesionar el cerebro de ratas se mantiene congelado en una solución salina tamponada con fosfato a un pH de 7,4 y se puede conservar hasta un año sin pérdida de toxicidad. La inyección de 0,05 a 0,1 microlitros de ácido iboténico en el hipocampo a una velocidad de 0,1 microlitros / min dio como resultado una lesión semi-selectiva. La lesión del hipocampo provocó una pérdida considerable de células en las células piramidales (CA1-CA3), así como de células granulares en la circunvolución dentada . La lesión con ácido iboténico también causa algún daño a los axones a lo largo de la vía perforante .
Normalmente, cuando la lesión se realiza con otros productos químicos, el sujeto no puede volver a aprender una tarea. Sin embargo, debido a la reactividad del ácido iboténico con los receptores de glutamato como el receptor NMDA, la lesión del ácido iboténico permite al sujeto volver a aprender las tareas. Por lo tanto, la lesión con ácido iboténico se prefiere en estudios en los que es esencial volver a aprender una tarea después de la lesión. Comparado con otros agentes lesivos, el ácido iboténico es uno de los más específicos del sitio; sin embargo, actualmente se buscan alternativas menos dañinas. [13]
Biosíntesis [ editar ]
Los genes biosintéticos del ácido iboténico están organizados en un grupo de genes biosintéticos ligados físicamente . La vía biosintética se inicia mediante la hidroxilación del ácido glutámico mediante una oxigenasa específica dependiente de Fe (II) / 2-oxoglutarato . La reacción produce ácido treo -3-hidroxiglutámico, que se convierte en ácido iboténico, probablemente mediante enzimas codificadas en el grupo de genes biosintéticos. [14]
Ver también [ editar ]
- Ácido quiscualico
Referencias [ editar ]
- ^ a b c Tommy Liljefors; Povl Krogsgaard-Larsen; Ulf Madsen (25 de julio de 2002). Libro de texto de diseño y descubrimiento de fármacos, tercera edición . Prensa CRC. págs. 263–. ISBN 978-0-415-28288-8.
- ^ Becker, A; Grecksch, G; Bernstein, HG; Höllt, V; Bogerts, B (1999). "Comportamiento social en ratas lesionadas con ácido iboténico en el hipocampo: análisis cuantitativo y cualitativo". Psicofarmacología . 144 (4): 333–8. doi : 10.1007 / s002130051015 . PMID 10435405 . S2CID 25172395 .
- ^ Isacson, O; Brundin, P; Kelly, PA; Gage, FH; Björklund, A (1984). "Reemplazo neuronal funcional por neuronas estriatales injertadas en el cuerpo estriado de rata lesionada con ácido iboténico". Naturaleza . 311 (5985): 458–60. Código bibliográfico : 1984Natur.311..458I . doi : 10.1038 / 311458a0 . PMID 6482962 . S2CID 4342937 .
- ↑ a b c Wantanabe (23 de julio de 1999). Investigación farmacológica sobre medicamentos tradicionales a base de plantas . Prensa CRC. págs. 107–. ISBN 978-90-5702-054-4.
- ^ Ermitaño MB, Greenwood JR, Nielsen B, Bunch L, Jørgensen CG, Vestergaard HT, Stensbøl TB, Sanchez C, Krogsgaard-Larsen P, Madsen U, Bräuner-Osborne H (2004). "Ácido iboténico y ácido tioiboténico: una diferencia notable en la actividad en los receptores de glutamato metabotrópicos del grupo III". EUR. J. Pharmacol . 486 (3): 241–50. doi : 10.1016 / j.ejphar.2003.12.033 . PMID 14985045 .
- ^ Chilton 1975; Theobald y col. 1968
- ^ Chilton 1975; Ott 1976a
- ^ a b Zinkand, William; Moore, W .; Thompson, Carolann; Salama, Andre; Patel, Jitendra (febrero de 1992). "El ácido iboténico media la neurotoxicidad y la hidrólisis de fosfoinositidos por mecanismos receptores independientes". Neuropatología molecular y química . 16 (1–2): 1–10. doi : 10.1007 / bf03159956 . PMID 1325800 .
- ^ Sureda, F. "Excitotoxicidad y el receptor de NMDA" . eurosiva . Consultado el 30 de abril de 2015 .
- ^ Michelot, Didier; Meléndez-Howell, Leda Maria (2003). "Amanita muscaria: química, biología, toxicología y etnomicología" (PDF) . Investigación Micológica . 107 (2): 131–146. doi : 10.1017 / s0953756203007305 . PMID 12747324 .
- ^ a b Duffy, Thomas. "Síntomas de intoxicación por iboténico / muscimol (intoxicación por isoxazol)" . Hongos tóxicos del oeste de América del Norte . MykoWeb . Consultado el 30 de abril de 2015 .
- ^ Rolston-Cregler, Louis. "Toxicidad de hongos alucinógenos" . MedScape . Consultado el 30 de abril de 2015 .
- ^ Jarrard, Leonard (2 de febrero de 1989). "Sobre el uso de ácido iboténico para lesionar selectivamente diferentes componentes de la formación del hipocampo". Revista de métodos de neurociencia . 29 (3): 251-259. doi : 10.1016 / 0165-0270 (89) 90149-0 . PMID 2477650 . S2CID 3767525 .
- ^ Obermaier, Sebastián; Müller, Michael (31 de marzo de 2020). "La biosíntesis de ácido iboténico en el agárico de mosca se inicia por hidroxilación de glutamato" . Angewandte Chemie International Edition . 59 (30): 12432-12435. doi : 10.1002 / anie.202001870 . PMC 7383597 . PMID 32233056 .