Prueba de yodo-almidón
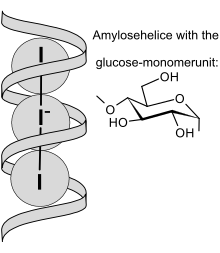 Vista esquemática de I 3 - iones incrustados en amilosa hélice | |
| Clasificación | Método colorimétrico |
|---|---|
| Analitos | Almidón |
La prueba de yodo-almidón es una reacción química que se utiliza para comprobar la presencia de almidón o yodo . La combinación de almidón y yodo es intensamente azul-negra. [1] [2]
La interacción entre el almidón y el anión triyoduro ( I-
3) es la base de la yodometría .
Historia y principios
La prueba de yodo-almidón fue descrita por primera vez por JJ Colin y HF Gaultier de Claubry, [3] e independientemente por F. Stromeyer, [4] en 1814. [5]
El anión triyoduro produce instantáneamente un color negro azulado intenso al entrar en contacto con el almidón. La intensidad del color disminuye al aumentar la temperatura y con la presencia de disolventes orgánicos miscibles en agua como el etanol. La prueba no se puede realizar a un pH muy bajo debido a la hidrólisis del almidón en estas condiciones. [6] Se cree que la mezcla de yodo-yoduro se combina con el almidón para formar un homopolímero de poliyoduro infinito . Esto se racionalizó mediante cristalografía de rayos X de cristal único y espectroscopía Raman comparativa. [7]
Almidón como indicador
El almidón se utiliza a menudo en química como indicador de valoraciones redox en las que hay triyoduro. [1] El almidón forma un complejo negro azulado muy oscuro con triyoduro. Sin embargo, el complejo no se forma si solo está presente yodo o solo yoduro (I - ). El color del complejo de almidón es tan profundo que puede detectarse visualmente cuando la concentración de yodo es tan baja como 20 µM a 20 ° C. [8] Durante las valoraciones de yodo, las soluciones de yodo concentrado deben reaccionar con algo de valorante, a menudo tiosulfato., para eliminar la mayor parte del yodo antes de agregar el almidón. Esto se debe a la insolubilidad del complejo almidón-triyoduro que puede evitar que parte del yodo reaccione con el titulante. Cerca del punto final, se agrega el almidón y se reanuda el proceso de titulación teniendo en cuenta la cantidad de tiosulfato agregada antes de agregar el almidón.
El cambio de color se puede utilizar para detectar la humedad o la transpiración, como en la prueba Minor o la prueba de almidón y yodo.
Ver también
Referencias
- ^ a b Cochran, Beverly; Lunes, Deborah; Miskevich, Frank (2008). "Análisis cinético de amilasa usando reactivos cuantitativos de almidón de Benedicto y yodo". Revista de educación química . 85 (3): 401. Código Bibliográfico : 2008JChEd..85..401C . doi : 10.1021 / ed085p401 .
- ^ Naiman, Barnet (1937). "Indicador de conservación de almidón". Revista de educación química . 14 (3): 138. Código Bibliográfico : 1937JChEd..14..138N . doi : 10.1021 / ed014p138.1 .
- ^ Colin, JJ; Gaultier de Clauby, HF (1814). "Mémoire sur les Combinaisons de l'Iode con les Substances Végétales et Animales". Annales de Chimie . 90 : 87-100.
- ^ Stromeyer, F. (1815). "Ein sehr empfindliches Reagens für Jodine, aufgefunden in der Stärke (Amidon)" [Un reactivo muy sensible para los yodos, que se encuentra en el almidón (amidona)]. Annalen der Physik . 49 (1-2): 146-153. Código Bibliográfico : 1815AnP .... 49..146S . doi : 10.1002 / yp.18150490108 .
- ^ Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ "Prueba de yodo para almidón" . Brillante Laboratorio de Biología para estudiantes de Máster en Biología . Consultado el 1 de diciembre de 2015 .
- ^ Madhu, Sheri; Evans, Hayden A .; Doan-Nguyen, Vicky VT; Labram, John G .; Wu, Guang; Chabinyc, Michael L .; Seshadri, Ram; Wudl, Fred (4 de julio de 2016). "Cadenas infinitas de poliyoduro en el complejo pirroloperileno-yodo: conocimientos sobre los complejos almidón-yodo y perileno-yodo" . Angewandte Chemie International Edition . 55 (28): 8032–8035. doi : 10.1002 / anie.201601585 . PMID 27239781 .
- ^ Bertrand, Gary. "Reacción del reloj de yodo" . Universidad de Ciencia y Tecnología de Missouri . Consultado el 18 de mayo de 2019 .
Otras lecturas
- Libro de texto de Vogel's de análisis químico cuantitativo, 5ª edición.
enlaces externos
- ¿Cómo indica el almidón el yodo? Química general en línea
- Prueba de yodo en Braukaiser
- Titrations.info: Titulación potenciométrica - Soluciones utilizadas en titulaciones yodométricas
- Ensayos quimicos
- Técnicas de laboratorio
- Yodo
- Polihaluros
- Almidón