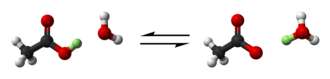Constante de disociación ácida
Una constante de disociación ácida , K a , (también conocida como constante de acidez o constante de ionización ácida ) es una medida cuantitativa de la fuerza de un ácido en solución . Es la constante de equilibrio de una reacción química.
donde las cantidades entre corchetes representan las concentraciones de la especie en equilibrio. [nota 3] [2]
La constante de disociación ácida de un ácido es una consecuencia directa de la termodinámica subyacente de la reacción de disociación; el valor de p K a es directamente proporcional al cambio de energía libre de Gibbs estándar para la reacción. El valor de p K a cambia con la temperatura y puede entenderse cualitativamente con base en el principio de Le Châtelier : cuando la reacción es endotérmica , K a aumenta y p K a disminuye al aumentar la temperatura; lo contrario es cierto para las reacciones exotérmicas .
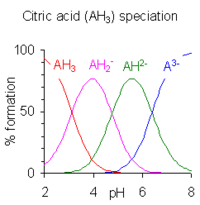
El valor de p K a también depende de la estructura molecular del ácido de muchas formas. Por ejemplo, Pauling propuso dos reglas: uno para los sucesivos p K una de ácidos polipróticos (véase ácidos polipróticos abajo), y uno para estimar la p K una de oxiácidos basado en el número de grupos -OH = O y (ver Factores que afectan p K a valores a continuación). Otros factores estructurales que influyen en la magnitud de la constante de disociación ácida incluyen efectos inductivos , efectos mesoméricos y enlaces de hidrógeno . Ecuaciones tipo Hammettse han aplicado con frecuencia a la estimación de p K a . [3] [4]
El comportamiento cuantitativo de ácidos y bases en solución sólo puede entenderse si se conocen sus valores de p K a . En particular, el pH de una solución se puede predecir cuando se conocen la concentración analítica y los valores de p K a de todos los ácidos y bases; a la inversa, es posible calcular la concentración de equilibrio de los ácidos y bases en solución cuando se conoce el pH. Estos cálculos encuentran aplicación en muchas áreas diferentes de la química, la biología, la medicina y la geología. Por ejemplo, muchos compuestos utilizados para la medicación son ácidos o bases débiles, y un conocimiento de los valores de p K a , junto con el coeficiente de partición octanol-agua., se puede utilizar para estimar la medida en que el compuesto entra en el torrente sanguíneo. Las constantes de disociación ácida también son fundamentales en la química acuática y la oceanografía química , donde la acidez del agua juega un papel fundamental. En los organismos vivos, la homeostasis ácido-base y la cinética enzimática dependen de los valores de p K a de los muchos ácidos y bases presentes en la célula y en el cuerpo. En química, el conocimiento de los valores de p K a es necesario para la preparación de soluciones tampón y también es un requisito previo para una comprensión cuantitativa de la interacción entre ácidos o bases e iones metálicos para formar complejos.. Experimentalmente, los valores de p K a pueden determinarse mediante titulación potenciométrica (pH) , pero para valores de p K a inferiores a aproximadamente 2 o más de aproximadamente 11, pueden ser necesarias mediciones espectrofotométricas o de RMN debido a dificultades prácticas con las mediciones de pH.
Según Arrhenius 's definición molecular originales , un ácido es una sustancia que se disocia en solución acuosa, liberando el ión hidrógeno H + (un protón): [5]