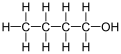
1-butanol
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Butan-1-ol [1] | |||
| Otros nombres n -butanol n -butil alcohol n -Butil hidróxido n -Propylcarbinol n -Propylmethanol 1-hidroxibutano Methylolpropane | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| 3DMet | |||
| 969148 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA | 100.000.683 | ||
| Número CE |
| ||
| 25753 | |||
| KEGG | |||
| Malla | 1-butanol | ||
PubChem CID | |||
| Número RTECS |
| ||
| UNII | |||
| un numero | 1120 | ||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 4 H 10 O | |||
| Masa molar | 74,123 g · mol −1 | ||
| Apariencia | Líquido refractivo incoloro | ||
| Olor | similar al plátano , [2] áspero, alcohólico y dulce | ||
| Densidad | 0,81 g / cm 3 | ||
| Punto de fusion | −89,8 ° C (−129,6 ° F; 183,3 K) | ||
| Punto de ebullición | 117,7 ° C (243,9 ° F; 390,8 K) | ||
solubilidad en agua | 73 g / L a 25 ° C | ||
| Solubilidad | muy soluble en acetona miscible con etanol , éter etílico | ||
| log P | 0,839 | ||
| Presión de vapor | 0,58 kPa (20 ° C) Tarjetas internacionales de seguridad química de la OIT (ICSC) | ||
| Acidez (p K a ) | 16.10 | ||
Susceptibilidad magnética (χ) | −56,536 · 10 −6 cm 3 / mol | ||
Índice de refracción ( n D ) | 1.3993 (20 ° C) | ||
| Viscosidad | 2.573 mPa · s (a 25 ° C) [3] | ||
Momento bipolar | 1,66 D | ||
| Termoquímica | |||
Entropía molar estándar ( S | 225,7 J / (K · mol) | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −328 (4) kJ / mol | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | −2670 (20) kJ / mol | ||
| Riesgos | |||
| Ficha de datos de seguridad | ICSC 0111 | ||
| Pictogramas GHS | |||
| NFPA 704 (diamante de fuego) |  1 3 0 | ||
| punto de inflamabilidad | 35 ° C (95 ° F; 308 K) | ||
autoignición temperatura | 343 ° C (649 ° F; 616 K) | ||
| Límites explosivos | 1,45-11,25% | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 790 mg / kg (rata, oral) | ||
LD Lo ( más bajo publicado ) | 3484 mg / kg (conejo, oral) 790 mg / kg (rata, oral) 1700 mg / kg (perro, oral) [5] | ||
LC 50 ( concentración media ) | 9221 ppm (mamífero) 8000 ppm (rata, 4 h ) [5] | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
PEL (permitido) | TWA 100 ppm (300 mg / m 3 ) [4] | ||
REL (recomendado) | C 50 ppm (150 mg / m 3 ) [piel] [4] | ||
IDLH (peligro inmediato) | 1400 ppm [4] | ||
| Compuestos relacionados | |||
Compuestos relacionados | Éter dietílico de butanotiol n- butilamina pentano | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
El 1-butanol (IUPAC: butan-1-ol ) también conocido como n-butanol es un alcohol primario con la fórmula química C 4 H 9 OH y una estructura lineal. Los isómeros del 1-butanol son isobutanol , 2-butanol y terc- butanol . El término butanol sin modificar normalmente se refiere al isómero de cadena lineal.
El 1-butanol se produce de forma natural como un producto menor de la fermentación de azúcares y otros carbohidratos [6] y está presente en muchos alimentos y bebidas. [7] [8] También es un aromatizante artificial permitido en los Estados Unidos, [9] utilizado en mantequilla, nata, fruta, ron, whisky, helados y helados, dulces, productos horneados y cordiales. [10] También se utiliza en una amplia gama de productos de consumo. [7]
El uso más grande de 1-butanol es como intermedio industrial, particularmente para la fabricación de acetato de butilo (en sí mismo un aromatizante artificial y solvente industrial). Es un petroquímico derivado del propileno . Las cifras de producción estimadas para 1997 son: Estados Unidos 784.000 toneladas; Europa occidental 575.000 toneladas; Japón 225.000 toneladas. [8]
Producción
Desde la década de 1950, la mayor parte del 1-butanol se produce mediante la hidroformilación de propileno ( proceso oxo ) para formar preferentemente el butiraldehído n-butanal. Los catalizadores típicos se basan en cobalto y rodio. A continuación, se hidrogena butiraldehído para producir butanol.
Un segundo método para producir butanol implica la reacción de Reppe del propileno con CO y agua: [11]
- CH 3 CH = CH 2 + H 2 O + 2 CO → CH 3 CH 2 CH 2 CH 2 OH + CO 2
En épocas anteriores, el butanol se preparaba a partir de crotonaldehído , que se puede obtener a partir de acetaldehído .
El butanol también se puede producir por fermentación de biomasa por bacterias. Antes de la década de 1950, Clostridium acetobutylicum se usaba en la fermentación industrial para producir butanol. La investigación en las últimas décadas mostró resultados de otros microorganismos que pueden producir butanol a través de la fermentación .
Uso industrial
Constituyendo el 85% de su uso, el 1-butanol se utiliza principalmente en la producción de barnices . Es un solvente popular, por ejemplo, para nitrocelulosa . Se utilizan diversos ésteres de butilo como disolventes, por ejemplo, butoxietanol . Muchos plastificantes se basan en ésteres de butilo, por ejemplo, ftalato de dibutilo . El monómero acrilato de butilo se utiliza para producir polímeros. Es el precursor de las n-butilaminas . [11]
Biocombustible
Se ha propuesto el 1-butanol como sustituto del combustible diesel y la gasolina . Se produce en pequeñas cantidades en casi todas las fermentaciones (ver aceite de fusel ). Clostridium produce rendimientos mucho más altos de butanol. Se están realizando investigaciones para aumentar el rendimiento de biobutanol a partir de biomasa .
El butanol se considera un biocombustible potencial ( combustible de butanol ). El butanol al 85 por ciento se puede usar en automóviles diseñados para gasolina (gasolina) sin ningún cambio en el motor (a diferencia del etanol al 85%), y proporciona más energía para un volumen dado que el etanol, debido al menor contenido de oxígeno del butanol [12 ] y casi tanto como la gasolina. Por lo tanto, un vehículo que usa butanol generaría un consumo de combustible más comparable al de la gasolina que al del etanol. El butanol también se puede agregar al combustible diesel para reducir las emisiones de hollín. [13]
La producción o, en algunos casos, el uso de las siguientes sustancias puede provocar la exposición al 1-butanol: cuero artificial , ésteres butílicos , cemento de caucho , tintes, esencias de frutas, lacas, películas cinematográficas y fotográficas, impermeables, perfumes, plásticos de piroxilina , rayón , vidrio de seguridad, barniz de goma laca y tela impermeabilizada. [7]
Ocurrencia en la naturaleza
El 1-butanol se produce naturalmente como resultado de la fermentación de carbohidratos en una serie de bebidas alcohólicas, incluidas la cerveza, [14] aguardientes de uva, [15] vino, [16] y whisky. [17] Se ha detectado en los volátiles del lúpulo, [18] la fruta de jurel, [19] leches tratadas térmicamente, [20] melón almizclero, [21] queso, [22] semillas de guisantes del sur, [23] y cocidas arroz. [24] El 1-butanol también se forma durante la fritura profunda de aceite de maíz, aceite de semilla de algodón, trilinoleína y trioleína. [25]
El 1-butanol es uno de los " alcoholes fusel " (del alemán para "licor malo"), que incluye alcoholes que tienen más de dos átomos de carbono y tienen una solubilidad significativa en agua. [26] Es un componente natural de muchas bebidas alcohólicas, aunque en concentraciones bajas y variables. [27] [28] Se dice que (junto con alcoholes fusel similares ) es responsable de resacas severas , aunque los experimentos en modelos animales no muestran evidencia de esto. [29]
El 1-butanol se utiliza como ingrediente en aromatizantes artificiales y elaborados, [30] y para la extracción de proteínas sin lípidos de la yema de huevo, [31] aromatizantes naturales y aceites vegetales, la fabricación de extracto de lúpulo para la elaboración de cerveza y como un disolvente para eliminar los pigmentos del concentrado de proteína de hoja de cuajada húmeda . [32]
Metabolismo y toxicidad
La toxicidad aguda del 1-butanol es relativamente baja, con valores de LD 50 por vía oral de 790 a 4360 mg / kg (rata; los valores comparables para el etanol son de 7 000 a 15 000 mg / kg). [8] [33] [11] Se metaboliza completamente en los vertebrados de una manera similar al etanol : la alcohol deshidrogenasa convierte el 1-butanol en butiraldehído ; esto luego se convierte en ácido butírico por la aldehído deshidrogenasa . El ácido butírico se puede metabolizar completamente en dióxido de carbono y agua por la vía de la β-oxidación . En la rata, solo el 0,03% de una dosis oral de 2000 mg / kg se excretó en la orina.[34] En dosis subletales, el 1-butanol actúa como un depresor del sistema nervioso central , similar al etanol: un estudio en ratas indicó que la potencia intoxicante del 1-butanol es aproximadamente 6 veces mayor que la del etanol, posiblemente debido a su transformación más lenta por la alcohol deshidrogenasa. [35]
Otros peligros
El 1-butanol líquido, como es común con la mayoría de los solventes orgánicos, es extremadamente irritante para los ojos; El contacto repetido con la piel también puede causar irritación. [8] Se cree que esto es un efecto genérico de "desgrasado". No se ha observado sensibilización cutánea. La irritación de las vías respiratorias ocurre solo a concentraciones muy altas (> 2400 ppm). [36]
Con un punto de inflamación de 35 ° C, el 1-butanol presenta un riesgo de incendio moderado: es un poco más inflamable que el queroseno o el combustible diesel, pero menos inflamable que muchos otros disolventes orgánicos comunes. El efecto depresor sobre el sistema nervioso central (similar a la intoxicación por etanol) es un peligro potencial cuando se trabaja con 1-butanol en espacios cerrados, aunque el umbral de olor (0,2-30 ppm) está muy por debajo de la concentración que tendría algún efecto neurológico. [36] [37]
Ver también
- Combustible de butanol
enlaces externos
- Tarjeta internacional de seguridad química 0111
- Guía de bolsillo de NIOSH sobre peligros químicos. "# 0076" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- Informe de evaluación inicial de los pequeños Estados insulares en desarrollo para el n- butanol de la Organización para la Cooperación y el Desarrollo Económicos (OCDE)
- IPCS Environmental Health Criteria 65: Butanoles: cuatro isómeros
- Guía de salud y seguridad del IPCS 3: 1-butanol
Referencias
- ^ "1-Butanol - Resumen compuesto" . El Proyecto PubChem . EE.UU .: Centro Nacional de Información Biotecnológica.
- ^ [Información del producto n-butanol, The Dow Chemical Company, formulario No. 327-00014-1001, página 1]
- ^ Dubey, Gyan (2008). "Estudio de densidades, viscosidades y velocidades de sonido de mezclas líquidas binarias de butan-1-ol con n-alcanos (C6, C8 y C10) en T = (298.15, 303.15 y 308.15) K". La revista de termodinámica química . 40 (2): 309–320. doi : 10.1016 / j.jct.2007.05.016 .
- ^ a b c Guía de bolsillo de NIOSH sobre peligros químicos. "# 0076" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ a b "alcohol N-butílico" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Hazelwood, Lucie A .; Daran, Jean-Marc; van Maris, Antonius JA; Pronk, Jack T .; Dickinson, J. Richard (2008), "La vía de Ehrlich para la producción de alcohol fusel: un siglo de investigación sobre el metabolismo de Saccharomyces cerevisiae ", Appl. Reinar. Microbiol. , 74 (8): 2259–66, Bibcode : 2008ApEnM..74.2259H , doi : 10.1128 / AEM.02625-07 , PMC 2293160 , PMID 18281432 .
- ^ a b c Butanoles: cuatro isómeros , monografía de Criterios de salud ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ a b c d n- Butanol (PDF) , Informe de evaluación inicial de los PEID, Ginebra: Programa de las Naciones Unidas para el Medio Ambiente, abril de 2005.
- ^ Título 21 del Código de Reglamentaciones Federales, sección 172.515; 42 FR 14491, 15 de marzo de 1977, según enmendada.
- ^ Hall, RL; Oser, BL (1965), "Progresos recientes en la consideración de ingredientes aromatizantes bajo la enmienda de aditivos alimentarios. III. Sustancias gras", Food Technol. : 151, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ a b c Hahn, Heinz-Dieter; Dämbkes, Georg; Rupprich, Norbert (2005). "Butanoles". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a04_463 ..
- ^ Schmidt-Rohr, K. (2015). "Por qué las combinaciones son siempre exotérmicas, produciendo alrededor de 418 kJ por mol de O 2 ", J. Chem. Educ. 92 : 2094-2099. https://dx.doi.org/10.1021/acs.jchemed.5b00333
- ^ Antoni, D .; Zverlov, V. y Schwarz, WH (2007). "Biocombustibles de microbios". Microbiología y Biotecnología Aplicadas . 77 (1): 23–35. doi : 10.1007 / s00253-007-1163-x . PMID 17891391 . S2CID 35454212 .
- ^ Bonte, W. (1979), "Sustancias conjuntas en cervezas alemanas y extranjeras", Blutalkohol , 16 : 108-24, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ Schreier, Peter; Drawert, Friedrich; Winkler, Friedrich (1979), "Composición de constituyentes volátiles neutros en brandies de uva", J. Agric. Food Chem. , 27 (2): 365–72, doi : 10.1021 / jf60222a031.
- ^ Bonte, W. (1978), "Contenido de congéneres de vino y bebidas similares", Blutalkohol , 15 : 392–404, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ Postel, W .; Adam, L. (1978), "Caracterización cromatográfica de gases del whisky. III. Whisky irlandés", Branntweinwirtschaft , 118 : 404–7, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ Tressl, Roland; Friese, Lothar; Fendesack, Friedrich; Koeppler, Hans (1978), "Estudios de la composición volátil del lúpulo durante el almacenamiento", J. Agric. Food Chem. , 26 (6): 1426–30, doi : 10.1021 / jf60220a036.
- ^ Espadas, G .; Bobbio, PA; Hunter, GLK (1978), "Componentes volátiles de la fruta de la jurel ( Arthocarpus heterophyllus )", J. Food Sci. , 43 (2): 639–40, doi : 10.1111 / j.1365-2621.1978.tb02375.x.
- ^ Jaddou, Haytham A .; Pavey, John A .; Manning, Donald J. (1978), "Análisis químico de aromatizantes volátiles en leches tratadas térmicamente", J. Dairy Res. , 45 (3): 391–403, doi : 10.1017 / S0022029900016617.
- ↑ Yabumoto, K .; Yamaguchi, M .; Jennings, WG (1978), "Producción de compuestos volátiles por Muskmelon, Cucumis melo ", Food Chem. , 3 (1): 7–16, doi : 10.1016 / 0308-8146 (78) 90042-0.
- ^ Dumont, Jean Pierre; Adda, Jacques (1978), "Ocurrencia de sesquiterpones en volátiles de queso de montaña", J. Agric. Food Chem. , 26 (2): 364–67, doi : 10.1021 / jf60216a037.
- ^ Fisher, Gordon S .; Legendre, Michael G .; Lovgren, Norman V .; Schuller, Walter H .; Wells, John A. (1979), "Componentes volátiles de la semilla del fríjol sureño [ Vigna unguiculata (L.) Walp.]", J. Agric. Food Chem. , 27 (1): 7–11, doi : 10.1021 / jf60221a040.
- ^ Yajima, Izumi; Yanai, Tetsuya; Nakamura, Mikio; Sakakibara, Hidemasa; Habu, Tsutomu (1978), "Componentes volátiles del sabor del arroz cocido" , Agric. Biol. Chem. , 42 (6): 1229–33, doi : 10.1271 / bbb1961.42.1229.
- ^ Chang, SS; Peterson, KJ; Ho, C. (1978), "Reacciones químicas implicadas en la fritura de alimentos con mucha grasa", J. Am. Oil Chem. Soc. , 55 (10): 718–27, doi : 10.1007 / BF02665369 , PMID 730972 , S2CID 97273264 , citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ Atsumi, S .; Hanai, T .; Liao, JC (2008). "Vías no fermentativas para la síntesis de alcoholes superiores de cadena ramificada como biocombustibles". Naturaleza . 451 (7174): 86–89. Código Bibliográfico : 2008Natur.451 ... 86A . doi : 10.1038 / nature06450 . PMID 18172501 . S2CID 4413113 .
- ^ Woo, Kang-Lyung (2005), "Determinación de alcoholes de bajo peso molecular, incluido el aceite de fusel en varias muestras mediante extracción con éter dietílico y cromatografía de gases capilar", J. AOAC Int. , 88 (5): 1419–27, doi : 10.1093 / jaoac / 88.5.1419 , PMID 16385992 .
- ^ Lachenmeier, Dirk W .; Haupt, Simone; Schulz, Katja (2008), "Definición de niveles máximos de alcoholes superiores en bebidas alcohólicas y productos alcohólicos sustitutos", Regul. Toxicol. Pharmacol. , 50 (3): 313–21, doi : 10.1016 / j.yrtph.2007.12.008 , PMID 18295386 .
- ^ Hori, Hisako; Fujii, Wataru; Hatanaka, Yutaka; Suwa, Yoshihide (2003), "Efectos del aceite de fusel en modelos de resaca animal", Alcohol. Clin. Exp. Res. , 27 (8 Suppl): 37S – 41S, doi : 10.1097 / 01.ALC.0000078828.49740.48 , PMID 12960505 .
- ^ Mellan, I. (1950), Solventes industriales , Nueva York: Van Nostrand Reinhold, págs. 482–88, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ Meslar, Harry W .; White, Harold B., III (1978), "Preparación de extractos proteicos libres de lípidos de yema de huevo", Anal. Biochem. , 91 (1): 75–81, doi : 10.1016 / 0003-2697 (78) 90817-5 , PMID 9762085 .
- ^ Bray, Walter J .; Humphries, Catherine (1978), "Fraccionamiento con disolvente de jugo de hojas para preparar productos proteicos verdes y blancos", J. Sci. Alimentos Agric. , 29 (10): 839–46, doi : 10.1002 / jsfa.2740291003.
- ^ Etanol (PDF) , Informe de evaluación inicial de SIDS, Ginebra: Programa de las Naciones Unidas para el Medio Ambiente, agosto de 2005 .
- ^ Gaillard, D .; Derache, R. (1965), "Métabilisation de différents alcools présents dans les biossons alcooliques chez le rat", Trav. Soc. Pharmacol. Montpellier , 25 : 541–62, citado en Butanoles: cuatro isómeros , monografía de Criterios de Salud Ambiental No. 65, Ginebra: Organización Mundial de la Salud, 1987, ISBN 92-4-154265-9.
- ^ McCreery, Nueva Jersey; Hunt, WA (1978), "Correlaciones fisicoquímicas de la intoxicación por alcohol", Neuropharmacology , 17 (7): 451–61, doi : 10.1016 / 0028-3908 (78) 90050-3 , PMID 567755 , S2CID 19914287 .
- ^ a b Wysocki, CJ; Dalton, P. (1996), Umbrales de olor e irritación para el 1-butanol en humanos , Filadelfia: Monell Chemical Senses Center, citado en n- Butanol (PDF) , Informe de evaluación inicial de los PEID, Ginebra: Programa de las Naciones Unidas para el Medio Ambiente, abril de 2005.
- ^ Cometto-Muñiz, J. Enrique; Cain, William S. (1998), "Sensibilidad olfativa y del trigémino: Comparación de modalidades y métodos de medición" , Int. Arco. Ocupar. Reinar. Salud , 71 (2): 105–10, doi : 10.1007 / s004200050256 , PMID 9580447 , S2CID 25246408 .
- Disolventes de alcohol
- Alcoholes primarios
- Moduladores alostéricos positivos del receptor GABAA
- Sedantes
- Hipnóticos
- Alcanoles
