Acetato de níquel (II)
(Redirigido de acetato de níquel )
Saltar a navegación Saltar a búsqueda_acetate_tetrahydrate.jpg/440px-Nickel(II)_acetate_tetrahydrate.jpg) | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC sistemático Diacetato de níquel (2+) | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| Tarjeta de información ECHA | 100.006.147 |
| Número CE |
|
PubChem CID | |
| UNII |
|
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 4 H 6 Ni O 4 | |
| Masa molar | 176,781 g · mol −1 |
| Apariencia | Verde Sólido |
| Olor | ácido acético ligero |
| Densidad | 1.798 g / cm 3 (anhidro) 1.744 g / cm 3 (tetrahidrato) |
| Punto de fusion | se descompone cuando se calienta [1] [2] |
| Fácilmente soluble en agua fría, agua caliente. | |
| Solubilidad | Soluble en metanol insoluble en éter dietílico , n-octanol |
| + 4,690.0 · 10 −6 cm 3 / mol | |
| Estructura | |
| monoclínico | |
| P 2 1 / c | |
a = 4.764, b = 11.771, c = 8.425 Å α = 90 °, β = 93,6 °, γ = 90 ° [3] tetrahidrato | |
Volumen de celosía ( V ) | 471,5 |
Unidades de fórmula ( Z ) | 2 |
| octaédrico distorsionado | |
| Riesgos | |
| NFPA 704 (diamante de fuego) | |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis media ) | 350 mg / kg (rata, oral) 410 mg / kg (ratón, oral) [4] |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
Acetato de níquel (II) es el nombre de los compuestos de coordinación con la fórmula Ni (CH 3 CO 2 ) 2 · x H 2 O donde x puede ser 0, 2 y 4. El tetrahidrato verde Ni (CH 3 CO 2 ) 2 · 4 H 2 O es el más común. Se utiliza para galvanoplastia .
Síntesis y estructura
El compuesto se puede preparar tratando níquel o carbonato de níquel (II) con ácido acético:
- NiCO 3 + 2 CH 3 CO 2 H + 3 H 2 O → Ni (CH 3 CO 2 ) 2 · 4 H 2 O + CO 2
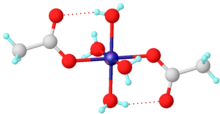
Se ha demostrado mediante cristalografía de rayos X que el tetrahidrato verde adopta una estructura octaédrica, estando coordinado el centro de níquel central por cuatro moléculas de agua y dos ligandos de acetato . [5] Puede deshidratarse al vacío , por reacción con anhídrido acético [6] o por calor. [7]
La seguridad
Las sales de níquel son cancerígenas e irritan la piel.
Referencias
- ^ MA Mohamed, SA Halawy, MM Ebrahim: "Descomposición no isotérmica de acetato de níquel tetrahidratado", en: Journal of Analytical and Applied Pyrolysis , 1993 , 27 (2), S. 109-110. doi : 10.1016 / 0165-2370 (93) 80002-H .
- ^ GAM Hussein, AKH Nohman, KMA Attyia: "Caracterización del curso de descomposición del acetato de níquel tetrahidrato en el aire", en: Journal of Thermal Analysis and Calorimetry , 1994 , 42 , S. 1155-1165; doi : 10.1007 / BF02546925 .
- ^ Downie, TC; Harrison, W .; Raper, ES; Hepworth, MA (15 de marzo de 1971). "Un estudio tridimensional de la estructura cristalina del acetato de níquel tetrahidratado" . Acta Crystallographica Sección B . 27 (3): 706–712. doi : 10.1107 / S0567740871002802 .
- ^ "Níquel metal y otros compuestos (como Ni)" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Van Niekerk, JN; Schoening, FRL (1953). "Las estructuras cristalinas de acetato de níquel, Ni (CH 3 COO) 2 · 4H 2 O, y acetato de cobalto, Co (CH 3 COO) 2 · 4H 2 O". Acta Crystallogr. 6 (7): 609–612. doi : 10.1107 / S0365110X5300171X .
- ^ Lascelles, Keith; Morgan, Lindsay G .; Nicholls, David; Beyersmann, Detmar (2005). "Compuestos de níquel". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a17_235.pub2 .
- ^ Tappmeyer, WP; Davidson, Arthur W. (1963). "Acetatos de cobalto y níquel en ácido acético anhidro". Inorg. Chem. 2 (4): 823–825. doi : 10.1021 / ic50008a039 .
Categorías :
- Compuestos de níquel
- Acetatos
Contribute a better translation
