Saltar a navegación Saltar a búsqueda
| Nombres | |||
|---|---|---|---|
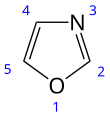
| Nombre IUPAC 1,3-oxazol | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| CHEBI | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.005.474 | ||
| Número CE |
| ||
| Malla | D010080 | ||
PubChem CID | |||
| UNII | |||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 3 H 3 N O | |||
| Masa molar | 69,06 g / mol | ||
| Densidad | 1.050 g / cm 3 | ||
| Punto de ebullición | 69 a 70 ° C (156 a 158 ° F; 342 a 343 K) | ||
| Acidez (p K a ) | 0,8 (de ácido conjugado) [1] | ||
| Página de datos complementarios | |||
| Índice de refracción ( n ), constante dieléctrica (ε r ), etc. | |||
Datos termodinámicos | Comportamiento de fase sólido-líquido-gas | ||
| UV , IR , RMN , MS | |||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
El oxazol es el compuesto original de una amplia clase de compuestos orgánicos aromáticos heterocíclicos . Estos son azoles con oxígeno y nitrógeno separados por un carbono. [2] Los oxazoles son compuestos aromáticos, pero menos que los tiazoles. El oxazol es una base débil; su ácido conjugado tiene un p K a de 0,8, en comparación con 7 del imidazol .
Preparación [ editar ]
Los métodos clásicos de síntesis de oxazol en química orgánica son
- la síntesis de Robinson-Gabriel por deshidratación de 2-acilaminocetonas
- la síntesis de oxazol de Fischer a partir de cianohidrinas y aldehídos
- la reacción de Bredereck con α- halocetonas y formamida
- la reacción de Van Leusen con aldehídos y TosMIC
Otros metodos:
- Oxazolinas también se puede obtener de cicloisomerización de ciertos propargilo amidas . En un estudio, se prepararon [3] oxazoles mediante una síntesis en un solo recipiente que consistía en la condensación de propargilamina y cloruro de benzoílo en la amida , seguida de un acoplamiento de Sonogashira del extremo alquino terminal con otro equivalente de cloruro de benzoílo, y concluyendo con p - cicloisomerización catalizada por ácido toluenosulfónico :
- En una síntesis de oxazol informada, los reactivos son un cloruro de benzoílo sustituido con nitro y un isonitrilo : [4] [5]
Biosíntesis [ editar ]
En las biomoléculas , los oxazoles resultan de la ciclación y oxidación de péptidos no ribosomales de serina o treonina :
- Donde X = H, CH
3para serina y treonina respectivamente, B = base.
(1) Ciclación enzimática. (2) Eliminación. (3) [O] = oxidación enzimática.
Los oxazoles no son tan abundantes en biomoléculas como los tiazoles relacionados con oxígeno reemplazado por un átomo de azufre.
Reacciones [ editar ]
- La desprotonación de oxazoles en C2 suele ir acompañada de apertura del anillo al isonitrilo.
- La sustitución aromática electrófila tiene lugar en C5 y requiere grupos activadores .
- La sustitución aromática nucleófila tiene lugar con grupos salientes en C2.
- Las reacciones de Diels-Alder con oxazol dienos pueden ir seguidas de una pérdida de oxígeno para formar piridinas .
- La transposición de Cornforth de 4-aciloxazoles es una reacción de transposición térmica con el residuo de acilo orgánico y el sustituyente C5 cambiando de posición.
- Varias reacciones de oxidación . Un estudio [6] informa sobre la oxidación de 4,5-difeniloxazol con 3 equivalentes de CAN a la imida y el ácido benzoico correspondientes :
- En la semirreacción balanceada se consumen tres equivalentes de agua por cada equivalente de oxazolina, generando 4 protones y 4 electrones (este último derivado de Ce IV ).
Uso de un oxazol en la síntesis de un precursor de piridoxina , que se convierte en vitamina B6 . [7]
Ver también [ editar ]
- Isoxazol , un análogo con el átomo de nitrógeno en la posición 2.
- Imidazol , un análogo con el oxígeno reemplazado por un nitrógeno.
- Tiazol , un análogo con el oxígeno reemplazado por azufre.
- Benzoxazol , donde el oxazol se fusiona con otro anillo aromático.
- Pirrol , un análogo sin el átomo de oxígeno.
- Furano , un análogo sin el átomo de nitrógeno.
- Oxazolina , que tiene un doble enlace reducido.
- Oxazolidina , que tiene ambos dobles enlaces reducidos.
- Oxadiazoles con dos nitrógenos en lugar de uno (p . Ej. Furazan ).
- Oxazolona , un análogo con un grupo carbonilo
Referencias [ editar ]
- ^ Zoltewicz, JA & Deady, LW Cuaternización de compuestos heteroaromáticos. Aspectos cuantitativos. Adv. Heterocycl. Chem. 22, 71 - 121 (1978).
- ^ Química heterocíclica TL Gilchrist, The Bath Press 1985 ISBN 0-582-01421-2
- ^ Una nueva síntesis consecutiva de oxazol de tres componentes mediante una secuencia de amidación-acoplamiento-cicloisomerización (ACCI) Eugen Merkul y Thomas JJ Müller Chem. Comun. , 2006 , 4817 - 4819, doi : 10.1039 / b610839c
- ^ Síntesis de flujo continuo completamente automatizada de oxazoles 4,5-disustituidos Marcus Baumann, Ian R. Baxendale, Steven V. Ley , Christoper D. Smith y Geoffrey K. Tranmer Org. Letón. ; 2006 ; 8 (23) págs. 5231 - 5234; (Carta) doi : 10.1021 / ol061975c
- ^ Reaccionan juntos en la primera fase en un reactor de flujo continuo al enol intermedioy luego en la segunda fase en una base de fosfaceno (PS-BEMP) inducida por ciclación por síntesis en fase sólida .
- ^ "Nitrato de amonio cérico promovió la oxidación de oxazoles", David A. Evans , Pavel Nagorny y Risheng Xu. Org. Letón. ; 2006 ; 8 (24) págs. 5669 - 5671; (Carta) doi : 10.1021 / ol0624530
- ^ Gérard Moine, Hans-Peter Hohmann, Roland Kurth, Joachim Paust, Wolfgang Hähnlein, Horst Pauling, Bernd-Jürgen Weimann, Bruno Kaesler (2011). "Vitaminas, 6. Vitaminas B". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.o27_o09 .Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )