Clorato de sodio
 | |
 | |
 Célula unitaria de clorato de sodio | |
| Nombres | |
|---|---|
| Nombre IUPAC Clorato de sodio | |
| Otros nombres Clorato de sodio (V) | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.028.989 |
| Número CE |
|
| KEGG | |
| Malla | Sodio + clorato |
PubChem CID | |
| Número RTECS |
|
| UNII | |
| un numero | 1495, 2428 |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| NaClO 3 | |
| Masa molar | 106,44 g mol -1 |
| Apariencia | Sólido incoloro o blanco, higroscópico |
| Olor | Inodoro |
| Densidad | 2,49 g / cm 3 (15 ° C) [1] 2,54 g / cm 3 (20,2 ° C) [2] |
| Punto de fusion | 248–261 ° C (478–502 ° F; 521–534 K) |
| Punto de ebullición | 300–400 ° C (572–752 ° F; 573–673 K) se descompone [1] |
| 79 g / 100 mL (0 ° C) 89 g / 100 mL (10 ° C) 105,7 g / 100 mL (25 ° C) 125 g / 100 mL (40 ° C) 220,4 g / 100 mL (100 ° C) [3] | |
| Solubilidad | Soluble en glicerol , hidracina , metanol Ligeramente soluble en etanol , amoniaco [1] |
| Solubilidad en acetona | Escasamente soluble [1] |
| Solubilidad en glicerol | 20 g / 100 g (15,5 ° C) [1] |
| Solubilidad en etanol | 14,7 g / 100 g [1] |
| Presión de vapor | <0,35 mPa [2] |
Susceptibilidad magnética (χ) | −34,7 · 10 −6 cm 3 / mol |
Índice de refracción ( n D ) | 1,515 (20 ° C) [4] |
| Estructura [5] | |
Estructura cristalina | cúbico |
Grupo de puntos | P2 1 3 |
Constante de celosía | a = 6,57584 Å |
Unidades de fórmula ( Z ) | 4 |
| Termoquímica | |
Capacidad calorífica ( C ) | 104,6 J / mol · K [1] |
Entropía molar estándar ( S | 129,7 J / mol · K [1] |
Entalpía estándar de formación (Δ f H ⦵ 298 ) | -365,4 kJ / mol [1] |
Energía libre de Gibbs (Δ f G ˚) | -275 kJ / mol [1] |
| Riesgos | |
| Ficha de datos de seguridad | ICSC 1117 |
| Pictogramas GHS | [6] |
| Palabra de señal GHS | Peligro |
Declaraciones de peligro GHS | H271 , H302 , H411 [6] |
Consejos de prudencia del SGA | P220 , P273 [6] |
| NFPA 704 (diamante de fuego) |  2 0 3 BUEY |
| punto de inflamabilidad | No es inflamable |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis media ) | 6500 mg / kg (ratas, oral) 700 mg / kg (perros, oral) [1] |
| Compuestos relacionados | |
Otros aniones | Cloruro de sodio Hipoclorito de sodio Clorito de sodio Perclorato de sodio Bromato de sodio Yodato de sodio |
Otros cationes | Clorato de amonio Clorato de potasio Clorato de bario |
Compuestos relacionados | Ácido clorhídrico |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
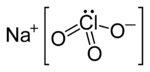
El clorato de sodio es un compuesto inorgánico con la fórmula química Na ClO 3 . Es un polvo cristalino blanco que es fácilmente soluble en agua. Es higroscópico . Se descompone por encima de los 300 ° C para liberar oxígeno [4] y deja cloruro de sodio . Se producen varios cientos de millones de toneladas anualmente, principalmente para aplicaciones en el blanqueo de pulpa para producir papel de alto brillo . [7]
Síntesis
Industrialmente, el clorato de sodio se produce mediante la electrólisis de una solución caliente de cloruro de sodio: [7]
- NaCl + 3 H 2 O → NaClO 3 + 3 H 2
Esta reacción progresa en calor (al menos 70 ° C) y pH controlado . En temperaturas más bajas o con un pH alto, progresa otra reacción: [ cita requerida ]
- 2 NaCl + H 2 O → NaClO + NaCl + H 2
El proceso de clorato de sodio no debe confundirse con el proceso de cloro-álcali , que es un proceso industrial para la producción electrolítica de hidróxido de sodio y cloro gaseoso.
Usos
El principal uso comercial del clorato de sodio es para producir dióxido de cloro (ClO 2 ). La mayor aplicación de ClO 2 , que representa aproximadamente el 95% del uso de clorato, es en el blanqueo de pulpa. Todos los compuestos de perclorato se producen industrialmente por oxidación de soluciones de clorato de sodio por electrólisis. [7]
Herbicidas
El clorato de sodio se utiliza como herbicida no selectivo . Se considera fitotóxico para todas las partes verdes de las plantas. También puede matar a través de la absorción de raíces.
El clorato de sodio se puede usar para controlar una variedad de plantas, como la gloria de la mañana , el cardo de Canadá , la hierba johnson , el bambú , la hierba cana y la hierba de San Juan . El herbicida se usa principalmente en tierras no cultivadas para el tratamiento local y para el control total de la vegetación en áreas que incluyen bordes de carreteras, vallas y zanjas. El clorato de sodio también se usa como defoliante y desecante para:
- Maíz
- Algodón
- Frijoles secos
- Linaza
- Sorgo de grano
- Pimientos
- Arroz
- Cártamo
- Guisantes sureños
- Soja
- Girasoles
Si se usa en combinación con atrazina , aumenta la persistencia del efecto. Si se usa en combinación con 2,4-D , se mejora el rendimiento. El clorato de sodio tiene un efecto esterilizante del suelo . La mezcla con otros herbicidas en solución acuosa es posible hasta cierto punto, siempre que no sean susceptibles a la oxidación.
La venta de clorato de sodio como herbicida fue prohibida en la Unión Europea en 2009 citando peligros para la salud, y las existencias existentes se utilizarán durante el año siguiente. [8]
Generación de oxígeno químico
Los generadores de oxígeno químico , como los de los aviones comerciales, proporcionan oxígeno de emergencia a los pasajeros para protegerlos de las caídas de presión en la cabina. El oxígeno se genera por descomposición a alta temperatura del clorato de sodio: [9]
- 2 NaClO 3 → 2 NaCl + 3 O 2
El calor necesario para iniciar esta reacción se genera por oxidación de una pequeña cantidad de polvo de hierro mezclado con el clorato de sodio, y la reacción consume menos oxígeno del que se produce. El peróxido de bario ( Ba O 2 ) se usa para absorber el cloro que es un producto menor en la descomposición. [10] La carga del encendedor se activa tirando de la máscara de emergencia. De manera similar, el sistema de soldadura Solidox utilizó gránulos de clorato de sodio mezclados con fibras combustibles para generar oxígeno.
Combustión sin oxígeno
El clorato de sodio se puede mezclar con azúcar de sacarosa para hacer un combustible altamente explosivo, similar al de la pólvora , que arde en espacios herméticos. Esta es la reacción:
8 NaClO 3 + C 12 H 22 O 11 → 8 NaCl + 12 CO 2 + 11 H 2 O
Sin embargo, este clorato de sodio se reemplaza principalmente por clorato de potasio . [ cita requerida ]
Toxicidad en humanos
El clorato de sodio es tóxico: "dosis de unos pocos gramos de clorato son letales". [7] El efecto oxidativo sobre la hemoglobina conduce a la formación de metahemoglobina , que es seguida por la desnaturalización de la proteína globina y una reticulación de las proteínas de la membrana de los eritrocitos con el daño resultante a las enzimas de la membrana. Esto conduce a una mayor permeabilidad de la membrana y a una hemólisis grave . La desnaturalización de la hemoglobina sobrepasa la capacidad de la vía metabólica G6PD . Además, esta enzima es directamente desnaturalizada por clorato.
Resultados de hemólisis aguda grave, con insuficiencia multiorgánica , incluida la CID e insuficiencia renal . Además, existe una toxicidad directa para el túbulo renal proximal . [11] El tratamiento consistirá en exanguinotransfusión , diálisis peritoneal o hemodiálisis . [12]
Formulaciones
El clorato de sodio viene en formulaciones en polvo , en aerosol y en gránulos . Las mezclas de cloratos y compuestos orgánicos presentan un grave riesgo de explosión [13]
Las formulaciones comercializadas contienen un retardante de fuego . La mayoría de los herbicidas con clorato disponibles en el mercado contienen aproximadamente un 53% de clorato de sodio y el resto es un depresor del fuego, como el metaborato de sodio o los fosfatos de amonio .
Nombres comerciales
El clorato de sodio es el ingrediente activo en una variedad de herbicidas comerciales. Algunos nombres comerciales de productos que contienen clorato de sodio incluyen Atlacide, Defol, De-Fol-Ate, Drop-Leaf, Fall, Harvest-Aid, Kusatol, Leafex y Tumbleaf. El compuesto se puede usar en combinación con otros herbicidas como atrazina, 2,4-D, bromacilo , diurón y metaborato de sodio.
El clorato de sodio fue un herbicida muy utilizado dentro de la UE, hasta 2009, cuando fue retirado después de una decisión tomada bajo los términos de las regulaciones de la UE. Su uso como herbicida fuera de la UE no se ve afectado, al igual que su uso en otras aplicaciones no herbicidas, como en la producción de biocidas de dióxido de cloro y para el blanqueo de pulpa y papel.
Referencias culturales
El historiador James Watson de la Universidad de Massey en Nueva Zelanda escribió un artículo ampliamente divulgado, "La importancia de los pantalones explosivos del Sr. Richard Buckley " [14] [15] sobre accidentes con clorato de sodio cuando se usó como herbicida para controlar la hierba cana en la década de 1930. [16] Esto más tarde le valió un Premio Ig Nobel en 2005, [17] y fue la base para el episodio "Exploding Pants" de mayo de 2006 de MythBusters .
Ver también
- Cloruro de sodio
Referencias
- ^ a b c d e f g h i j k http://chemister.ru/Database/properties-en.php?dbid=1&id=786
- ^ a b "Resumen de seguridad GPS del clorato de sodio" (PDF) . arkema.com . Arkema . Consultado el 25 de mayo de 2014 .
- ^ Seidell, Atherton; Linke, William F. (1952). Solubilidades de compuestos orgánicos e inorgánicos . Van Nostrand.
- ^ a b CID 516902 de PubChem
- ^ SC Abrahams, JL Bernstein (1977). "Remedición de NaClO 3 y NaBrO 3 ópticamente activos " . Acta Crystallographica . B33 (11): 3601–3604. doi : 10.1107 / S0567740877011637 .
- ^ a b c Sigma-Aldrich Co. , Clorato de sodio . Consultado el 25 de mayo de 2014.
- ^ a b c d Vogt, Helmut; Balej, Jan; Bennett, John E .; Wintzer, Peter; Jeque, Saeed Akbar; Gallone, Patrizio (2000). "Óxidos de cloro y ácidos oxigenados de cloro". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a06_483 .
- ^ "Clorato de sodio prohibido por la CE" . Semana de la horticultura . 28 de agosto de 2008.
- ^ Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Yunchang Zhang; Girish Kshirsagar y James C. Cannon (1993). "Funciones del peróxido de bario en el oxígeno químico del clorato de sodio". Ind. Eng. Chem. Res . 32 (5): 966–969. doi : 10.1021 / ie00017a028 .
- ^ Oliver J .; MacDowell M., Tracy A (1951). "La patogenia de la insuficiencia renal aguda asociada con lesiones traumáticas y tóxicas. Isquemia renal, daño nefrotóxico y el episodio isquémico 1" . J Clin Invest . 30 (12): 1307–439. doi : 10.1172 / JCI102550 . PMC 441312 . PMID 14897900 .
- ^ Emergencias toxicológicas de Goldfrank, McGraw-Hill Professional; 8a edición (28 de marzo de 2006), ISBN 978-0-07-143763-9
- ^ Beveridge, Alexander (1998). Investigación forense de explosiones . Taylor & Francis Ltd . ISBN 0-7484-0565-8.
- ^ "La importancia de los pantalones explosivos del Sr. Richard Buckley: reflexiones sobre un aspecto del cambio tecnológico en la producción lechera de Nueva Zelanda entre las guerras mundiales" Archivado el 23 de octubre de 2013 en la Wayback Machine , revista de historia agrícola
- ^ "Historias: pantalones explosivos del granjero Buckley" , New Scientist
- ^ "Los pantalones explotan , Evening Post, 21 de abril de 1933
- ^ James Watson por "La importancia de los pantalones explosivos del Sr. Richard Buckley". , improbable.com
Otras lecturas
- "Clorato de potasio. Clorato de sodio", Fiche toxicol. n ° 217 , París: Institut national de recherche et de sécurité, 2000. 4pp.
enlaces externos
| Wikimedia Commons tiene medios relacionados con clorato de sodio . |
- Tarjeta internacional de seguridad química 1117
- Cloratos
- Compuestos de sodio
- Desecantes
- Oxidantes pirotécnicos
- Agentes oxidantes