| |||
| |||
| Nombres | |||
|---|---|---|---|
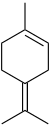
| Nombres IUPAC α: 4-Metil-1- (1-metiletil) -1,3-ciclohexadieno β: 4-Metilen-1- (1-metiletil) ciclohexeno γ: 4-Metil-1- (1-metiletil) -1,4 -ciclohexadieno δ: 1-metil-4- (propan-2-iliden) ciclohex-1-eno | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| CHEBI | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.029.440 | ||
| UNII |
| ||
| |||
| |||
| Propiedades | |||
| C 10 H 16 | |||
| Masa molar | 136,238 g · mol −1 | ||
| Densidad | α: 0,8375 g / cm 3 β: 0,838 g / cm 3 γ: 0,853 g / cm 3 | ||
| Punto de fusion | α: 60-61 ° C | ||
| Punto de ebullición | α: 173,5-174,8 ° C β: 173-174 ° C γ: 183 ° C | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
Los terpinenos son un grupo de hidrocarburos isoméricos que se clasifican como monoterpenos . Cada uno tiene la misma fórmula molecular y estructura de carbono, pero difieren en la posición de los dobles enlaces carbono-carbono. El α-terpineno se ha aislado de los aceites de cardamomo y mejorana y de otras fuentes naturales. El β-terpineno no tiene una fuente natural conocida, pero se ha preparado a partir de sabineno . Se han aislado γ-terpineno y δ-terpineno (también conocido como terpinoleno ) de una variedad de fuentes vegetales. Todos son líquidos incoloros con olor a trementina. [1]
Producción y usos [ editar ]
El α-terpineno se produce industrialmente mediante la transposición catalizada por ácido de α- pineno . Tiene propiedades perfumantes y aromatizantes, pero se utiliza principalmente para conferir un olor agradable a los fluidos industriales. La hidrogenación da el derivado saturado p -metano . [1]
Biosíntesis de α-terpineno [ editar ]
La biosíntesis de α-terpineno y otros terpenoides se produce a través de la vía del mevalonato porque su reactivo de partida, pirofosfato de dimetilalilo (DMAPP), se deriva del ácido mevalónico .
El pirofosfato de geranilo (GPP) se produce a partir de la reacción de un catión alílico estable a la resonancia, formado por la pérdida del grupo pirofosfato de DMAPP y el pirofosfato de isopentenilo (IPP), y la posterior pérdida de un protón. GPP luego pierde el grupo pirofosfato para formar el catión geranilo estable a la resonancia. La reintroducción del grupo pirofosfato en el catión produce el isómero GPP, conocido como pirofosfato de linalilo (LPP). Luego, LPP forma un catión estable a la resonancia al perder su grupo pirofosfato. La ciclación se completa gracias a esta estereoquímica más favorable del catión LPP, que ahora produce un catión terpinilo. Finalmente, un cambio de 1,2-hidruro a través de un reordenamiento de Wagner-Meerweinproduce el catión terpinen-4-ilo. Es la pérdida de un hidrógeno de este catión lo que genera α-terpineno.
Plantas que producen terpineno [ editar ]
- Cuminum cyminum [3] [4] [5]
- Melaleuca alternifolia
- Cannabis [6]
- Origanum syriacum
- Coriandrum sativum [7]
Referencias [ editar ]
- ↑ a b M. Eggersdorfer (2005). "Terpenos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a26_205 . ISBN 3527306730.Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Dewick, PM (2009). Productos medicinales naturales: un enfoque biosintético . Reino Unido: John Wiley & Sons. pp. 187 -197.
- ^ Li, Rong; Zi-Tao Jiang (2004). "Composición química del aceite esencial de Cuminum cyminum L. de China". Diario de sabores y fragancias . 19 (4): 311–313. doi : 10.1002 / ffj.1302 .
- ^ Wang, Lu; Wang, Z; Zhang, H; Li, X; Zhang, H; et al. (2009). "Extracción por nebulización ultrasónica junto con microextracción de gota única de espacio de cabeza y cromatografía de gases-espectrometría de masas para el análisis del aceite esencial en Cuminum cyminum L.". Analytica Chimica Acta . 647 (1): 72–77. doi : 10.1016 / j.aca.2009.05.030 . PMID 19576388 .
- ↑ Iacobellis, Nicola S .; Lo Cantore, P; Capasso, F; Senatore, F; et al. (2005). "Actividad antibacteriana de Cuminum cyminum L. y Carum carvi L. Aceites esenciales". Revista de Química Agrícola y Alimentaria . 53 (1): 57–61. doi : 10.1021 / jf0487351 . PMID 15631509 .
- ^ Hillig, Karl W (octubre de 2004). "Un análisis quimiotaxonómico de la variación terpenoide en el cannabis". Sistemática bioquímica y ecología . 32 (10): 875–891. doi : 10.1016 / j.bse.2004.04.004 . ISSN 0305-1978 .
- ^ Shahwar, Muhammad Khuram; El-Ghorab, Ahmed Hassan; Anjum, Faqir Muhammad; Butt, Masood Sadiq; Hussain, Shahzad; Nadeem, Muhammad (1 de julio de 2012). "Caracterización de semillas y hojas de cilantro (Coriandrum sativum L.): extractos volátiles y no volátiles" . Revista internacional de propiedades alimentarias . 15 (4): 736–747. doi : 10.1080 / 10942912.2010.500068 . ISSN 1094-2912 .