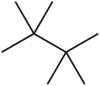
Tetrametilbutano
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido 2,2,3,3-tetrametilbutano [1] | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.008.961 |
| Número CE |
|
PubChem CID | |
| UNII | |
| un numero | 1325 |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 8 H 18 | |
| Masa molar | 114,232 g · mol −1 |
| Apariencia | Cristales cerosos, blancos y opacos |
| Olor | Inodoro |
| Punto de fusion | 98 a 104 ° C; 208 a 219 ° F; 371 hasta 377 K |
| Punto de ebullición | 106,0 a 107,0 ° C; 222,7 a 224,5 ° F; 379,1 hasta 380,1 K |
Constante de la ley de Henry ( k H ) | 2,9 nmol Pa −1 kg −1 |
| Termoquímica | |
Capacidad calorífica ( C ) | 232,2 JK −1 mol −1 (a 2,8 ° C) |
Entropía molar estándar ( S | 273,76 JK −1 mol −1 |
| −270,3 - −267,9 kJ mol −1 | |
| −5,4526 - −5,4504 MJ mol −1 | |
| Riesgos | |
| Frases R (desactualizadas) | R11 , R38 , R65 , R67 , R50 / 53 |
| Frases S (desactualizadas) | (S2) , S16 , S29 , S33 |
| punto de inflamabilidad | 4 ° C (39 ° F; 277 K) |
| Límites explosivos | 1 -?% |
| Compuestos relacionados | |
Alcanos relacionados |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El tetrametilbutano , a veces llamado hexametiletano , es un hidrocarburo de fórmula C 8 H 18 o (H 3 C-) 3 C-C (-CH 3 ) 3 . Es el más ramificado y más compacto de los muchos isómeros de octano , el único con una columna vertebral de butano (C4). Debido a su estructura altamente simétrica, tiene un punto de fusión muy alto y un rango de líquido corto; de hecho, es el hidrocarburo acíclico saturado más pequeño que aparece como un sólido a una temperatura ambiente de 25 ° C. (Entre hidrocarburos cíclicos, cubane , C 8 H 8 es aún más pequeño y también es sólido a temperatura ambiente).
El compuesto se puede obtener por reacción del reactivo de Grignard, bromuro de terc -butilmagnesio con bromuro de etilo , o de bromuro de etilmagnesio con bromuro de terc -butilo en presencia de iones manganeso ( II ). [2] Se cree que esta transformación pasa por la dimerización de dos radicales terc-butilo, que se generan por descomposición de los compuestos de organomanganeso generados in situ.
El nombre IUPAC completo del compuesto es 2,2,3,3-tetrametilbutano , pero los números son superfluos en este caso porque no hay otra disposición posible de "tetrametilbutano".
Referencias
- ^ "Hexametiletano - Resumen de compuestos" . Compuesto PubChem . EE.UU .: Centro Nacional de Información Biotecnológica. 26 de marzo de 2005. Identificación e información relacionada . Consultado el 11 de marzo de 2012 .
- ^ MS KHARASCH; JW HANCOCK; W. NUDENBERG; PO TAWNEY (1956). "Factores que influyen en el curso y mecanismo de las reacciones de Grignard. XXII. La reacción de los reactivos de Grignard con haluros de alquilo y cetonas en presencia de sales manganosas". Revista de Química Orgánica . 21 (3): 322–327. doi : 10.1021 / jo01109a016 .
- Alcanos