 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido Etano-1,2-ditiol | |
| Otros nombres Dimercaptoetano 1,2-Etanoditiol | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.007.958 |
| Número CE |
|
PubChem CID | |
| Número RTECS |
|
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 2 H 6 S 2 | |
| Masa molar | 94,19 g · mol −1 |
| Apariencia | Líquido incoloro |
| Densidad | 1,123 g / cm 3 |
| Punto de fusion | −41 ° C (−42 ° F; 232 K) |
| Punto de ebullición | 146 ° C (295 ° F; 419 K) 46 mmHg |
| Ligeramente sol | |
| Solubilidad en otros disolventes. | Buena solubilidad en la mayoría de disolventes orgánicos. |
| Acidez (p K a ) | ≈11 |
Índice de refracción ( n D ) | 1.5589 (línea D, 25 ° C) |
| Riesgos | |
| Pictogramas GHS |    |
| Palabra de señal GHS | Peligro |
| H226 , H301 , H302 , H310 , H312 , H319 , H330 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P262 , P264 , P270 , P271 , P280 , P284 , P301 + 310 , P301 + 312 , P302 + 350 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P310 , P312 , P320 , P321 , P322 | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | 50 ° C (122 ° F; 323 K) |
| Compuestos relacionados | |
Tioles relacionados | 1,1-etanoditiol ; Etanetiol ; 1,3-propanoditiol ; 1,2-bencenoditiol ; Tiofenol |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
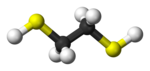
El etano-1,2-ditiol , también conocido como EDT , [1] es un líquido incoloro con la fórmula C 2 H 4 ( SH ) 2 . Tiene un olor muy característico que muchas personas comparan con el repollo podrido . Es un bloque de construcción común en la síntesis orgánica y un excelente ligando para los iones metálicos.
Preparación
El etano-1,2-ditiol se fabrica comercialmente mediante la reacción de 1,2-dicloroetano con bisulfuro de sodio acuoso . En el laboratorio, también se puede preparar mediante la acción del 1,2-dibromoetano sobre la tiourea seguida de hidrólisis . [2]
Aplicaciones
Como 1,2- ditiol , este compuesto se usa ampliamente en química orgánica porque reacciona con aldehídos y cetonas para dar 1,3- ditiolanos , que son intermedios útiles.[3]
- C 2 H 4 (SH) 2 + RR'CO → C 2 H 4 S 2 CRR '+ H 2 O

Otros 1,2- y 1,3-ditioles experimentan esta reacción para dar 1,3-ditiolanos y 1,3-ditianos relacionados (anillos de seis miembros). Los dioles como el etilenglicol experimentan reacciones análogas a los 1,3- dioxolanos y 1,3- dioxanos . Una característica distintiva de los ditiolanos y ditianos derivados de aldehídos es que el grupo metino puede desprotonarse y alquilarse el carbanión resultante.
El 1,2-etanoditiol se usa comúnmente como eliminador en la síntesis de escisión de péptidos.
Ver también
- Etano-1,1-ditiol
Referencias
- ^ Choi, H .; Aldrich, Jv (1 de julio de 1993). "Comparación de métodos para la síntesis en fase sólida de Fmoc y escisión de un péptido que contiene tanto triptófano como arginina". Revista Internacional de Investigación de Péptidos y Proteínas . 42 (1): 58–63. doi : 10.1111 / j.1399-3011.1993.tb00350.x . ISSN 1399-3011 . PMID 8103765 .
- ↑ Speziale, AJ (1963). "Etanoditiol" . Síntesis orgánicas .; Volumen colectivo , 4 , p. 401
- ^ RE Conrow "Etanoditiol" en Enciclopedia de reactivos para síntesis orgánica (Ed: L. Paquette) 2004, J. Wiley & Sons, Nueva York. doi : 10.1002 / 047084289X
