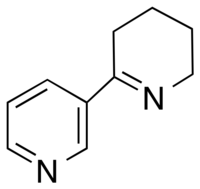
Anabaseine
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido 3,4,5,6-tetrahidro-2,3′-bipiridina | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| ChemSpider | |
| KEGG | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 10 H 12 N 2 | |
| Masa molar | 160,220 g · mol −1 |
| Apariencia | Petróleo |
| Olor | Inodoro |
| Punto de ebullición | 110-120 ℃ |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
La anabaseína (3,4,5,6-tetrahidro-2,3′-bipiridina) es una toxina alcaloide producida por las hormigas Nemertinas y Aphaenogaster . [1] Es estructuralmente similar a la nicotina y la anabasina . [2] De manera similar, se ha demostrado que actúa como agonista en la mayoría de los receptores nicotínicos de acetilcolina en el sistema nervioso central y el sistema nervioso periférico . [2]
Mecanismo de acción
El iminio forma de Se liga anabaseına a la mayoría de receptores de la acetilcolina nicotínicos , tanto en el sistema nervioso periférico y el sistema nervioso central . Sin embargo, existe una mayor afinidad de unión por los receptores en el cerebro con una subunidad α7, así como por los receptores del músculo esquelético. [3] La unión provoca la despolarización de las neuronas e induce la liberación de dopamina y noradrenalina . [2]
Efectos biologicos
La anabaseína causa parálisis en crustáceos e insectos , pero no en vertebrados , presumiblemente al actuar como agonista de los receptores de acetilcolina nicotínicos neuromusculares periféricos. [2]
Estructura
La molécula de anabaseína consiste en un anillo de tetrahidropiridina no aromático conectado al 3er carbono de un anillo 3- piridilo . Puede existir en tres formas a pH fisiológico: una estructura de cetona , imina o iminio . [2] Debido a la conjugación entre la imina y el anillo 3-piridilo, la anabaseína existe como una molécula casi coplanar.
Síntesis
Spath y Mamoli sintetizaron anabaseína por primera vez en 1936. [4] Los investigadores hicieron reaccionar el anhídrido benzoico con δ- valerolactama para producir N -benzoilpiperidona. Luego, se hace reaccionar N -benzoilpiperidona con éster etílico del ácido nicotínico para producir α-nicotinoil- N -benzoil-2-piperidona. Este producto luego se descarboxila , se somete a un cierre de anillo e hidrólisis de amida para formar anabaseína.
Desde entonces, Bloom, [5] Zoltewicz, [6] Smith, [7] y Villemin han desarrollado estrategias sintéticas adicionales . [8]
Derivados
Debido a la unión bastante inespecífica de la anabaseína a los receptores nicotínicos de acetilcolina, la molécula se descartó en gran medida como una herramienta útil en la investigación o la medicina. Sin embargo, se han identificado derivados de anabaseína con un perfil de unión de α7 más selectivo. Uno de tales derivados ( GTS-21 , 3- (2,4-dimetoxibenciliden) -anabaseína) se ha estudiado como candidato a fármaco para los déficits cognitivos y de memoria, particularmente asociados con la esquizofrenia ; se ha estudiado en ensayos clínicos de fase II sin progresión a la fase III. [9] Además, la modificación del núcleo de piridina anabaseína condujo a la obtención de nuevos derivados dotados de unión y selectividad funcional para el subtipo de receptor nicotínico de acetilcolina α3β4.[10]
Referencias
- ^ Wheeler, JW; Olubajo, O; Storm, CB; Duffield, RM (6 de marzo de 1981). "Anabaseine: alcaloide del veneno de las hormigas aphaenogaster". Ciencia . 211 (4486): 1051–2. doi : 10.1126 / science.211.4486.1051 . PMID 17744933 .
- ^ a b c d e Kem, William; Soti, Ferenc; Wildeboer, Kristin; LeFrancois, Susan; MacDougall, Kelly; Wei, Dong-Qing; Chou, Kuo-Chen; Arias, Hugo R. (6 de abril de 2006). "La anabaseína de la toxina nemertina y su derivado DMXBA (GTS-21): propiedades químicas y farmacológicas" . Drogas marinas . 4 (3): 255-273. doi : 10.3390 / md403255 . PMC 3663414 .
- ^ Kem, WR; Mahnir, VM; Papke, RL; Lingle, CJ (diciembre de 1997). "La anabaseína es un potente agonista de los receptores nicotínicos sensibles a la alfa-bungarotoxina muscular y neuronal". La Revista de Farmacología y Terapéutica Experimental . 283 (3): 979–92. PMID 9399967 .
- ^ Padilla, editado por Dean F. Martin [y] George M. (1973). Farmacognosia marina; acción de las biotoxinas marinas a nivel celular (Primera ed.). Nueva York: Academic Press. págs. 54–55 . ISBN 978-0124745506.CS1 maint: texto adicional: lista de autores ( enlace )
- ^ Bloom, Linda. "Influencia del disolvente en el equilibrio de hidrólisis de la cadena de anillo de anabaseína y síntesis de análogos de anabaseína y nicotina" . Universidad de Florida . Consultado el 5 de mayo de 2015 .
- ^ Zoltewicz, John A .; Cruskie, Michael P. (agosto de 1995). "Una síntesis superior de anabaseína colinérgica". Preparaciones y Procedimientos Orgánicos Internacional . 27 (4): 510–513. doi : 10.1080 / 00304949509458490 .
- ^ Smith, Aaron. "Síntesis y radiomarcaje de derivados de trifluoroborato de potasio bencilideno anabaseína". Universidad de Tennessee - Knoxville. Cite journal requiere
|journal=( ayuda ) - ^ Villemin, Didier; Hachemi, Messaoud (2001). "Fluoruro de cesio sobre óxido de calcio como catalizador fuertemente básico. Síntesis de flavonas y alcaloides del tabaco". Cinética de reacción y letras de catálisis . 72 (1): 3–10. doi : 10.1023 / A: 1010597826749 .
- ^ Celanire, Sylvain; Poli, Sonia (13 de octubre de 2014). Terapéutica de moléculas pequeñas para la esquizofrenia . Saltador. pag. 248. ISBN 9783319115023. Consultado el 20 de abril de 2015 .
- ^ Matera, Carlo; Quadri, Marta; Sciaccaluga, Miriam; Pomè, Diego Yuri; Fasoli, Francesca; De Amici, Marco; Fucile, Sergio; Gotti, Cecilia; Dallanoce, Clelia (27 de enero de 2016). "La modificación del núcleo de piridina anabaseína permite lograr la unión y selectividad funcional para el subtipo de receptor nicotínico de acetilcolina α3β4". Revista europea de química medicinal . 108 : 392–405. doi : 10.1016 / j.ejmech.2015.11.045 . PMID 26706350 .
- Neurofarmacología
- Agonistas nicotínicos
- Alcaloides de piridina
- Descubrimiento de medicamento