| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Ácido benzoico [1] | |||
| Nombre IUPAC sistemático Ácido bencenocarboxílico | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| 3DMet | |||
| 636131 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA | 100.000.562 | ||
| Número CE |
| ||
| Número e | E210 (conservantes) | ||
| 2946 | |||
| KEGG | |||
| Malla | ácido benzoico | ||
PubChem CID | |||
| Número RTECS |
| ||
| UNII | |||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 7 H 6 O 2 | |||
| Masa molar | 122,123 g · mol −1 | ||
| Apariencia | Sólido cristalino incoloro | ||
| Olor | Olor leve y agradable | ||
| Densidad | 1.2659 g / cm 3 (15 ° C) 1.0749 g / cm 3 (130 ° C) [2] | ||
| Punto de fusion | 122 ° C (252 ° F; 395 K) [7] | ||
| Punto de ebullición | 250 ° C (482 ° F; 523 K) [7] | ||
solubilidad en agua | 1,7 g / L (0 ° C) 2,7 g / L (18 ° C) 3,44 g / L (25 ° C) 5,51 g / L (40 ° C) 21,45 g / L (75 ° C) 56,31 g / L ( 100 ° C) [2] [3] | ||
| Solubilidad | soluble en acetona , benceno , CCl 4 , CHCl 3 , alcohol , éter etílico , hexano , fenilos , amoníaco líquido , acetatos | ||
| Solubilidad en metanol | 30 g / 100 g (-18 ° C) 32,1 g / 100 g (-13 ° C) 71,5 g / 100 g (23 ° C) [2] | ||
| Solubilidad en etanol | 25,4 g / 100 g (-18 ° C) 47,1 g / 100 g (15 ° C) 52,4 g / 100 g (19,2 ° C) 55,9 g / 100 g (23 ° C) [2] | ||
| Solubilidad en acetona | 54,2 g / 100 g (20 ° C) [2] | ||
| Solubilidad en aceite de oliva | 4,22 g / 100 g (25 ° C) [2] | ||
| Solubilidad en 1,4-dioxano | 55,3 g / 100 g (25 ° C) [2] | ||
| log P | 1,87 | ||
| Presión de vapor | 0,16 Pa (25 ° C) 0,19 kPa (100 ° C) 22,6 kPa (200 ° C) [4] | ||
| Acidez (p K a ) |
| ||
Susceptibilidad magnética (χ) | -70,28 · 10 −6 cm 3 / mol | ||
Índice de refracción ( n D ) | 1.5397 (20 ° C) 1.504 (132 ° C) [2] | ||
| Viscosidad | 1,26 mPa (130 ° C) | ||
| Estructura | |||
Estructura cristalina | Monoclínico | ||
Forma molecular | planar | ||
Momento bipolar | 1,72 D en dioxano | ||
| Termoquímica | |||
Capacidad calorífica ( C ) | 146,7 J / mol · K [4] | ||
Entropía molar estándar ( S | 167,6 J / mol · K [2] | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | -385,2 kJ / mol [2] | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | -3228 kJ / mol [4] | ||
| Peligros | |||
| Principales peligros | Irritante | ||
| Ficha de datos de seguridad | JT Baker | ||
| Pictogramas GHS | [8] | ||
| Palabra de señal GHS | Peligro | ||
Declaraciones de peligro GHS | H318 , H335 [8] | ||
Consejos de prudencia del SGA | P261 , P280 , P305 + 351 + 338 [8] | ||
| NFPA 704 (diamante de fuego) |  2 1 0 | ||
| punto de inflamabilidad | 121,5 ° C (250,7 ° F; 394,6 K) [7] | ||
autoignición temperatura | 571 ° C (1060 ° F; 844 K) [7] | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis mediana ) | 1700 mg / kg (rata, oral) | ||
| Compuestos relacionados | |||
Ácidos carboxílicos relacionados | Ácidos hidroxibenzoicos Ácidos aminobenzoicos , Ácidos nitrobenzoicos , Ácido fenilacético | ||
Compuestos relacionados | Benzaldehído , alcohol bencílico , cloruro de benzoílo , bencilamina , benzamida | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
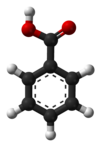
El ácido benzoico / b ɛ n z oʊ . ɪ k / es un sólido blanco (o incoloro) con la fórmula C 6 H 5 CO 2 H. Es el ácido carboxílico aromático más simple . El nombre se deriva de la goma de mascar benjuí , que fue durante mucho tiempo su única fuente. El ácido benzoico se encuentra naturalmente en muchas plantas [9] y sirve como intermediario en la biosíntesis de muchos metabolitos secundarios . Salesde ácido benzoico se utilizan como conservantes de alimentos. El ácido benzoico es un precursor importante para la síntesis industrial de muchas otras sustancias orgánicas. Las sales y ésteres de ácido benzoico son conocidos como benzoatos / b ɛ n z oʊ . eɪ t / .
Historia [ editar ]
El ácido benzoico se descubrió en el siglo XVI. La destilación en seco de goma benjuí fue descrita por primera vez por Nostradamus (1556), y luego por Alexius Pedemontanus (1560) y Blaise de Vigenère (1596). [10]
Justus von Liebig y Friedrich Wöhler determinaron la composición del ácido benzoico. [11] Estos últimos también investigaron cómo se relaciona el ácido hipúrico con el ácido benzoico.
En 1875, Salkowski descubrió las capacidades antifúngicas del ácido benzoico, que se utilizó durante mucho tiempo en la conservación de frutos de mora azul que contienen benzoato . [12]
Producción [ editar ]
Preparaciones industriales [ editar ]
El ácido benzoico se produce comercialmente por oxidación parcial del tolueno con oxígeno . El proceso es catalizado por naftenatos de cobalto o manganeso . El proceso utiliza abundantes materiales y tiene un alto rendimiento. [13]
El primer proceso industrial implicó la reacción de benzotricloruro (triclorometilbenceno) con hidróxido de calcio en agua, utilizando hierro o sales de hierro como catalizador . El benzoato de calcio resultante se convierte en ácido benzoico con ácido clorhídrico . El producto contiene cantidades significativas de derivados clorados del ácido benzoico. Por este motivo, el ácido benzoico para consumo humano se obtuvo mediante destilación en seco de goma de benjuí. El ácido benzoico de grado alimenticio ahora se produce sintéticamente.
Síntesis de laboratorio [ editar ]
El ácido benzoico es barato y fácilmente disponible, por lo que la síntesis de laboratorio de ácido benzoico se practica principalmente por su valor pedagógico. Es una preparación universitaria común.
El ácido benzoico se puede purificar mediante recristalización en agua debido a su alta solubilidad en agua caliente y escasa solubilidad en agua fría. La evitación de disolventes orgánicos para la recristalización hace que este experimento sea particularmente seguro. Este proceso suele dar un rendimiento de alrededor del 65% [14].
Por hidrólisis [ editar ]
Como otros nitrilos y amidas , el benzonitrilo y la benzamida se pueden hidrolizar a ácido benzoico o su base conjugada en condiciones ácidas o básicas.
De reactivo de Grignard [ editar ]
El bromobenceno se puede convertir en ácido benzoico mediante "carboxilación" del bromuro de fenilmagnesio intermedio . [15] Esta síntesis ofrece un ejercicio conveniente para que los estudiantes lleven a cabo una reacción de Grignard , una clase importante de reacción de formación de enlaces carbono-carbono en química orgánica. [16] [17] [18] [19] [20]
Oxidación de compuestos bencílicos [ editar ]
El alcohol bencílico [21] [22] y el cloruro de bencilo y prácticamente todos los derivados de bencilo se oxidan fácilmente a ácido benzoico.
Usos [ editar ]
El ácido benzoico se consume principalmente en la producción de fenol por descarboxilación oxidativa a 300-400 ° C: [23]
- C 6 H 5 CO 2 H + 1/2O 2 → C 6 H 5 OH + CO 2
La temperatura requerida se puede reducir a 200 ° C mediante la adición de cantidades catalíticas de sales de cobre (II). El fenol se puede convertir en ciclohexanol , que es un material de partida para la síntesis de nailon .
Precursor de plastificantes [ editar ]
Los plastificantes de benzoato , tales como los ésteres de glicol, dietilenglicol y trietilenglicol, se obtienen por transesterificación de benzoato de metilo con el diol correspondiente . [23] Estos plastificantes, que se utilizan de manera similar a los derivados del éster del ácido tereftálico , representan alternativas a los ftalatos . [23]
[ editar ]
El ácido benzoico y sus sales se utilizan como conservantes de alimentos , representados por los números E E210 , E211 , E212 y E213 . El ácido benzoico inhibe el crecimiento de moho , levadura [24] y algunas bacterias . Se agrega directamente o se crea a partir de reacciones con su sal de sodio , potasio o calcio . El mecanismo comienza con la absorción de ácido benzoico en la célula. Si el pH intracelular cambia a 5 o menos, la fermentación anaeróbica de glucosa a través dela fosfofructoquinasa se reduce en un 95%. La eficacia del ácido benzoico y el benzoato depende, por tanto, del pH del alimento. [25] Los alimentos y bebidas ácidos como jugos de frutas ( ácido cítrico ), bebidas gaseosas ( dióxido de carbono ), refrescos ( ácido fosfórico ), encurtidos ( vinagre ) u otros alimentos acidificados se conservan con ácido benzoico y benzoatos.
Los niveles típicos de uso del ácido benzoico como conservante en los alimentos se encuentran entre el 0,05 y el 0,1%. Los alimentos en los que se puede utilizar ácido benzoico y los niveles máximos para su aplicación están controlados por las leyes alimentarias locales. [26] [27]
Se ha expresado la preocupación de que el ácido benzoico y sus sales puedan reaccionar con el ácido ascórbico (vitamina C) en algunos refrescos, formando pequeñas cantidades de benceno cancerígeno . [28]
Medicinal [ editar ]
El ácido benzoico es un componente de la pomada de Whitfield que se utiliza para el tratamiento de enfermedades cutáneas fúngicas como la tiña , la tiña y el pie de atleta . [29] [30] Como componente principal de la goma de benjuí , el ácido benzoico es también un ingrediente importante tanto en la tintura de benjuí como en el bálsamo de fraile. Estos productos tienen una larga historia de uso como antisépticos tópicos y descongestionantes inhalantes .
El ácido benzoico se utilizó como expectorante , analgésico y antiséptico a principios del siglo XX. [31]
Usos de nicho y laboratorio [ editar ]
En los laboratorios de enseñanza, el ácido benzoico es un estándar común para calibrar un calorímetro de bomba . [32]
Efectos sobre la biología y la salud [ editar ]
El ácido benzoico se encuentra de forma natural, al igual que sus ésteres en muchas especies de plantas y animales. Se encuentran cantidades apreciables en la mayoría de las bayas (alrededor del 0,05%). Los frutos maduros de varias especies de Vaccinium (p. Ej., Arándano , V. vitis macrocarpon ; arándano , V. myrtillus ) contienen entre 0,03 y 0,13% de ácido benzoico libre. El ácido benzoico también se forma en las manzanas después de la infección con el hongo Nectria galligena . Entre los animales, el ácido benzoico se ha identificado principalmente en especies omnívoras o fitófagas, por ejemplo, en las vísceras y músculos de la perdiz blanca ( Lagopus muta ), así como en las secreciones de las glándulas de los machos de buey almizclero.( Ovibos moschatus ) o elefantes toro asiáticos ( Elephas maximus ). [33] La goma benjuí contiene hasta un 20% de ácido benzoico y un 40% de ésteres de ácido benzoico. [34]
En cuanto a su biosíntesis, el benzoato se produce en las plantas a partir del ácido cinámico. [35] Se ha identificado una vía a partir del fenol a través del 4-hidroxibenzoato . [36]
Reacciones [ editar ]
Las reacciones del ácido benzoico pueden ocurrir en el anillo aromático o en el grupo carboxilo .
Anillo aromático [ editar ]
La reacción de sustitución aromática electrófila tendrá lugar principalmente en la posición 3 debido al grupo carboxílico captador de electrones ; es decir benzoico ácido es meta de dirección . [37]
Grupo carboxilo [ editar ]
Las reacciones típicas de los ácidos carboxílicos se aplican también al ácido benzoico. [23]
- Los ésteres de benzoato son el producto de la reacción catalizada por ácido con alcoholes .
- Las amidas del ácido benzoico se preparan habitualmente a partir de cloruro de benzoílo .
- La deshidratación a anhídrido benzoico se induce con anhídrido acético o pentóxido de fósforo .
- Los derivados de ácidos altamente reactivos, como los haluros de ácido, se obtienen fácilmente mezclando con agentes de halogenación como cloruros de fósforo o cloruro de tionilo .
- Los ortoésteres se pueden obtener mediante la reacción de alcoholes en condiciones ácidas sin agua con benzonitrilo .
- La reducción a benzaldehído y alcohol bencílico es posible usando DIBAL-H , LiAlH 4 o borohidruro de sodio .
- La descarboxilación a benceno se puede efectuar calentando en quinolina en presencia de sales de cobre. La descarboxilación de Hunsdiecker se puede lograr calentando la sal de plata.
Seguridad y metabolismo de los mamíferos [ editar ]
Se excreta como ácido hipúrico . [38] El ácido benzoico es metabolizado por butirato-CoA ligasa en un producto intermedio, benzoil-CoA , [39] que luego es metabolizado por glicina N- aciltransferasa en ácido hipúrico. [40] Los seres humanos metabolizan el tolueno y el ácido benzoico que se excreta como ácido hipúrico . [41]
Para los seres humanos, la Organización Mundial de la Salud 's Programa Internacional de Seguridad Química (IPCS) sugiere una ingesta tolerable provisional sería de 5 mg / kg de peso corporal por día. [33] Los gatos tienen una tolerancia significativamente menor contra el ácido benzoico y sus sales que las ratas y los ratones . La dosis letal para gatos puede ser tan baja como 300 mg / kg de peso corporal. [42] La vía oral LD 50 para ratas es 3040 mg / kg, para los ratones es 1940 a 2263 mg / kg. [33]
En Taipei , Taiwán, una encuesta de salud de la ciudad en 2010 encontró que el 30% de los productos alimenticios secos y en escabeche tenían ácido benzoico. [43]
Referencias [ editar ]
- ^ Nomenclatura de la química orgánica: Recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: La Real Sociedad de Química . 2014. p. 745. doi : 10.1039 / 9781849733069-00648 . ISBN 978-0-85404-182-4.
- ^ a b c d e f g h i j "ácido benzoico" . chemister.ru . Consultado el 24 de octubre de 2018 .
- ^ Seidell, Atherton; Linke, William F. (1952). Solubilidades de compuestos orgánicos e inorgánicos . Van Nostrand.
- ^ a b c Ácido benzoico en Linstrom, Peter J .; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69 , National Institute of Standards and Technology, Gaithersburg (MD), http://webbook.nist.gov (consultado el 23 de mayo de 2014)
- ^ Harris, Daniel (2010). Análisis químico cuantitativo (8 ed.). Nueva York: WH Freeman and Company. págs. AP12. ISBN 9781429254366.
- ^ Olmstead, William N .; Bordwell, Frederick G. (1980). "Constantes de asociación de pares de iones en dimetilsulfóxido". La Revista de Química Orgánica . 45 (16): 3299–3305. doi : 10.1021 / jo01304a033 .
- ^ a b c d Registro en la base de datos de sustancias GESTIS del Instituto de seguridad y salud ocupacional
- ^ a b c Sigma-Aldrich Co. , ácido benzoico . Consultado el 23 de mayo de 2014.
- ^ "Los científicos descubren los últimos pasos para la creación de ácido benzoico en las plantas" . Noticias de agricultura de Purdue.
- ^ Neumüller OA (1988). Römpps Chemie-Lexikon (6 ed.). Stuttgart: Frankh'sche Verlagshandlung. ISBN 978-3-440-04516-9. OCLC 50969944 .
- ^ Liebig J ; Wöhler F (1832). "Untersuchungen über das Radikal der Benzoesäure". Annalen der Chemie . 3 (3): 249-282. doi : 10.1002 / jlac.18320030302 . hdl : 2027 / hvd.hxdg3f .
- ↑ Salkowski E (1875). Berl Klin Wochenschr . 12 : 297-298. Falta o vacío
|title=( ayuda ) - ^ Wade, Leroy G. (2014). Química orgánica (nueva edición internacional de Pearson). Harlow: Pearson Education Limited. pag. 985. ISBN 978-1-292-02165-2.
- ^ DD Perrin; WLF Armarego (1988). Purificación de productos químicos de laboratorio (3ª ed.). Pergamon Press. pp. 94 . ISBN 978-0-08-034715-8.
- ^ Donald L. Pavia (2004). Introducción a las técnicas orgánicas de laboratorio: un enfoque a pequeña escala . Thomson Brooks / Cole. págs. 312–314. ISBN 978-0-534-40833-6.
- ^ Shirley, DA (1954). "La síntesis de cetonas a partir de haluros de ácido y compuestos organometálicos de magnesio, zinc y cadmio". Org. Reaccionar. 8 : 28–58.
- ^ Huryn, DM (1991). "Carbaniones de cationes alcalinos y alcalinotérreos: (ii) selectividad de reacciones de adición de carbonilo". En Trost, BM ; Fleming, I. (eds.). Síntesis orgánica integral, Volumen 1: Adiciones a los enlaces C — X π, Parte 1 . Ciencia de Elsevier . págs. 49–75. doi : 10.1016 / B978-0-08-052349-1.00002-0 . ISBN 978-0-08-052349-1.
- ^ "La reacción de Grignard. Preparación de ácido benzoico" (PDF) . Colegio Comunitario de Portland. Archivado desde el original (PDF) el 26 de febrero de 2015 . Consultado el 12 de marzo de 2015 . >
- ^ "Experimento 9: síntesis de ácido benzoico mediante carbonilación de un reactivo de Grignard" (PDF) . Universidad de Wisconsin-Madison. Archivado desde el original (PDF) el 23 de septiembre de 2015 . Consultado el 12 de marzo de 2015 .
- ^ "Experimento 3: preparación de ácido benzoico" (PDF) . Universidad de Towson. Archivado desde el original (PDF) el 13 de abril de 2015 . Consultado el 12 de marzo de 2015 . >
- ^ Amakawa, Kazuhiko; Kolen'Ko, Yury V .; Villa, Alberto; Schuster, Manfred E /; Csepei, Lénárd-István; Weinberg, Gisela; Wrabetz, Sabine; Naumann d'Alnoncourt, Raoul; Girgsdies, Frank; Prati, Laura; Schlögl, Robert; Trunschke, Annette (2013). "Multifuncionalidad de catalizadores de óxido cristalino MoV (TeNb) M1 en oxidación selectiva de propano y alcohol bencílico" . Catálisis ACS . 3 (6): 1103-1113. doi : 10.1021 / cs400010q .
- ↑ Santonastaso, Marco; Freakley, Simon J .; Miedziak, Peter J .; Brett, Gemma L .; Edwards, Jennifer K .; Hutchings, Graham J. (21 de noviembre de 2014). "Oxidación de alcohol bencílico usando peróxido de hidrógeno generado in situ". Investigación y desarrollo de procesos orgánicos . 18 (11): 1455-1460. doi : 10.1021 / op500195e . ISSN 1083-6160 .
- ^ a b c d Maki, Takao; Takeda, Kazuo (2000). Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a03_555 ..
- ^ AD Warth (1 de diciembre de 1991). "Mecanismo de acción del ácido benzoico sobre Zygosaccharomyces bailii: efectos sobre los niveles de metabolitos glucolíticos, producción de energía y pH intracelular" . Appl Environ Microbiol . 57 (12): 3410–4. doi : 10.1128 / AEM.57.12.3410-3414.1991 . PMC 183988 . PMID 1785916 .
- ^ Pastrorova I, de Koster CG, Boom JJ (1997). "Estudio analítico de ácidos benzoicos y cinámicos libres y unidos a éster de resinas de goma benjuí por GC-MS HPLC-frit FAB-MS". Phytochem Anal . 8 (2): 63–73. doi : 10.1002 / (SICI) 1099-1565 (199703) 8: 2 <63 :: AID-PCA337> 3.0.CO; 2-Y .
- ^ Detalles del grupo de aditivos alimentarios en línea de la GSFA: benzoatos (2006) Archivado el 26 de septiembre de 2007 en la Wayback Machine.
- ^ DIRECTIVA DEL PARLAMENTO EUROPEO Y DEL CONSEJO No 95/2 / CE de 20 de febrero de 1995 sobre aditivos alimentarios distintos de los colorantes y edulcorantes (las versiones de Consleg no contienen los últimos cambios en una ley) Archivado el 19 de abril de 2003 en la Wayback Machine.
- ^ Indicaciones del artículo de BfR sobre la posible formación de benceno a partir del ácido benzoico en los alimentos , Opinión de experto de BfR No. 013/2006, 1 de diciembre de 2005
- ^ "Ungüento de Whitfield" . Archivado desde el original el 9 de octubre de 2007 . Consultado el 15 de octubre de 2007 .
- ^ Charles Owens Wilson; Ole Gisvold; John H. Block (2004). Wilson y Gisvold's Textbook of Organic Medicinal and Pharmaceutical . Lippincott Williams y Wilkins. págs. 234 . ISBN 978-0-7817-3481-3.
- ^ Lillard, Benjamin (1919). "Trochas de ácido benzoico" . Práctica de boticario y revisión farmacéutica de revisiones .
- ^ Experimento 2: Uso de calorimetría de bomba para determinar la energía de resonancia del benceno Archivado el 9 de marzo de 2012 en la Wayback Machine.
- ^ a b c "Documento de evaluación química internacional conciso 26: ÁCIDO BENZOICO Y BENZOATO DE SODIO" .
- ^ Tomokuni K, Ogata M (1972). "Determinación colorimétrica directa de ácido hipúrico en orina". Clin Chem . 18 (4): 349–351. doi : 10.1093 / clinchem / 18.4.349 . PMID 5012256 .
- ^ Vogt, T. (2010). "Biosíntesis de fenilpropanoides". Planta molecular . 3 : 2-20. doi : 10.1093 / mp / ssp106 . PMID 20035037 .
- ^ Juteau, Pierre; Valérie Côté; Marie-France Duckett; Réjean Beaudet; François Lépine; Richard Villemur; Jean-Guy Bisaillon (enero de 2005). "Cryptanaerobacter phenolicus gen. Nov., Sp. Nov., Un anaerobio que transforma el fenol en benzoato a través de 4-hidroxibenzoato" . Revista Internacional de Microbiología Sistemática y Evolutiva . 55 (1): 245–250. doi : 10.1099 / ijs.0.02914-0 . PMID 15653882 .
- ^ Brewster, RQ; Williams, B .; Phillips, R. (1955). "Ácido 3,5-dinitrobenzoico" . Síntesis orgánicas .; Volumen colectivo , 3 , p. 337
- ^ Panel de expertos de revisión de ingredientes cosméticos Bindu Nair (2001). "Informe final sobre la evaluación de la seguridad del alcohol bencílico, el ácido benzoico y el benzoato de sodio". Int J Tox . 20 (Suplemento 3): 23–50. doi : 10.1080 / 10915810152630729 . PMID 11766131 . S2CID 13639993 .
- ^ "Ligasa butirato-CoA" . BRENDA . Technische Universität Braunschweig . Consultado el 7 de mayo de 2014 . Sustrato / Producto
- ^ "glicina N-aciltransferasa" . BRENDA . Technische Universität Braunschweig . Consultado el 7 de mayo de 2014 . Sustrato / Producto
- ^ Krebs HA, Wiggins D, Stubbs M (1983). "Estudios sobre el mecanismo de acción antifúngica del benzoato" . Biochem J . 214 (3): 657–663. doi : 10.1042 / bj2140657 . PMC 1152300 . PMID 6226283 .
- ^ Bedford PG, Clarke EG (1972). "Intoxicación experimental con ácido benzoico en el gato". Vet Rec . 90 (3): 53–58. doi : 10.1136 / vr.90.3.53 . PMID 4672555 . S2CID 2553612 .
- ^ Chen, Jian; YL Kao (18 de enero de 2010). "Casi el 30% de los alimentos secos y en escabeche no pasan las inspecciones de seguridad" . The China Post .
Enlaces externos [ editar ]
| Wikimedia Commons tiene medios relacionados con el ácido benzoico . |
- Tarjeta internacional de seguridad química 0103
- Informe de evaluación inicial de los pequeños Estados insulares en desarrollo para el ácido benzoico de la Organización para la Cooperación y el Desarrollo Económicos (OCDE)
- ChemicalLand