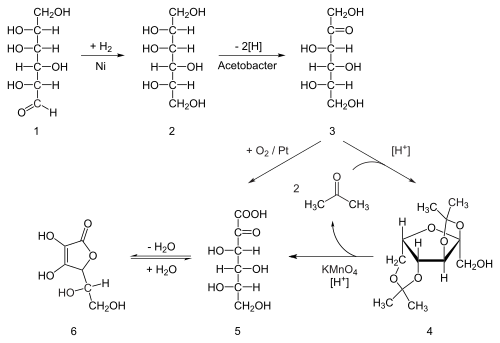
Química del ácido ascórbico
El ácido ascórbico es un compuesto orgánico de fórmula C
6H
8O
6, originalmente llamado ácido hexurónico . Es un sólido blanco, pero las muestras impuras pueden aparecer amarillentas. Se disuelve bien en agua para dar soluciones ligeramente ácidas. Es un agente reductor suave .
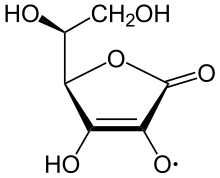
El ácido ascórbico existe como dos enantiómeros ( isómeros de imagen especular ), comúnmente denominados " l " (para "levo") y " d " (para "dextro"). El isómero l es el que se encuentra con más frecuencia: se encuentra naturalmente en muchos alimentos y es una forma (" vitamer ") de vitamina C , un nutriente esencial para los seres humanos y muchos animales. La deficiencia de vitamina C provoca el escorbuto , que anteriormente era una de las principales enfermedades de los marineros en los viajes largos por mar. Se utiliza como aditivo alimentario y complemento dietético por sus propiedades antioxidantes . La forma " d " se puede hacer a través desíntesis química pero no tiene un papel biológico significativo.
Las propiedades antiescorbúticas de ciertos alimentos fueron demostradas en el siglo XVIII por James Lind . En 1907, Axel Holst y Theodor Frølich descubrieron que el factor antiescorbútico era una sustancia química soluble en agua, distinta de la que impedía el beriberi . Entre 1928 y 1932, Albert Szent-Györgyi aisló un candidato para esta sustancia, a la que llamó "ácido hexurónico", primero de plantas y luego de glándulas suprarrenales de animales. En 1932, Charles Glen King confirmó que efectivamente se trataba del factor antiescorbútico.
En 1933, el químico del azúcar Walter Norman Haworth , trabajando con muestras de "ácido hexurónico" que Szent-Györgyi había aislado del pimentón y le envió el año anterior, dedujo la estructura correcta y la naturaleza óptico-isomérica del compuesto, y en 1934 informó su primera síntesis. [2] [3] En referencia a las propiedades antiescorbúticas del compuesto, Haworth y Szent-Györgyi propusieron cambiarle el nombre a "ácido a-escórbico" para el compuesto, y más tarde específicamente ácido l -ascórbico. [4] Debido a su trabajo, en 1937 los premios Nobel de química y medicina fueron otorgados a Haworth y Szent-Györgyi, respectivamente.
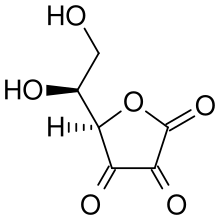
El ácido ascórbico es un ácido vinílogo y forma el anión ascorbato cuando se desprotona en uno de los hidroxilos. Esta propiedad es característica de las reductonas : enodioles con un grupo carbonilo adyacente al grupo enodiol, es decir, con el grupo –C (OH) = C (OH) –C (= O) -. El anión ascorbato se estabiliza mediante la deslocalización electrónica que resulta de la resonancia entre dos formas:
Por esta razón, el ácido ascórbico es mucho más ácido de lo que cabría esperar si el compuesto solo contuviera grupos hidroxilo aislados.