Metilprednisolona
 | |
 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Medrol, Depo-Medrol (como acetato ), Solu-Medrol (como succinato ), otros |
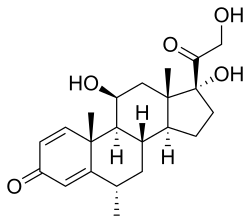
| Otros nombres | 6α-metilprednisolona; 11 $ β $, 17,21 trihidroxi 6 $ α $ metil $ δ $ 1 progesterona; 11β, 17,21-Trihidroxi-6α-metilpregna-1,4-dieno-3,20-diona |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a682795 |
| Datos de licencia |
|
| Categoría de embarazo |
|
| Vías de administración | Por vía oral , IM (como acetato ), IA (como acetato ), IV (como succinato , suleptanato ) |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Enlace proteico | 78% |
| Metabolismo | Hígado principalmente, riñón , tejidos ; CYP3A4 |
| Vida media de eliminación | 18 a 26 horas |
| Excreción | Orina |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| CHEBI |
|
| CHEMBL |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.001.343 |
| Datos químicos y físicos | |
| Fórmula | C 22 H 30 O 5 |
| Masa molar | 374,477 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusion | 228 a 237 ° C (442 a 459 ° F) |
| solubilidad en agua | 1,20x10 + 2 mg / ml (20 ° C) |
Sonrisas
| |
InChI
| |
| (verificar) | |
La metilprednisolona (Depo-Medrol, Medrol, Solu-Medrol) es un glucocorticoide sintético , prescrito principalmente por sus efectos antiinflamatorios e inmunosupresores. [3] [4] [5] Se usa en dosis bajas para enfermedades crónicas o se usa concomitantemente en dosis altas durante los brotes agudos. La metilprednisolona y sus derivados se pueden administrar por vía oral o parenteral. [6]
Independientemente de la vía de administración, la metilprednisolona se integra sistémicamente como lo demuestra su eficacia para reducir rápidamente la inflamación durante los brotes agudos. [7] Se asocia con muchas reacciones adversas que requieren disminuir gradualmente el medicamento tan pronto como la enfermedad esté bajo control. [8] Los efectos secundarios graves incluyen síndrome de Cushing iatrogénico, hipertensión, osteoporosis, diabetes, infecciones y atrofia de la piel. [8]
Químicamente, la metilprednisolona es una hormona esteroide pregnana sintética derivada de la hidrocortisona y la prednisolona . Pertenece a una clase de glucocorticoides sintéticos y, más generalmente, a los corticosteroides . Actúa como agonista del receptor de mineralocorticoides y glucocorticoides. En comparación con otros glucocorticoides exógenos, la metilprednisolona tiene una mayor afinidad por los receptores de glucocorticoides que por los de mineralocorticoides.
El nombre de los glucocorticoides se derivó después del descubrimiento de su participación en la regulación del metabolismo de los carbohidratos. [8] Ahora se sabe que las funciones celulares de los glucocorticoides, como la metilprednisolona, regulan la homeostasis, el metabolismo, el desarrollo, la cognición y la inflamación. [8] Desempeñan un papel fundamental en la adaptación y respuesta al estrés ambiental, físico y emocional. [8]
La metilprednisolona fue sintetizada y fabricada por primera vez por The Upjohn Company (ahora Pfizer) y aprobada por la FDA en los Estados Unidos el 2 de octubre de 1957. [9] En 2018, fue el medicamento 153o más comúnmente recetado en los Estados Unidos, con más de 4 millones de recetas. [10] [11] La metilprednisolona ha sido una terapia recetada en medio de la pandemia de COVID-19 , pero no hay evidencia de que sea segura o efectiva para este propósito. [12] [13]
Farmacodinamia
La metilprednisolona es un glucocorticoide sintético (GC) que exhibe efectos pleiotrópicos en una variedad de mecanismos fisiológicos. [4] Sin embargo, se han recetado ampliamente por sus efectos sobre la inflamación y la inmunidad. [5] Los efectos de los glucocorticoides sintéticos, como la metilprednisolona, dependen de su asociación con los receptores de glucocorticoides (GR) intracelulares y, en menor medida, con los receptores de mineralocorticoides (MR). Los GR están ampliamente distribuidos en contraste con los MR que muestran una distribución tisular restringida. [8] Mediante este mecanismo, el receptor unido al ligando se traslada al núcleo y modula la expresión génica. [5]
Transducción de señales
En ausencia de GC endógenos o sintéticos, los GR monoméricos se encuentran en el citoplasma y forman complejos multiproteicos con proteínas de choque térmico (HSP), inmunofilinas y otras chaperonas como src y p23. [3] El GR actúa de manera dependiente del ligando, con el complejo manteniendo al GR en una forma inactiva con alta especificidad por el ligando. [5] Cuando la metilprednisolona del plasma o del líquido intersticial se difunde pasivamente a través de la membrana celular, se une al GR induciendo un cambio conformacional y la dimerización del GC-GR. Anteriormente se pensaba que este cambio conformacional era necesario para disociar el complejo multiproteico para permitir que el receptor unido al ligando se trasladara al núcleo. [3] [4]Sin embargo, estudios recientes han indicado que los acompañantes juegan un papel en la importación nuclear. [14] El complejo de metilprednisolona-GR, ahora activo, puede transducir cambios no genómicos en el citoplasma o translocarse al núcleo y regular la actividad transcripcional de los genes diana mediante mecanismos directos, de unión o compuestos. [4]
Señalización genómica
Los mecanismos genómicos, independientemente del tipo, provocan respuestas de inicio lento y disipación lenta. [15] Esto se atribuye a la duración de la transcripción y traducción del ARNm. [15] Los glucocorticoides tienen la capacidad de regular aproximadamente de 100 a 1000 genes con especificidad para el tipo de célula. [15]
Tres mecanismos principales han descrito cómo el complejo MP-GR altera la expresión génica al unirse al ADN o a los moduladores de la transcripción. [4] Un mecanismo de señalización genómica ocurre cuando el complejo MP-GR se une directamente a secuencias de ADN llamadas elementos de respuesta a glucocorticoides (GRE). [4] Los GRE se encuentran en regiones reguladoras de genes diana y median su transactivación o transrepresión. [5] Por ejemplo, la activación de lipocortina 1 (ANAX1) interfiere negativamente con la producción de prostaglandinas y leucotrienos , señales proinflamatorias conocidas. Asimismo, los GRE negativos (nGRE) son responsables de reprimir los genes implicados en la activación de las células inmunes.[4]
Modificaciones postranscripcionales
Las modificaciones postraduccionales (PTM) también contribuyen a la señalización de metilprednisolona y pueden producir efectos genómicos y no genómicos. [14] El GR contiene varios sitios para la fosforilación, sumoilación, ubiquitinación y acetilación que ocurren principalmente después de la unión intracelular de metilprednisolona al GR. [5] [16] Los PTM modulan muchas funciones, incluida la translocación nuclear, la fuerza y duración de la señalización del receptor y la interacción del cofactor. [14] Un ejemplo específico es la desacetilación por histona desacetilasa 2 (HDACe) que fue necesaria para la transrepresión de NF-κB. [5] [16]
Señalización no genómica
Los mecanismos de señalización no genómica son distintos de la señalización genómica, pero median vías similares y proporcionan relevancia terapéutica. [17] [18] Estos mecanismos se caracterizan por tener un inicio rápido (menos de 15 minutos), porque no dependen de una transcripción o traducción que requiera mucho tiempo y no son modificados por inhibidores de la transcripción. [15]
La señalización no genómica inducida por metilprednisolona se clasifica por tres mecanismos: (1) efectos no genómicos mediados por el receptor citoplasmático de glucocorticoides (cGR), (2) efectos no genómicos del receptor de glucocorticoides unido a la membrana (mGR) y (3) interacciones fisicoquímicas con membranas celulares (efectos no genómicos inespecíficos). [15] [17]
Las proteínas que se disocian del complejo GC-cGR activado inician mecanismos intracelulares independientes de la transcripción. [19] [20] Existe evidencia de que el SRC disociado es responsable de inhibir la liberación de ácido araquidónico (AA) de los fosfolípidos de la membrana celular. [17] El AA es necesario para la síntesis de mediadores inflamatorios (prostaglandinas y leucotrienos) y, por tanto, la inhibición del AA media en varias vías importantes como el crecimiento celular, el metabolismo y la inflamación. [19] [20]
Estudios anteriores identificaron mGR en células de linfoma, pero no fue hasta 2004 que se identificaron mGR en células mononucleares periféricas humanas. [17] La prevalencia de mGR varía según el tipo de célula, con la concentración más alta en linfocitos B de hasta el 12,3%, hasta el 9,2% en los monocitos y ausente en los linfocitos T. [17] Los estudios han demostrado una correlación positiva entre las células positivas para mGR y la actividad relacionada con la enfermedad. [17] No existen vías de señalización probadas asociadas con mGR en este momento. Algunos investigadores plantean la hipótesis de que la alta actividad de la enfermedad activa la expresión de mGR y, al administrar metilprednisolona, crea un ciclo de retroalimentación negativa al inducir la apoptosis. [17]
Altas concentraciones de metilprednisolona se intercalan en el plasma y las membranas celulares mitocondriales. Esta asociación cambia las propiedades fisicoquímicas de la membrana; activando las proteínas de la membrana, alterando las funciones celulares y, en última instancia, influyendo en el transporte de cationes a través de la membrana plasmática y estimulando la fuga de protones a través de la membrana mitocondrial interna. [15] [17] La fosforilación oxidativa obstaculizada compromete la producción de ATP, una fuente de energía importante para el metabolismo energético celular y la función inmunológica. Se ha demostrado que los estudios in vivo de timocitos estimulados con Con-A (en ratas) y células inmunitarias humanas a las que se les administraron dosis altas de metilprednisolona inhiben la respiración de una manera dependiente de la dosis, inhiben la captación de calcio y sodio en plasma y aumentan la concentración de calcio citoplásmico. [17]El proceso sumativo es el siguiente: la metilprednisolona se intercala en la membrana plasmática, provoca cambios fisicoquímicos, activa las proteínas de la membrana que inhiben la captación plasmática de calcio y sodio (imitando un estado de déficit energético). El consumo de ATP cae (similar a la respiración inhibida), lo que da como resultado la permeabilidad de las proteínas en la membrana mitocondrial interna y el desacoplamiento de la fosforilación oxidativa. De notable importancia, la síntesis de ADN / ARN no se vio obstaculizada. [17] La dependencia de las células domésticas y las células inmunitarias del ATP, da como resultado inmunosupresión durante el déficit de ATP. Las funciones inmunes específicas afectadas por este proceso son citocinesis, migración, fagocitosis, procesamiento y presentación de antígenos, síntesis de anticuerpos, citotoxicidad y regulación. [17]
El eje HPA
La activación del eje hipotalámico-hipofisario (eje HPA) estimula la producción de glucocorticoides endógenos dentro de la corteza suprarrenal. [14] El eje HPA interpreta los estímulos (estrés, inflamación y señales circadianas) y transduce una respuesta fisicoquímica correspondiente. [5] Los glucocorticoides liberados en la sangre sirven como mensajeros al unirse a los receptores de glucocorticoides en una amplia distribución por todo el cuerpo, incluido el propio eje HPA. [14] Por lo tanto, el rango fisiológico de los GC es monitoreado por el ciclo de retroalimentación negativa que los GC ejercen en cualquier parte del eje HPA. [5] La metilprednisolona imita estructural y funcionalmente a los corticoides endógenos y actuará sobre el eje HPA de manera similar.
Farmacocinética
La metilprednisolona está aprobada para administración oral y parenteral. La metilprednisolona (Medrol) para administración oral está disponible en una formulación de tableta en concentraciones de 2 mg, 4 mg, 8 mg, 16 mg o 32 mg. [21] Tanto el acetato de metilprednisolona (Depo-Medrol) como el succinato de metilprednisolona (Solu-Medrol) están aprobados para inyección intramuscular. [22] [23] Depo-Medrol también está aprobado para inyecciones intralesionales, intraarticulares y de tejidos blandos. Depo-Medrol está disponible como solución acuosa estéril en concentraciones de 20 mg / ml, 40 mg / ml u 80 mg / ml. [22]Solu-Medrol es el único derivado de metilprednisolona aprobado para infusión intravenosa, ya que el polvo estéril es soluble en agua y se puede mezclar con un diluyente. Las concentraciones varían de 40 mg a 2 g. [23]
Los glucocorticoides sintéticos son similares a los esteroides endógenos en el metabolismo, pero difieren en la afinidad por los receptores de glucocorticoides y mineralocorticoides, la afinidad por la unión a proteínas, la velocidad de eliminación y los productos metabólicos. [3]
La metilprednisolona oral se absorbe fácilmente en el tracto gastrointestinal con una biodisponibilidad del 89,9%. [24] A diferencia de los GC endógenos, la metilprednisolona no se une a la glicoproteína transcortina (globulina transportadora de corticosteroides, CBG), pero tiene una unión proteica moderada a la albúmina. [15] Por lo tanto, la farmacocinética de la metilprednisolona es lineal y no muestra dependencia de la dosis. [15] Los pacientes que presentan concentraciones bajas de albúmina corren el riesgo de sufrir efectos adversos durante el tratamiento con glucocorticoides. [15] La metilprednisolona oral tiene una distribución moderada en los tejidos a 1,38 l / kg. [25]
La metilprednisolona se elimina principalmente por metabolismo hepático y excreción renal de metabolitos; con excreción renal de metilprednisolona inalterada de sólo 1,3 a 9,2%. [25] La metilprednisolona se puede interconvertir con metilprednisona. [15] El metabolismo hepático está mediado por 11 beta-hidroxiesteroide deshidrogenasas (11 [beta] -HSD) y 20-cetoesteroides reductasas. [25] La metilprednisolona experimenta la excreción renal de metabolitos inactivos hidrófilos, que incluyen 20-carboximetilprednisolona y 6? -Hidroxi-20? -Hidroximetilprednisolona. [15]
| Glucocorticoide sintético | Dosis equivalente (mg) | Actividad antiinflamatoria 1 | Actividad mineralocorticoide 1 | Vida media biológica (horas) | Referencias |
|---|---|---|---|---|---|
| Glucocorticoides de acción corta a media | |||||
| Hidrocortisona | 20 | 1 | 1 | 8-12 | [3] [8] |
| Cortisona | 25 | 0,8 | 0,8 | 8-12 | [3] [8] |
| Prednisona | 5 | 4 | 0,3 | 12-36 | [3] [8] |
| Prednisolona | 5 | 4 - 5 | 0,3 | 12-36 | [3] [8] |
| Metilprednisolona | 4 | 5 | 0,25-0,5 | 12-36 | [3] [8] |
| Meprednisona | 4 | 5 | 0 | [3] | |
| Glucocorticoides de acción intermedia | |||||
| Triamcinolona | 4 | 5 | 0 | 12-36 | [3] [8] |
| Parametasona | 2 | 10 | 0 | N / A | [3] [8] |
| Fluprednisolona | 1,5 | 15 | 0 | [3] | |
| Glucocorticoides de acción prolongada | |||||
| Betametasona | 0,6 | 25-40 | 0 | 36-72 | [3] [8] [26] |
| Dexametasona | 0,75 | 30 | 0 | 36-72 | [3] [8] |
| Mineralocorticoides | |||||
| Fludrocortisona | 2 | 10 | 250 | 18-36 | [3] [8] |
| Acetato de desoxicorticosterona | 0 | 20 | |||
Usos médicos
Como se indicó anteriormente, el uso principal de la metilprednisolona es suprimir las respuestas inflamatorias e inmunes. La metilprednisolona logra esto principalmente mediante la regulación del número y función de leucocitos, citocinas y quimiocinas. [3] Su control inflamatorio generalizado es propicio para su uso en múltiples trastornos independientemente de la patología. [3] La metilprednisolona se prescribe comúnmente como terapia a corto plazo para los brotes agudos, como se observa en la artritis gotosa aguda. Se puede prescribir durante la terapia en curso en dosis más bajas dependiendo de la monitorización de los efectos adversos. [4] La dosis y la formulación se optimizan según el uso médico. [5]
Asma
En 2001–2002, al 11,4% de los pacientes diagnosticados de asma y atendidos en una visita ambulatoria se les recetaron corticosteroides orales como terapia de control a largo plazo. [27] El Programa Nacional de Educación y Prevención del Asma (NAEPP) indica metilprednisolona sistémica en terapias a corto y largo plazo para controlar rápidamente y suprimir el asma persistente, respectivamente. [28] Para las exacerbaciones que resultan en una visita al Departamento de Emergencias (SU), se prefiere la metilprednisolona oral a la administración intravenosa, a menos que haya problemas de adherencia o vómitos. [28] [29] La metilprednisolona oral es menos invasiva y los estudios han demostrado una eficacia equivalente en comparación con la metilprednisolona intravenosa. [28] [29] No se recomienda una dosis superior a 60 a 80 mg / día o 2 mg / kg / día, ya que no se ha demostrado que altere la función pulmonar, la tasa de ingreso ni la duración de la estancia en el hospital en comparación con dosis más bajas. [29] Después del alta del servicio de urgencias, se recomienda prescribir un ciclo de cinco días de metilprednisolona para disminuir la probabilidad de recaída o síntomas de abstinencia. [28] [29]
Enfermedades reumáticas
La metilprednisolona se usa para tratar varias enfermedades reumáticas, como el lupus eritematoso sistémico (LES) y la artritis reumatoide (AR). La dosificación y administración de metilprednisolona para estas enfermedades es muy variable debido a la variada fisiopatología entre las enfermedades y dentro de los pacientes diagnosticados con una enfermedad determinada. [30] [31] En la nefritis lúpica, una manifestación común del LES, a los pacientes a menudo se les prescribe metilprednisolona concomitantemente con inmunosupresores. Las manifestaciones graves a menudo se tratan con ciclofosfamida o rituximab y tres dosis de tratamiento con pulsos intravenosos de metilprednisolona (según lo recomendado por las pautas del ACR) antes de cambiar a prednisolona y azatioprina orales para el mantenimiento. [30] [31]
Las inyecciones de corticosteroides intraarticulares (IACI) son una terapia de segunda línea para aliviar el dolor articular resultante de la artritis reumatoide. [32] Se inyecta con mayor frecuencia en las articulaciones de las rodillas y los hombros. [32] Aunque la inyección es local, los estudios han demostrado la absorción sistémica como lo demuestran los efectos beneficiosos en las articulaciones distantes. [32] En un intento por minimizar la supresión de HPA, las pautas de la FDA han restringido los IACI a tres por año, con un mínimo de 30 días entre inyecciones. [33]
Insuficiencia adrenocortical primaria o secundaria
La metilprednisolona no se recomienda típicamente para la insuficiencia adrenocortical primaria o secundaria en comparación con otros corticosteroides que tienen una mayor afinidad por el receptor de mineralocorticoides y las propiedades de retención de sal. [3]
Indicaciones etiquetadas
Las indicaciones etiquetadas a continuación están clasificadas por vía de administración y luego por disciplina médica.
Metilprednisolona oral
- Alergia e inmunología: edema angioneurótico , [28] asma , urticaria , rinitis alérgica estacional o perenne, reacciones de hipersensibilidad a fármacos y enfermedad del suero . [21]
- Dermatología: necrólisis epidérmica tóxica, [28] dermatitis atópica , dermatitis de contacto , pénfigo , eritema multiforme , síndrome de Steven-Johnson , dermatitis herpetiforme bullosa, dermatitis seborreica grave , dermatitis exfoliativa, micosis fungoide y psoriasis grave . [21]
- Endocrinología: hiperplasia suprarrenal congénita , hipercalcemia asociada a cáncer , tiroiditis no supurativa e insuficiencia adrenocortical primaria o secundaria . [21]
- Gastroenterología: enfermedad inflamatoria intestinal y colitis ulcerosa . [21]
- Hematología: anemia hemolítica adquirida (autoinmune) , púrpura trombocitopénica idiopática , trombocitopenia secundaria, eritroblastopenia, leucemia , linfoma y anemia hipoplásica congénita (eritroide). [21]
- Pulmonar: neumonitis por aspiración , enfermedad crónica por berilio , neumonía eosinofílica , sarcoidosis sintomática y tuberculosis pulmonar junto con quimioterapia antituberculosa. [21]
- Nefrología: síndrome nefrótico , tipo idiopático o secundario a nefritis lúpica . [21]
- Neurología: esclerosis múltiple . [21]
- Oftalmología: escleritis , vasculitis retiniana , [28] uveítis , coroiditis, iritis, iridociclitis, queratitis , neuritis óptica , conjuntivitis alérgica, úlceras marginales corneales alérgicas, herpes zoster oftálmico , oftalmía simpática y coriorretinitis. [21]
- Reumatología: artritis reumatoide , carditis reumática , artritis gotosa aguda , espondilitis anquilosante , dermatomiositis y polimiositis , artritis psoriásica , lupus eritematoso sistémico , bursitis aguda y subaguda , sinovitis de osteoartritis, osteoartritis postraumática y epicondilitis . [21]
- Varios: triquinosis con afectación neurológica o miocárdica. [21]
Metilprednisolona parenteral
- Inyecciones intraarticulares o de tejidos blandos: artritis gotosa aguda, bursitis aguda y subaguda, tenosinovitis aguda, epicondilitis y sinovitis de la osteoartritis. [31]
- Inyecciones intralesionales: alopecia areata , lupus eritematoso discoide , queloides , granuloma anular , liquen plano , liquen simple crónico , placas psoriásicas, necrobiosis lipoidica diabeticorum . [31]
- Las inyecciones intramusculares se prescriben para tratar muchas de las mismas afecciones indicadas para la administración oral. Las inyecciones intramusculares se administran como alternativa a la terapia oral. [31]
Indicaciones extraoficiales
Algunas de las indicaciones no autorizadas de la metilprednisolona incluyen lesión aguda de la médula espinal , síndrome de dificultad respiratoria aguda , hepatitis alcohólica , reanimación hormonal en la recuperación de órganos cadavéricos y enfermedad pulmonar obstructiva crónica . [28]
Formas disponibles
| Ingrediente activo | Nombre de la marca | ROA | Formulario | Fuerza 1 | ingredientes inactivos |
|---|---|---|---|---|---|
| metilprednisolona | Medrol | Oral | tableta | 2, 4, 8, 16, 32 mg | estearato de calcio, almidón de maíz, lactosa, aceite mineral, ácido sórbico, sacarosa y eritrosina sódica (solo 2 mg), amarillo FD&C No. 6 (solo 8 y 32 mg) |
| metilprednisolona | Medrol | Oral | tableta | 4 mg; 21 pastillas (paquete de dosis) | estearato de calcio, maicena, lactosa, sacarosa |
| acetato de metilprednisolona | Depo-Medrol | Parenteral: intraarticular o de tejido blando, intralesional o intramuscular | suspensión | 20, 40, 80 mg / ml | Polietilenglicol 3350, polisorbato 80, fosfato de sodio monobásico, fosfato de sodio dibásico USP, alcohol bencílico 2 añadido como conservante |
| acetato de metilprednisolona 3 | Depo-Medrol | Parenteral: intraarticular o de tejido blando, intralesional o intramuscular | suspensión | 40 u 80 mg / ml (vial de dosis única) | Polietilenglicol 3350 Cloruro de miristil-gamma-picolinio |
| succinato de metilprednisolona | Solu-Medrol | Parenteral: intravenosa o intramuscular | solución reconstituida | 500, 1000, 2000 mg / vial, 2000 mg con diluyente (vial multidosis) | fosfato de sodio monobásico anhidro, fosfato de sodio dibásico seco y lactosa hidratada. Agua bacteriostática añadida como diluyente con alcohol bencílico 2 añadido como conservante |
| succinato de metilprednisolona 3 | Solu-Medrol | Parenteral: intravenosa o intramuscular | solución reconstituida | 40, 125, 500, 1000 mg / vial (vial de dosis única) | fosfato de sodio monobásico anhidro, fosfato de sodio dibásico seco y lactosa hidratada. |
Notas a pie de página:
1 Significa diferentes fortalezas de las formas disponibles. No es indicativo de frecuencia ni dosis acumulativa diaria; varía según el paciente y la condición.
2 El alcohol bencílico no debe usarse en recién nacidos.
3 Formulación sin conservantes
Contraindicaciones
Las personas que tienen infecciones fúngicas sistémicas no deben tomar metilprednisolona por vía oral, con la excepción de Depo-Medrol cuando se administra como una inyección intraarticular para afecciones articulares localizadas. [22] La metilprednisolona está contraindicada en personas con hipersensibilidad conocida a la metilprednisolona o sus componentes. [21] Los esteroides deben usarse con precaución en pacientes con colitis ulcerosa, enfermedad cardíaca o hipertensión, úlcera péptica, insuficiencia renal, osteoporosis, miastenia grave, glaucoma y diabetes. [3] [21]Pueden aparecer manifestaciones psíquicas mientras toma metilprednisolona, que van desde euforia, insomnio, cambios de personalidad hasta depresión. Se requiere precaución en pacientes con psicosis predispuesta, ya que las tendencias psicóticas pueden exacerbarse mientras se toman corticosteroides. [21]
La dosis de Solu-Medrol 40 mg contiene lactosa monohidrato producida a partir de la leche de vaca; No debe tomarlo ninguna persona con hipersensibilidad conocida a los productos lácteos o sus componentes. [23] Se han asociado eventos médicos graves con la administración epidural de Solu-Medrol y Depo-Medrol, que incluyen infarto de la médula espinal, paraplejía, cuadriplejía, ceguera cortical y accidente cerebrovascular. Las inyecciones intramusculares no deben administrarse a personas con púrpura trombocitopénica idiopática. Las formulaciones de Solu-Medrol y Depo-Medrol que contienen alcohol bencílico están contraindicadas para su uso en bebés prematuros. [23] La exposición del tejido neural a cantidades excesivas de alcohol bencílico se ha asociado con toxicidad y, en raras ocasiones, ha provocado la muerte. [22]
Reacciones adversas
Las reacciones adversas pueden eclipsar los efectos terapéuticos de la metilprednisolona. [8]
Sistema nervioso central
Existen criterios mínimos de diagnóstico clínico para definir los efectos adversos psíquicos (PAE) asociados con el uso de metilprednisolona en pacientes con lupus eritematoso sistémico (LES). [26] La prevalencia varía del 1,3 al 62% de los pacientes adultos tratados. [26] El tipo y la gravedad de los síntomas neuropsiquiátricos también varían significativamente entre los pacientes; el 33% de los pacientes informaron una EAP leve a moderada y el 5-10% informaron una EAP grave. [26] La dosis y la duración de la metilprednisolona se han relacionado con el desarrollo de PAE. 20 mg / día de prednisona (16 mg / día de metilprednisolona) es la dosis umbral para el desarrollo de PAE acordada por muchos estudios. [26]La terapia intravenosa de pulsos a corto plazo a dosis altas se asocia con la aparición rápida de síntomas maníacos e hipomaníacos, mientras que la terapia a largo plazo da lugar a síntomas depresivos (intentos de suicidio infrecuentes). [26] Los PAE son reversibles con la reducción o interrupción del tratamiento. [26]
Metabólico y endocrino
El síndrome de Cushing iatrogénico es una complicación directa de la terapia con glucocorticoides y la causa más común de síndrome de Cushing exógeno. [34] Las características clínicas del síndrome de Cushing incluyen muchos efectos adversos en la terapia con glucocorticoides. [34] Los síntomas tradicionales incluyen aumento de peso, miopatía, osteoporosis, mayor riesgo de infección, hipertensión y efectos psicológicos. La deposición de grasa se centraliza en el tronco, entre los hombros ("joroba de búfalo") y en la cara ("cara de luna"). [34] La educación del paciente y el seguimiento del proveedor es el primer paso para reconocer y diagnosticar el síndrome de Cushing iatrogénico. Los glucocorticoides exógenos suprimen la hormona adrenocorticotrópica(ATCH), que puede verificarse mediante análisis bioquímico AM. [34] La aparición de efectos secundarios varía; Los síntomas neuropsiquiátricos pueden surgir en unas pocas horas, mientras que la osteoporosis tardaría meses en desarrollarse. [34]
Los efectos metabólicos de tomar metilprednisolona implican la degradación continua de proteínas para que la gluconeogénesis aumente la necesidad de insulina. Esto da como resultado hiperlipidemia, aumento de peso y miopatía que pueden llevar al paciente a iniciar el tratamiento. [3]
Infecciones
- Ver: glucocorticoides § inmunodeficiencia
La sección de Inmunodeficiencia tabula los patógenos conocidos de interés en la inmunodeficiencia inducida por glucocorticoides.
Musculoesquelético
La osteoporosis es un tipo de enfermedad ósea caracterizada por una pérdida de densidad, masa y arquitectura óseas que deja al paciente susceptible a fracturas. [35] La Organización Mundial de la Salud (OMS) define la osteoporosis en mujeres posmenopáusicas caucásicas como una densidad mineral ósea (DMO) y una puntuación T de -2,5 o menos. [20] [36] La prevalencia de osteoporosis en pacientes con LES varía geográficamente y algunos la atribuyen a la idoneidad diagnóstica de la DMO y la puntuación T. [20] Británicos 10,3%, chinos 21,7% Las Guías de Práctica Clínica Canadienses y el Colegio Americano de Reumatología han cambiado al uso de una puntuación Z como marcador de diagnóstico para la osteoporosis, pero no han logrado encontrar un umbral de diagnóstico clínico. [20]Además, un estudio realizado en el Reino Unido mostró que la DMO puede representar infrarrepresentadamente a un paciente con LES, ya que su riesgo de fracturas es un 22% más alto que el de un individuo sano. [20]
Los corticosteroides exógenos inducen osteoporosis aumentando la resorción ósea y reduciendo la formación de hueso. [20] La pérdida ósea puede ser pronunciada dentro de los primeros meses de iniciar la metilprednisolona con una disminución constante con el uso crónico. La pérdida de hueso trabecular en la columna lumbar precede a la pérdida de hueso cortical en el cuello femoral. [20]
Lista exhaustiva
Alérgico: reacciones alérgicas o de hipersensibilidad, reacción anafilactoide, anafilaxia y urticaria. [21]
Cardiovascular: hipertensión, insuficiencia cardíaca congestiva en pacientes susceptibles, [21] enfermedad aterosclerótica prematura, arritmias y posible hiperlipidemia. [34]
Dermatológico: alteración de la cicatrización de heridas, petequias y equimosis, adelgazamiento de la piel, eritema facial y aumento de la sudoración. [21]
Endocrino: características cushingoides, supresión del crecimiento en niños, falta de respuesta adrenocortical e hipofisaria secundaria, irregularidades menstruales, intolerancia a los carbohidratos disminuida y diabetes mellitus latente. En pacientes con diabetes, aumento de las necesidades de insulina o agentes hipoglucemiantes orales. [21]
Alteraciones de líquidos y electrolitos: retención de sodio, retención de líquidos, pérdida de potasio, alcalosis hipopotasémica o insuficiencia cardíaca congestiva en pacientes susceptibles. [21]
Gastrointestinal: úlcera péptica, pancreatitis, distensión abdominal y esofagitis ulcerosa. [21]
Metabólico: catabolismo proteico que provoca un balance nitrogenado negativo. [21]
Musculoesquelético: debilidad muscular, pérdida de masa muscular, miopatía por esteroides, osteoporosis, rotura de tendones (especialmente de Aquiles), fracturas vertebrales por compresión, necrosis aséptica de las cabezas femoral y humeral y fractura patológica de huesos largos. [21]
Neurológico: aumento de la presión intracraneal con papiledema, convulsiones, vértigo y cefalea. [21]
Oftalmológico: cataratas subcapsulares posteriores, aumento de la presión intraocular, glaucoma y exoftalmos. [21]
Retiro
La retroalimentación de los glucocorticoides exógenos en el eje hipotalámico-pituitario-suprarrenal (HPA) inhibe la secreción de la hormona liberadora de corticotropina (CRH) y la hormona adrenocorticotrópica (ATCH) en el hipotálamo y las glándulas pituitarias, respectivamente. [37] La supresión prolongada conduce a respuestas inadecuadas al estrés físico y emocional, como enfermedades y traumas. [37] La supresión de ATCH puede resultar en hipoplasia suprarrenal o atrofia secundaria de la glándula suprarrenal dentro de las 6 semanas de tratamiento con metilprednisolona, lo que deja al paciente en riesgo de desarrollar una crisis de insuficiencia suprarrenal potencialmente mortal. [8] [37]Los factores que contribuyen al grado de supresión del eje HPA incluyen la potencia de las hormonas esteroides (tipo de compuesto y vía de administración), dosis acumulada, duración del tratamiento y uso concomitante de fármacos. [8] Cualquier individuo que haya tomado hormonas esteroides durante más de 2 semanas corre el riesgo de desarrollar supresión del eje HPA. [37] t El riesgo sistémico de metilprednisolona se ha marcado como moderado dentro de la clase de glucocorticoides sintéticos. [37]
Consulte con su médico antes de suspender la metilprednisolona por cualquier motivo. [38] La interrupción abrupta del fármaco suele causar síntomas transitorios no específicos como pérdida de apetito, malestar estomacal, vómitos, somnolencia, confusión, dolor de cabeza, fiebre, dolor articular y muscular, descamación de la piel y pérdida de peso. [37] [38] Estos síntomas se pueden atribuir al síndrome de abstinencia de esteroides, insuficiencia suprarrenal o recaída de la enfermedad. [37] Aquellos que han estado tomando metilprednisolona como tratamiento a largo plazo pueden reducirse gradualmente para minimizar los síntomas de abstinencia y la posibilidad de recaída. [38] [37] Si los síntomas se exacerban, el aumento temporal de la dosis de metilprednisolona ha mostrado relevancia clínica.[37] Los estudios que volvieron a evaluar a los pacientes con la abstinencia de metilprednisolona mostraron insuficiencia suprarrenal persistente, y un estudio mostró un 15% después de 3 años. [8] [39] Sin embargo, hubo una amplia gama de prevalencia y falta de uniformidad en el cronograma de seguimiento. [39]
Interacciones con la drogas
Se recomienda precaución al tomar metilprednisolona al mismo tiempo que los medicamentos que se describen a continuación.
Inductores de enzimas
Todos los medicamentos que pertenecen a la clase de inductores enzimáticos aumentan el aclaramiento y disminuyen la vida media de la metilprednisolona cuando se administran de forma conjunta. [15] El fenobarbital , la fenitoína , la rifampicina , la carbamazepina y los barbitúricos aumentan las enzimas hepáticas y la velocidad de eliminación, reduciendo así el efecto inmunosupresor de la metilprednisolona. [15] Es posible que se requieran dosis mayores para lograr el efecto deseado de la metilprednisolona. [15]
Inhibidores del citocromo P450 (CYP) 3A4
La troleandomicina , ketoconazol y claritromicina inhiben el metabolismo; y puede disminuir la tasa de eliminación y aumentar la vida media de la metilprednisolona. [21] [15] Las dosis deben reducirse en consecuencia para evitar efectos secundarios. Otro inhibidor de CYP 3A4, el jugo de toronja, prolonga la vida media de la metilprednisolona oral. [15]
Anticonceptivos orales
Los anticonceptivos orales inhiben los procesos oxidativos, como lo destaca su capacidad para disminuir el aclaramiento de metilprednisolona. [15]
Inhibidores de la glicoproteína P
Se muestra que la metilprednisolona es un sustrato de la glicoproteína P; se cree que su inhibición aumenta la absorción y distribución de metilprednisona. No se ha vinculado ninguna relevancia clínica. [15]
Ciclosporina, tacrolimus, sirolimus (rapamicina)
La metilprednisolona y la ciclosporina inhiben el metabolismo y, por lo tanto, aumentan la probabilidad de experimentar efectos secundarios asociados con cualquiera de los fármacos individuales. Además de los efectos secundarios individuales conocidos, se han informado convulsiones. [21]
Inhibidores de Cox1
La metilprednisolona puede aumentar la tasa de eliminación con aspirina crónica en dosis altas . Los pacientes son susceptibles a un aumento de los niveles séricos de salicilato o toxicidad por salicilato tras la interrupción de la metilprednisolona. Se debe tener una precaución excesiva al prescribir metilprednisolona y aspirina a pacientes con hipoprotrombinemia . [21]
Anticoagulantes
Los anticoagulantes exhiben interacciones variables; Se recomienda monitorear los índices de coagulación para lograr el efecto deseado. [21]
Propiedades físicas
La metilprednisolona oral (Medrol) y sus derivados son un polvo cristalino blanco e inodoro. Su solubilidad varía desde prácticamente insoluble en agua, muy ligeramente soluble en éter, ligeramente soluble en acetona y cloroformo hasta escasamente soluble en alcohol, dioxano y metanol. [40] La suspensión de acetato de metilprednisolona (Depo-Medrol) es un derivado 6-metilo de prednisolona que se funde a 215 grados Celsius con cierta descomposición. [22] El succinato sódico de metilprednisolona (Solu-Medrol) es el éster succinato sódico de la metilprednisolona. Contrariamente a las solubilidades anteriores, el succinato sódico de metilprednisolona es soluble en agua y alcohol, ligeramente soluble en acetona e insoluble en cloroformo [23]
Propiedades químicas
La metilprednisolona, o 6α-metilprednisolona, también conocida como 11β, 17,21-trihidroxi-6α-metilpregna-1,4-dieno-3,20-diona, es un esteroide pregnano sintético y un derivado de la hidrocortisona (11β, 17α, 21 -trihidroxipregn-4-eno-3,20-diona) y prednisolona (11β, 17α, 21-trihidroxipregn-1,4-dieno-3,20-diona). [41] [42] Existe una variedad de ésteres de metilprednisolona con diferentes características y se han comercializado para uso médico. [41] [42] Incluyen aceponato de metilprednisolona (Advantan), acetato de metilprednisolona (Depo-Medrol), succinato de metilprednisolona (Solu-Medrol) y suleptanato de metilprednisolona (Medrosol, Promedrol). [41] [42]
Síntesis
Los esteroides sintéticos se sintetizan a partir del ácido cólico y las sapogeninas obtenidas de ganado y plantas, respectivamente. [3]
Historia, sociedad y cultura
La metilprednisolona fue sintetizada y fabricada por primera vez por The Upjohn Company (ahora Pfizer) y la Administración de Alimentos y Medicamentos (FDA) aprobada en los Estados Unidos el 2 de octubre de 1957. [9] Desde entonces, la patente ha expirado y los genéricos ahora están disponibles. En 2021, se clasifica como el medicamento 153o más comúnmente recetado en los Estados Unidos, con más de cuatro millones de recetas. [43] Ha saltado cuatro lugares en la clasificación desde 2017. La metilprednisolona ha sido una terapia recetada en medio de la pandemia de COVID-19 , pero no hay evidencia de que sea segura o efectiva para este propósito. [44] [45]
Referencias
- ^ "Uso de metilprednisolona durante el embarazo" . Drugs.com . 20 de agosto de 2019 . Consultado el 20 de febrero de 2020 .
- ^ https://www.ema.europa.eu/documents/psusa/methylprednisolone-list-nationally-authorised-medicinal-products-psusa/00002026/202011_en.pdf
- ^ a b c d e f g h i j k l m n o p q r s t u v Katzung BG, Masters SB, Trevor AJ (2012). Farmacología básica y clínica (12ª ed.). Nueva York: McGraw-Hill Medical. ISBN 978-0-07-176401-8. OCLC 761378641 .
- ↑ a b c d e f g h Timmermans S, Souffriau J, Libert C (2019). "Una introducción general a la biología de los glucocorticoides" . Fronteras en inmunología . 10 : 1545. doi : 10.3389 / fimmu.2019.01545 . PMC 6621919 . PMID 31333672 .
- ↑ a b c d e f g h i j Xavier AM, Anunciato AK, Rosenstock TR, Glezer I (2016). "Control de la expresión génica por receptores de glucocorticoides durante las respuestas inmunitarias innatas" . Fronteras en endocrinología . 7 : 31. doi : 10.3389 / fendo.2016.00031 . PMC 4835445 . PMID 27148162 .
- ^ Ocejo A, Correa R (2020). "Metilprednisolona". StatPearls . La isla del tesoro (FL): StatPearls Publishing. PMID 31335060 . Consultado el 10 de noviembre de 2020 .
- ^ Habib GS (julio de 2009). "Efectos sistémicos de los corticosteroides intraarticulares". Reumatología clínica . 28 (7): 749–56. doi : 10.1007 / s10067-009-1135-x . PMID 19252817 . S2CID 5645348 .
- ^ a b c d e f g h i j k l m n o p q r s t Paragliola RM, Papi G, Pontecorvi A, Corsello SM (octubre de 2017). "Tratamiento con Glucocorticoides Sintéticos y Eje Hipotálamo-Pituitario-Adrenal" . Revista Internacional de Ciencias Moleculares . 18 (10): 2201. doi : 10.3390 / ijms18102201 . PMC 5666882 . PMID 29053578 .
- ^ a b "Medicamentos @ FDA: medicamentos aprobados por la FDA" . www.accessdata.fda.gov . Consultado el 5 de diciembre de 2020 .
- ^ "El Top 300 de 2021" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ "Metilprednisolona - estadísticas de uso de drogas" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ Kosaka M, Yamazaki Y, Maruno T, Sakaguchi K, Sawaki S (enero de 2021). "Corticosteroides como terapia adyuvante en el tratamiento de la enfermedad por coronavirus 2019: informe de dos casos y revisión de la literatura" . Revista de Infección y Quimioterapia . 27 (1): 94–98. doi : 10.1016 / j.jiac.2020.09.007 . PMC 7480527 . PMID 32988730 .
- ^ Yousefifard M, Mohamed Ali K, Aghaei A, Zali A, Madani Neishaboori A, Zarghi A, et al. (Agosto de 2020). "Corticosteroides en el manejo de la enfermedad por coronavirus 2019 (COVID-19): una revisión sistémica y un metanálisis" . Revista Iraní de Salud Pública . 49 (8): 1411–1421. doi : 10.18502 / ijph.v49i8.3863 . PMC 7554375 . PMID 33083317 .
- ↑ a b c d e Cain DW, Cidlowski JA (abril de 2017). "Regulación inmunológica por glucocorticoides". Reseñas de la naturaleza. Inmunologia . 17 (4): 233–247. doi : 10.1038 / nri.2017.1 . PMID 28192415 . S2CID 47176122 .
- ^ a b c d e f g h i j k l m n o p q r Czock D, Keller F, Rasche FM, Häussler U (2005). "Farmacocinética y farmacodinámica de glucocorticoides administrados sistémicamente". Farmacocinética clínica . 44 (1): 61–98. doi : 10.2165 / 00003088-200544010-00003 . PMID 15634032 . S2CID 24458998 .
- ^ a b Kino T, Chrousos GP. Regulación epigenética mediada por acetilación de la actividad del receptor de glucocorticoides: alteraciones asociadas al ritmo circadiano de las acciones de los glucocorticoides en los tejidos diana. Mol Cell Endocrinol . 2011; 336 (1-2): 23-30. doi: 10.1016 / j.mce.2010.12.001
- ^ a b c d e f g h i j k Song IH, Buttgereit F (febrero de 2006). "Efectos de glucocorticoides no genómicos para proporcionar la base para el desarrollo de nuevos fármacos". Endocrinología molecular y celular . 246 (1–2): 142–6. doi : 10.1016 / j.mce.2005.11.012 . PMID 16388891 . S2CID 40239838 .
- ^ Panettieri RA, Schaafsma D, Amrani Y, Koziol-White C, Ostrom R, Tliba O (enero de 2019). "Efectos no genómicos de los glucocorticoides: una vista actualizada" . Tendencias en Ciencias Farmacológicas . 40 (1): 38–49. doi : 10.1016 / j.tips.2018.11.002 . PMC 7106476 . PMID 30497693 .
- ↑ a b Stahn C, Buttgereit F (octubre de 2008). "Efectos genómicos y no genómicos de los glucocorticoides". Práctica Clínica Nature. Reumatología . 4 (10): 525–33. doi : 10.1038 / ncprheum0898 . PMID 18762788 . S2CID 22686260 .
- ↑ a b c d e f g h Phang KF, Cho J, Lee W, Mak A (2018). "Osteoporosis inducida por glucocorticoides en el lupus eritematoso sistémico" . Práctica e Investigación en Reumatología . 3 : 205990211880251. doi : 10.1177 / 2059902118802510 .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad "Información de prescripción del médico de Medrol en EE. UU . " . Pfizer y Upjohn Company LLC . 2019-02-01 . Consultado el 10 de noviembre de 2020 .
- ^ a b c d e "Información de prescripción del médico de EE. UU. del vial multidosis de DEPO-MEDROL" . Pfizer. Julio de 2018.
- ^ a b c d e f "Información de prescripción del médico de EE. UU. del vial multidosis de SOLU-MEDROL" . Pfizer. Septiembre de 2020.
- ^ Garg DC, Wagner JG, Sakmar E, Weidler DJ, Albert KS (agosto de 1979). "Absorción rectal y oral de acetato de metilprednisolona". Farmacología clínica y terapéutica . 26 (2): 232–9. doi : 10.1002 / cpt1979262232 . hdl : 2027,42 / 117227 . PMID 455892 . S2CID 28001411 .
- ↑ a b c Szefler SJ, Ebling WF, Georgitis JW, Jusko WJ (1986). "Metilprednisolona versus farmacocinética de prednisolona en relación con la dosis en adultos". Revista europea de farmacología clínica . 30 (3): 323–9. doi : 10.1007 / BF00541537 . PMID 3732369 . S2CID 21550959 .
- ↑ a b c d e f g Fietta P, Fietta P, Delsante G (octubre de 2009). "Efectos del sistema nervioso central de los glucocorticoides naturales y sintéticos" . Psiquiatría y neurociencias clínicas . 63 (5): 613–22. doi : 10.1111 / j.1440-1819.2009.02005.x . PMID 19788629 . S2CID 28778979 .
- ^ Centro nacional de estadísticas de salud. Health, Estados Unidos, 2004 con Chartbook on Trends in the Health of Americans. Hyattsville, Maryland: 2004 https://www.cdc.gov/nchs/data/hus/hus04.pdf
- ^ a b c d e f g h Programa nacional de prevención y educación del asma (noviembre de 2007). "Informe del panel de expertos 3 (EPR-3): Directrices para el diagnóstico y tratamiento del asma-Informe resumido 2007" (PDF) . La Revista de Alergia e Inmunología Clínica . 120 (5 Suppl): S94-138. doi : 10.1016 / j.jaci.2007.09.043 . PMID 17983880 .
- ↑ a b c d Alangari AA (julio de 2010). "Acciones genómicas y no genómicas de los glucocorticoides en el asma" . Annals of Thoracic Medicine . 5 (3): 133–9. doi : 10.4103 / 1817-1737.65040 . PMC 2930650 . PMID 20835306 .
- ↑ a b Kaul A, Gordon C, Crow M, Touma Z, Urowitz MB, van Vollenhoven R, Ruiz-Irastorza G, Hughes G (2016). "Lupus eritematoso sistémico". Primers Nat Rev Dis . 2 : 16039. doi : 10.1038 / nrdp.2016.39 . PMID 27306639 . S2CID 2628865 .
- ^ a b c d e f Chan TM (enero de 2015). "Tratamiento de la nefritis lúpica severa: el nuevo horizonte". Reseñas de la naturaleza. Nefrología . 11 (1): 46–61. doi : 10.1038 / nrneph.2014.215 . PMID 25421826 . S2CID 19814440 .
- ^ a b c Habib, GS Efectos sistémicos de los corticosteroides intraarticulares. Clin. Rheumatol. 2009, 28, 749–756.
- ^ Johnston PC, Lansang MC, Chatterjee S, Kennedy L (marzo de 2015). "Inyecciones intraarticulares de glucocorticoides y su efecto sobre la función del eje hipotalámico-pituitario-adrenal (HPA)". Endocrino . 48 (2): 410–6. doi : 10.1007 / s12020-014-0409-5 . PMID 25182149 . S2CID 207363039 .
- ↑ a b c d e f Hopkins RL, Leinung MC (junio de 2005). "Síndrome de Cushing exógeno y abstinencia de glucocorticoides". Clínicas de Endocrinología y Metabolismo de Norteamérica . Síndrome de Cushing. 34 (2): 371–84, ix. doi : 10.1016 / j.ecl.2005.01.013 . PMID 15850848 .
- ^ "Descripción general de la osteoporosis | Centro de recursos nacional de osteoporosis y enfermedades óseas relacionadas de los NIH" . www.bones.nih.gov . Consultado el 7 de diciembre de 2020 .
- ^ Jeremiah MP, Unwin BK, Greenawald MH, Casiano VE (agosto de 2015). "Diagnóstico y tratamiento de la osteoporosis" . Médico de familia estadounidense . 92 (4): 261–8. PMID 26280231 .
- ↑ a b c d e f g h i Iliopoulou A, Abbas A, Murray R (mayo de 2013). "Cómo gestionar la retirada de la terapia con glucocorticoides". Prescriptor . 24 (10): 23–9. doi : 10.1002 / psb.1060 . S2CID 72082017 .
- ^ a b c "Metilprednisolona" . Información sobre medicamentos de MedlinePlus . Biblioteca Nacional de Medicina de EE. UU. Septiembre de 2017.
- ^ a b Joseph RM, Hunter AL, Ray DW, Dixon WG (agosto de 2016). "Terapia sistémica con glucocorticoides e insuficiencia suprarrenal en adultos: una revisión sistemática" . Seminarios de Artritis y Reumatismo . 46 (1): 133–41. doi : 10.1016 / j.semarthrit.2016.03.001 . PMC 4987145 . PMID 27105755 .
- ^ PubChem. "Metilprednisolona" . pubchem.ncbi.nlm.nih.gov . Consultado el 16 de noviembre de 2020 .
- ↑ a b c Elks J (14 de noviembre de 2014). El diccionario de drogas: datos químicos: datos químicos, estructuras y bibliografías . Saltador. págs. 811–. ISBN 978-1-4757-2085-3.
- ^ a b c Índice Nominum 2000: Directorio internacional de medicamentos . Taylor y Francis. 2000. págs. 675–. ISBN 978-3-88763-075-1.
- ^ "El Top 300 de 2021" . clincalc.com . Consultado el 5 de diciembre de 2020 .
- ^ Kosaka M, Yamazaki Y, Maruno T, Sakaguchi K, Sawaki S (enero de 2021). "Corticosteroides como terapia adyuvante en el tratamiento de la enfermedad por coronavirus 2019: informe de dos casos y revisión de la literatura" . Revista de Infección y Quimioterapia . 27 (1): 94–98. doi : 10.1016 / j.jiac.2020.09.007 . PMC 7480527 . PMID 32988730 .
- ^ Yousefifard M, Mohamed Ali K, Aghaei A, Zali A, Madani Neishaboori A, Zarghi A, et al. (Agosto de 2020). "Corticosteroides en el manejo de la enfermedad por coronavirus 2019 (COVID-19): una revisión sistémica y un metanálisis" . Revista Iraní de Salud Pública . 49 (8): 1411–1421. doi : 10.18502 / ijph.v49i8.3863 . PMC 7554375 . PMID 33083317 .
enlaces externos
- "Metilprednisolona" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- Alcoholes
- Sustancias químicas para medicina de emergencia
- Glucocorticoides
- Cetonas
- Marcas de Pfizer
- Pregnanes
- Medicamentos esenciales de la Organización Mundial de la Salud