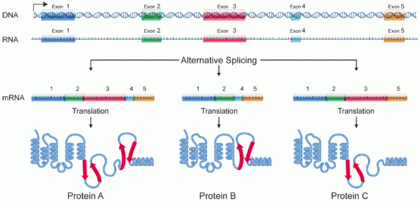
Una isoforma de proteína , o " variante de proteína ", [1] es un miembro de un conjunto de proteínas muy similares que se originan a partir de un solo gen o familia de genes y son el resultado de diferencias genéticas. [2] Si bien muchos desempeñan funciones biológicas iguales o similares, algunas isoformas tienen funciones únicas. Puede formarse un conjunto de isoformas de proteínas a partir de empalmes alternativos , uso de promotores variables u otras modificaciones postranscripcionales de un solo gen; Las modificaciones postraduccionales generalmente no se consideran. A través de mecanismos de empalme de ARN , ARNmtiene la capacidad de seleccionar diferentes segmentos codificantes de proteínas ( exones ) de un gen, o incluso diferentes partes de exones del ARN para formar diferentes secuencias de ARNm. Cada secuencia única produce una forma específica de proteína.
El descubrimiento de isoformas podría explicar la discrepancia entre el pequeño número de genes de regiones codificantes de proteínas revelados por el proyecto del genoma humano y la gran diversidad de proteínas observadas en un organismo: diferentes proteínas codificadas por el mismo gen podrían aumentar la diversidad del proteoma . Las isoformas a nivel de ARN se caracterizan fácilmente mediante estudios de transcripción de ADNc . Muchos genes humanos poseen isoformas de corte y empalme alternativas confirmadas . Se ha estimado que alrededor de 100.000 etiquetas de secuencia expresada ( EST ) pueden identificarse en seres humanos. [1] Las isoformas a nivel de proteína pueden manifestarse en la eliminación de dominios completos o bucles más cortos, generalmente ubicados en la superficie de la proteína.[3]
Definición [ editar ]
Un solo gen tiene la capacidad de producir múltiples proteínas que difieren tanto en estructura como en composición; [4] [5] este proceso está regulado por el empalme alternativo de ARNm, aunque no está claro en qué medida dicho proceso afecta la diversidad del proteoma humano, ya que la abundancia de isoformas de transcripción de ARNm no se correlaciona necesariamente con la abundancia de isoformas de proteínas. [6] La especificidad de las isoformas traducidas se deriva de la estructura / función de la proteína, así como del tipo de célula y la etapa de desarrollo durante la cual se producen. [4] [5] La determinación de la especificidad se vuelve más complicada cuando una proteína tiene múltiples subunidades y cada subunidad tiene múltiples isoformas.
Por ejemplo, la proteína quinasa 5 'activada por AMP (AMPK), una enzima que desempeña diferentes funciones en las células humanas, tiene 3 subunidades: [7]
- α, dominio catalítico, tiene dos isoformas: α1 y α2 que están codificadas por PRKAA1 y PRKAA2
- β, dominio regulador, tiene dos isoformas: β1 y β2 que están codificadas por PRKAB1 y PRKAB2
- γ, dominio regulador, tiene tres isoformas: γ1, γ2 y γ3 que están codificadas por PRKAG1 , PRKAG2 y PRKAG3
En el músculo esquelético humano, la forma preferida es α2β2γ1. [7] Pero en el hígado humano, la forma más abundante es α1β2γ1. [7]
Mecanismo [ editar ]
Los mecanismos principales que producen isoformas de proteínas son el empalme alternativo y el uso de promotores variables, aunque las modificaciones debidas a cambios genéticos, como mutaciones y polimorfismos , a veces también se consideran isoformas distintas. [8]
El empalme alternativo es el principal proceso de modificación postranscripcional que produce isoformas de transcripción de ARNm y es un mecanismo molecular importante que puede contribuir a la diversidad de proteínas. [5] El espliceosoma , una ribonucleoproteína grande , es la máquina molecular dentro del núcleo responsable de la escisión y ligación del ARN , eliminando segmentos codificantes no proteicos ( intrones ). [9]
Debido a que el empalme es un proceso que ocurre entre la transcripción y la traducción , sus efectos primarios se han estudiado principalmente mediante técnicas genómicas ; por ejemplo, se han utilizado análisis de microarrays y secuenciación de ARN para identificar transcripciones empalmadas alternativamente y medir su abundancia. [8] La abundancia de transcripciones se usa a menudo como un proxy de la abundancia de isoformas de proteínas, aunque los experimentos proteómicos que utilizan electroforesis en gel y espectrometría de masas han demostrado que la correlación entre la transcripción y los recuentos de proteínas es a menudo baja y que una isoforma de proteína suele ser dominante. [10]Un estudio de 2015 afirma que la causa de esta discrepancia probablemente ocurre después de la traducción, aunque el mecanismo es esencialmente desconocido. [11] En consecuencia, aunque el empalme alternativo ha sido implicado como un vínculo importante entre la variación y la enfermedad, no hay evidencia concluyente de que actúe principalmente produciendo nuevas isoformas de proteínas. [10]
El empalme alternativo generalmente describe un proceso estrictamente regulado en el que la maquinaria de empalme genera intencionalmente transcripciones alternativas. Sin embargo, estas transcripciones también se producen mediante errores de empalme en un proceso llamado "empalme ruidoso" y también se traducen potencialmente en isoformas de proteínas. Aunque se cree que ~ 95% de los genes multi-exónicos están empalmados alternativamente, un estudio sobre empalmes ruidosos observó que la mayoría de las diferentes transcripciones de baja abundancia son ruido, y predice que la mayoría de las isoformas de proteínas y transcripciones alternativas presentes en una célula no son funcionalmente pertinente. [12]
Otros pasos reguladores transcripcionales y postranscripcionales también pueden producir diferentes isoformas de proteínas. [13] El uso de promotor variable ocurre cuando la maquinaria transcripcional de una célula ( ARN polimerasa , factores de transcripción y otras enzimas ) comienza la transcripción en diferentes promotores, la región del ADN cerca de un gen que sirve como sitio de unión inicial, lo que resulta en una modificación leve transcripciones e isoformas de proteínas.
Características [ editar ]
Generalmente, una isoforma de proteína se etiqueta como la secuencia canónica basándose en criterios como su prevalencia y similitud con secuencias ortólogas —o funcionalmente análogas— de otras especies. [14] Se supone que las isoformas tienen propiedades funcionales similares, ya que la mayoría tienen secuencias similares y comparten algunos con la mayoría de los exones con la secuencia canónica. Sin embargo, algunas isoformas muestran una divergencia mucho mayor (por ejemplo, a través del empalme trans ) y pueden compartir pocos o ningún exón con la secuencia canónica. Además, pueden tener diferentes efectos biológicos —por ejemplo, en un caso extremo, la función de una isoforma puede promover la supervivencia celular, mientras que otra promueve la muerte celular— o pueden tener funciones básicas similares pero diferir en su localización subcelular.[15] Sin embargo, un estudio de 2016 caracterizó funcionalmente todas las isoformas de 1492 genes y determinó que la mayoría de las isoformas se comportan como "aloformas funcionales". Los autores llegaron a la conclusión de que las isoformas se comportan como proteínas distintas después de observar que las funciones de la mayoría de las isoformas no se superponen. [16] Debido a que el estudio se realizó en células in vitro , no se sabe si las isoformas en el proteoma humano expresado comparten estas características. Además, debido a que la función de cada isoforma generalmente debe determinarse por separado, la mayoría de las isoformas identificadas y predichas todavía tienen funciones desconocidas.
Concepto relacionado [ editar ]
Glicoforma [ editar ]
Una glicoforma es una isoforma de una proteína que difiere solo con respecto al número o tipo de glicano unido . Las glicoproteínas a menudo constan de varias glicoformas diferentes, con alteraciones en el sacárido u oligosacárido adjunto . Estas modificaciones pueden resultar de diferencias en la biosíntesis durante el proceso de glicosilación , o debido a la acción de glicosidasas o glicosiltransferasas . Las glicoformas pueden detectarse mediante un análisis químico detallado de las glicoformas separadas, pero es más conveniente detectarlas mediante una reacción diferencial con lectinas , como encromatografía de afinidad de lectina y electroforesis de afinidad de lectina . Ejemplos típicos de glicoproteínas que consisten en glicoformas son las proteínas sanguíneas como orosomucoide , antitripsina y haptoglobina . Se observa una variación de glicoforma inusual en la molécula de adhesión celular neuronal, NCAM, que involucra ácidos polisiálicos, PSA .
Ejemplos [ editar ]
- G-actina : a pesar de su naturaleza conservada, tiene un número variable de isoformas (al menos seis en mamíferos).
- La creatina quinasa , cuya presencia en la sangre puede utilizarse como ayuda en el diagnóstico de infarto de miocardio , existe en 3 isoformas.
- La hialuronano sintasa , la enzima responsable de la producción de hialuronano, tiene tres isoformas en las células de los mamíferos.
- La UDP-glucuronosiltransferasa , una superfamilia de enzimas responsable de la vía de desintoxicación de muchos fármacos, contaminantes ambientales y compuestos endógenos tóxicos, tiene 16 isoformas conocidas codificadas en el genoma humano. [17]
- G6PDA: la proporción normal de isoformas activas en las células de cualquier tejido se comparte 1: 1 con G6PDG. Ésta es precisamente la proporción de isoformas normal en la hiperplasia. Solo una de estas isoformas se encuentra durante la neoplasia. [18]
La monoamino oxidasa , una familia de enzimas que catalizan la oxidación de monoaminas, existe en dos isoformas, MAO-A y MAO-B.
Ver también [ editar ]
- Isoforma genética
Referencias [ editar ]
- ↑ a b Brett D, Pospisil H, Valcárcel J, Reich J, Bork P (enero de 2002). "Empalme alternativo y complejidad del genoma". Genética de la naturaleza . 30 (1): 29–30. doi : 10.1038 / ng803 . PMID 11743582 .
- ^ Schlüter H, Apweiler R, Holzhütter HG, Jungblut PR (septiembre de 2009). "Encontrar el camino en la proteómica: una nomenclatura de especies de proteínas" . Revista Central de Química . 3 : 11. doi : 10.1186 / 1752-153X-3-11 . PMC 2758878 . PMID 19740416 .
- ^ Kozlowski, L .; Orlowski, J .; Bujnicki, JM (2012). "Predicción de estructura para proteínas empalmadas alternativamente". Empalme alternativo de pre-ARNm . pag. 582. doi : 10.1002 / 9783527636778.ch54 . ISBN 9783527636778.
- ↑ a b Andreadis A, Gallego ME, Nadal-Ginard B (1 de enero de 1987). "Generación de diversidad de isoformas de proteínas por empalme alternativo: implicaciones mecánicas y biológicas". Revisión anual de biología celular . 3 (1): 207–42. doi : 10.1146 / annurev.cb.03.110187.001231 . PMID 2891362 .
- ↑ a b c Breitbart RE, Andreadis A, Nadal-Ginard B (1 de enero de 1987). "Empalme alternativo: un mecanismo ubicuo para la generación de múltiples isoformas de proteínas a partir de genes únicos". Revisión anual de bioquímica . 56 (1): 467–95. doi : 10.1146 / annurev.bi.56.070187.002343 . PMID 3304142 .
- ^ Liu Y, Beyer A, Aebersold R (abril de 2016). "Sobre la dependencia de los niveles de proteína celular en la abundancia de ARNm" . Celular . 165 (3): 535–50. doi : 10.1016 / j.cell.2016.03.014 . PMID 27104977 .
- ↑ a b c Dasgupta B, Chhipa RR (marzo de 2016). "Evolución de las lecciones sobre el papel complejo de AMPK en la fisiología normal y el cáncer" . Tendencias en Ciencias Farmacológicas . 37 (3): 192–206. doi : 10.1016 / j.tips.2015.11.007 . PMC 4764394 . PMID 26711141 .
- ↑ a b Kornblihtt AR, Schor IE, Alló M, Dujardin G, Petrillo E, Muñoz MJ (marzo de 2013). "Empalme alternativo: un paso fundamental entre la transcripción eucariota y la traducción". Nature Reviews Biología celular molecular . 14 (3): 153–65. doi : 10.1038 / nrm3525 . PMID 23385723 .
- ↑ Lee Y, Rio DC (1 de enero de 2015). "Mecanismos y regulación del empalme alternativo de pre-ARNm" . Revisión anual de bioquímica . 84 (1): 291–323. doi : 10.1146 / annurev-biochem-060614-034316 . PMC 4526142 . PMID 25784052 .
- ^ a b Tress ML, Abascal F, Valencia A (febrero de 2017). "El empalme alternativo puede no ser la clave para la complejidad del proteoma" . Tendencias en Ciencias Bioquímicas . 42 (2): 98-110. doi : 10.1016 / j.tibs.2016.08.008 . PMC 6526280 . PMID 27712956 .
- ^ Batalla A, Khan Z, Wang SH, Mitrano A, Ford MJ, Pritchard JK, Gilad Y (febrero de 2015). "Variación genómica. Impacto de la variación reguladora de ARN a proteína" . Ciencia . 347 (6222): 664–7. doi : 10.1126 / science.1260793 . PMC 4507520 . PMID 25657249 .
- ^ Pickrell JK, Pai AA, Gilad Y, Pritchard JK (diciembre de 2010). "El empalme ruidoso impulsa la diversidad de isoformas de ARNm en células humanas" . PLoS Genetics . 6 (12): e1001236. doi : 10.1371 / journal.pgen.1001236 . PMC 3000347 . PMID 21151575 .
- ^ Smith LM, Kelleher NL (marzo de 2013). "Proteoforma: un solo término que describe la complejidad de la proteína" . Métodos de la naturaleza . 10 (3): 186–7. doi : 10.1038 / nmeth.2369 . PMC 4114032 . PMID 23443629 .
- ^ Li HD, Menon R, Omenn GS, Guan Y (diciembre de 2014). "Revisando la identificación de isoformas de empalme canónicas a través de la integración de pruebas genómicas y proteómicas funcionales" (PDF) . Proteómica . 14 (23-24): 2709-18. doi : 10.1002 / pmic.201400170 . PMC 4372202 . PMID 25265570 .
- ^ Sundvall M, Veikkolainen V, Kurppa K, Salah Z, Tvorogov D, van Zoelen EJ, Aqeilan R, Elenius K (diciembre de 2010). "Muerte celular o supervivencia promovida por isoformas alternativas de ErbB4" . Biología molecular de la célula . 21 (23): 4275–86. doi : 10.1091 / mbc.E10-04-0332 . PMC 2993754 . PMID 20943952 .
- ^ Yang X, Coulombe-Huntington J, Kang S, Sheynkman GM, Hao T, Richardson A, et al. (Febrero de 2016). "Amplia expansión de las capacidades de interacción de proteínas por empalme alternativo" . Celular . 164 (4): 805-17. doi : 10.1016 / j.cell.2016.01.029 . PMC 4882190 . PMID 26871637 .
- ^ Barre L, Fournel-Gigleux S, Finel M, Netter P, Magdalou J, Ouzzine M (marzo de 2007). "Especificidad de sustrato de la UDP-glucuronosiltransferasa humana UGT2B4 y UGT2B7. Identificación de un residuo de aminoácido aromático crítico en la posición 33" . La revista FEBS . 274 (5): 1256–64. doi : 10.1111 / j.1742-4658.2007.05670.x . PMID 17263731 .
- ^ Patoma, fundamentos de patología
Enlaces externos [ editar ]
| Busque isoforma en Wiktionary, el diccionario gratuito. |
- Isoformas de proteínas de entrada MeSH
- Definiciones Isoforma