 | |
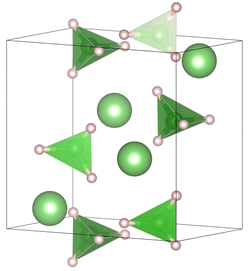 Celda unitaria de borohidruro de litio a temperatura ambiente | |
| Nombres | |
|---|---|
| Nombre IUPAC Tetrahidridoborato de litio (1–) | |
| Otros nombres Hidroborato de litio, tetrahidroborato de litio borato (1-), tetrahidro-, litio, boranato de litio | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.037.277 |
PubChem CID | |
| Número RTECS |
|
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| LiBH 4 | |
| Masa molar | 21,784 g / mol |
| Apariencia | Blanco sólido |
| Densidad | 0,666 g / cm 3 [1] |
| Punto de fusion | 268 ° C (514 ° F; 541 K) |
| Punto de ebullición | 380 ° C (716 ° F; 653 K) se descompone |
| reacciona | |
| Solubilidad en éter | 2,5 g / 100 ml |
| Estructura [2] | |
| ortorrómbico | |
| Pnma | |
a = 7,17858 (4), b = 4,43686 (2), c = 6,80321 (4) | |
Volumen de celosía ( V ) | 216.685 (3) A 3 |
Unidades de fórmula ( Z ) | 4 |
| [4] B | |
| Termoquímica | |
Capacidad calorífica ( C ) | 82,6 J / mol K |
Entropía molar estándar ( S | 75,7 J / mol K |
| -198,83 kJ / mol | |
| Riesgos | |
| > 180 ° C (356 ° F; 453 K) | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El borohidruro de litio (LiBH 4 ) es un borohidruro y se conoce en síntesis orgánica como agente reductor de ésteres . Aunque es menos común que el borohidruro de sodio relacionado , la sal de litio ofrece algunas ventajas, siendo un agente reductor más fuerte y altamente soluble en éteres, mientras que sigue siendo más segura de manejar que el hidruro de litio y aluminio . [3]
Preparación
El borohidruro de litio se puede preparar mediante la reacción de metátesis que se produce al triturar con bolas el borohidruro de sodio y el bromuro de litio más comúnmente disponibles : [4]
- NaBH 4 + LiBr → NaBr + LiBH 4
Alternativamente, se puede sintetizar tratando trifluoruro de boro con hidruro de litio en éter dietílico : [5]
- BF 3 + 4 LiH → LiBH 4 + 3 LiF
Reacciones
El borohidruro de litio es un agente reductor más fuerte que el borohidruro de sodio . [6] En mezclas de metanol y éter dietílico , el borohidruro de litio puede reducir los ésteres a alcoholes y las amidas primarias a aminas . [7] Por el contrario, estos sustratos no se ven afectados por el borohidruro de sodio. La reactividad mejorada se atribuye a la polarización del sustrato de carbonilo por complejación con el catión de litio. [3]
Quimioselectividad
El uso de borohidruro de litio es particularmente ventajoso en algunas preparaciones debido a su mayor quimioselectividad con respecto a otros agentes reductores populares tales como hidruro de litio y aluminio . Por ejemplo, a diferencia del hidruro de litio y aluminio, el borohidruro de litio reducirá los ésteres, nitrilos , lactonas , amidas primarias y epóxidos mientras evita los grupos nitro , ácidos carbámicos , haluros de alquilo y amidas secundarias / terciarias . [7]
Generación de hidrógeno
El borohidruro de litio reacciona con el agua para producir hidrógeno. Esta reacción se puede utilizar para la generación de hidrógeno. [8]
Almacenamiento de energía


El borohidruro de litio es reconocido como uno de los portadores de energía química de mayor densidad energética . Aunque actualmente no tiene importancia práctica, el sólido liberará 65 MJ / kg de calor tras el tratamiento con oxígeno atmosférico. Puesto que tiene una densidad de 0,67 g / cm 3 , la oxidación de borohidruro de litio líquido da 43 MJ / L . En comparación, la gasolina proporciona 44 MJ / kg (o 35 MJ / L), mientras que el hidrógeno líquido proporciona 120 MJ / kg (o 8,0 MJ / L). [nb 1] La alta densidad de energía específica del borohidruro de litio lo ha convertido en un candidato atractivo para ser propuesto como combustible para automóviles y cohetes, pero a pesar de la investigación y la promoción, no se ha utilizado ampliamente. Como ocurre con todos los portadores de energía basados en hidruros químicos, el borohidruro de litio es muy complejo de reciclar (es decir, recargar) y, por lo tanto, adolece de una baja eficiencia de conversión de energía . Si bien las baterías, como las de iones de litio, tienen una densidad de energía de hasta 0,72 MJ / kg y 2,0 MJ / L, su eficiencia de conversión de CC a CC puede llegar hasta el 90%. [ cita requerida ] En vista de la complejidad de los mecanismos de reciclaje de hidruros metálicos, [9] Estas elevadas eficiencias de conversión de energía no son prácticas con la tecnología actual.
| Sustancia | Energía específica MJ / kg | Densidad g / cm 3 | Densidad de energía MJ / L |
|---|---|---|---|
| LiBH 4 | 65,2 | 0,666 | 43,4 |
| Gasolina regular | 44 | 0,72 | 34,8 |
| Hidrógeno líquido | 120 | 0.0708 | 8 |
| batería de iones de litio | 0,72 | 2.8 | 2 |
Ver también
- Hidruro de litio y aluminio
- Borohidruro de sodio
- Pila de combustible de borohidruro directo
Notas
- ^ La mayor relación entre la densidad de energía y la energía específica del hidrógeno se debe a la muy baja densidad de masa (0,071 g / cm 3 ).
Referencias
- ^ Página de detalles del producto Sigma-Aldrich
- ^ J-Ph. Soulie, G. Renaudin, R. Cerny, K. Yvon (18 de noviembre de 2002). "Borohidruro de litio LiBH 4 : I. Estructura cristalina". Revista de aleaciones y compuestos . 346 (1–2): 200–205. doi : 10.1016 / S0925-8388 (02) 00521-2 .CS1 maint: varios nombres: lista de autores ( enlace )
- ^ a b Luca Banfi, Enrica Narisano, Renata Riva, Ellen W. Baxter "Borohidruro de litio" e-EROS Enciclopedia de reactivos para síntesis orgánica, 2001 John Wiley & Sons. doi : 10.1002 / 047084289X.rl061.pub2 .
- ^ Peter Rittmeyer, Ulrich Wietelmann "Hidruros" en Enciclopedia de química industrial de Ullmann, 2002, Wiley-VCH, Weinheim. doi : 10.1002 / 14356007.a13_199
- ^ Brauer, Georg (1963). Manual de Química Inorgánica Preparativa Vol. 1, 2ª Ed . Nueva York: Academic Press. pag. 775. ISBN 978-0121266011.
- ^ Barrett, Anthony GM (1991). "Reducción de derivados de ácidos carboxílicos a alcoholes, éteres y aminas". En Trost, Barry; Fleming, Ian; Schreiber, Stuart (eds.). Reducción: selectividad, estrategia y eficiencia en la química orgánica moderna (1ª ed.). Nueva York: Pergamon Press. pag. 244. doi : 10.1016 / B978-0-08-052349-1.00226-2 . ISBN 9780080405995.
- ^ a b Ookawa, Atsuhiro; Soai, Kenso (1986). "Disolventes mixtos que contienen metanol como medio de reacción útil para reducciones quimioselectivas únicas dentro del borohidruro de litio". La Revista de Química Orgánica . 51 (21): 4000–4005. doi : 10.1021 / jo00371a017 .
- ^ Y. Kojima et al., "Generación de hidrógeno por reacción de hidrólisis de borohidruro de litio", International Journal of Hydrogen Energy, 29 (12): 1213-1217, agosto de 2004; DOI: 10.1016 / j.ijhydene.2003.12.009 enlace sciencedirect
- ^ Patente de EE. UU. 4002726 (1977) Reciclaje de borohidruro de litio a partir de borato de litio a través de un intermedio de borato de metilo