 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Metalutin, otros |
| Otros nombres | Normetandrona; Metilestrenolona; Metiloestrenolona; Metilnortestosterona; Normetiltestosterona; Normethandrolona; Normetisterona; Metilnandrolona; NMT; 17α-Metil-19-nortestosterona; 17α-Metilestr-4-en-17β-ol-3-ona; P-6051; RU-598; NSC-10039 |
| Vías de administración | Oral |
| Clase de droga | Progestágeno ; Progestina ; Andrógeno ; Esteroide anabólico |
| Código ATC | |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.007.440 |
| Datos químicos y físicos | |
| Fórmula | C 19 H 28 O 2 |
| Masa molar | 288,431 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
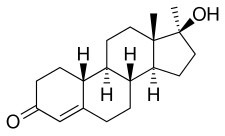
Normethandrone , también conocida como metlestrenolona o metilnortestosterona y vendida bajo la marca Metalutin entre otros, es un medicamento de progestina y andrógeno / esteroide anabólico (AAS) que se usa en combinación con un estrógeno en el tratamiento de la amenorrea y los síntomas de la menopausia en mujeres. [1] [2] [3] [4] Se toma por vía oral . [5]
Los efectos secundarios de la normendrona incluyen síntomas de masculinización como acné , aumento del crecimiento del cabello , cambios en la voz y aumento del deseo sexual . [6] También puede causar daño hepático . [7] Normethandrone es una progestina, o un progestágeno sintético , y por lo tanto es un agonista del receptor de progesterona , el objetivo biológico de progestágenos como la progesterona . [5] También es un AAS sintético y, por lo tanto, es unagonista del receptor de andrógenos , el objetivo biológico de andrógenos como la testosterona y la dihidrotestosterona (DHT). [4] [8] También tiene alguna actividad estrogénica y ninguna otra actividad hormonal importante . [9] [1] [3]
La normethandrone se introdujo para uso médico en 1957. [10] Está disponible sólo en unos pocos países, incluidos Brasil , Indonesia y Venezuela , y sólo está disponible en combinación con metilestradiol o valerato de estradiol . [2] [1]
Usos médicos [ editar ]
Normethandrone se usa en combinación con un estrógeno , ya sea metilestradiol o valerato de estradiol , en el tratamiento de la amenorrea y los síntomas de la menopausia en mujeres. [1] [2] [11] También se ha utilizado para tratar la dismenorrea en mujeres. [12] Normethandrone se ha utilizado con éxito para inhibir la libido en hombres con desviación sexual . [13] Aunque la normendrona puede clasificarse como un AAS y tiene fuertes efectos en dosis suficientemente altas, no se usa típicamente como tal y, en cambio, se usa médicamente solo como progestina.[3] [1] [4] Esto se debe a que es muy progestágeno en comparación. [4]
| Ruta | Medicamento | Principales marcas | Formulario | Dosis |
|---|---|---|---|---|
| Oral | Undecanoato de testosterona | Andriol, Jatenzo | Cápsula | 40 a 80 mg 1 vez / 1 a 2 días |
| Metiltestosterona | Metandren, Estratest | Tableta | 0,5 a 10 mg / día | |
| Fluoximesterona | Halotestin | Tableta | 1 a 2,5 mg 1 vez / 1 a 2 días | |
| Normethandrone a | Ginecósido | Tableta | 5 mg / día | |
| Tibolona | Livial | Tableta | 1,25 a 2,5 mg / día | |
| Prasterona ( DHEA ) b | - | Tableta | 10-100 mg / día | |
| Sublingual | Metiltestosterona | Metandren | Tableta | 0,25 mg / día |
| Transdérmico | Testosterona | Intrinsa | Parche | 150–300 μg / día |
| AndroGel | Gel, crema | 1 a 10 mg / día | ||
| Vaginal | Prasterona ( DHEA ) | Intrarosa | Insertar | 6,5 mg / día |
| Inyección | Propionato de testosterona a | Testoviron | Solución de aceite | 25 mg 1 vez / 1 a 2 semanas |
| Enantato de testosterona | Delatestryl, Primodian Depot | Solución de aceite | 25-100 mg 1 vez / 4-6 semanas | |
| Cipionato de testosterona | Depo-testosterona, Depo-Testadiol | Solución de aceite | 25-100 mg 1 vez / 4-6 semanas | |
| Isobutirato de testosterona a | Femandren M, folivirina | Suspensión acuosa | 25 a 50 mg 1 vez / 4 a 6 semanas | |
| Ésteres de testosterona mixtos | Climacteron a | Solución de aceite | 150 mg 1 vez / 4 a 8 semanas | |
| Omnadren, Sustanon | Solución de aceite | 50–100 mg 1 vez / 4–6 semanas | ||
| Decanoato de nandrolona | Deca-Durabolin | Solución de aceite | 25–50 mg 1 vez / 6–12 semanas | |
| Enantato de prasterona a | Depósito Gynodian | Solución de aceite | 200 mg 1 vez / 4 a 6 semanas | |
| Implante | Testosterona | Testopel | Bolita | 50-100 mg 1 vez / 3-6 meses |
| Notas: Las mujeres premenopáusicas producen alrededor de 230 ± 70 μg de testosterona por día (6,4 ± 2,0 mg de testosterona por 4 semanas), con un rango de 130 a 330 μg por día (3,6 a 9,2 mg por 4 semanas). Notas a pie de página: a = Principalmente descontinuado o no disponible. b = Sin receta . Fuentes: Ver plantilla. | ||||
| Ruta | Medicamento | Formulario | Dosis | |
|---|---|---|---|---|
| Oral | Metiltestosterona | Tableta | 30-200 mg / día | |
| Fluoximesterona | Tableta | 10 a 40 mg 3 veces al día | ||
| Calusterone | Tableta | 40 a 80 mg 4 veces al día | ||
| Normethandrone | Tableta | 40 mg / día | ||
| Bucal | Metiltestosterona | Tableta | 25-100 mg / día | |
| Inyección ( IM o SC ) | Propionato de testosterona | Solución de aceite | 50-100 mg 3 veces por semana | |
| Enantato de testosterona | Solución de aceite | 200–400 mg 1 vez / 2–4 semanas | ||
| Cipionato de testosterona | Solución de aceite | 200–400 mg 1 vez / 2–4 semanas | ||
| Ésteres de testosterona mixtos | Solución de aceite | 250 mg 1x / semana | ||
| Metandriol | Suspensión acuosa | 100 mg 3 veces / semana | ||
| Androstanolona ( DHT ) | Suspensión acuosa | 300 mg 3 veces / semana | ||
| Propionato de drostanolona | Solución de aceite | 100 mg 1 a 3 veces por semana | ||
| Enantato de metenolona | Solución de aceite | 400 mg 3 veces / semana | ||
| Decanoato de nandrolona | Solución de aceite | 50–100 mg 1 vez / 1–3 semanas | ||
| Fenilpropionato de nandrolona | Solución de aceite | 50-100 mg / semana | ||
| Nota: Las dosis no son necesariamente equivalentes. Fuentes: Ver plantilla. | ||||
Formas disponibles [ editar ]
La normendrona se comercializa en combinación con metilestradiol en forma de comprimidos orales que contienen 5 mg de normendrona y 0,3 mg de metilestradiol. [11] [14]
Efectos secundarios [ editar ]
La normendrona se ha asociado con síntomas de masculinización y hepatotoxicidad . [6] [7] [15]
Farmacología [ editar ]
Farmacodinámica [ editar ]
Normethandrone muestra una alta actividad progestágena . [5] Con la administración sublingual en mujeres, tiene al menos 150 veces la potencia de la progesterona sublingual y 50 veces la potencia de la etisterona sublingual . [5] También tiene 10 veces la potencia de la progesterona inyectada a través de esta ruta. [5] La potencia oral de la normendrona en términos de transformación endometrial es similar a la de la noretisterona . [16] [17] Se ha informado que inhibe la ovulación en las mujeres. [18]
Además de su actividad progestágena, la normendrona tiene actividad anabólica y androgénica y puede producir efectos asociados a esta actividad. [1] [4] Tiene una alta proporción de actividad anabólica a androgénica. [19] La potencia anabólica de la normethandrone es similar a la de la norethandrolone y es mucho mayor que la de la nandrolone o metandienone . [8] También es mayor que la del etilestrenol . [8] Se ha descubierto que la normendrona aumenta la retención de nitrógeno., una medida del efecto anabólico, a una dosis de 30 mg / día. [20] De manera análoga a la nandrolona y la noretandrolona , la 5α-dihidronormendrona , el metabolito 5α reducido de la normendrona, muestra una afinidad reducida por el receptor de andrógenos en relación con la normendrona. [21] [22] Su afinidad por el receptor de andrógenos es específicamente alrededor del 33 al 60% de la de la normendrona. [21]
Normethandrone tiene actividad estrogénica a través de la aromatización en metilestradiol . [3]
| Compuesto | PR | Arkansas | ER | GRAMO | SRES | SHBG | CBG |
|---|---|---|---|---|---|---|---|
| Normethandrone | 75-125 | 125-150 | <1 | 1–5 | <1 | ? | ? |
| 5α-dihidronormendrona | 15-25 | 50–75 | ? | <1 | ? | ? | ? |
| Notas: Los valores son porcentajes (%). Los ligandos de referencia (100%) fueron progesterona para el PR , testosterona para el AR , estradiol para el RE , dexametasona para el GR y aldosterona para el MR . Fuentes: Ver plantilla. | |||||||
Farmacocinética [ editar ]
La normendrona es metabolizada por la aromatasa a metilestradiol en pequeñas cantidades, de manera similar a la metiltestosterona y la metandienona . [3] [23] [24] Los metabolitos de la normendrona no se han estudiado bien, pero la 5α-dihidronormendrona es un metabolito probable formado por la 5α-reductasa . [25] [26]
Se ha revisado la farmacocinética de normendrona. [27]
Química [ editar ]
Normethandrone, también conocido como 17α-metil-19-nortestosterona o como 17α-metilestr-4-en-17β-ol-3-ona, es un sintético estrano esteroide y un 17α-alquilados derivado de nandrolona (19-nortestosterona; 19- NUEVO TESTAMENTO). Es específicamente la 17α- metil derivado de nandrolona, así como la variante 17α-metil de norentandrolona (17α-etil-19-NT) y noretisterona (17α-etinil-19-NT). [28]
Síntesis [ editar ]
Se han publicado síntesis químicas de normendrona. [27]
Historia [ editar ]
La normendrona se comercializa para uso médico desde 1957. [10] La combinación de normendrona y metilestradiol se introdujo al menos en 1966. [14]
Sociedad y cultura [ editar ]
Nombres genéricos [ editar ]
A Normethandrone no se le ha asignado una DCI u otras denominaciones formales. [28] [29] [2] También se conoce como metlestrenolona , metilnortestosterona , normethandrolona y normetisterona . [28] [29] [2]
Nombres de marca [ editar ]
Las marcas de normethandrone incluyen Batynid, Ginecosid, Ginecoside, Gynomin, Lutenin, Matronal, Mediol, Metalutin, Methalutin, Orgasteron, Orosteron y Renodiol. [28] [29] [2] [1] [30] [11]
Disponibilidad [ editar ]
La normethandrone se comercializa en Brasil , Indonesia y Venezuela en combinación con metilestradiol o valerato de estradiol . [2] [1]
Referencias [ editar ]
- ^ a b c d e f g h https://www.medicinescomplete.com/about/
- ^ a b c d e f g https://www.drugs.com/international/normethandrone.html
- ↑ a b c d e Friedl KE (1990). "Reevaluación de los riesgos para la salud asociados con el uso de altas dosis de esteroides androgénicos orales e inyectables". NIDA Res. Monogr . 102 : 142–77. PMID 1964199 .
- ^ a b c d e H.-L. Krüskemper (22 de octubre de 2013). Esteroides anabólicos . Elsevier. págs. 10–. ISBN 978-1-4832-6504-9.
- ↑ a b c d e Ferin J (1956). "Una nueva sustancia con actividad progestacional; ensayos comparativos en mujeres ovariectomizadas; resultados clínicos". Acta Endocrinol . 22 (4): 303-17. doi : 10.1530 / acta.0.0220303 . PMID 13354223 .
- ↑ a b Lundberg, PO (1962). "Profilaxis de la migraña con progestágenos". Revista europea de endocrinología . 40 (4 supl.): S5 – S22. doi : 10.1530 / acta.0.040S0005 . ISSN 0804-4643 .
- ↑ a b Delorimier AA, Gordan GS, Lowe RC, Carbone JV (1965). "Metiltestosterona, esteroides relacionados y función hepática". Arco. Interno. Med . 116 (2): 289–94. doi : 10.1001 / archinte.1965.03870020129023 . PMID 14315662 .
- ↑ a b c Brueggemeier, Robert W. (2006). "Hormonas sexuales (masculinas): análogos y antagonistas". Enciclopedia de Biología Celular Molecular y Medicina Molecular . pag. 42. doi : 10.1002 / 3527600906.mcb.200500066 . ISBN 3527600906.
- ^ Erich Heftmann (1970). Bioquímica de esteroides . Prensa académica. pag. 72. ISBN 9780123366504.
Normethandrone (Fig. 49) es un derivado de la 19-nortestosterona que tiene actividad progestacional así como androgénica y anabólica.
- ^ a b Estados Unidos. Oficina de Patentes (1957). Gaceta Oficial de la Oficina de Patentes de Estados Unidos . Oficina de Patentes de Estados Unidos.
- ^ a b c Medicamentos no listados . Sección Farmacéutica, Asociación de Bibliotecas Especiales. 1982.
Batynid.
C. Cada gragea contiene: normendrona, 5 mg;
y metilestradiol, 0,3 mg.
E. (Anteriormente) Gynaekosid.
M. Boehringer Biochemia, Florencia.
A. estrogénico;
Rx de amenorrea secundaria.
R. Notiz Med Farm 32; 295, noviembre-diciembre del 81.
- ^ Begni-Calvet, D. (1959). "Dos propiedades de la metilestrenolona (17-alfa-metil-19-nortestosterona): su eficacia en el tratamiento de la dismenorrea, su acción anabólica". Gynécologie Pratique . 10 : 261-272. PMID 13798272 .
- ^ Servais, J. (1973). "Un estudio clínico de casos de trastornos psicosexuales en hombres tratados por un inhibidor de la libido: metilestrenolona". Archivos de comportamiento sexual . 2 (4): 387–390. doi : 10.1007 / BF01541012 . ISSN 0004-0002 . S2CID 145090184 .
- ↑ a b Akingba JB, Ayodeji EA (febrero de 1966). "La amenorrea como síntoma principal del coriocarcinoma". J Obstet Gynaecol Br Commonw . 73 (1): 153–5. doi : 10.1111 / j.1471-0528.1966.tb05137.x . PMID 5948541 . S2CID 38008851 .
- ^ Feldman, Elaine Bossak; Carter, Anne C .; Kossa, Jane L .; Mccarrick, James F .; Schwartz, Harold L. (1960). "Efectos endocrinológicos y metabólicos de 17α-metil-19-nortestosterona en mujeres". La Revista de Endocrinología Clínica y Metabolismo . 20 (6): 842–857. doi : 10.1210 / jcem-20-6-842 . ISSN 0021-972X . PMID 13822027 .
- ↑ Horský, Jan; Presl, Jiří (1981). "Tratamiento hormonal de los trastornos del ciclo menstrual" . En J. Horsky; J. Presl (eds.). Función ovárica y sus trastornos: diagnóstico y terapia . Springer Science & Business Media. págs. 309–332. doi : 10.1007 / 978-94-009-8195-9_11 . ISBN 978-94-009-8195-9.
- ^ Boschann HW (julio de 1958). "Observaciones del papel de los agentes progestacionales en los trastornos ginecológicos humanos y las complicaciones del embarazo". Ana. NY Acad. Sci . 71 (5): 727–52. doi : 10.1111 / j.1749-6632.1958.tb46803.x . PMID 13583829 .
- ^ Camerino, B .; Sala, G. (1960). "Esteroides anabólicos". Fortschritte der Arzneimittelforschung / Progresos en la investigación de medicamentos / Progrès des recherches pharmaceutiques . Fortschritte der Arzneimittelforschung. Progresos en la investigación de fármacos. Progres des Recherches Pharmaceutiques . 2 . págs. 71-134. doi : 10.1007 / 978-3-0348-7038-2_2 . ISBN 978-3-0348-7040-5. PMID 14448579 .
- ^ Charles D. Kochakian (6 de diciembre de 2012). Esteroides anabólico-androgénicos . Springer Science & Business Media. págs. 379–. ISBN 978-3-642-66353-6.
- ^ Ralph I. Dorfman (5 de diciembre de 2016). Actividad esteroidea en animales experimentales y en el hombre . Ciencia de Elsevier. págs. 68–. ISBN 978-1-4832-7300-6.
- ↑ a b Ojasoo T, Delettré J, Mornon JP, Turpin-VanDycke C, Raynaud JP (1987). "Hacia el mapeo de los receptores de progesterona y andrógenos". J. Steroid Biochem . 27 (1-3): 255–69. doi : 10.1016 / 0022-4731 (87) 90317-7 . PMID 3695484 .
- ^ Behre HM, Kliesch S, Lemcke B, von Eckardstein S, Nieschlag E (diciembre de 2001). "La supresión de la espermatogénesis a azoospermia mediante la administración combinada de antagonista de GnRH y 19-nortestosterona no puede mantenerse con este andrógeno no aromatizable solo" . Tararear. Reprod . 16 (12): 2570–7. doi : 10.1093 / humrep / 16.12.2570 . PMID 11726576 .
- ^ Detlef Thieme; Peter Hemmersbach (18 de diciembre de 2009). Dopaje en los deportes . Springer Science & Business Media. págs. 470–. ISBN 978-3-540-79088-4.
- ^ William Llewellyn (2011). Anabolizantes . Nutrición Molecular Llc. págs. 444–454, 533. ISBN 978-0-9828280-1-4.
- ^ Fragkaki AG, Angelis YS, Tsantili-Kakoulidou A, Koupparis M, Georgakopoulos C (mayo de 2009). "Esquemas de patrones metabólicos de esteroides androgénicos anabólicos para la estimación de metabolitos de esteroides de diseño en orina humana". J. Steroid Biochem. Mol. Biol . 115 (1–2): 44–61. doi : 10.1016 / j.jsbmb.2009.02.016 . PMID 19429460 . S2CID 10051396 .
- ↑ Schjølberg, TH (2013). Síntesis in vitro de metabolitos de tres esteroides androgénicos anabólicos, por microsomas hepáticos humanos (tesis de maestría, Institutt for bioteknologi). https://brage.bibsys.no/xmlui/handle/11250/246018
- ^ a b Die Gestagene . Springer-Verlag. 27 de noviembre de 2013. págs. 12-13, 282. ISBN 978-3-642-99941-3.
- ↑ a b c d J. Elks (14 de noviembre de 2014). El diccionario de drogas: datos químicos: datos químicos, estructuras y bibliografías . Saltador. págs. 888–. ISBN 978-1-4757-2085-3.
- ^ a b c I.K. Morton; Judith M. Hall (6 de diciembre de 2012). Diccionario conciso de agentes farmacológicos: propiedades y sinónimos . Springer Science & Business Media. págs. 202–. ISBN 978-94-011-4439-1.
- ^ Martin Negwer; Hans-Georg Scharnow (2001). Drogas orgánico-químicas y sus sinónimos: (una encuesta internacional) . Wiley-VCH. pag. 1831. ISBN 978-3-527-30247-5.