 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / Æ m f ɛ t ə m i n / ( escuchar ) |
| Nombres comerciales | Evekeo, Adderall [nota 1] , otros |
| Otros nombres | α-metilfenetilamina |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a616004 |
| Datos de licencia |
|
Responsabilidad por dependencia | Moderado [1] |
Responsabilidad por adicción | Moderar |
| Vías de administración | Médico: oral , intravenoso [2] Recreativo: oral , insuflación , rectal , intravenoso , intramuscular |
| Clase de droga | Estimulante del SNC , anoréxico |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | Oral: 75-100% [3] |
| Enlace proteico | 20% [4] |
| Metabolismo | CYP2D6 , [5] DAP , [13] [14] FMO3 [13] [15] [16] |
| Metabolitos | 4-hidroxianfetamina , 4-hidroxinorefedrina , 4-hidroxifenilacetona , ácido benzoico , ácido hipúrico , norefedrina , fenilacetona [5] [6] |
| Inicio de acción | Dosis de IR : 30 a 60 minutos [7] Dosis de XR : 1,5 a 2 horas [8] [9] |
| Vida media de eliminación | D-amph : 9-11 horas [5] [10] L-amph : 11-14 horas [5] [10] Dependiente del pH : 7-34 horas [11] |
| Duración de la acción | Dosis de IR : 3 a 6 horas [1] [8] [12] Dosis de XR : 8 a 12 horas [1] [8] [12] |
| Excreción | Principalmente renal ; Rango dependiente del pH : 1-75% [5] |
| Identificadores | |
Nombre IUPAC
| |
| Número CAS |
|
| PubChem CID |
|
| IUPHAR / BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| CHEBI |
|
| CHEMBL |
|
| NIAID ChemDB |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.005.543 |
| Datos químicos y físicos | |
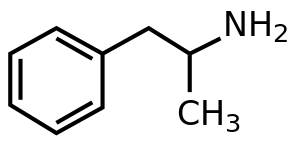
| Fórmula | C 9 H 13 N |
| Masa molar | 135,210 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
| Quiralidad | Mezcla racémica [17] |
| Densidad | 0,936 g / cm 3 a 25 ° C [18] |
| Punto de fusion | 11,3 ° C (52,3 ° F) (previsto) [19] |
| Punto de ebullición | 203 ° C (397 ° F) a 760 mmHg [20] |
Sonrisas
| |
InChI
| |
| (verificar) | |
La anfetamina [nota 2] (se contrajo de un lpha - m acetato de pH en et hyl amina ) es un sistema nervioso central (CNS) estimulante que se utiliza en el tratamiento de trastorno por déficit de atención con hiperactividad (ADHD), la narcolepsia , y la obesidad . La anfetamina se descubrió en 1887 y existe como dos enantiómeros : [nota 3] levoanfetamina y dextroanfetamina . La anfetamina se refiere correctamente a una sustancia química específica, la base libre racémica. , que es partes iguales de los dos enantiómeros, levoanfetamina y dextroanfetamina, en sus formas de amina pura. El término se usa frecuentemente de manera informal para referirse a cualquier combinación de enantiómeros, o a cualquiera de ellos solo. Históricamente, se ha utilizado para tratar la congestión nasal y la depresión. La anfetamina también se usa como potenciador del rendimiento deportivo y potenciador cognitivo , y de forma recreativa como afrodisíaco y euforizante . Es un medicamento recetado en muchos países, y la posesión y distribución no autorizadas de anfetamina a menudo están estrictamente controladas debido a los importantes riesgos para la salud asociados con el uso recreativo . [fuentes 1]
El primer producto farmacéutico de anfetaminas fue Benzedrine , una marca que se usaba para tratar una variedad de afecciones. Actualmente, la anfetamina farmacéutica se prescribe como anfetamina racémica, Adderall , [nota 4] dextroanfetamina o el profármaco inactivo lisdexanfetamina . La anfetamina aumenta la neurotransmisión excitadora y de monoaminas en el cerebro, con sus efectos más pronunciados dirigidos a los sistemas neurotransmisores de noradrenalina y dopamina . [fuentes 2]
En dosis terapéuticas, la anfetamina provoca efectos emocionales y cognitivos como euforia , cambios en el deseo sexual , aumento de la vigilia y mejora del control cognitivo . Induce efectos físicos como un mejor tiempo de reacción, resistencia a la fatiga y aumento de la fuerza muscular. Las dosis más grandes de anfetamina pueden afectar la función cognitiva e inducir una rápida degradación muscular . La adicción es un riesgo grave con el uso intensivo de anfetaminas recreativas, pero es poco probable que se produzca por el uso médico a largo plazo en dosis terapéuticas. Las dosis muy altas pueden provocar psicosis (p. Ej., Delirios y paranoia) que rara vez ocurre a dosis terapéuticas incluso durante un uso prolongado. Las dosis recreativas son generalmente mucho mayores que las dosis terapéuticas prescritas y conllevan un riesgo mucho mayor de efectos secundarios graves. [fuentes 3]
La anfetamina pertenece a la clase de fenetilamina . También es el compuesto original de su propia clase estructural, las anfetaminas sustituidas , [nota 5] que incluye sustancias prominentes como bupropión , catinona , MDMA y metanfetamina . Como miembro de la clase de fenetilamina, la anfetamina también está relacionada químicamente con los neuromoduladores de trazas de amina de origen natural , específicamente fenetilamina y N -metilfenetilamina , ambos producidos dentro del cuerpo humano. La fenetilamina es el compuesto original de la anfetamina, mientras que N-metilfenetilamina es un isómero posicional de la anfetamina que difiere solo en la ubicación del grupo metilo . [fuentes 4]
Usos
Médico
La anfetamina se usa para tratar el trastorno por déficit de atención con hiperactividad (TDAH), la narcolepsia (un trastorno del sueño) y la obesidad , y algunas veces se prescribe de forma no autorizada para sus indicaciones médicas pasadas , particularmente para la depresión y el dolor crónico . [1] [34] [48] Se sabe que la exposición prolongada a las anfetaminas en dosis suficientemente altas en algunas especies animales produce un desarrollo anormal del sistema dopaminérgico o daño a los nervios, [49] [50] pero, en los seres humanos con TDAH, las anfetaminas farmacéuticas, en dosis terapéuticas, parecen mejorar el desarrollo del cerebro y el crecimiento de los nervios.[51] [52] [53] Las revisiones deestudios de imágenes por resonancia magnética (IRM) sugieren que el tratamiento a largo plazo con anfetamina disminuye las anomalías en la estructura y función del cerebro que se encuentran en sujetos con TDAH y mejora la función en varias partes del cerebro, como como el núcleo caudado derechode los ganglios basales . [51] [52] [53]
Las revisiones de la investigación clínica sobre estimulantes han establecido la seguridad y eficacia del uso continuo de anfetaminas a largo plazo para el tratamiento del TDAH. [42] [54] [55] Los ensayos controlados aleatorios de la terapia estimulante continua para el tratamiento del TDAH durante dos años han demostrado la eficacia y seguridad del tratamiento. [42] [54] Dos revisiones han indicado que la terapia estimulante continua a largo plazo para el TDAH es eficaz para reducir los síntomas centrales del TDAH (es decir, hiperactividad, falta de atención e impulsividad), mejorar la calidad de vida y el rendimiento académico y producir mejoras en una gran cantidad de resultados funcionales [nota 6]en 9 categorías de resultados relacionados con lo académico, comportamiento antisocial, conducción, uso de drogas no medicinales, obesidad, ocupación, autoestima, uso de servicios (es decir, servicios académicos, ocupacionales, de salud, financieros y legales) y función social. [42] [55] Una revisión destacó un ensayo controlado aleatorio de nueve meses de tratamiento con anfetaminas para el TDAH en niños que encontró un aumento promedio de 4.5 puntos de CI , aumentos continuos en la atención y disminuciones continuas en conductas disruptivas e hiperactividad. [54] Otra revisión indicó que, sobre la base de los estudios de seguimiento más largosllevada a cabo hasta la fecha, la terapia estimulante de por vida que comienza durante la infancia es continuamente eficaz para controlar los síntomas del TDAH y reduce el riesgo de desarrollar un trastorno por uso de sustancias en la edad adulta. [42]
Los modelos actuales de TDAH sugieren que está asociado con deficiencias funcionales en algunos de los sistemas neurotransmisores del cerebro ; [56] estas deficiencias funcionales implican una alteración de la neurotransmisión de dopamina en la proyección mesocorticolímbica y la neurotransmisión de norepinefrina en las proyecciones noradrenérgicas desde el locus coeruleus hasta la corteza prefrontal . [56] Los psicoestimulantes como el metilfenidato y la anfetamina son eficaces para tratar el TDAH porque aumentan la actividad de los neurotransmisores en estos sistemas. [25] [56] [57]Aproximadamente el 80% de los que usan estos estimulantes ven mejoras en los síntomas del TDAH. [58] Los niños con TDAH que usan medicamentos estimulantes generalmente tienen mejores relaciones con sus compañeros y miembros de la familia, se desempeñan mejor en la escuela, se distraen menos e impulsan menos y tienen períodos de atención más prolongados. [59] [60] Las revisiones Cochrane [nota 7] sobre el tratamiento del TDAH en niños, adolescentes y adultos con anfetaminas farmacéuticas indicaron que los estudios a corto plazo han demostrado que estos medicamentos disminuyen la gravedad de los síntomas, pero tienen una mayor interrupción tasas que los medicamentos no estimulantes debido a sus efectos secundarios adversos . [62] [63]Una revisión Cochrane sobre el tratamiento del TDAH en niños con trastornos de tics como el síndrome de Tourette indicó que los estimulantes en general no empeoran los tics , pero las dosis altas de dextroanfetamina podrían exacerbar los tics en algunas personas. [64]
Mejorando el desempeño
Rendimiento cognitivo
En 2015, una revisión sistemática y un metanálisis de ensayos clínicos de alta calidad encontraron que, cuando se usa en dosis bajas (terapéuticas), la anfetamina produce mejoras modestas pero inequívocas en la cognición, incluida la memoria de trabajo , la memoria episódica a largo plazo , el control inhibitorio , y algunos aspectos de la atención , en adultos sanos normales; [65] [66] Se sabe que estos efectos de mejora de la cognición de la anfetamina están mediados parcialmente a través de la activación indirecta del receptor de dopamina D 1 y del receptor adrenérgico α 2 en elcorteza prefrontal . [25] [65] Una revisión sistemática de 2014 encontró que las dosis bajas de anfetamina también mejoran la consolidación de la memoria , lo que a su vez conduce a una mejor recuperación de la información . [67] Las dosis terapéuticas de anfetamina también mejoran la eficiencia de la red cortical, un efecto que media las mejoras en la memoria de trabajo en todos los individuos. [25] [68] La anfetamina y otros estimulantes del TDAH también mejoran la relevancia de la tarea (motivación para realizar una tarea) y aumentan la excitación (vigilia), lo que a su vez promueve el comportamiento dirigido a objetivos. [25] [69] [70]Los estimulantes como la anfetamina pueden mejorar el desempeño en tareas difíciles y aburridas y algunos estudiantes los utilizan como ayuda para estudiar y tomar exámenes. [25] [70] [71] Según estudios sobre el uso de estimulantes ilícitos autoinformado, entre el 5 y el 35% de los estudiantes universitarios utilizan estimulantes del TDAH desviados , que se utilizan principalmente para mejorar el rendimiento académico en lugar de como drogas recreativas. [72] [73] [74] Sin embargo, las dosis altas de anfetamina que están por encima del rango terapéutico pueden interferir con la memoria de trabajo y otros aspectos del control cognitivo. [25] [70]
Desempeño físico
Algunos atletas utilizan la anfetamina por sus efectos psicológicos y atléticos que mejoran el rendimiento , como una mayor resistencia y estado de alerta; [26] [38] sin embargo, el uso de anfetaminas no médicas está prohibido en eventos deportivos regulados por agencias antidopaje colegiadas, nacionales e internacionales. [75] [76] En personas sanas en dosis terapéuticas orales, se ha demostrado que la anfetamina aumenta la fuerza muscular , la aceleración, el rendimiento deportivo en condiciones anaeróbicas y la resistencia (es decir, retrasa la aparición de la fatiga ), al tiempo que mejora el tiempo de reacción . [26] [77] [78]La anfetamina mejora la resistencia y el tiempo de reacción principalmente mediante la inhibición de la recaptación y la liberación de dopamina en el sistema nervioso central. [77] [78] [79] Las anfetaminas y otras drogas dopaminérgicas también aumentan la producción de energía a niveles fijos de esfuerzo percibido al anular un "interruptor de seguridad", lo que permite que el límite de temperatura central aumente para acceder a una capacidad de reserva que normalmente está inactiva -límites. [78] [80] [81] En dosis terapéuticas, los efectos adversos de la anfetamina no impiden el rendimiento deportivo; [26] [77]sin embargo, en dosis mucho más altas, la anfetamina puede inducir efectos que perjudican gravemente el rendimiento, como una rápida degradación muscular y una temperatura corporal elevada . [27] [77]
Contraindicaciones
De acuerdo con el Programa Internacional de Seguridad Química (IPCS) y la Administración de Drogas y Alimentos de los Estados Unidos (USFDA), [nota 8] la anfetamina está contraindicada en personas con antecedentes de abuso de drogas , [nota 9] enfermedad cardiovascular , agitación severa o ansiedad severa. [34] [27] [83] También está contraindicado en personas con arteriosclerosis avanzada (endurecimiento de las arterias), glaucoma (aumento de la presión ocular), hipertiroidismo (producción excesiva de hormona tiroidea) o de moderada a grave.hipertensión . [34] [27] [83] Estas agencias indican que las personas que han experimentado reacciones alérgicas a otros estimulantes o que están tomando inhibidores de la monoaminooxidasa (IMAO) no deben tomar anfetaminas, [34] [27] [83] aunque el uso concurrente es seguro de inhibidores de anfetamina y monoamino oxidasa. [84] [85] Estas agencias también afirman que cualquier persona con anorexia nerviosa , trastorno bipolar , depresión, hipertensión, problemas hepáticos o renales, manía , psicosis , fenómeno de Raynaud ,convulsiones , problemas de tiroides , tics o síndrome de Tourette deben controlar sus síntomas mientras toma anfetamina. [27] [83] La evidencia de estudios en humanos indica que el uso terapéutico de anfetaminas no causa anomalías del desarrollo en el feto o en los recién nacidos (es decir, no es un teratógeno humano ), pero el abuso de anfetaminas presenta riesgos para el feto. [83] También se ha demostrado que la anfetamina pasa a la leche materna, por lo que el IPCS y la USFDA recomiendan a las madres que eviten amamantar cuando la consuman. [27] [83] Debido al potencial de deterioro reversible del crecimiento, [nota 10]la USFDA aconseja controlar la altura y el peso de los niños y adolescentes a los que se les recetó un fármaco de anfetamina. [27]
Efectos adversos
Los efectos secundarios adversos de la anfetamina son muchos y variados, y la cantidad de anfetamina utilizada es el factor principal para determinar la probabilidad y la gravedad de los efectos adversos. [27] [38] Los productos de anfetamina como Adderall , Dexedrine y sus equivalentes genéricos están actualmente aprobados por la USFDA para uso terapéutico a largo plazo. [35] [27] El uso recreativo de anfetamina generalmente implica dosis mucho mayores, que tienen un mayor riesgo de efectos adversos graves de los medicamentos que las dosis utilizadas con fines terapéuticos. [38]
Físico
Los efectos secundarios cardiovasculares pueden incluir hipertensión o hipotensión por una respuesta vasovagal , fenómeno de Raynaud (reducción del flujo sanguíneo a las manos y pies) y taquicardia (aumento de la frecuencia cardíaca). [27] [38] [86] Los efectos secundarios sexuales en los hombres pueden incluir disfunción eréctil , erecciones frecuentes o erecciones prolongadas . [27] Los efectos secundarios gastrointestinales pueden incluir dolor abdominal , estreñimiento , diarrea y náuseas . [1] [27] [87]Otros posibles efectos secundarios físicos incluyen pérdida del apetito , visión borrosa , boca seca , rechinar excesivo de los dientes , hemorragia nasal, sudoración profusa, rinitis medicamentosa (congestión nasal inducida por fármacos), umbral convulsivo reducido , tics (un tipo de trastorno del movimiento) y Pérdida de peso . [fuentes 5] Los efectos secundarios físicos peligrosos son raros en dosis farmacéuticas típicas. [38]
La anfetamina estimula los centros respiratorios medulares , produciendo respiraciones más rápidas y profundas. [38] En una persona normal a dosis terapéuticas, este efecto generalmente no se nota, pero cuando la respiración ya está comprometida, puede ser evidente. [38] La anfetamina también induce la contracción del esfínter de la vejiga urinaria , el músculo que controla la micción, lo que puede resultar en dificultad para orinar. [38] Este efecto puede ser útil para tratar la enuresis nocturna y la pérdida del control de la vejiga . [38] Los efectos de la anfetamina en el tracto gastrointestinal son impredecibles. [38]Si la actividad intestinal es alta, la anfetamina puede reducir la motilidad gastrointestinal (la velocidad a la que el contenido se mueve a través del sistema digestivo); [38] sin embargo, la anfetamina puede aumentar la motilidad cuando el músculo liso del tracto está relajado. [38] La anfetamina también tiene un ligero efecto analgésico y puede mejorar los efectos analgésicos de los opioides . [1] [38]
Los estudios encargados por la USFDA de 2011 indican que en niños, adultos jóvenes y adultos no existe una asociación entre los eventos cardiovasculares adversos graves ( muerte súbita , ataque cardíaco y accidente cerebrovascular ) y el uso médico de anfetaminas u otros estimulantes del TDAH. [fuentes 6] Sin embargo, los productos farmacéuticos de anfetamina están contraindicados en personas con enfermedades cardiovasculares . [fuentes 7]
Psicológico
En dosis terapéuticas normales, los efectos secundarios psicológicos más comunes de la anfetamina incluyen aumento del estado de alerta , aprensión, concentración , iniciativa, autoconfianza y sociabilidad, cambios de humor ( estado de ánimo eufórico seguido de un estado de ánimo levemente deprimido ), insomnio o vigilia y disminución de la sensación de fatiga . [27] [38] Los efectos secundarios menos comunes incluyen ansiedad , cambio en la libido , grandiosidad , irritabilidad , comportamientos repetitivos u obsesivos e inquietud; [fuentes 8]estos efectos dependen de la personalidad del usuario y del estado mental actual. [38] La psicosis anfetamínica (p. Ej., Delirios y paranoia ) puede ocurrir en consumidores habituales. [27] [39] [40] Aunque es muy poco común, esta psicosis también puede ocurrir en dosis terapéuticas durante la terapia a largo plazo. [27] [40] [41] Según la USFDA, "no hay evidencia sistemática" de que los estimulantes produzcan un comportamiento agresivo u hostilidad. [27]
También se ha demostrado que la anfetamina produce una preferencia de lugar condicionada en los seres humanos que toman dosis terapéuticas, [62] [94] lo que significa que los individuos adquieren una preferencia por pasar tiempo en lugares donde previamente han consumido anfetamina. [94] [95]
Trastornos de refuerzo
Adiccion
| Glosario de adicciones y dependencia [95] [96] [97] [98] | |
|---|---|
| |
| Glosario de factores de transcripción | |
|---|---|
| |
Cascada de señalización en el núcleo accumbens que resulta en adicción a las anfetaminas |
La adicción es un riesgo grave con el uso intensivo de anfetaminas recreativas, pero es poco probable que se produzca por el uso médico a largo plazo en dosis terapéuticas; [42] [43] [44] de hecho, la terapia estimulante de por vida para el TDAH que comienza durante la niñez reduce el riesgo de desarrollar trastornos por uso de sustancias en la edad adulta. [42] La sobreactivación patológica de la vía mesolímbica , una vía de la dopamina que conecta el área tegmental ventral con el núcleo accumbens , juega un papel central en la adicción a las anfetaminas. [105] [106] Individuos que frecuentemente se autoadministranlas dosis altas de anfetamina tienen un alto riesgo de desarrollar una adicción a las anfetaminas, ya que el uso crónico en dosis altas aumenta gradualmente el nivel de ΔFosB accumbal , un "interruptor molecular" y "proteína de control maestro" para la adicción. [96] [107] [108] Una vez que el núcleo accumbens ΔFosB se sobreexpresa suficientemente, comienza a aumentar la gravedad de la conducta adictiva (es decir, búsqueda compulsiva de drogas) con aumentos adicionales en su expresión. [107] [109] Si bien actualmente no existen medicamentos efectivos para tratar la adicción a las anfetaminas, la práctica regular de ejercicio aeróbico sostenido parece reducir el riesgo de desarrollar tal adicción. [110] [111]El ejercicio aeróbico sostenido de forma regular también parece ser un tratamiento eficaz para la adicción a las anfetaminas; [fuentes 9] la terapia con ejercicios mejora los resultados del tratamiento clínico y puede usarse como terapia complementaria con terapias conductuales para la adicción. [110] [112]
Mecanismos biomoleculares
El uso crónico de anfetamina en dosis excesivas provoca alteraciones en la expresión génica en la proyección mesocorticolímbica , que surgen por mecanismos transcripcionales y epigenéticos . [108] [113] [114] Los factores de transcripción más importantes [nota 11] que producen estas alteraciones son el homólogo B del oncogén viral del osteosarcoma murino Delta FBJ ( ΔFosB ), la proteína de unión al elemento de respuesta al AMPc ( CREB ) y el factor nuclear kappa B ( NF-κB ). [108]ΔFosB es el mecanismo biomolecular más importante en la adicción porque la sobreexpresión de ΔFosB (es decir, un nivel anormalmente alto de expresión génica que produce un fenotipo pronunciado relacionado con el gen ) en las neuronas espinosas medianas de tipo D1 en el núcleo accumbens es necesaria y suficiente [nota 12 ] para muchas de las adaptaciones neuronales y regula múltiples efectos conductuales (p. ej., sensibilización a la recompensa y aumento de la autoadministración de drogas ) implicados en la adicción. [96] [107] [108]Una vez que ΔFosB se sobreexpresa suficientemente, induce un estado adictivo que se vuelve cada vez más severo con aumentos adicionales en la expresión de ΔFosB. [96] [107] Se ha relacionado con adicciones al alcohol , cannabinoides , cocaína , metilfenidato , nicotina , opioides , fenciclidina , propofol y anfetaminas sustituidas , entre otros. [fuentes 10]
ΔJunD , un factor de transcripción, y G9a , una enzima histona metiltransferasa , ambos se oponen a la función de ΔFosB e inhiben los aumentos en su expresión. [96] [108] [118] La sobreexpresión suficiente de ΔJunD en el núcleo accumbens con vectores virales puede bloquear por completo muchas de las alteraciones neuronales y conductuales que se observan en el abuso crónico de drogas (es decir, las alteraciones mediadas por ΔFosB). [108] De manera similar, la hiperexpresión de accumbal G9a da como resultado un aumento notable de la dimetilación del residuo de lisina 3 de la histona 3 ( H3K9me2 ) y bloquea la inducción de ΔFosB plasticidad neuronal y conductual por el uso crónico de drogas, [fuentes 11] que se produce mediante la represión de factores de transcripción mediada por H3K9me2 para la represión mediada por ΔFosB y H3K9me2 de varios objetivos transcripcionales de ΔFosB (p. ej., CDK5 ). [108] [118] [119] ΔFosB también juega un papel importante en la regulación de las respuestas conductuales a las recompensas naturales , como la comida apetecible, el sexo y el ejercicio. [109] [108] [122] Dado que tanto las recompensas naturales como las drogas adictivas inducen la expresiónde ΔFosB (es decir, hacen que el cerebro produzca más), la adquisición crónica de estas recompensas puede resultar en un estado patológico similar de adicción. [109] [108] En consecuencia, ΔFosB es el factor más importante involucrado tanto en la adicción a las anfetaminas como en las adicciones sexuales inducidas por anfetaminas , que son conductas sexuales compulsivas que resultan de la actividad sexual excesiva y el uso de anfetaminas. [109] [123] [124] Estas adicciones sexuales están asociadas con un síndrome de desregulación de la dopamina que ocurre en algunos pacientes que toman fármacos dopaminérgicos . [109] [122]
Los efectos de la anfetamina sobre la regulación génica dependen tanto de la dosis como de la ruta. [114] La mayor parte de la investigación sobre la regulación genética y la adicción se basa en estudios en animales con administración intravenosa de anfetaminas en dosis muy altas. [114] Los pocos estudios que han utilizado dosis terapéuticas humanas equivalentes (ajustadas por peso) y administración oral muestran que estos cambios, si ocurren, son relativamente menores. [114] Esto sugiere que el uso médico de anfetaminas no afecta significativamente la regulación genética. [114]
Tratamientos farmacológicos
A diciembre de 2019, [update]no existe una farmacoterapia eficaz para la adicción a las anfetaminas. [125] [126] [127] Las revisiones de 2015 y 2016 indicaron que los agonistas selectivos de TAAR1 tienen un potencial terapéutico significativo como tratamiento para las adicciones a los psicoestimulantes; [37] [128] sin embargo, a febrero de 2016, [update]los únicos compuestos que se sabe que funcionan como agonistas selectivos de TAAR1 son fármacos experimentales . [37] [128] La adicción a las anfetaminas está mediada en gran medida por una mayor activación de los receptores de dopamina y los receptores de NMDA co-localizados [nota 13]en el núcleo accumbens; [106] Los iones de magnesio inhiben los receptores NMDA bloqueando el canal de calcio del receptor . [106] [129] Una revisión sugirió que, según las pruebas con animales, el uso de psicoestimulantes patológicos (que inducen la adicción) reduce significativamente el nivel de magnesio intracelular en todo el cerebro. [106] Se ha demostrado que el tratamiento suplementario de magnesio [nota 14] reduce la autoadministración de anfetaminas (es decir, las dosis que se administran a uno mismo) en humanos, pero no es una monoterapia eficaz para la adicción a las anfetaminas. [106]
Una revisión sistemática y un metanálisis de 2019 evaluaron la eficacia de 17 farmacoterapias diferentes utilizadas en ECA para la adicción a las anfetaminas y metanfetaminas; [126] sólo encontró pruebas de baja concentración de que el metilfenidato podría reducir la autoadministración de anfetaminas o metanfetaminas. [126] Hubo pruebas de concentración baja a moderada de ningún beneficio para la mayoría de los otros medicamentos utilizados en los ECA, que incluían antidepresivos (bupropión, mirtazapina , sertralina ), antipsicóticos ( aripiprazol ), anticonvulsivos ( topiramato , baclofeno , gabapentina ), naltrexona , vareniclina ,citicolina , ondansetrón , prometa , riluzol , atomoxetina , dextroanfetamina y modafinilo . [126]
Tratamientos conductuales
Una revisión sistemática de 2018 y un metanálisis en red de 50 ensayos que incluían 12 intervenciones psicosociales diferentes para la adicción a las anfetaminas, metanfetaminas o cocaína encontraron que la terapia combinada con el manejo de contingencias y el enfoque de refuerzo comunitario tuvo la mayor eficacia (es decir, tasa de abstinencia) y aceptabilidad ( es decir, la tasa de deserción más baja). [130] Otras modalidades de tratamiento examinadas en el análisis incluyeron monoterapia con manejo de contingencias o enfoque de refuerzo comunitario, terapia cognitivo-conductual , programas de 12 pasos , terapias no contingentes basadas en recompensas, terapia psicodinámicay otras terapias combinadas que los involucran. [130]
Además, la investigación sobre los efectos neurobiológicos del ejercicio físico sugiere que el ejercicio aeróbico diario, especialmente el ejercicio de resistencia (p. Ej., Correr un maratón ), previene el desarrollo de la adicción a las drogas y es una terapia complementaria eficaz (es decir, un tratamiento complementario) para la adicción a las anfetaminas. [fuentes 9] El ejercicio conduce a mejores resultados del tratamiento cuando se usa como tratamiento adjunto, particularmente para las adicciones a los psicoestimulantes. [110] [112] [131] En particular, el ejercicio aeróbico disminuye la autoadministración de psicoestimulantes, reduce el restablecimiento (es decir, la recaída) de la búsqueda de drogas e induce un aumentoDensidad del receptor de dopamina D 2 (DRD2) en el cuerpo estriado . [109] [131] Esto es lo opuesto al uso de estimulantes patológicos, que induce una disminución de la densidad de DRD2 estriatal. [109] Una revisión señaló que el ejercicio también puede prevenir el desarrollo de una adicción a las drogas al alterar la inmunorreactividad de ΔFosB o c-Fos en el cuerpo estriado u otras partes del sistema de recompensa . [111]
| Forma de neuroplasticidad o plasticidad conductual. | Tipo de reforzador | Fuentes | |||||
|---|---|---|---|---|---|---|---|
| Opiáceos | Psicoestimulantes | Alimentos ricos en grasas o azúcares | Relaciones sexuales | Ejercicio físico (aeróbico) | Enriquecimiento ambiental | ||
| Expresión de ΔFosB en MSN de tipo D1 del núcleo accumbens | ↑ | ↑ | ↑ | ↑ | ↑ | ↑ | [109] |
| Plasticidad conductual | |||||||
| Escalada de ingesta | sí | sí | sí | [109] | |||
| Sensibilización cruzada con psicoestimulantes | sí | No aplica | sí | sí | Atenuado | Atenuado | [109] |
| Psicoestimulantes autoadministración | ↑ | ↑ | ↓ | ↓ | ↓ | [109] | |
| Preferencia de lugar condicionada por psicoestimulantes | ↑ | ↑ | ↓ | ↑ | ↓ | ↑ | [109] |
| Restablecimiento del comportamiento de búsqueda de drogas | ↑ | ↑ | ↓ | ↓ | [109] | ||
| Plasticidad neuroquímica | |||||||
| Fosforilación de CREB en el núcleo accumbens | ↓ | ↓ | ↓ | ↓ | ↓ | [109] | |
| Respuesta de dopamina sensibilizada en el núcleo accumbens | No | sí | No | sí | [109] | ||
| Señalización de dopamina estriatal alterada | ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD2 | ↑ DRD2 | [109] | |
| Señalización de opioides estriatal alterada | Sin cambios o ↑ receptores μ-opioides | ↑ receptores μ-opioides ↑ receptores κ-opioides | ↑ receptores μ-opioides | ↑ receptores μ-opioides | Ningún cambio | Ningún cambio | [109] |
| Cambios en los péptidos opioides estriatales | ↑ dinorfina Sin cambios: encefalina | ↑ dinorfina | ↓ encefalina | ↑ dinorfina | ↑ dinorfina | [109] | |
| Plasticidad sináptica mesocorticolímbica | |||||||
| Número de dendritas en el núcleo accumbens | ↓ | ↑ | ↑ | [109] | |||
| Densidad de la columna dendrítica en el núcleo accumbens | ↓ | ↑ | ↑ | [109] | |||
Dependencia y abstinencia
La tolerancia a las drogas se desarrolla rápidamente en el abuso de anfetaminas (es decir, el uso recreativo de anfetaminas), por lo que los períodos de abuso prolongado requieren dosis cada vez mayores de la droga para lograr el mismo efecto. [132] [133] Según una revisión Cochrane sobre abstinencia en personas que consumen anfetamina y metanfetamina de forma compulsiva, "cuando los consumidores crónicos intensos interrumpen abruptamente el consumo de anfetaminas, muchos informan de un síndrome de abstinencia de duración limitada que se produce dentro de las 24 horas posteriores a la última dosis. " [134] Esta revisión señaló que los síntomas de abstinencia en los consumidores crónicos de dosis altas son frecuentes, ocurren en aproximadamente el 88% de los casos y persisten durante 3-4 semanas con una fase marcada de "choque" que ocurre durante la primera semana. [134]Los síntomas de abstinencia de anfetaminas pueden incluir ansiedad, ansia de drogas , estado de ánimo deprimido , fatiga , aumento del apetito , aumento del movimiento o disminución del movimiento , falta de motivación, insomnio o somnolencia y sueños lúcidos . [134] La revisión indicó que la gravedad de los síntomas de abstinencia se correlaciona positivamente con la edad del individuo y el grado de dependencia. [134] Los síntomas leves de abstinencia por la interrupción del tratamiento con anfetaminas en dosis terapéuticas pueden evitarse disminuyendo la dosis. [1]
Sobredosis
Una sobredosis de anfetaminas puede provocar muchos síntomas diferentes, pero rara vez es mortal con la atención adecuada. [1] [83] [135] La gravedad de los síntomas de sobredosis aumenta con la dosis y disminuye con la tolerancia del fármaco a la anfetamina. [38] [83] Se sabe que las personas tolerantes toman hasta 5 gramos de anfetamina en un día, que es aproximadamente 100 veces la dosis terapéutica diaria máxima. [83] Los síntomas de una sobredosis moderada y extremadamente grande se enumeran a continuación; El envenenamiento fatal por anfetaminas generalmente también involucra convulsiones y coma . [27] [38] En 2013, una sobredosis de anfetamina, metanfetamina y otros compuestos implicados en un "El trastorno por consumo de anfetaminas "resultó en un estimado de 3.788 muertes en todo el mundo ( 3.425–4.145 muertes, 95% de confianza ). [nota 15] [136]
| Sistema | Sobredosis leve o moderada [27] [38] [83] | Sobredosis grave [fuentes 12] |
|---|---|---|
| Cardiovascular |
|
|
| Nervioso central Sistema |
|
|
| Musculoesquelético |
|
|
| Respiratorio |
|
|
| Urinario |
|
|
| Otro |
|
|
Toxicidad
En roedores y primates, dosis suficientemente altas de anfetamina causan neurotoxicidad dopaminérgica o daño a las neuronas dopaminérgicas, que se caracteriza por degeneración terminal de dopamina y función reducida del transportador y receptor. [138] [139] No hay evidencia de que la anfetamina sea directamente neurotóxica en los seres humanos. [140] [141] Sin embargo, grandes dosis de anfetamina pueden causar indirectamente neurotoxicidad dopaminérgica como resultado de la hiperpirexia , la formación excesiva de especies reactivas de oxígeno y el aumento de la autooxidación de la dopamina. [fuentes 13] Modelos animales de neurotoxicidad por exposición a altas dosis de anfetaminas indican que la aparición de hiperpirexia (es decir, temperatura corporal central ≥ 40 ° C) es necesaria para el desarrollo de neurotoxicidad inducida por anfetaminas. [139] Las elevaciones prolongadas de la temperatura cerebral por encima de 40 ° C probablemente promuevan el desarrollo de neurotoxicidad inducida por anfetaminas en animales de laboratorio al facilitar la producción de especies reactivas de oxígeno, alterar la función de las proteínas celulares y aumentar transitoriamente la permeabilidad de la barrera hematoencefálica . [139]
Psicosis
Una sobredosis de anfetaminas puede resultar en una psicosis estimulante que puede involucrar una variedad de síntomas, como delirios y paranoia. [39] [40] Una revisión Cochrane sobre el tratamiento de la psicosis de anfetamina, dextroanfetamina y metanfetamina indica que alrededor del 5 al 15% de los usuarios no se recuperan por completo. [39] [144] Según la misma revisión, hay al menos un ensayo que muestra que los medicamentos antipsicóticos resuelven eficazmente los síntomas de la psicosis anfetamínica aguda. [39] La psicosis rara vez surge de un uso terapéutico. [27] [40] [41]
Interacciones con la drogas
Se sabe que muchos tipos de sustancias interactúan con la anfetamina, lo que da como resultado una acción farmacológica alterada o el metabolismo de la anfetamina, la sustancia que interactúa o ambas. [27] Los inhibidores de las enzimas que metabolizan la anfetamina (p. Ej., CYP2D6 y FMO3 ) prolongarán su vida media de eliminación , lo que significa que sus efectos durarán más. [15] [27] La anfetamina también interactúa con los IMAO , en particular los inhibidores de la monoamino oxidasa A , ya que tanto los IMAO como la anfetamina aumentan las catecolaminas plasmáticas (es decir, norepinefrina y dopamina); [27]por lo tanto, el uso simultáneo de ambos es peligroso. [27] La anfetamina modula la actividad de la mayoría de las drogas psicoactivas. En particular, la anfetamina puede disminuir los efectos de los sedantes y depresores y aumentar los efectos de los estimulantes y antidepresivos . [27] La anfetamina también puede disminuir los efectos de los antihipertensivos y antipsicóticos debido a sus efectos sobre la presión arterial y la dopamina, respectivamente. [27] La suplementación con zinc puede reducir la dosis mínima efectiva de anfetamina cuando se usa para el tratamiento del TDAH. [nota 16] [149]
En general, no existe una interacción significativa cuando se consume anfetamina con alimentos, pero el pH del contenido gastrointestinal y la orina afecta la absorción y excreción de anfetamina, respectivamente. [27] Las sustancias ácidas reducen la absorción de anfetamina y aumentan la excreción urinaria, y las sustancias alcalinas hacen lo contrario. [27] Debido al efecto de pH tiene sobre la absorción, la anfetamina también interactúa con los reductores de ácido gástrico, tales como inhibidores de la bomba de protones y H 2 antihistamínicos , los cuales aumentan el pH gastrointestinal (es decir, hacer que sea menos ácido). [27]
Farmacología
Farmacodinámica
Farmacodinámica de la anfetamina en una neurona de dopamina |
La anfetamina ejerce sus efectos conductuales al alterar el uso de monoaminas como señales neuronales en el cerebro, principalmente en las neuronas catecolaminas en las vías de recompensa y función ejecutiva del cerebro. [36] [57] Las concentraciones de los principales neurotransmisores involucrados en los circuitos de recompensa y el funcionamiento ejecutivo, la dopamina y la norepinefrina, aumentan dramáticamente de una manera dependiente de la dosis por la anfetamina debido a sus efectos sobre los transportadores de monoamina . [36] [57] [150] Los efectos reforzantes y estimulantes de la prominencia motivacional de la anfetamina se deben principalmente a una mayor actividad dopaminérgica en elvía mesolímbica . [25] Los efectos eufóricos y estimulantes del aparato locomotor de la anfetamina dependen de la magnitud y la velocidad con la que aumenta las concentraciones sinápticas de dopamina y noradrenalina en el cuerpo estriado . [2]
La anfetamina se ha identificado como un potente agonista completo de traza receptor amina-asociado 1 (TAAR1), un G s -junto y G q -junto G receptor acoplado a proteína (GPCR) descubierto en 2001, que es importante para la regulación de las monoaminas cerebrales . [36] [156] La activación de TAAR1 aumenta la producción de cAMP a través de la activación de la adenilil ciclasa e inhibe la función transportadora de monoaminas . [36] [157] Autorreceptores de monoaminas (p. Ej., D 2 corto, presináptica α 2 y presináptica 5-HT 1A ) tienen el efecto opuesto de TAAR1, y juntos estos receptores proporcionan un sistema regulador de monoaminas. [36] [37] En particular, las anfetaminas y las trazas de aminas poseen altas afinidades de unión por TAAR1, pero no por los autorreceptores de monoaminas. [36] [37] Los estudios de imágenes indican que la inhibición de la recaptación de monoaminas por parte de anfetaminas y trazas de aminas es específica del sitio y depende de la presencia de co-localización de TAAR1 en las neuronas de monoaminas asociadas. [36]
Además de los transportadores de monoaminas neuronales , la anfetamina también inhibe los transportadores de monoaminas vesiculares , VMAT1 y VMAT2 , así como SLC1A1 , SLC22A3 y SLC22A5 . [fuentes 14] SLC1A1 es un transportador de aminoácidos excitadores 3 (EAAT3), un transportador de glutamato ubicado en neuronas, SLC22A3 es un transportador de monoamina extraneuronal que está presente en astrocitos y SLC22A5 es un transportador de carnitina de alta afinidad . [fuentes 14] Se sabe que la anfetamina induce fuertemente la transcripción regulada por cocaína y anfetamina(CART) expresión génica , [4] [163] un neuropéptido involucrado en la conducta alimentaria, el estrés y la recompensa, que induce aumentos observables en el desarrollo neuronal y la supervivencia in vitro . [4] [164] [165] El receptor CART aún no se ha identificado, pero hay evidencia significativa de que CART se une a un GPCR acoplado a G i / G o único . [165] [166] La anfetamina también inhibe las monoamino oxidasas en dosis muy altas, lo que resulta en menos metabolismo de monoaminas y trazas de amina y, en consecuencia, concentraciones más altas de monoaminas sinápticas.[21] [167] En los seres humanos, el único receptor postsináptico al que se sabe que se une la anfetamina es el receptor 5-HT1A , donde actúa como un agonista con bajaafinidad micromolar . [168] [169]
El perfil completo de los efectos farmacológicos a corto plazo de la anfetamina en los seres humanos se deriva principalmente de una mayor comunicación celular o neurotransmisión de dopamina , [36] serotonina , [36] norepinefrina , [36] epinefrina , [150] histamina , [150] péptidos CART , [4] [163] opioides endógenos , [170] [171] [172] hormona adrenocorticotrópica , [173] [174] corticosteroides , [173] [174] y glutamato ,[154] [159] que afecta a través de interacciones con CART , 5-HT1A , EAAT3 , TAAR1 , VMAT1 , VMAT2 y posiblemente otras dianas biológicas . [fuentes 15] La anfetamina también activa sieteenzimas anhidrasa carbónica humana, varias de las cuales se expresan en el cerebro humano. [175]
La dextroanfetamina es un agonista de TAAR1 más potente que la levoanfetamina. [176] En consecuencia, la dextroanfetamina produce una mayor estimulación del SNC que la levoanfetamina, aproximadamente de tres a cuatro veces más, pero la levoanfetamina tiene efectos cardiovasculares y periféricos ligeramente más fuertes. [38] [176]
Dopamina
En ciertas regiones del cerebro, la anfetamina aumenta la concentración de dopamina en la hendidura sináptica . [36] La anfetamina puede ingresar a la neurona presináptica a través de DAT o difundiéndose directamente a través de la membrana neuronal. [36] Como consecuencia de la captación de DAT, la anfetamina produce una inhibición competitiva de la recaptación en el transportador. [36] Al entrar en la neurona presináptica, la anfetamina activa TAAR1 que, a través de la señalización de la proteína quinasa A (PKA) y la proteína quinasa C (PKC), causa la fosforilación de DAT . [36]La fosforilación por cualquiera de las proteínas quinasas puede resultar en la internalización de DAT ( inhibición de la recaptación no competitiva ), pero la fosforilación mediada por PKC sola induce la inversión del transporte de dopamina a través de DAT (es decir, salida de dopamina ). [nota 16] [36] [177] También se sabe que la anfetamina aumenta el calcio intracelular, un efecto que se asocia con la fosforilación de DAT a través de una vía no identificada dependiente de Ca2 + / proteína quinasa dependiente de calmodulina (CAMK), que a su vez produce flujo de dopamina. [156] [154] [155] Mediante la activación directa deLos canales de potasio rectificadores internos acoplados a la proteína G , TAAR1 , reduce la velocidad de activación de las neuronas de dopamina, previniendo un estado hiperdopaminérgico. [152] [153] [178]
La anfetamina también es un sustrato para el transportador de monoamina vesicular presináptico , VMAT2 . [150] [151] Después de la absorción de anfetamina en VMAT2, la anfetamina induce el colapso del gradiente de pH vesicular, lo que da como resultado la liberación de moléculas de dopamina de las vesículas sinápticas al citosol a través del flujo de salida de dopamina a través de VMAT2. [150] [151] Posteriormente, las moléculas de dopamina citosólica se liberan desde la neurona presináptica hacia la hendidura sináptica mediante transporte inverso en DAT . [36] [150] [151]
Noradrenalina
Al igual que la dopamina, la anfetamina aumenta de manera dependiente de la dosis el nivel de norepinefrina sináptica, el precursor directo de la epinefrina . [45] [57] Según la expresión del ARNm de TAAR1 neuronal , se cree que la anfetamina afecta la noradrenalina de forma análoga a la dopamina. [36] [150] [177] En otras palabras, la anfetamina induce el flujo de salida mediado por TAAR1 y la inhibición de la recaptación no competitiva en el NET fosforilado , la inhibición de la recaptación competitiva de NET y la liberación de norepinefrina del VMAT2 . [36] [150]
Serotonina
La anfetamina ejerce efectos análogos, aunque menos pronunciados, sobre la serotonina como sobre la dopamina y la norepinefrina. [36] [57] La anfetamina afecta a la serotonina a través de VMAT2 y, al igual que la noradrenalina, se cree que fosforila SERT a través de TAAR1 . [36] [150] Al igual que la dopamina, la anfetamina tiene una afinidad micromolar baja en el receptor 5-HT1A humano . [168] [169]
Otros neurotransmisores, péptidos, hormonas y enzimas
| Enzima | K A ( nM ) | Fuentes |
|---|---|---|
| hCA4 | 94 | [175] |
| hCA5A | 810 | [175] [179] |
| hCA5B | 2560 | [175] |
| hCA7 | 910 | [175] [179] |
| hCA12 | 640 | [175] |
| hCA13 | 24100 | [175] |
| hCA14 | 9150 | [175] |
La administración aguda de anfetaminas en humanos aumenta la liberación de opioides endógenos en varias estructuras cerebrales del sistema de recompensa . [170] [171] [172] Se ha demostrado que los niveles extracelulares de glutamato , el principal neurotransmisor excitador del cerebro, aumentan en el cuerpo estriado después de la exposición a anfetaminas. [154] Este aumento de glutamato extracelular probablemente se produce a través de la internalización inducida por anfetaminas de EAAT3 , un transportador de recaptación de glutamato, en las neuronas de dopamina. [154] [159] La anfetamina también induce la liberación selectiva de histamina demastocitos y eflujo de neuronas histaminérgicas a través de VMAT2 . [150] La administración aguda de anfetaminas también puede aumentar los niveles de hormona adrenocorticotrópica y corticosteroides en el plasma sanguíneo al estimular el eje hipotalámico-pituitario-adrenal . [34] [173] [174]
En diciembre de 2017, se publicó el primer estudio que evaluó la interacción entre la anfetamina y las enzimas anhidrasa carbónica humana ; [175] de las once enzimas de la anhidrasa carbónica que examinó, encontró que la anfetamina activa siete, cuatro de las cuales están altamente expresadas en el cerebro humano , con efectos de activación de bajo nanomolar a bajo micromolar. [175] Según la investigación preclínica, la activación de la anhidrasa carbónica cerebral tiene efectos que mejoran la cognición; [180] pero, basado en el uso clínico de los inhibidores de la anhidrasa carbónica , la activación de la anhidrasa carbónica en otros tejidos pueden estar asociados con efectos adversos, tales como ocularactivación que exacerba el glaucoma . [180]
Farmacocinética
La biodisponibilidad oral de la anfetamina varía con el pH gastrointestinal; [27] Se absorbe bien en el intestino y la biodisponibilidad suele ser superior al 75% para la dextroanfetamina. [3] La anfetamina es una base débil con un p K a de 9,9; [5] en consecuencia, cuando el pH es básico, una mayor parte del fármaco se encuentra en su forma de base libre soluble en lípidos y se absorbe más a través de las membranas celulares ricas en lípidos del epitelio intestinal . [5] [27] Por el contrario, un pH ácido significa que el fármaco se encuentra predominantemente en un catiónico soluble en agua.(sal) y se absorbe menos. [5] Aproximadamente el 20% de la anfetamina que circula en el torrente sanguíneo se une a las proteínas plasmáticas . [4] Después de la absorción, la anfetamina se distribuye fácilmente en la mayoría de los tejidos del cuerpo, con concentraciones altas en el líquido cefalorraquídeo y el tejido cerebral . [11]
Las vidas medias de los enantiómeros de anfetamina difieren y varían con el pH de la orina. [5] Con un pH urinario normal, las vidas medias de la dextroanfetamina y la levoanfetamina son de 9 a 11 horas y de 11 a 14 horas, respectivamente. [5] La orina muy ácida reducirá la vida media del enantiómero a 7 horas; [11] La orina altamente alcalina aumentará la vida media hasta 34 horas. [11] Las variantes de liberación inmediata y de liberación prolongada de las sales de ambos isómeros alcanzan concentraciones plasmáticas máximas a las 3 horas y 7 horas después de la dosis, respectivamente. [5] La anfetamina se elimina a través de los riñones , conEl 30-40% del fármaco se excreta sin cambios a un pH urinario normal. [5] Cuando el pH urinario es básico, la anfetamina está en su forma de base libre, por lo que se excreta menos. [5] Cuando el pH de la orina es anormal, la recuperación urinaria de anfetamina puede variar desde un mínimo del 1% hasta un máximo del 75%, dependiendo principalmente de si la orina es demasiado básica o ácida, respectivamente. [5] Después de la administración oral, la anfetamina aparece en la orina dentro de las 3 horas. [11] Aproximadamente el 90% de la anfetamina ingerida se elimina 3 días después de la última dosis oral. [11]
El profármaco lisdexanfetamina no es tan sensible al pH como la anfetamina cuando se absorbe en el tracto gastrointestinal; [181] después de la absorción en el torrente sanguíneo, las enzimas asociadas a los glóbulos rojos la convierten en dextroanfetamina a través de la hidrólisis . [181] La semivida de eliminación de lisdexanfetamina es generalmente inferior a 1 hora. [181]
CYP2D6 , dopamina β-hidroxilasa (DBH), monooxigenasa 3 que contiene flavina (FMO3), butirato-CoA ligasa (XM-ligasa) y glicina N- aciltransferasa (GLYAT) son las enzimas conocidas por metabolizar la anfetamina o sus metabolitos en humanos. [fuentes 16] La anfetamina tiene una variedad de productos metabólicos excretados, que incluyen 4-hidroxianfetamina , 4-hidroxinorefedrina , 4-hidroxifenilacetona , ácido benzoico , ácido hipúrico , norefedrina y fenilacetona . [5][6] Entre estos metabolitos, los simpaticomiméticos activosson 4-hidroxianfetamina , [182] 4-hidroxinorefedrina , [183] y norefedrina. [184] Las principales vías metabólicas implican laparahidroxilaciónaromática, la alfa y beta hidroxilación alifática, la N- oxidación, la N- desalquilación y la desaminación. [5] [185] Las vías metabólicas conocidas, los metabolitos detectables y las enzimas metabolizadoras en los seres humanos incluyen las siguientes:
Vías metabólicas de la anfetamina en humanos [fuentes 16] |
Farmacomicrobiomia
El metagenoma humano (es decir, la composición genética de un individuo y todos los microorganismos que residen en o dentro del cuerpo del individuo) varía considerablemente entre individuos. [191] [192] Dado que el número total de células microbianas y virales en el cuerpo humano (más de 100 billones) supera en gran medida a las células humanas (decenas de billones), [nota 18] [191] [193] existe un potencial considerable de interacciones entre los fármacos y el microbioma de un individuo, que incluyen: fármacos que alteran la composición del microbioma humano , metabolismo de fármacos por enzimas microbianas que modifican la farmacocinética del fármacoperfil y metabolismo microbiano de fármacos que afectan la eficacia clínica y el perfil de toxicidad de un fármaco . [191] [192] [194] El campo que estudia estas interacciones se conoce como farmacomicrobiomica . [191]
Al igual que la mayoría de las biomoléculas y otros xenobióticos administrados por vía oral (es decir, fármacos), se prevé que la anfetamina sufra un metabolismo promiscuo por la microbiota gastrointestinal humana (principalmente bacterias) antes de su absorción en el torrente sanguíneo . [194] En 2019 se identificó la primera enzima microbiana metabolizadora de anfetaminas, la tiramina oxidasa de una cepa de E. coli que se encuentra comúnmente en el intestino humano. [194] Se descubrió que esta enzima metaboliza anfetamina, tiramina y fenetilamina con aproximadamente el misma afinidad de unión para los tres compuestos. [194]
Compuestos endógenos relacionados
La anfetamina tiene una estructura y función muy similar a las trazas de aminas endógenas , que son moléculas neuromoduladoras de origen natural producidas en el cuerpo y el cerebro humanos. [36] [45] [195] Entre este grupo, los compuestos más estrechamente relacionados son la fenetilamina , el compuesto original de la anfetamina, y la N -metilfenetilamina , un isómero de la anfetamina (es decir, tiene una fórmula molecular idéntica). [36] [45] [196] En los seres humanos, la fenetilamina se produce directamente a partir de la L-fenilalanina por el aminoácido aromático descarboxilasa(AADC), que también convierte la L-DOPA en dopamina. [45] [196] A su vez, la N -metilfenetilamina se metaboliza a partir de la fenetilamina por la feniletanolamina N -metiltransferasa , la misma enzima que metaboliza la norepinefrina en epinefrina. [45] [196] Al igual que la anfetamina, tanto la fenetilamina como la N -metilfenetilamina regulan la neurotransmisión de monoaminas a través de TAAR1 ; [36] [195] [196] a diferencia de la anfetamina, ambas sustancias son degradadas por la monoamino oxidasa B, y por lo tanto tienen una vida media más corta que la anfetamina. [45] [196]
Química
Anfetamina racémica |
Fenil-2-nitropropeno (vasos derechos)
La anfetamina es un metilo homólogo del neurotransmisor de mamíferos fenetilamina con la fórmula química C 9 H 13 N. El átomo de carbono adyacente a la amina primaria es un centro estereogénico y la anfetamina se compone de una mezcla racémica 1: 1 de dos enantiómeros . [22] Esta mezcla racémica se puede separar en sus isómeros ópticos: [nota 19] levoanfetamina y dextroanfetamina . [22] A temperatura ambiente, la base libre pura de anfetamina es un gas incoloro, y el móvil, volátil líquido con un característicamente fuertes amina olor, y acre, sabor ardiente. [20] Las sales sólidas de anfetamina que se preparan con frecuencia incluyen adipato de anfetamina, [197] aspartato,[27] clorhidrato, [198] fosfato, [199] sacarato, [27] sulfato, [27] y tanato. [200] El sulfato de dextroanfetamina es la sal enantiopura más común. [46] La anfetamina es también el compuesto original de su propia clase estructural , que incluye varios derivados psicoactivos. [13] [22] En química orgánica, la anfetamina es un excelente ligando quiral para la síntesis estereoselectiva de 1,1'-bi-2-naftol . [201]
Derivados sustituidos
Los derivados sustituidos de la anfetamina, o "anfetaminas sustituidas", son una amplia gama de productos químicos que contienen anfetamina como "columna vertebral"; [13] [47] [202] específicamente, esta clase química incluye compuestos derivados que se forman reemplazando uno o más átomos de hidrógeno en la estructura del núcleo de la anfetamina con sustituyentes . [13] [47] [203] La clase incluye la anfetamina misma, estimulantes como la metanfetamina, empatógenos serotoninérgicos como la MDMA y descongestionantes como la efedrina , entre otros subgrupos. [13] [47][202]
Síntesis
Desde que se informó sobre la primera preparación en 1887, [204] se han desarrollado numerosas rutas sintéticas para la anfetamina. [205] [206] La ruta más común de síntesis de anfetaminas tanto legal como ilícita emplea una reducción no metálica conocida como reacción de Leuckart (método 1). [46] [207] En el primer paso, una reacción entre fenilacetona y formamida , ya sea utilizando ácido fórmico adicional o la formamida misma como agente reductor, produce N -formilanfetamina.. A continuación, este intermedio se hidroliza usando ácido clorhídrico y posteriormente se alcaliniza, se extrae con un disolvente orgánico, se concentra y se destila para producir la base libre. A continuación, la base libre se disuelve en un disolvente orgánico, se añade ácido sulfúrico y la anfetamina precipita como sal sulfato. [207] [208]
Se han desarrollado varias resoluciones quirales para separar los dos enantiómeros de la anfetamina. [205] Por ejemplo, la anfetamina racémica se puede tratar con ácido d- tartárico para formar una sal diastereoisomérica que se cristaliza fraccionalmente para producir dextroanfetamina. [209] La resolución quiral sigue siendo el método más económico para obtener anfetamina ópticamente pura a gran escala. [210] Además, se han desarrollado varias síntesis enantioselectivas de anfetamina. En un ejemplo, ( R ) -1-fenil-etanamina ópticamente pura se condensa con fenilacetona para producir una base de Schiff quiral . En el paso clave, este intermedio se reduce mediante hidrogenación catalítica con una transferencia de quiralidad al átomo de carbono alfa al grupo amino. La escisión del enlace amina bencílico por hidrogenación produce dextroanfetamina ópticamente pura. [210]
Se ha desarrollado un gran número de rutas sintéticas alternativas a la anfetamina basadas en reacciones orgánicas clásicas. [205] [206] Un ejemplo es la alquilación de Friedel-Crafts de benceno con cloruro de alilo para producir beta cloropropilbenceno que luego se hace reaccionar con amoníaco para producir anfetamina racémica (método 2). [211] Otro ejemplo emplea la reacción de Ritter (método 3). En esta ruta, el alilbenceno se hace reaccionar con acetonitrilo en ácido sulfúrico para producir un organosulfato que a su vez se trata con hidróxido de sodio para dar anfetamina a través de un intermedio de acetamida .[212] [213] Una tercera ruta comienza con 3-oxobutanoato de etilo que mediante una doble alquilación con yoduro de metilo seguida de cloruro de bencilo se puede convertir enácido 2-metil-3-fenilpropanoico . Este intermedio sintético se puede transformar en anfetamina utilizando un reordenamiento de Hofmann o de Curtius (método 4). [214]
Un número significativo de síntesis de anfetamina cuentan con una reducción de un nitro , imina , oxima , u otros que contienen nitrógeno grupos funcionales . [206] En uno de esos ejemplos, una condensación de Knoevenagel de benzaldehído con nitroetano produce fenil-2-nitropropeno . El doble enlace y el grupo nitro de este intermedio se reducen usando hidrogenación catalítica o por tratamiento con hidruro de litio y aluminio (método 5). [207] [215] Otro método es la reacción defenilacetona con amoníaco , que produce un intermedio de imina que se reduce a la amina primaria usando hidrógeno sobre un catalizador de paladio o hidruro de litio y aluminio (método 6). [207]
|
|
Detección en fluidos corporales
La anfetamina se mide con frecuencia en orina o sangre como parte de una prueba de drogas para deportes, empleo, diagnóstico de intoxicaciones y análisis forense. [fuentes 17] Técnicas como el inmunoensayo , que es la forma más común de prueba de anfetaminas, pueden producir reacciones cruzadas con varios fármacos simpaticomiméticos. [219] Se emplean métodos cromatográficos específicos para la anfetamina para prevenir resultados falsos positivos. [220] Se pueden emplear técnicas de separación quiral para ayudar a distinguir la fuente del fármaco, ya sea anfetamina recetada, profármacos de anfetamina recetados (p. Ej., Selegilina ), productos farmacéuticos de venta libre que contienen levometanfetamina ,[nota 20] o anfetaminas sustituidas obtenidas ilícitamente. [220] [223] [224] Varios medicamentos recetados producen anfetamina como metabolito , incluyendo benzfetamina , clobenzorex , famprofazona , fenproporex , lisdexanfetamina , mesocarb , metanfetamina, prenilamina y selegilina , entre otros. [2] [225] [226] Estos compuestos pueden producir resultados positivos para la anfetamina en las pruebas de drogas. [225] [226]Por lo general, la anfetamina solo es detectable mediante una prueba estándar de drogas durante aproximadamente 24 horas, aunque una dosis alta puede detectarse durante 2 a 4 días. [219]
Para los ensayos, un estudio señaló que un ensayo de técnica de inmunoensayo multiplicado por enzimas (EMIT) para anfetamina y metanfetamina puede producir más falsos positivos que la cromatografía líquida-espectrometría de masas en tándem . [223] Cromatografía de gases-espectrometría de masas (GC-MS) de anfetamina y metanfetamina con el agente derivatizante ( S ) - (-) - cloruro de trifluoroacetilprolilo permite la detección de metanfetamina en la orina. [220] La GC-MS de anfetamina y metanfetamina con el agente derivatizante quiral Cloruro de ácido de Mosher permite la detección de dextroanfetamina y dextrometanfetamina en la orina. [220]Por lo tanto, el último método puede usarse en muestras que dan positivo usando otros métodos para ayudar a distinguir entre las diversas fuentes del fármaco. [220]
Historia, sociedad y cultura
| Sustancia | Mejor estimación | Estimación baja | Estimación alta |
|---|---|---|---|
| Anfetamínico estimulantes de tipo | 34,16 | 13.42 | 55,24 |
| Canabis | 192.15 | 165,76 | 234.06 |
| Cocaína | 18.20 | 13,87 | 22,85 |
| Éxtasis | 20.57 | 8,99 | 32,34 |
| Opiáceos | 19,38 | 13.80 | 26.15 |
| Opioides | 34,26 | 27.01 | 44,54 |
La anfetamina fue sintetizada por primera vez en 1887 en Alemania por el químico rumano Lazăr Edeleanu, quien la llamó fenilisopropilamina ; [204] [228] [229] sus efectos estimulantes permanecieron desconocidos hasta 1927, cuando fue resintetizado independientemente por Gordon Alles y se informó que tenía propiedades simpaticomiméticas . [229] La anfetamina no tuvo uso médico hasta finales de 1933, cuando Smith, Kline y French comenzaron a venderla como inhalador bajo la marca Benzedrine como descongestionante. [28] El sulfato de benzedrina se introdujo 3 años después y se utilizó para tratar una amplia variedad decondiciones médicas , que incluyen narcolepsia , obesidad , presión arterial baja , libido baja y dolor crónico , entre otras. [48] [28] Durante la Segunda Guerra Mundial, tanto las fuerzas aliadas como las del Eje consumieron anfetamina y metanfetamina por sus efectos estimulantes y de mejora del rendimiento. [204] [230] [231] A medida que se conocieron las propiedades adictivas de la droga, los gobiernos comenzaron a imponer controles estrictos sobre la venta de anfetaminas. [204] Por ejemplo, a principios de la década de 1970 en los Estados Unidos, la anfetamina se convirtió en una sustancia controlada de la Lista II bajo laLey de Sustancias Controladas . [232] [233] A pesar de los estrictos controles gubernamentales, la anfetamina ha sido consumida legal o ilícitamente por personas de diversos orígenes, incluidos autores, [234] músicos, [235] matemáticos, [236] y atletas. [26]
La anfetamina todavía se sintetiza ilegalmente en laboratorios clandestinos y se vende en el mercado negro , principalmente en países europeos. [237] Entre los estados miembros de la Unión Europea (UE) en 2018, [update]11,9 millones de adultos de entre 15 y 64 años han consumido anfetamina o metanfetamina al menos una vez en la vida y 1,7 millones han consumido cualquiera de las dos en el último año. [238] Durante 2012, se incautaron aproximadamente 5,9 toneladas métricas de anfetamina ilícita en los Estados miembros de la UE; [239] el "precio de venta al público" de la anfetamina ilícita en la UE osciló entre 6 y 38 euros por gramo durante el mismo período. [239]Fuera de Europa, el mercado ilícito de anfetamina es mucho más pequeño que el mercado de metanfetamina y MDMA. [237]
Estatus legal
Como resultado de la Convención de las Naciones Unidas de 1971 sobre Sustancias Psicotrópicas , la anfetamina se convirtió en una sustancia controlada de Lista II, según se define en el tratado, en los 183 estados partes. [29] En consecuencia, está fuertemente regulado en la mayoría de los países. [240] [241] Algunos países, como Corea del Sur y Japón, han prohibido las anfetaminas sustituidas incluso para uso médico. [242] [243] En otras naciones, como Canadá ( medicamento de la lista I ), [244] los Países Bajos ( medicamento de la Lista I ), [245] los Estados Unidos ( medicamento de la lista II ), [27] Australia (Lista 8 ), [246] Tailandia ( narcótico de categoría 1 ), [247] y Reino Unido ( droga de clase B ), [248] la anfetamina se encuentra en una lista de medicamentos nacional restrictiva que permite su uso como tratamiento médico. [237] [30]
Productos farmaceuticos
Varias formulaciones de anfetaminas comercializadas actualmente contienen ambos enantiómeros, incluidos los comercializados con las marcas Adderall, Adderall XR, Mydayis, [nota 1] Adzenys ER, Adzenys XR-ODT , Dyanavel XR, Evekeo y Evekeo ODT. De ellos, Evekeo (incluido Evekeo ODT) es el único producto que contiene solo anfetamina racémica (como sulfato de anfetamina) y, por lo tanto, es el único cuya fracción activa puede denominarse con precisión simplemente "anfetamina". [1] [34] [87] La dextroanfetamina, comercializada con las marcas Dexedrine y Zenzedi, es el único producto de anfetamina enantiopuro disponible actualmente. Una forma de profármaco de dextroanfetamina,lisdexanfetamina , también está disponible y se comercializa con la marca Vyvanse. Como es un profármaco, la lisdexanfetamina es estructuralmente diferente de la dextroanfetamina y permanece inactiva hasta que se metaboliza en dextroanfetamina. [35] [181] La base libre de la anfetamina racémica estaba disponible anteriormente como Benzedrine, Psychedrine y Sympatedrine. [2] La levoanfetamina estaba disponible anteriormente como Cydril. [2] Muchos productos farmacéuticos de anfetamina actuales son sales debido a la volatilidad comparativamente alta de la base libre. [2] [35] [46] Sin embargo, las formas de dosificación de suspensión oral y tableta de desintegración oral (ODT)compuestos por la base libre se introdujeron en 2015 y 2016, respectivamente. [87] [249] [250] Algunas de las marcas actuales y sus equivalentes genéricos se enumeran a continuación.
Nombre de marca | Nombre adoptado de Estados Unidos | (D: L) relación | Forma de dosificación | Fecha de inicio de marketing | Datos de precios al consumidor de EE. UU. | Fuentes |
|---|---|---|---|---|---|---|
| Adderall | - | 3: 1 (sales) | tableta | 1996 | GoodRx | [2] [35] |
| Adderall XR | - | 3: 1 (sales) | cápsula | 2001 | GoodRx | [2] [35] |
| Mydayis | - | 3: 1 (sales) | cápsula | 2017 | GoodRx | [251] [252] |
| Urgencias Adzenys | anfetamina | 3: 1 (base) | suspensión | 2017 | GoodRx | [253] |
| Adzenys XR-ODT | anfetamina | 3: 1 (base) | ODT | 2016 | GoodRx | [250] [254] |
| Dyanavel XR | anfetamina | 3,2: 1 (base) | suspensión | 2015 | GoodRx | [87] [249] |
| Evekeo | sulfato de anfetamina | 1: 1 (sales) | tableta | 2012 | GoodRx | [34] [255] |
| Evekeo ODT | sulfato de anfetamina | 1: 1 (sales) | ODT | 2019 | GoodRx | [256] |
| Dexedrina | sulfato de dextroanfetamina | 1: 0 (sales) | cápsula | 1976 | GoodRx | [2] [35] |
| Zenzedi | sulfato de dextroanfetamina | 1: 0 (sales) | tableta | 2013 | GoodRx | [35] [257] |
| Vyvanse | dimesilato de lisdexanfetamina | 1: 0 (profármaco) | cápsula | 2007 | GoodRx | [2] [181] [258] |
| tableta |
| droga | fórmula | masa molecular [nota 21] | base de anfetamina [nota 22] | base de anfetamina en dosis iguales | dosis con igual contenido de base [nota 23] | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| (g / mol) | (por ciento) | (Dosis de 30 mg) | ||||||||
| total | base | total | dextro- | levo- | dextro- | levo- | ||||
| sulfato de dextroanfetamina [260] [261] | (C 9 H 13 N) 2 • H 2 SO 4 | 368,49 | 270,41 | 73,38% | 73,38% | - | 22,0 magnesio | - | 30,0 mg | |
| sulfato de anfetamina [262] | (C 9 H 13 N) 2 • H 2 SO 4 | 368,49 | 270,41 | 73,38% | 36,69% | 36,69% | 11,0 mg | 11,0 mg | 30,0 mg | |
| Adderall | 62,57% | 47,49% | 15,08% | 14,2 magnesio | 4,5 mg | 35,2 magnesio | ||||
| 25% | sulfato de dextroanfetamina [260] [261] | (C 9 H 13 N) 2 • H 2 SO 4 | 368,49 | 270,41 | 73,38% | 73,38% | - | |||
| 25% | sulfato de anfetamina [262] | (C 9 H 13 N) 2 • H 2 SO 4 | 368,49 | 270,41 | 73,38% | 36,69% | 36,69% | |||
| 25% | sacarato de dextroanfetamina [263] | (C 9 H 13 N) 2 • C 6 H 10 O 8 | 480,55 | 270,41 | 56,27% | 56,27% | - | |||
| 25% | aspartato de anfetamina monohidrato [264] | (C 9 H 13 N) • C 4 H 7 NO 4 • H 2 O | 286,32 | 135,21 | 47,22% | 23,61% | 23,61% | |||
| dimesilato de lisdexanfetamina [181] | C 15 H 25 N 3 O • (CH 4 O 3 S) 2 | 455,49 | 135,21 | 29,68% | 29,68% | - | 8,9 magnesio | - | 74,2 magnesio | |
| suspensión a base de anfetaminas [87] | C 9 H 13 N | 135,21 | 135,21 | 100% | 76,19% | 23,81% | 22,9 magnesio | 7,1 mg | 22,0 magnesio | |
Notas
- ^ a b Adderall y otros productos de sales de anfetaminas mixtas como Mydayis no son anfetaminas racémicas , son una mezcla compuesta de partes iguales de racemato y dextroanfetamina .
Consulte Sales mixtas de anfetamina para obtener más información sobre la mezcla, y esta sección para obtener información sobre las diversas mezclas de enantiómeros de anfetamina que se comercializan actualmente. - ^ Los sinónimos y grafías alternativas incluyen: 1-fenilpropan-2-amina (nombre IUPAC ), α-metilfenetilamina , anfetamina ( denominación común internacional [DCI] ), β-fenilisopropilamina y velocidad . [21] [22] [23]
- ^ Los enantiómeros son moléculas que son imágenes especulares entre sí; son estructuralmente idénticos, pero de orientación opuesta. [24] La
levoanfetamina y la dextroanfetamina también se conocen como L-amph o levanfetamina ( DCI ) y D-amph o dexanfetamina (DCI), respectivamente. [21] - ^ La marca Adderall se usa principalmente en este artículo para referirse a la mezcla de sal de anfetamina que contiene porque la composición de cuatro sales del medicamento hace que su nombre común (sulfato de dextroanfetamina al 25%, sacarato de dextroanfetamina al 25%, sulfato de anfetamina al 25% y aspartato de anfetamina 25%) excesivamente largo. [35]
- ^ El término "anfetaminas" también se refiere a una clase química, pero, a diferencia de la clase de anfetaminas sustituidas, [13] la clase "anfetaminas" no tiene una definición estandarizada en la literatura académica. [17] Una de las definiciones más restrictivas de esta clase incluye solo el racemato y los enantiómeros de anfetamina y metanfetamina. [17] La definición más general de la clase abarca una amplia gama de compuestos relacionados farmacológica y estructuralmente. [17]
Debido a la confusión que puede surgir del uso de la forma plural, este artículo solo usará los términos "anfetamina" y "anfetaminas" para referirse a la anfetamina racémica, levoanfetamina y dextroanfetamina y reserva el término "anfetaminas sustituidas" para su clase estructural. - ^ Los dominios de resultados relacionados con el TDAH con la mayor proporción de resultados significativamente mejorados de la terapia estimulante continua a largo plazo incluyen académicos (≈55% de los resultados académicos mejoraron), conducción (100% de los resultados de conducción mejorados), uso de drogas no médicas ( El 47% de los resultados relacionados con la adicción mejoraron), la obesidad (≈65% de los resultados relacionados con la obesidad mejoraron), la autoestima (el 50% de los resultados de la autoestima mejoraron) y la función social (el 67% de los resultados de la función social mejoraron). [55]
Los tamaños de efecto más grandes para las mejoras de los resultados de la terapia estimulante a largo plazo ocurren en los dominios que involucran a académicos (p. Ej., Promedio de calificaciones, puntajes de las pruebas de rendimiento, duración de la educación y nivel de educación), autoestima (p. ej., evaluaciones del cuestionario de autoestima, número de intentos de suicidio y tasas de suicidio) y función social (p. ej., puntajes de nominación de pares, habilidades sociales y calidad de las relaciones románticas, familiares y con los compañeros). [55]
La terapia combinada a largo plazo para el TDAH (es decir, el tratamiento con un estimulante y terapia conductual) produce efectos aún mayores para mejorar los resultados y mejora una mayor proporción de resultados en cada dominio en comparación con la terapia estimulante a largo plazo sola. [55] - ^ Las revisiones Cochrane son revisiones sistemáticas metaanalíticas de alta calidad de ensayos controlados aleatorios. [61]
- ^ Las declaraciones respaldadas por la USFDA provienen de información de prescripción, que es propiedad intelectual con derechos de autor del fabricante y aprobada por la USFDA. Las contraindicaciones de la USFDA no tienen por qué limitar la práctica médica, sino limitar las afirmaciones de las compañías farmacéuticas. [82]
- ^ Según una revisión, se puede recetar anfetamina a personas con antecedentes de abuso siempre que se empleen controles de medicación adecuados, como por ejemplo, exigir la recogida diaria del medicamento por parte del médico que prescribe. [2]
- ^ En las personas que experimentan aumentos de peso y altura por debajo de lo normal, se espera que ocurra un rebote a los niveles normales si se interrumpe brevemente la terapia estimulante. [42] [54] [86] La reducción promedio en la estatura adulta final a partir de 3 años de terapia estimulante continua es de 2 cm. [86]
- ^ Los factores de transcripción son proteínas que aumentan o disminuyen la expresión de genes específicos. [115]
- ^ En términos más simples, esta relación necesaria y suficiente significa que la sobreexpresión de ΔFosB en el núcleo accumbens y las adaptaciones conductuales y neuronales relacionadas con la adicción siempre ocurren juntas y nunca ocurren solas.
- ^ Los receptores NMDA son canales iónicos dependientes de voltaje dependientes de ligando que requieren la unión simultánea de glutamato y un coagonista ( D- serina o glicina ) para abrir el canal iónico. [129]
- ^ La revisión indicó que el L-aspartato de magnesio y el cloruro de magnesio producen cambios significativos en el comportamiento adictivo; [106] no se mencionaron otras formas de magnesio.
- ^ El intervalo de confianza del 95% indica que existe una probabilidad del 95% de que el número real de muertes se encuentre entre 3.425 y 4.145.
- ^ a b El transportador de dopamina humano (hDAT) contiene un sitio de unión de Zn 2+ (ion zinc) extracelular y alostérico de alta afinidad que, al unirse al zinc, inhibe la recaptación de dopamina , inhibe la internalización de hDAT inducida por anfetaminas y amplifica la anfetamina. flujo de dopamina inducido . [145] [146] [147] [148] El transportador de serotonina humana y el transportador de norepinefrina no contienen sitios de unión al zinc. [147]
- ^ 4-hydroxyamphetamine se ha demostrado para ser metabolizado en 4-hydroxynorephedrine por la dopamina beta-hidroxilasa (DBH) in vitro y se presume que son metabolizados de manera similar in vivo . [13] [186] La evidencia de estudios que midieron el efecto de las concentraciones séricas de DAP sobre elmetabolismo de la 4-hidroxianfetamina en humanos sugiere que una enzima diferente puede mediar la conversión de 4-hidroxianfetamina en 4-hidroxinorrefedrina ; [186] [188] sin embargo, otra evidencia de estudios en animales sugiere que esta reacción es catalizada por DAP en vesículas sinápticasdentro de las neuronas noradrenérgicas del cerebro. [189] [190]
- ^ Existe una variación sustancial en la composición del microbioma y las concentraciones microbianas según el sitio anatómico. [191] [192] El líquido del colon humano, que contiene la mayor concentración de microbios de cualquier sitio anatómico, contiene aproximadamente un billón (10 ^ 12) de células bacterianas / ml. [191]
- ^ Los enantiómeros son moléculas que son imágenes especulares entre sí; son estructuralmente idénticos, pero de orientación opuesta. [24]
- ^ El ingrediente activo en algunos inhaladores de venta libre en los Estados Unidos está listado como levmetamfetamina , el INN y USAN de la levometanfetamina. [221] [222]
- ^ Para la uniformidad, las masas moleculares se calcularon utilizando la calculadora de peso molecular de Lenntech [259] y estaban dentro de 0,01 g / mol de los valores farmacéuticos publicados.
- ^ Porcentaje de base de anfetamina = base de masa molecular / masa molecular total . Porcentaje de base de anfetaminas para Adderall = suma de porcentajes de componentes / 4.
- ^ dosis = (1 / porcentaje de base de anfetamina) × factor de escala = (masa molecular total / base de masa molecular) × factor de escala. Los valores de esta columna se ajustaron a una dosis de 30 mg de sulfato de dextroanfetamina. Debido a las diferencias farmacológicas entre estos medicamentos (p. Ej., Diferencias en la liberación, absorción, conversión, concentración, efectos diferentes de los enantiómeros, vida media, etc.), los valores enumerados no deben considerarse dosis equipotentes.
- Leyenda de la imagen
- ^ Canal de ionesProteínas G y receptores ligados(Color del texto) Factores de transcripción
Notas de referencia
- ^ [2] [17] [25] [26] [27] [28] [29] [30] [31] [32] [33] [34]
- ^ [2] [10] [25] [28] [34] [36] [37]
- ^ [10] [25] [26] [27] [31] [38] [39] [40] [41] [42] [43] [44]
- ^ [45] [46] [47]
- ^ [1] [27] [38] [86] [87] [88]
- ^ [89] [90] [91] [92]
- ^ [27] [83] [89] [91]
- ^ [31] [27] [38] [93]
- ^ a b [109] [110] [111] [112] [131]
- ^ [107] [109] [108] [116] [117]
- ^ [108] [119] [120] [121]
- ^ [23] [27] [38] [135] [137]
- ^ [49] [139] [142] [143]
- ^ a b [150] [154] [158] [159] [160] [161] [162]
- ^ [36] [150] [158] [159] [163] [168]
- ^ a b [5] [13] [14] [15] [16] [6] [186] [187]
- ^ [26] [216] [217] [218]
Referencias
- ^ a b c d e f g h i j Stahl SM (marzo de 2017). "Anfetamina (D, L)" . Guía del prescriptor: Psicofarmacología esencial de Stahl (6ª ed.). Cambridge, Reino Unido: Cambridge University Press. págs. 45–51. ISBN 9781108228749. Consultado el 5 de agosto de 2017 .
- ^ a b c d e f g h i j k l m Heal DJ, Smith SL, Gosden J, Nutt DJ (junio de 2013). "Anfetamina, pasado y presente: una perspectiva farmacológica y clínica" . Revista de Psicofarmacología . 27 (6): 479–496. doi : 10.1177 / 0269881113482532 . PMC 3666194 . PMID 23539642 .
El uso intravenoso de d-anfetamina y otros estimulantes todavía presenta importantes riesgos de seguridad para las personas que se entregan a esta práctica. Parte de este abuso intravenoso se deriva del desvío de ampollas de d-anfetamina, que todavía se recetan ocasionalmente en el Reino Unido para el control de la narcolepsia grave y otros trastornos de sedación excesiva. ... Por estas razones, las observaciones de dependencia y abuso de d-anfetamina recetada son raras en la práctica clínica, y este estimulante incluso se puede recetar a personas con antecedentes de abuso de drogas siempre que se realicen ciertos controles, como la recogida diaria de recetas. , se ponen en marcha (Jasinski y Krishnan, 2009b).
- ^ a b "Farmacología" . Dextroanfetamina . DrugBank . Universidad de Alberta. 8 de febrero de 2013 . Consultado el 5 de noviembre de 2013 .
- ^ a b c d e "Farmacología" . Anfetamina . DrugBank . Universidad de Alberta. 8 de febrero de 2013 . Consultado el 5 de noviembre de 2013 .
- ^ a b c d e f g h i j k l m n o p q r s "Información de prescripción de Adderall XR" (PDF) . Administración de Drogas y Alimentos de los Estados Unidos . Shire US Inc. Diciembre de 2013. págs. 12–13 . Consultado el 30 de diciembre de 2013 .
- ↑ a b c d Santagati NA, Ferrara G, Marrazzo A, Ronsisvalle G (septiembre de 2002). "Determinación simultánea de anfetamina y uno de sus metabolitos por HPLC con detección electroquímica". Revista de análisis farmacéutico y biomédico . 30 (2): 247-255. doi : 10.1016 / S0731-7085 (02) 00330-8 . PMID 12191709 .
- ^ "Farmacología" . anfetamina / dextroanfetamina . Medscape . WebMD . Consultado el 21 de enero de 2016 .
Inicio de acción: 30 a 60 min.
- ↑ a b c Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: Guía del médico sobre el TDAH (2ª ed.). Nueva York, Estados Unidos: Springer. pag. 112. ISBN 9781441913968.
Tabla 9.2 Formulaciones de dextroanfetamina de la medicación estimulante
Dexedrine [Pico: 2-3 h] [Duración: 5-6 h] ...
Adderall [Pico: 2-3 h] [Duración: 5-7 h]
Dexedrine spansules [Pico: 7 –8 h] [Duración: 12 h] ...
Adderall XR [Pico: 7-8 h] [Duración: 12 h]
Vyvanse [Pico: 3-4 h] [Duración: 12 h] - ^ Brams M, Mao AR, Doyle RL (septiembre de 2008). "Inicio de la eficacia de los psicoestimulantes de acción prolongada en el trastorno por déficit de atención con hiperactividad pediátrica". Postgrado en Medicina . 120 (3): 69–88. doi : 10.3810 / pgm.2008.09.1909 . PMID 18824827 . S2CID 31791162 .
- ^ a b c d "Adderall- sacarato de dextroanfetamina, aspartato de anfetamina, sulfato de dextroanfetamina y tableta de sulfato de anfetamina" . DailyMed . Teva Pharmaceuticals USA, Inc.8 de noviembre de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ a b c d e f "Metabolismo / farmacocinética". Anfetamina . Biblioteca Nacional de Medicina de los Estados Unidos - Red de datos de toxicología . Banco de datos de sustancias peligrosas. Archivado desde el original el 2 de octubre de 2017 . Consultado el 2 de octubre de 2017 .
La duración del efecto varía según el agente y el pH de la orina. La excreción aumenta en orina más ácida. La vida media es de 7 a 34 horas y depende, en parte, del pH de la orina (la vida media es más larga con orina alcalina). ... Las anfetaminas se distribuyen en la mayoría de los tejidos corporales con altas concentraciones en el cerebro y el LCR. La anfetamina aparece en la orina aproximadamente 3 horas después de la administración oral. ... Tres días después de una dosis de (+ o -) - anfetamina, los sujetos humanos habían excretado el 91% de la (14) C en la orina
- ^ a b Mignot EJ (octubre de 2012). "Una guía práctica para la terapia de los síndromes de narcolepsia e hipersomnia" . Neuroterapéutica . 9 (4): 739–752. doi : 10.1007 / s13311-012-0150-9 . PMC 3480574 . PMID 23065655 .
- ↑ a b c d e f g h i Glennon RA (2013). "Estimulantes de fenilisopropilamina: agentes relacionados con las anfetaminas" . En Lemke TL, Williams DA, Roche VF, Zito W (eds.). Principios de química medicinal de Foye (7ª ed.). Filadelfia, Estados Unidos: Wolters Kluwer Health / Lippincott Williams & Wilkins. págs. 646–648. ISBN 9781609133450.
La fenilisopropilamina no sustituida más simple, el 1-fenil-2-aminopropano o anfetamina, sirve como plantilla estructural común para los alucinógenos y psicoestimulantes. La anfetamina produce acciones estimulantes centrales, anoréxicas y simpaticomiméticas, y es el miembro prototipo de esta clase (39). ... El metabolismo de fase 1 de los análogos de anfetaminas está catalizado por dos sistemas: el citocromo P450 y la flavina monooxigenasa. ... La anfetamina también puede sufrir hidroxilación aromática a p -hidroxianfetamina. ... La oxidación posterior en la posición bencílica por DA β-hidroxilasa produce p -hidroxinorefedrina. Alternativamente, la oxidación directa de anfetamina por DA β-hidroxilasa puede producir norefedrina.
- ^ a b Taylor KB (enero de 1974). "Dopamina-beta-hidroxilasa. Curso estereoquímico de la reacción" (PDF) . Revista de Química Biológica . 249 (2): 454–458. PMID 4809526 . Consultado el 6 de noviembre de 2014 .
La dopamina-β-hidroxilasa catalizó la eliminación del átomo de hidrógeno pro-R y la producción de 1-norefedrina, (2
S
, 1
R
) -2-amino-1-hidroxil-1-fenilpropano, a partir de d-anfetamina.
- ↑ a b c Krueger SK, Williams DE (junio de 2005). "Monooxigenasas que contienen flavina de mamíferos: estructura / función, polimorfismos genéticos y papel en el metabolismo de fármacos" . Farmacología y terapéutica . 106 (3): 357–387. doi : 10.1016 / j.pharmthera.2005.01.001 . PMC 1828602 . PMID 15922018 .
Tabla 5: Fármacos que contienen N y xenobióticos oxigenados por FMO - ↑ a b Cashman JR, Xiong YN, Xu L, Janowsky A (marzo de 1999). "N-oxigenación de anfetamina y metanfetamina por la monooxigenasa que contiene flavina humana (forma 3): papel en la bioactivación y desintoxicación". Revista de Farmacología y Terapéutica Experimental . 288 (3): 1251-1260. PMID 10027866 .
- ↑ a b c d e Yoshida T (1997). "Capítulo 1: Uso y uso indebido de anfetaminas: una visión internacional" . En Klee H (ed.). Uso indebido de anfetaminas: perspectivas internacionales sobre las tendencias actuales . Amsterdam, Países Bajos: Harwood Academic Publishers. pag. 2 . ISBN 9789057020810.
La anfetamina, en forma singular, se aplica correctamente al racemato de 2-amino-1-fenilpropano. ... En su contexto más amplio, sin embargo, el término [ anfetaminas ] puede incluso abarcar un gran número de sustancias relacionadas estructural y farmacológicamente.
- ^ "Densidad" . Anfetamina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica. 5 de noviembre de 2016 . Consultado el 9 de noviembre de 2016 .
- ^ "Propiedades: Previsto - EPISuite" . Anfetamina . ChemSpider . Real Sociedad de Química . Consultado el 6 de noviembre de 2013 .
- ^ a b "Propiedades químicas y físicas" . Anfetamina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 13 de octubre de 2013 .
- ^ a b c "Resumen compuesto" . Anfetamina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica. 11 de abril de 2015 . Consultado el 17 de abril de 2015 .
- ^ a b c d "Identificación" . Anfetamina . DrugBank . Universidad de Alberta. 8 de febrero de 2013 . Consultado el 13 de octubre de 2013 .
- ↑ a b Greene SL, Kerr F, Braitberg G (octubre de 2008). "Artículo de revisión: anfetaminas y drogas de abuso relacionadas". Medicina de emergencia Australasia . 20 (5): 391–402. doi : 10.1111 / j.1742-6723.2008.01114.x . PMID 18973636 . S2CID 20755466 .
- ^ a b "Enantiómero" . Compendio de terminología química de la IUPAC . IUPAC Goldbook . Unión internacional de Química Pura Aplicada. 2009. doi : 10.1351 / goldbook.E02069 . ISBN 9780967855097. Archivado desde el original el 17 de marzo de 2013 . Consultado el 14 de marzo de 2014 .
Uno de un par de entidades moleculares que son imágenes especulares entre sí y no superponibles.
- ↑ a b c d e f g h i j Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 13: función cognitiva superior y control del comportamiento". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. págs. 318, 321. ISBN 9780071481274.
Las dosis terapéuticas (relativamente bajas) de psicoestimulantes, como el metilfenidato y la anfetamina, mejoran el rendimiento en las tareas de la memoria de trabajo tanto en sujetos normales como en aquellos con TDAH. ... los estimulantes actúan no solo sobre la función de la memoria de trabajo, sino también sobre los niveles generales de excitación y, dentro del núcleo accumbens, mejoran la relevancia de las tareas. Por lo tanto, los estimulantes mejoran el rendimiento en tareas laboriosas pero tediosas ... a través de la estimulación indirecta de los receptores de dopamina y norepinefrina. ...
Más allá de estos efectos permisivos generales, la dopamina (que actúa a través de los receptores D1) y la noradrenalina (que actúa en varios receptores) pueden, en niveles óptimos, mejorar la memoria de trabajo y los aspectos de la atención. - ^ a b c d e f g Liddle DG, Connor DJ (junio de 2013). "Suplementos nutricionales y SIDA ergogénico". Atención Primaria: Clínicas en Consultorio . 40 (2): 487–505. doi : 10.1016 / j.pop.2013.02.009 . PMID 23668655 .
Las anfetaminas y la cafeína son estimulantes que aumentan el estado de alerta, mejoran la concentración, disminuyen el tiempo de reacción y retrasan la fatiga, lo que permite una mayor intensidad y duración del entrenamiento ...
Efectos fisiológicos y de rendimiento
• Las anfetaminas aumentan la liberación de dopamina / norepinefrina e inhiben su recaptación, lo que lleva a estimulación del sistema nervioso central (SNC)
• Las anfetaminas parecen mejorar el rendimiento deportivo en condiciones anaeróbicas 39 40
• Tiempo de reacción mejorado
• Mayor fuerza muscular y fatiga muscular retardada
• Mayor aceleración
• Mayor alerta y atención a la tarea - ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an "Adderall XR- sulfato de dextroanfetamina, sacarato de dextroanfetamina , cápsula de sulfato de anfetamina y aspartato de anfetamina, liberación prolongada " . DailyMed . Shire US Inc.17 de julio de 2019 . Recuperado22 de diciembre de 2019 .
- ↑ a b c d Rasmussen N (julio de 2006). "Fabricación del primer antidepresivo: anfetamina en la medicina estadounidense, 1929-1950". Revista de Historia de la Medicina y Ciencias Afines . 61 (3): 288–323. doi : 10.1093 / jhmas / jrj039 . PMID 16492800 . S2CID 24974454 .
Sin embargo, la empresa descubrió el medicamento, SKF lo empaquetó primero como un inhalador para aprovechar la volatilidad de la base y, después de patrocinar algunos ensayos realizados por especialistas en otorrinolaringología de la costa este, comenzó a publicitar el inhalador de bencedrina como descongestionante a fines de 1933.
- ^ a b "Convenio sobre sustancias psicotrópicas" . Colección de tratados de las Naciones Unidas . Naciones Unidas. Archivado desde el original el 31 de marzo de 2016 . Consultado el 11 de noviembre de 2013 .
- ^ a b Wilens TE, Adler LA, Adams J, Sgambati S, Rotrosen J, Sawtelle R, Utzinger L, Fusillo S (enero de 2008). "Mal uso y desvío de estimulantes prescritos para el TDAH: una revisión sistemática de la literatura". Revista de la Academia Estadounidense de Psiquiatría Infantil y Adolescente . 47 (1): 21–31. doi : 10.1097 / chi.0b013e31815a56f1 . PMID 18174822 .
El uso indebido de estimulantes parece producirse tanto para mejorar el rendimiento como para sus efectos euforogénicos; estos últimos están relacionados con las propiedades intrínsecas de los estimulantes (p. Ej., Perfil de RI versus ER) ...
Aunque útiles en el tratamiento del TDAH, los estimulantes son sustancias controladas II con antecedentes de estudios preclínicos y en humanos que muestran una posible propensión al abuso. - ↑ a b c Montgomery KA (junio de 2008). "Trastornos del deseo sexual" . Psiquiatría . 5 (6): 50–55. PMC 2695750 . PMID 19727285 .
- ^ "Anfetamina" . Encabezamientos de materias médicas . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 16 de diciembre de 2013 .
- ^ "Directrices sobre el uso de denominaciones comunes internacionales (DCI) para sustancias farmacéuticas" . Organización Mundial de la Salud. 1997 . Consultado el 1 de diciembre de 2014 .
En principio, las DCI se seleccionan solo por la parte activa de la molécula que suele ser la base, el ácido o el alcohol. En algunos casos, sin embargo, las moléculas activas necesitan expandirse por diversas razones, tales como propósitos de formulación, biodisponibilidad o tasa de absorción. En 1975, los expertos designados para la selección de DCI decidieron adoptar una nueva política para nombrar tales moléculas. En el futuro, los nombres de diferentes sales o ésteres de la misma sustancia activa deberían diferir solo con respecto al resto inactivo de la molécula. ... Estos últimos se denominan DCI modificados (INNM).
- ^ a b c d e f g h i "Evekeo- tableta de sulfato de anfetamina" . DailyMed . Arbor Pharmaceuticals, LLC. 14 de agosto de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ a b c d e f g h "Resultados de la búsqueda de anfetaminas del Código Nacional de Drogas" . Directorio del Código Nacional de Drogas . Administración de Drogas y Alimentos de los Estados Unidos. Archivado desde el original el 16 de diciembre de 2013 . Consultado el 16 de diciembre de 2013 .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad Miller GM (enero de 2011). "El papel emergente del receptor 1 asociado a trazas de amina en la regulación funcional de los transportadores de monoamina y la actividad dopaminérgica" . Revista de neuroquímica . 116 (2): 164-176. doi : 10.1111 / j.1471-4159.2010.07109.x . PMC 3005101 . PMID 21073468 .
- ^ a b c d e Grandy DK, Miller GM, Li JX (febrero de 2016). " " TAARgeting Addiction "-The Alamo da testimonio de otra revolución: una descripción general del simposio plenario de la Conferencia de 2015 sobre comportamiento, biología y química" . Dependencia de drogas y alcohol . 159 : 9-16. doi : 10.1016 / j.drugalcdep.2015.11.014 . PMC 4724540 . PMID 26644139 .
Cuando se considera junto con la literatura en rápido crecimiento en el campo, surge un caso convincente en apoyo del desarrollo de agonistas selectivos de TAAR1 como medicamentos para prevenir la recaída en el abuso de psicoestimulantes.
- ^ a b c d e f g h i j k l m n o p q r s t u v w Westfall DP, Westfall TC (2010). "Agonistas simpaticomiméticos diversos". En Brunton LL, Chabner BA, Knollmann BC (eds.). Bases farmacológicas de la terapéutica de Goodman & Gilman (12ª ed.). Nueva York, Estados Unidos: McGraw-Hill. ISBN 9780071624428.
- ^ a b c d e Shoptaw SJ, Kao U, Ling W (enero de 2009). Shoptaw SJ, Ali R (ed.). "Tratamiento para la psicosis anfetamínica" . Base de datos Cochrane de revisiones sistemáticas (1): CD003026. doi : 10.1002 / 14651858.CD003026.pub3 . PMC 7004251 . PMID 19160215 .
Una minoría de personas que usan anfetaminas desarrollan psicosis en toda regla que requieren atención en departamentos de emergencia u hospitales psiquiátricos. En tales casos, los síntomas de la psicosis anfetamínica suelen incluir delirios paranoicos y persecutorios, así como alucinaciones auditivas y visuales en presencia de agitación extrema. Más común (alrededor del 18%) es que los consumidores frecuentes de anfetaminas reporten síntomas psicóticos que son subclínicos y que no requieren una intervención de alta intensidad ...
Alrededor del 5 al 15% de los consumidores que desarrollan una psicosis anfetamínica no se recuperan por completo (Hofmann 1983) ...
Los resultados de un ensayo indican que el uso de fármacos antipsicóticos resuelve eficazmente los síntomas de la psicosis anfetamínica aguda.
Los síntomas psicóticos de las personas con psicosis anfetamínica pueden deberse exclusivamente al uso intensivo de la droga o el uso intensivo de la droga puede exacerbar una vulnerabilidad subyacente a la esquizofrenia. - ↑ a b c d e Bramness JG, Gundersen ØH, Guterstam J, Rognli EB, Konstenius M, Løberg EM, Medhus S, Tanum L, Franck J (diciembre de 2012). "Psicosis inducida por anfetaminas: ¿una entidad de diagnóstico separada o psicosis primaria desencadenada en los vulnerables?" . Psiquiatría BMC . 12 : 221. doi : 10.1186 / 1471-244X-12-221 . PMC 3554477 . PMID 23216941 .
En estos estudios, la anfetamina se administró en dosis sucesivamente más altas hasta que se precipitó la psicosis, a menudo después de 100-300 mg de anfetamina ... En segundo lugar, la psicosis se ha considerado un evento adverso, aunque raro, en niños con TDAH que han sido tratados con anfetamina
- ^ a b c Greydanus D. "Uso indebido de estimulantes: estrategias para gestionar un problema creciente" (PDF) . American College Health Association (artículo de revisión). Programa de desarrollo profesional de ACHA. pag. 20. Archivado desde el original (PDF) el 3 de noviembre de 2013 . Consultado el 2 de noviembre de 2013 .
- ^ a b c d e f g h Huang YS, Tsai MH (julio de 2011). "Resultados a largo plazo con medicamentos para el trastorno por déficit de atención con hiperactividad: estado actual del conocimiento". Medicamentos para el SNC . 25 (7): 539–554. doi : 10.2165 / 11589380-000000000-00000 . PMID 21699268 . S2CID 3449435 .
Varios otros estudios,
[97-101],
incluida una revisión metaanalítica
[98]
y un estudio retrospectivo,
[97]
sugirió que la terapia con estimulantes en la infancia está asociada con un riesgo reducido de abuso de sustancias, tabaquismo y trastornos por consumo de alcohol. ... Estudios recientes han demostrado que los estimulantes, junto con los no estimulantes atomoxetina y guanfacina de liberación prolongada, son continuamente efectivos durante períodos de tratamiento de más de 2 años con pocos y tolerables efectos adversos. La efectividad de la terapia a largo plazo incluye no solo los síntomas centrales del TDAH, sino también una mejor calidad de vida y logros académicos. Los efectos adversos a corto plazo más preocupantes de los estimulantes, como la hipertensión arterial y la frecuencia cardíaca, disminuyeron en los estudios de seguimiento a largo plazo. ... Los datos actuales no apoyan el impacto potencial de los estimulantes en el empeoramiento o desarrollo de tics o abuso de sustancias en la edad adulta.En el estudio de seguimiento más largo (de más de 10 años), el tratamiento estimulante de por vida para el TDAH fue eficaz y protector contra el desarrollo de trastornos psiquiátricos adversos.
- ↑ a b Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Capítulo 16: Refuerzo y trastornos adictivos". Neurofarmacología molecular: una base para la neurociencia clínica (3ª ed.). Nueva York: McGraw-Hill Medical. ISBN 9780071827706.
Dichos agentes también tienen importantes usos terapéuticos; la cocaína, por ejemplo, se usa como anestésico local (Capítulo 2), y las anfetaminas y el metilfenidato se usan en dosis bajas para tratar el trastorno por déficit de atención con hiperactividad y en dosis más altas para tratar la narcolepsia (Capítulo 12). A pesar de sus usos clínicos, estos medicamentos son un fuerte refuerzo y su uso a largo plazo en dosis altas está relacionado con una posible adicción, especialmente cuando se administran rápidamente o cuando se administran formas de alta potencia.
- ^ a b Kollins SH (mayo de 2008). "Una revisión cualitativa de los problemas que surgen en el uso de medicamentos psicoestimulantes en pacientes con TDAH y trastornos comórbidos por uso de sustancias". Investigación y opinión médica actual . 24 (5): 1345-1357. doi : 10.1185 / 030079908X280707 . PMID 18384709 . S2CID 71267668 .
Cuando se utilizan formulaciones orales de psicoestimulantes en las dosis y frecuencias recomendadas, es poco probable que produzcan efectos compatibles con el potencial de abuso en pacientes con TDAH.
- ↑ a b c d e f g Broadley KJ (marzo de 2010). "Los efectos vasculares de las trazas de aminas y anfetaminas". Farmacología y terapéutica . 125 (3): 363–375. doi : 10.1016 / j.pharmthera.2009.11.005 . PMID 19948186 .
- ^ a b c d "Anfetamina" . Observatorio Europeo de las Drogas y las Toxicomanías . Consultado el 19 de octubre de 2013 .
- ↑ a b c d Hagel JM, Krizevski R, Marsolais F, Lewinsohn E, Facchini PJ (2012). "Biosíntesis de análogos de anfetaminas en plantas". Tendencias en ciencia de las plantas . 17 (7): 404–412. doi : 10.1016 / j.tplants.2012.03.004 . PMID 22502775 .
Las anfetaminas sustituidas, que también se denominan alcaloides fenilpropilamino, son un grupo diverso de compuestos que contienen nitrógeno que presentan una cadena principal de fenetilamina con un grupo metilo en la posición α en relación con el nitrógeno (Figura 1). ... Más allá de (1
R
, 2
S
) -efedrina y (1
S
, 2
S)
) -seudoefedrina, una miríada de otras anfetaminas sustituidas tienen importantes aplicaciones farmacéuticas. ... Por ejemplo, la ( S ) -anfetamina (Figura 4b), un ingrediente clave en Adderall y Dexedrine, se usa para tratar el trastorno por déficit de atención con hiperactividad (TDAH) [79]. ...
[Figura 4] (b) Ejemplos de anfetaminas sintéticas sustituidas de importancia farmacéutica. - ↑ a b Bett WR (agosto de 1946). "Sulfato de bencedrina en medicina clínica; un estudio de la literatura" . Revista Médica de Postgrado . 22 (250): 205–218. doi : 10.1136 / pgmj.22.250.205 . PMC 2478360 . PMID 20997404 .
- ^ a b Carvalho M, Carmo H, Costa VM, Capela JP, Pontes H, Remião F, Carvalho F, Bastos Mde L (agosto de 2012). "Toxicidad de las anfetaminas: una actualización". Archivos de Toxicología . 86 (8): 1167-1231. doi : 10.1007 / s00204-012-0815-5 . PMID 22392347 . S2CID 2873101 .
- ^ Berman S, O'Neill J, Fears S, Bartzokis G, London ED (octubre de 2008). "Abuso de anfetaminas y anomalías estructurales en el cerebro" . Anales de la Academia de Ciencias de Nueva York . 1141 (1): 195–220. doi : 10.1196 / annals.1441.031 . PMC 2769923 . PMID 18991959 .
- ↑ a b Hart H, Radua J, Nakao T, Mataix-Cols D, Rubia K (febrero de 2013). "Metanálisis de estudios de imágenes de resonancia magnética funcional de inhibición y atención en el trastorno por déficit de atención / hiperactividad: exploración de la medicación estimulante específica de la tarea y los efectos de la edad" . Psiquiatría JAMA . 70 (2): 185-198. doi : 10.1001 / jamapsychiatry.2013.277 . PMID 23247506 .
- ^ a b Spencer TJ, Brown A, Seidman LJ, Valera EM, Makris N, Lomedico A, Faraone SV, Biederman J (septiembre de 2013). "Efecto de los psicoestimulantes en la estructura y función del cerebro en el TDAH: una revisión de la literatura cualitativa de estudios de neuroimagen basados en imágenes de resonancia magnética" . La Revista de Psiquiatría Clínica . 74 (9): 902–917. doi : 10.4088 / JCP.12r08287 . PMC 3801446 . PMID 24107764 .
- ↑ a b Frodl T, Skokauskas N (febrero de 2012). "El metanálisis de estudios de resonancia magnética estructural en niños y adultos con trastorno por déficit de atención con hiperactividad indica efectos del tratamiento" . Acta Psychiatrica Scandinavica . 125 (2): 114-126. doi : 10.1111 / j.1600-0447.2011.01786.x . PMID 22118249 . S2CID 25954331 .
Las regiones de los ganglios basales como el globo pálido derecho, el putamen derecho y el núcleo caudato se ven afectadas estructuralmente en los niños con TDAH. Estos cambios y alteraciones en regiones límbicas como ACC y amígdala son más pronunciados en poblaciones no tratadas y parecen disminuir con el tiempo desde la niñez hasta la edad adulta. El tratamiento parece tener efectos positivos sobre la estructura del cerebro.
- ↑ a b c d Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: Guía del médico sobre el TDAH (2ª ed.). Nueva York, Estados Unidos: Springer. págs. 121-123, 125-127. ISBN 9781441913968.
La investigación en curso ha proporcionado respuestas a muchas de las preocupaciones de los padres y ha confirmado la eficacia y seguridad del uso prolongado de medicamentos.
- ↑ a b c d e Arnold LE, Hodgkins P, Caci H, Kahle J, Young S (febrero de 2015). "Efecto de la modalidad de tratamiento sobre los resultados a largo plazo en el trastorno por déficit de atención con hiperactividad: una revisión sistemática" . PLOS ONE . 10 (2): e0116407. doi : 10.1371 / journal.pone.0116407 . PMC 4340791 . PMID 25714373 .
La mayor proporción de mejores resultados se informó con el tratamiento combinado (83% de los resultados). Entre los resultados significativamente mejorados, se encontraron los tamaños de efecto más grandes para el tratamiento combinado. Las mayores mejoras se asociaron con resultados académicos, de autoestima o de función social.
Figura 3: Beneficio del tratamiento por tipo de tratamiento y grupo de resultados - ↑ a b c Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 6: sistemas de proyección amplia: monoaminas, acetilcolina y orexina". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. págs. 154-157. ISBN 9780071481274.
- ^ a b c d e Bidwell LC, McClernon FJ, Kollins SH (agosto de 2011). "Potenciadores cognitivos para el tratamiento del TDAH" . Farmacología Bioquímica y Comportamiento . 99 (2): 262-274. doi : 10.1016 / j.pbb.2011.05.002 . PMC 3353150 . PMID 21596055 .
- ^ Parker J, Wales G, Chalhoub N, Harpin V (septiembre de 2013). "Los resultados a largo plazo de las intervenciones para el tratamiento del trastorno por déficit de atención con hiperactividad en niños y adolescentes: una revisión sistemática de ensayos controlados aleatorios" . Investigación en psicología y manejo de la conducta . 6 : 87–99. doi : 10.2147 / PRBM.S49114 . PMC 3785407 . PMID 24082796 .
Solo un artículo
53
el examen de los resultados después de los 36 meses cumplió con los criterios de revisión. ... Existe evidencia de alto nivel que sugiere que el tratamiento farmacológico puede tener un efecto beneficioso importante sobre los síntomas centrales del TDAH (hiperactividad, falta de atención e impulsividad) en aproximadamente el 80% de los casos en comparación con los controles de placebo, a corto plazo.
- ^ Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: Guía del médico sobre el TDAH (2ª ed.). Nueva York, Estados Unidos: Springer. págs. 111-113. ISBN 9781441913968.
- ^ "Estimulantes para el trastorno por déficit de atención con hiperactividad" . WebMD . Healthwise. 12 de abril de 2010 . Consultado el 12 de noviembre de 2013 .
- ^ Scholten RJ, Clarke M, Hetherington J (agosto de 2005). "La Colaboración Cochrane" . Revista europea de nutrición clínica . 59 (Supl. 1): S147 – S149, discusión S195 – S196. doi : 10.1038 / sj.ejcn.1602188 . PMID 16052183 . S2CID 29410060 .
- ↑ a b Castells X, Blanco-Silvente L, Cunill R (agosto de 2018). "Anfetaminas para el trastorno por déficit de atención con hiperactividad (TDAH) en adultos" . Base de datos Cochrane de revisiones sistemáticas . 8 : CD007813. doi : 10.1002 / 14651858.CD007813.pub3 . PMC 6513464 . PMID 30091808 .
- ^ Punja S, Shamseer L, Hartling L, Urichuk L, Vandermeer B, Nikles J, Vohra S (febrero de 2016). "Anfetaminas para el trastorno por déficit de atención con hiperactividad (TDAH) en niños y adolescentes". Base de datos Cochrane de revisiones sistemáticas . 2 : CD009996. doi : 10.1002 / 14651858.CD009996.pub2 . PMID 26844979 .
- ^ Osland ST, Steeves TD, Pringsheim T (junio de 2018). "Tratamiento farmacológico para el trastorno por déficit de atención con hiperactividad (TDAH) en niños con trastornos de tic comórbidos" . Base de datos Cochrane de revisiones sistemáticas . 6 : CD007990. doi : 10.1002 / 14651858.CD007990.pub3 . PMC 6513283 . PMID 29944175 .
- ^ a b Spencer RC, Devilbiss DM, Berridge CW (junio de 2015). "Los efectos de mejora de la cognición de los psicoestimulantes implican una acción directa en la corteza prefrontal" . Psiquiatría biológica . 77 (11): 940–950. doi : 10.1016 / j.biopsych.2014.09.013 . PMC 4377121 . PMID 25499957 .
Las acciones procognitivas de los psicoestimulantes solo se asocian con dosis bajas. Sorprendentemente, a pesar de casi 80 años de uso clínico, la neurobiología de las acciones procognitivas de los psicoestimulantes solo se ha investigado sistemáticamente recientemente. Los resultados de esta investigación demuestran de manera inequívoca que los efectos de mejora de la cognición de los psicoestimulantes implican la elevación preferencial de catecolaminas en la PFC y la activación posterior de los receptores de noradrenalina α2 y dopamina D1. ... Esta modulación diferencial de los procesos dependientes de PFC a través de la dosis parece estar asociada con la participación diferencial de los receptores α2 noradrenérgicos frente a los receptores α1. En conjunto, esta evidencia indica que a dosis bajas y clínicamente relevantes,Los psicoestimulantes carecen de las acciones conductuales y neuroquímicas que definen esta clase de fármacos y, en cambio, actúan en gran medida como potenciadores cognitivos (mejorando la función dependiente de la PFC). ... En particular, tanto en animales como en humanos, las dosis más bajas mejoran al máximo el rendimiento en las pruebas de memoria de trabajo e inhibición de la respuesta, mientras que la supresión máxima del comportamiento manifiesto y la facilitación de los procesos de atención se produce con dosis más altas.
- ^ Ilieva IP, Hook CJ, Farah MJ (junio de 2015). "Efectos de los estimulantes recetados sobre el control inhibitorio saludable, la memoria de trabajo y la memoria episódica: un metanálisis" . Revista de neurociencia cognitiva . 27 (6): 1069–1089. doi : 10.1162 / jocn_a_00776 . PMID 25591060 . S2CID 15788121 .
Específicamente, en un conjunto de experimentos limitados a diseños de alta calidad, encontramos una mejora significativa de varias habilidades cognitivas. ... Los resultados de este metanálisis ... confirman la realidad de los efectos de mejora cognitiva para los adultos sanos normales en general, al tiempo que indican que estos efectos son de tamaño modesto.
- ^ Bagot KS, Kaminer Y (abril de 2014). "Eficacia de los estimulantes para la mejora cognitiva en jóvenes con trastorno por déficit de atención con hiperactividad: una revisión sistemática" . Adicción . 109 (4): 547–557. doi : 10.1111 / add.12460 . PMC 4471173 . PMID 24749160 .
Se ha demostrado que la anfetamina mejora la consolidación de la información (0,02 ≥ P ≤ 0,05), lo que mejora la memoria.
- ^ Devous MD, Trivedi MH, Rush AJ (abril de 2001). "Respuesta del flujo sanguíneo cerebral regional al desafío de anfetaminas orales en voluntarios sanos". Revista de Medicina Nuclear . 42 (4): 535–542. PMID 11337538 .
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 10: Control neuronal y neuroendocrino del medio interno". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. pag. 266. ISBN 9780071481274.
La dopamina actúa en el núcleo accumbens para otorgar un significado motivacional a los estímulos asociados con la recompensa.
- ↑ a b c Wood S, Sage JR, Shuman T, Anagnostaras SG (enero de 2014). "Psicoestimulantes y cognición: un continuo de activación cognitiva y conductual" . Revisiones farmacológicas . 66 (1): 193–221. doi : 10.1124 / pr.112.007054 . PMC 3880463 . PMID 24344115 .
- ^ Twohey M (26 de marzo de 2006). "Las pastillas se convierten en una adictiva ayuda al estudio" . JS en línea . Archivado desde el original el 15 de agosto de 2007 . Consultado el 2 de diciembre de 2007 .
- ^ Teter CJ, McCabe SE, LaGrange K, Cranford JA, Boyd CJ (octubre de 2006). "Uso ilícito de estimulantes de prescripción específicos entre estudiantes universitarios: prevalencia, motivos y vías de administración" . Farmacoterapia . 26 (10): 1501-1510. doi : 10.1592 / phco.26.10.1501 . PMC 1794223 . PMID 16999660 .
- ^ Weyandt LL, Oster DR, Marraccini ME, Gudmundsdottir BG, Munro BA, Zavras BM, Kuhar B (septiembre de 2014). "Intervenciones farmacológicas para adolescentes y adultos con TDAH: medicamentos estimulantes y no estimulantes y mal uso de estimulantes recetados" . Investigación en psicología y manejo de la conducta . 7 : 223–249. doi : 10.2147 / PRBM.S47013 . PMC 4164338 . PMID 25228824 .
El uso indebido de estimulantes recetados se ha convertido en un problema grave en los campus universitarios de los EE. UU. y también se ha documentado recientemente en otros países. ... De hecho, un gran número de estudiantes afirman haber participado en el uso no médico de estimulantes recetados, lo que se refleja en tasas de prevalencia de por vida del uso indebido de estimulantes recetados que van desde el 5% hasta casi el 34% de los estudiantes.
- ^ Clemow DB, Walker DJ (septiembre de 2014). "El potencial de uso indebido y abuso de medicamentos en el TDAH: una revisión". Postgrado en Medicina . 126 (5): 64–81. doi : 10.3810 / pgm.2014.09.2801 . PMID 25295651 . S2CID 207580823 .
En general, los datos sugieren que el uso indebido y la desviación de medicamentos para el TDAH son problemas de atención médica comunes para los medicamentos estimulantes, y se cree que la prevalencia es aproximadamente del 5% al 10% de los estudiantes de secundaria y del 5% al 35% de los estudiantes universitarios, según el estudio. .
- ^ Bracken NM (enero de 2012). "Estudio nacional de las tendencias de uso de sustancias entre los estudiantes-atletas universitarios de la NCAA" (PDF) . Publicaciones de la NCAA . Asociación Nacional de Atletismo Colegiado . Consultado el 8 de octubre de 2013 .
- ^ Docherty JR (junio de 2008). "Farmacología de estimulantes prohibidos por la Agencia Mundial Antidopaje (WADA)" . Revista británica de farmacología . 154 (3): 606–622. doi : 10.1038 / bjp.2008.124 . PMC 2439527 . PMID 18500382 .
- ↑ a b c d Parr JW (julio de 2011). "Trastorno por déficit de atención con hiperactividad y el deportista: nuevos avances y comprensión". Clínicas de Medicina del Deporte . 30 (3): 591–610. doi : 10.1016 / j.csm.2011.03.007 . PMID 21658550 .
En 1980, Chandler y Blair
47
mostraron aumentos significativos en la fuerza de extensión de la rodilla, aceleración, capacidad anaeróbica, tiempo hasta el agotamiento durante el ejercicio, frecuencia cardíaca previa al ejercicio y máxima, y tiempo hasta el agotamiento durante la prueba de consumo máximo de oxígeno (VO2 máx.) después de la administración de 15 mg de dextroanfetamina versus placebo. La mayor parte de la información para responder a esta pregunta se ha obtenido en la última década a través de estudios de fatiga en lugar de un intento de investigar sistemáticamente el efecto de los medicamentos para el TDAH en el ejercicio.
- ↑ a b c Roelands B, de Koning J, Foster C, Hettinga F, Meeusen R (mayo de 2013). "Determinantes neurofisiológicos de los conceptos teóricos y los mecanismos implicados en la estimulación". Medicina deportiva . 43 (5): 301–311. doi : 10.1007 / s40279-013-0030-4 . PMID 23456493 . S2CID 30392999 .
En temperaturas ambiente elevadas, las manipulaciones dopaminérgicas mejoran claramente el rendimiento. La distribución de la producción de energía revela que después de la inhibición de la recaptación de dopamina, los sujetos pueden mantener una producción de energía más alta en comparación con el placebo. ... Los fármacos dopaminérgicos parecen anular un interruptor de seguridad y permiten a los atletas utilizar una capacidad de reserva que está "fuera de los límites" en una situación normal (placebo).
- ^ Parker KL, Lamichhane D, Caetano MS, Narayanan NS (octubre de 2013). "Disfunción ejecutiva en la enfermedad de Parkinson y déficits de sincronización" . Fronteras en neurociencia integrativa . 7 : 75. doi : 10.3389 / fnint.2013.00075 . PMC 3813949 . PMID 24198770 .
Las manipulaciones de la señalización dopaminérgica influyen profundamente en la sincronización del intervalo, lo que lleva a la hipótesis de que la dopamina influye en la actividad del marcapasos interno o "reloj". Por ejemplo, la anfetamina, que aumenta las concentraciones de dopamina en la hendidura sináptica, avanza el inicio de la respuesta durante el intervalo de tiempo, mientras que los antagonistas de los receptores de dopamina de tipo D2 suelen ralentizar el tiempo; ... El agotamiento de la dopamina en voluntarios sanos afecta el tiempo, mientras que la anfetamina libera sináptica dopamina y acelera el tiempo.
- ^ Rattray B, Argus C, Martin K, Northey J, Driller M (marzo de 2015). "¿Ha llegado el momento de centrar nuestra atención en los mecanismos centrales de las estrategias y el rendimiento de recuperación después del esfuerzo?" . Fronteras en fisiología . 6 : 79. doi : 10.3389 / fphys.2015.00079 . PMC 4362407 . PMID 25852568 .
Además de tener en cuenta el rendimiento reducido de los participantes mentalmente fatigados, este modelo racionaliza el RPE reducido y, por lo tanto, mejora el rendimiento en la prueba contrarreloj de los atletas que utilizan un enjuague bucal de glucosa (Chambers et al., 2009) y la mayor producción de potencia durante un tiempo de ciclismo emparejado con RPE. ensayo posterior a la ingestión de anfetaminas (Swart, 2009). ... Se sabe que los fármacos estimulantes de la dopamina mejoran aspectos del rendimiento físico (Roelands et al., 2008)
- ^ Roelands B, De Pauw K, Meeusen R (junio de 2015). "Efectos neurofisiológicos del ejercicio en el calor". Revista escandinava de medicina y ciencia en el deporte . 25 (Supl. 1): 65–78. doi : 10.1111 / sms.12350 . PMID 25943657 . S2CID 22782401 .
Esto indica que los sujetos no sintieron que estaban produciendo más potencia y, en consecuencia, más calor. Los autores concluyeron que el "interruptor de seguridad" o los mecanismos existentes en el cuerpo para prevenir los efectos nocivos son anulados por la administración del fármaco (Roelands et al., 2008b). En conjunto, estos datos indican fuertes efectos ergogénicos de una mayor concentración de DA en el cerebro, sin ningún cambio en la percepción del esfuerzo.
- ^ Kessler S (enero de 1996). "Farmacoterapia en el trastorno por déficit de atención con hiperactividad". Revista médica del sur . 89 (1): 33–38. doi : 10.1097 / 00007611-199601000-00005 . PMID 8545689 . S2CID 12798818 .
Las declaraciones en los prospectos del paquete no pretenden limitar la práctica médica. Más bien tienen la intención de limitar las declaraciones de las empresas farmacéuticas. ... la FDA afirma explícitamente, y los tribunales han sostenido que las decisiones clínicas deben ser tomadas por médicos y pacientes en situaciones individuales.
- ^ a b c d e f g h i j k Heedes G, Ailakis J. "Anfetamina (PIM 934)" . INCHEM . Programa Internacional de Seguridad Química . Consultado el 24 de junio de 2014 .
- ^ Feinberg SS (noviembre de 2004). "Combinación de estimulantes con inhibidores de la monoaminooxidasa: una revisión de usos y una posible indicación adicional". La Revista de Psiquiatría Clínica . 65 (11): 1520-1524. doi : 10.4088 / jcp.v65n1113 . PMID 15554766 .
- ^ Stewart JW, Deliyannides DA, McGrath PJ (junio de 2014). "¿Qué tan tratable es la depresión refractaria?". Revista de trastornos afectivos . 167 : 148-152. doi : 10.1016 / j.jad.2014.05.047 . PMID 24972362 .
- ↑ a b c d Vitiello B (abril de 2008). "Comprender el riesgo de utilizar medicamentos para el trastorno por déficit de atención con hiperactividad con respecto al crecimiento físico y la función cardiovascular" . Clínicas psiquiátricas de niños y adolescentes de América del Norte . 17 (2): 459–474. doi : 10.1016 / j.chc.2007.11.010 . PMC 2408826 . PMID 18295156 .
- ^ Ramey JT, Bailen E, Lockey RF (2006). "Rinitis medicamentosa" (PDF) . Revista de alergología e inmunología clínica en investigación . 16 (3): 148-155. PMID 16784007 . Consultado el 29 de abril de 2015 .
Tabla 2. Descongestionantes que causan rinitis medicamentosa
- Descongestionantes nasales:
- Simpaticomiméticos:
• Anfetamina
- ^ a b "Comunicación de la FDA sobre la seguridad de los medicamentos: actualización de la revisión de seguridad de los medicamentos utilizados para tratar el trastorno por déficit de atención con hiperactividad (TDAH) en niños y adultos jóvenes" . Administración de Drogas y Alimentos de los Estados Unidos . 1 de noviembre de 2011. Archivado desde el original el 25 de agosto de 2019 . Consultado el 24 de diciembre de 2019 .
- ^ Cooper WO, Habel LA, Sox CM, Chan KA, Arbogast PG, Cheetham TC, Murray KT, Quinn VP, Stein CM, Callahan ST, Bombero BH, Fish FA, Kirshner HS, O'Duffy A, Connell FA, Ray WA (Noviembre de 2011). "Medicamentos para el TDAH y eventos cardiovasculares graves en niños y adultos jóvenes" . Revista de Medicina de Nueva Inglaterra . 365 (20): 1896-1904. doi : 10.1056 / NEJMoa1110212 . PMC 4943074 . PMID 22043968 .
- ^ a b "Comunicación de la FDA sobre la seguridad de los medicamentos: actualización de la revisión de seguridad de los medicamentos utilizados para tratar el trastorno por déficit de atención con hiperactividad (TDAH) en adultos" . Administración de Drogas y Alimentos de los Estados Unidos . 12 de diciembre de 2011. Archivado desde el original el 14 de diciembre de 2019 . Consultado el 24 de diciembre de 2013 .
- ^ Habel LA, Cooper WO, Sox CM, Chan KA, Bombero BH, Arbogast PG, Cheetham TC, Quinn VP, Dublin S, Boudreau DM, Andrade SE, Pawloski PA, Raebel MA, Smith DH, Achacoso N, Uratsu C, Go AS, Sidney S, Nguyen-Huynh MN, Ray WA, Selby JV (diciembre de 2011). "Medicamentos para el TDAH y riesgo de eventos cardiovasculares graves en adultos jóvenes y de mediana edad" . JAMA . 306 (24): 2673–2683. doi : 10.1001 / jama.2011.1830 . PMC 3350308 . PMID 22161946 .
- ^ O'Connor PG (febrero de 2012). "Anfetaminas" . Manual Merck para profesionales de la salud . Merck . Consultado el 8 de mayo de 2012 .
- ↑ a b Childs E, de Wit H (mayo de 2009). "Preferencia de lugar inducida por anfetaminas en humanos" . Psiquiatría biológica . 65 (10): 900–904. doi : 10.1016 / j.biopsych.2008.11.016 . PMC 2693956 . PMID 19111278 .
Este estudio demuestra que los humanos, al igual que los no humanos, prefieren un lugar asociado con la administración de anfetaminas. Estos hallazgos apoyan la idea de que las respuestas subjetivas a un fármaco contribuyen a su capacidad para establecer el condicionamiento del lugar.
- ↑ a b Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 15: Refuerzo y trastornos adictivos". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York: McGraw-Hill Medical. págs. 364–375. ISBN 9780071481274.
- ^ a b c d e Nestler EJ (diciembre de 2013). "Base celular de la memoria para la adicción" . Diálogos en neurociencia clínica . 15 (4): 431–443. PMC 3898681 . PMID 24459410 .
A pesar de la importancia de numerosos factores psicosociales, en su esencia, la adicción a las drogas implica un proceso biológico: la capacidad de la exposición repetida a una droga de abuso para inducir cambios en un cerebro vulnerable que impulsa la búsqueda y el consumo compulsivo de drogas, y la pérdida de control. sobre el consumo de drogas, que definen un estado de adicción. ... Una gran cantidad de literatura ha demostrado que tal inducción de ΔFosB en neuronas de tipo D1 [núcleo accumbens] aumenta la sensibilidad de un animal al fármaco, así como a las recompensas naturales y promueve la autoadministración del fármaco, presumiblemente a través de un proceso de refuerzo positivo. Otro objetivo de ΔFosB es cFos: a medida que ΔFosB se acumula con la exposición repetida al fármaco, reprime el c-Fos y contribuye al cambio molecular mediante el cual ΔFosB se induce selectivamente en el estado crónico de tratamiento con fármaco. 41. ... Además, existe una creciente evidencia de que, a pesar de una variedad de riesgos genéticos de adicción en la población, la exposición a dosis suficientemente altas de una droga durante largos períodos de tiempo puede transformar a alguien que tiene una carga genética relativamente menor en un adicto.
- ^ "Glosario de términos" . Escuela de Medicina Mount Sinai . Departamento de Neurociencias . Consultado el 9 de febrero de 2015 .
- ^ Volkow ND, Koob GF, McLellan AT (enero de 2016). "Avances neurobiológicos del modelo de adicción a la enfermedad cerebral" . Revista de Medicina de Nueva Inglaterra . 374 (4): 363–371. doi : 10.1056 / NEJMra1511480 . PMC 6135257 . PMID 26816013 .
Trastorno por uso de sustancias: término de diagnóstico en la quinta edición del Manual diagnóstico y estadístico de trastornos mentales (DSM-5) que se refiere al uso recurrente de alcohol u otras drogas que causa un deterioro clínicamente y funcionalmente significativo, como problemas de salud, discapacidad, y no cumplir con las principales responsabilidades en el trabajo, la escuela o el hogar. Según el nivel de gravedad, este trastorno se clasifica como leve, moderado o grave.
Adicción: término que se utiliza para indicar la etapa crónica más grave del trastorno por uso de sustancias, en la que hay una pérdida sustancial de autocontrol, como lo indica el consumo compulsivo de drogas a pesar del deseo de dejar de tomarlas. En el DSM-5, el término adicción es sinónimo de la clasificación de trastorno grave por uso de sustancias. - ^ a b c Renthal W, Nestler EJ (septiembre de 2009). "Regulación de la cromatina en la adicción a las drogas y la depresión" . Diálogos en neurociencia clínica . 11 (3): 257–268. PMC 2834246 . PMID 19877494 .
Los [psicoestimulantes] aumentan los niveles de AMPc en el cuerpo estriado, lo que activa la proteína quinasa A (PKA) y conduce a la fosforilación de sus objetivos. Esto incluye la proteína de unión al elemento de respuesta a AMPc (CREB), cuya fosforilación induce su asociación con la histona acetiltransferasa, proteína de unión a CREB (CBP) para acetilar histonas y facilitar la activación de genes. Se sabe que esto ocurre en muchos genes, incluidos fosB y
c-fos.
en respuesta a la exposición a psicoestimulantes. ΔFosB también se regula positivamente mediante tratamientos psicoestimulantes crónicos, y se sabe que activa ciertos genes (p. Ej., Cdk5) y reprime otros (p. Ej., C-fos ) donde recluta HDAC1 como correpresor. ... La exposición crónica a psicoestimulantes aumenta la [señalización] glutamatérgica de la corteza prefrontal a la NAc. La señalización glutamatérgica eleva los niveles de Ca2 + en los elementos postsinápticos NAc donde activa la señalización de CaMK (calcio / calmodulina proteína quinasas) que, además de fosforilar CREB, también fosforila HDAC5.
Figura 2: Eventos de señalización inducidos por psicoestimulantes - ^ Broussard JI (enero de 2012). "Co-transmisión de dopamina y glutamato" . La Revista de Fisiología General . 139 (1): 93–96. doi : 10.1085 / jgp.201110659 . PMC 3250102 . PMID 22200950 .
La entrada coincidente y convergente a menudo induce plasticidad en una neurona postsináptica. El NAc integra información procesada sobre el entorno de la amígdala basolateral, el hipocampo y la corteza prefrontal (PFC), así como proyecciones de las neuronas dopaminérgicas del mesencéfalo. Estudios anteriores han demostrado cómo la dopamina modula este proceso integrador. Por ejemplo, la estimulación de alta frecuencia potencia las entradas del hipocampo al NAc mientras simultáneamente deprime las sinapsis de PFC (Goto y Grace, 2005). También se demostró que lo contrario era cierto; la estimulación en PFC potencia las sinapsis PFC-NAc pero deprime las sinapsis del hipocampo-NAc. A la luz de la nueva evidencia funcional de la co-transmisión de dopamina / glutamato en el mesencéfalo (referencias arriba),Los nuevos experimentos de la función NAc tendrán que probar si las entradas glutamatérgicas del mesencéfalo sesgan o filtran las entradas límbicas o corticales para guiar el comportamiento dirigido a objetivos.
- ^ Laboratorios Kanehisa (10 de octubre de 2014). "Anfetamina - Homo sapiens (humano)" . Camino KEGG . Consultado el 31 de octubre de 2014 .
La mayoría de las drogas adictivas aumentan las concentraciones extracelulares de dopamina (DA) en el núcleo accumbens (NAc) y la corteza prefrontal medial (mPFC), áreas de proyección de neuronas DA mesocorticolímbicas y componentes clave del "circuito de recompensa cerebral". La anfetamina logra esta elevación en los niveles extracelulares de DA al promover la salida de las terminales sinápticas. ... La exposición crónica a la anfetamina induce un factor de transcripción único delta FosB, que juega un papel esencial en los cambios adaptativos a largo plazo en el cerebro.
- ^ a b c Robison AJ, Nestler EJ (noviembre de 2011). "Mecanismos transcripcionales y epigenéticos de la adicción" . Nature Reviews Neurociencia . 12 (11): 623–637. doi : 10.1038 / nrn3111 . PMC 3272277 . PMID 21989194 .
ΔFosB sirve como una de las proteínas de control maestras que gobiernan esta plasticidad estructural. ... ΔFosB también reprime la expresión de G9a, lo que conduce a una metilación de histonas represiva reducida en el gen cdk5. El resultado neto es la activación de genes y una mayor expresión de CDK5. ... Por el contrario, ΔFosB se une a la
c-fos
gen y recluta varios correpresores, incluyendo HDAC1 (histona desacetilasa 1) y SIRT 1 (sirtuina 1). ... El resultado neto es la represión del gen c-fos .
Figura 4: Base epigenética de la regulación farmacológica de la expresión génica - ^ a b c Nestler EJ (diciembre de 2012). "Mecanismos transcripcionales de la adicción a las drogas" . Psicofarmacología Clínica y Neurociencia . 10 (3): 136–143. doi : 10.9758 / cpn.2012.10.3.136 . PMC 3569166 . PMID 23430970 .
Las isoformas de ΔFosB de 35-37 kD se acumulan con la exposición crónica al fármaco debido a sus vidas medias extraordinariamente largas. ... Como resultado de su estabilidad, la proteína ΔFosB persiste en las neuronas durante al menos varias semanas después del cese de la exposición al fármaco. ... La sobreexpresión de ΔFosB en el núcleo accumbens induce NFκB ... En contraste, la capacidad de ΔFosB para reprimir la
El gen c-Fos ocurre en concierto con el reclutamiento de una histona desacetilasa y presumiblemente varias otras proteínas represivas como una histona metiltransferasa represiva
- ^ Nestler EJ (octubre de 2008). "Mecanismos transcripcionales de la adicción: papel de ΔFosB" . Transacciones filosóficas de la Royal Society B: Ciencias biológicas . 363 (1507): 3245–3255. doi : 10.1098 / rstb.2008.0067 . PMC 2607320 . PMID 18640924 .
Evidencia reciente ha demostrado que ΔFosB también reprime el
gen
c-fos
que ayuda a crear el cambio molecular, desde la inducción de varias proteínas de la familia Fos de vida corta después de una exposición aguda al fármaco hasta la acumulación predominante de ΔFosB después de la exposición crónica al fármaco.
- ^ Laboratorios Kanehisa (10 de octubre de 2014). "Anfetamina - Homo sapiens (humano)" . Camino KEGG . Consultado el 31 de octubre de 2014 .
- ↑ a b c d e f Nechifor M (marzo de 2008). "Magnesio en las drogodependencias" . Investigación de magnesio . 21 (1): 5–15. doi : 10.1684 / mrh.2008.0124 (inactivo el 15 de enero de 2021). PMID 18557129 . CS1 maint: DOI inactive as of January 2021 (link)
- ↑ a b c d e Ruffle JK (noviembre de 2014). "Neurobiología molecular de la adicción: ¿de qué se trata todo el (Δ) FosB?". La Revista Estadounidense de Abuso de Drogas y Alcohol . 40 (6): 428–437. doi : 10.3109 / 00952990.2014.933840 . PMID 25083822 . S2CID 19157711 .
ΔFosB es un factor de transcripción esencial implicado en las vías moleculares y conductuales de la adicción después de la exposición repetida a las drogas.
- ^ a b c d e f g h i j k Robison AJ, Nestler EJ (noviembre de 2011). "Mecanismos transcripcionales y epigenéticos de la adicción" . Nature Reviews Neurociencia . 12 (11): 623–637. doi : 10.1038 / nrn3111 . PMC 3272277 . PMID 21989194 .
ΔFosB se ha relacionado directamente con varios comportamientos relacionados con la adicción ... Es importante destacar que la sobreexpresión genética o viral de ΔJunD, un mutante negativo dominante de JunD que antagoniza la actividad transcripcional mediada por ΔFosB y otras AP-1, en NAc u OFC bloquea estos efectos clave de la exposición a las drogas 14,22-24 . Esto indica que ΔFosB es necesario y suficiente para muchos de los cambios producidos en el cerebro por la exposición crónica a fármacos. ΔFosB también se induce en los NEM de NAc de tipo D1 por el consumo crónico de varias recompensas naturales, como sacarosa, alimentos ricos en grasas, sexo, correr ruedas, donde promueve ese consumo 14,26–30. Esto implica a ΔFosB en la regulación de las recompensas naturales en condiciones normales y quizás durante estados patológicos de tipo adictivo. ... ΔFosB sirve como una de las proteínas de control maestras que gobiernan esta plasticidad estructural.
- ^ a b c d e f g h i j k l m n o p q r s t u v Olsen CM (diciembre de 2011). "Recompensas naturales, neuroplasticidad y adicciones a las drogas" . Neurofarmacología . 61 (7): 1109–1122. doi : 10.1016 / j.neuropharm.2011.03.010 . PMC 3139704 . PMID 21459101 .
De manera similar al enriquecimiento ambiental, los estudios han encontrado que el ejercicio reduce la autoadministración y la recaída en las drogas de abuso (Cosgrove et al., 2002; Zlebnik et al., 2010). También hay alguna evidencia de que estos hallazgos preclínicos se traducen en poblaciones humanas, ya que el ejercicio reduce los síntomas de abstinencia y la recaída en fumadores abstinentes (Daniel et al., 2006; Prochaska et al., 2008), y un programa de recuperación de fármacos ha tenido éxito en los participantes. que entrenan y compiten en un maratón como parte del programa (Butler, 2005). ... En los seres humanos, el papel de la señalización de la dopamina en los procesos de sensibilización al incentivo se ha destacado recientemente por la observación de un síndrome de desregulación de la dopamina en algunos pacientes que toman fármacos dopaminérgicos.Este síndrome se caracteriza por un aumento (o compulsivo) inducido por medicamentos en la participación en recompensas no relacionadas con las drogas, como el juego, las compras o el sexo (Evans et al., 2006; Aiken, 2007; Lader, 2008).
- ↑ a b c d Lynch WJ, Peterson AB, Sanchez V, Abel J, Smith MA (septiembre de 2013). "El ejercicio como un tratamiento novedoso para la adicción a las drogas: una hipótesis neurobiológica y dependiente del estadio" . Revisiones de neurociencia y bioconducta . 37 (8): 1622–1644. doi : 10.1016 / j.neubiorev.2013.06.011 . PMC 3788047 . PMID 23806439 .
Estos hallazgos sugieren que el ejercicio puede prevenir de manera independiente el desarrollo de un fenotipo adicto, posiblemente al bloquear / revertir los cambios conductuales y neuroadaptativos que se desarrollan durante y después del acceso prolongado a la droga. ... Se ha propuesto el ejercicio como un tratamiento para la adicción a las drogas que puede reducir el ansia por las drogas y el riesgo de recaída. Aunque pocos estudios clínicos han investigado la eficacia del ejercicio para prevenir la recaída, los pocos estudios que se han realizado generalmente informan una reducción en el deseo de consumir drogas y mejores resultados del tratamiento ... En conjunto, estos datos sugieren que los beneficios potenciales del ejercicio durante la recaída, particularmente para la recaída a los psicoestimulantes, puede estar mediada por la remodelación de la cromatina y posiblemente conducir a mejores resultados del tratamiento.
- ^ a b c Zhou Y, Zhao M, Zhou C, Li R (julio de 2015). "Diferencias de sexo en la adicción a las drogas y la respuesta a la intervención del ejercicio: de estudios humanos a animales" . Fronteras en neuroendocrinología . 40 : 24–41. doi : 10.1016 / j.yfrne.2015.07.001 . PMC 4712120 . PMID 26182835 .
En conjunto, estos hallazgos demuestran que el ejercicio puede servir como un sustituto o una competencia para el abuso de drogas al cambiar la inmunorreactividad de ΔFosB o cFos en el sistema de recompensa para proteger contra el uso de drogas anterior o posterior. ... El postulado de que el ejercicio sirve como una intervención ideal para la adicción a las drogas ha sido ampliamente reconocido y utilizado en la rehabilitación humana y animal.
- ^ a b c Linke SE, Ussher M (enero de 2015). "Tratamientos basados en el ejercicio para los trastornos por uso de sustancias: evidencia, teoría y practicidad" . La Revista Estadounidense de Abuso de Drogas y Alcohol . 41 (1): 7–15. doi : 10.3109 / 00952990.2014.976708 . PMC 4831948 . PMID 25397661 .
La limitada investigación realizada sugiere que el ejercicio puede ser un tratamiento complementario eficaz para los TUS. En contraste con los escasos ensayos de intervención hasta la fecha, se ha publicado una relativa abundancia de literatura sobre las razones teóricas y prácticas que sustentan la investigación de este tema. ... numerosas razones teóricas y prácticas apoyan los tratamientos basados en el ejercicio para los TUS, incluidos los efectos psicológicos, conductuales, neurobiológicos, de seguridad casi universal y efectos positivos generales para la salud.
- ^ Hyman SE, Malenka RC, Nestler EJ (julio de 2006). "Mecanismos neuronales de la adicción: el papel del aprendizaje y la memoria relacionados con la recompensa" (PDF) . Revisión anual de neurociencia . 29 : 565–598. doi : 10.1146 / annurev.neuro.29.051605.113009 . PMID 16776597 . S2CID 15139406 .
- ↑ a b c d e Steiner H, Van Waes V (enero de 2013). "Regulación de genes relacionados con la adicción: riesgos de exposición a potenciadores cognitivos frente a otros psicoestimulantes" . Progresos en neurobiología . 100 : 60–80. doi : 10.1016 / j.pneurobio.2012.10.001 . PMC 3525776 . PMID 23085425 .
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 4: Transducción de señales en el cerebro". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. pag. 94. ISBN 9780071481274.
- ^ Laboratorios Kanehisa (29 de octubre de 2014). "Alcoholismo - Homo sapiens (humano)" . Camino KEGG . Consultado el 31 de octubre de 2014 .
- ^ Kim Y, Teylan MA, Baron M, Sands A, Nairn AC, Greengard P (febrero de 2009). "Formación de columna dendrítica inducida por metilfenidato y expresión de DeltaFosB en núcleo accumbens" . Actas de la Academia Nacional de Ciencias . 106 (8): 2915–2920. Código bibliográfico : 2009PNAS..106.2915K . doi : 10.1073 / pnas.0813179106 . PMC 2650365 . PMID 19202072 .
- ^ a b Nestler EJ (enero de 2014). "Mecanismos epigenéticos de la drogadicción" . Neurofarmacología . 76 Pt B: 259-268. doi : 10.1016 / j.neuropharm.2013.04.004 . PMC 3766384 . PMID 23643695 .
- ↑ a b Biliński P, Wojtyła A, Kapka-Skrzypczak L, Chwedorowicz R, Cyranka M, Studziński T (2012). "Regulación epigenética en la drogadicción" . Anales de Medicina Agrícola y Ambiental . 19 (3): 491–496. PMID 23020045 .
- ^ Kennedy PJ, Feng J, Robison AJ, Maze I, Badimon A, Mouzon E, Chaudhury D, Damez-Werno DM, Haggarty SJ, Han MH, Bassel-Duby R, Olson EN, Nestler EJ (abril de 2013). "La inhibición de HDAC de clase I bloquea la plasticidad inducida por la cocaína mediante cambios específicos en la metilación de histonas" . Neurociencia de la naturaleza . 16 (4): 434–440. doi : 10.1038 / nn.3354 . PMC 3609040 . PMID 23475113 .
- ^ Whalley K (diciembre de 2014). "Trastornos psiquiátricos: una hazaña de ingeniería epigenética". Reseñas de la naturaleza. Neurociencia . 15 (12): 768–769. doi : 10.1038 / nrn3869 . PMID 25409693 . S2CID 11513288 .
- ↑ a b Blum K, Werner T, Carnes S, Carnes P, Bowirrat A, Giordano J, Oscar-Berman M, Gold M (marzo de 2012). "Sexo, drogas y rock 'n' roll: hipotetizar la activación mesolímbica común en función de los polimorfismos del gen de recompensa" . Revista de Drogas Psicoactivas . 44 (1): 38–55. doi : 10.1080 / 02791072.2012.662112 . PMC 4040958 . PMID 22641964 .
Se ha descubierto que el gen deltaFosB en el NAc es fundamental para reforzar los efectos de la recompensa sexual. Pitchers y sus colegas (2010) informaron que se demostró que la experiencia sexual causa la acumulación de DeltaFosB en varias regiones límbicas del cerebro, incluidas NAc, corteza prefrontal medial, VTA, caudado y putamen, pero no el núcleo preóptico medial. ... estos hallazgos apoyan un papel crítico para la expresión de DeltaFosB en el NAc en los efectos reforzantes del comportamiento sexual y la facilitación del desempeño sexual inducida por la experiencia sexual. ... tanto la adicción a las drogas como la adicción sexual representan formas patológicas de neuroplasticidad junto con la aparición de comportamientos aberrantes que involucran una cascada de cambios neuroquímicos principalmente en los circuitos gratificantes del cerebro.
- ^ Jarras KK, Vialou V, Nestler EJ, Laviolette SR, Lehman MN, Coolen LM (febrero de 2013). "Las recompensas naturales y de drogas actúan sobre mecanismos de plasticidad neuronal comunes con ΔFosB como mediador clave" . La Revista de Neurociencia . 33 (8): 3434–3442. doi : 10.1523 / JNEUROSCI.4881-12.2013 . PMC 3865508 . PMID 23426671 .
- ^ Beloate LN, Weems PW, Casey GR, Webb IC, Coolen LM (febrero de 2016). "La activación del receptor de NMDA de Nucleus accumbens regula la sensibilización cruzada de anfetamina y la expresión deltaFosB después de la experiencia sexual en ratas macho". Neurofarmacología . 101 : 154-164. doi : 10.1016 / j.neuropharm.2015.09.023 . PMID 26391065 . S2CID 25317397 .
- ^ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Capítulo 16: Refuerzo y trastornos adictivos". Neurofarmacología molecular: una base para la neurociencia clínica (3ª ed.). Nueva York: McGraw-Hill Medical. ISBN 9780071827706.
El tratamiento farmacológico para la adicción a los psicoestimulantes es generalmente insatisfactorio. Como se discutió anteriormente, el cese del consumo de cocaína y el uso de otros psicoestimulantes en personas dependientes no produce un síndrome de abstinencia físico, pero puede producir disforia, anhedonia y un deseo intenso de reiniciar el consumo de drogas.
- ^ a b c d Chan B, Freeman M, Kondo K, Ayers C, Montgomery J, Paynter R, Kansagara D (diciembre de 2019). "Farmacoterapia para el trastorno por uso de metanfetamina / anfetamina: una revisión sistemática y un metanálisis". Adicción (Abingdon, Inglaterra) . 114 (12): 2122–2136. doi : 10.1111 / add.14755 . PMID 31328345 .
- ^ Se inclina WW, Rush CR (mayo de 2014). "Farmacoterapias combinadas para el trastorno por uso de estimulantes: una revisión de los hallazgos clínicos y recomendaciones para futuras investigaciones" . Revisión de expertos de farmacología clínica . 7 (3): 363–374. doi : 10.1586 / 17512433.2014.909283 . PMC 4017926 . PMID 24716825 .
A pesar de los esfuerzos concertados para identificar una farmacoterapia para controlar los trastornos por uso de estimulantes, no se han aprobado medicamentos ampliamente eficaces.
- ↑ a b Jing L, Li JX (agosto de 2015). "Traza el receptor asociado a aminas 1: un objetivo prometedor para el tratamiento de la adicción a los psicoestimulantes" . Revista europea de farmacología . 761 : 345–352. doi : 10.1016 / j.ejphar.2015.06.019 . PMC 4532615 . PMID 26092759 .
Los datos existentes proporcionaron pruebas preclínicas sólidas que respaldan el desarrollo de agonistas de TAAR1 como tratamiento potencial para el abuso y la adicción a psicoestimulantes.
- ↑ a b Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 5: Aminoácidos excitadores e inhibidores". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. págs. 124-125. ISBN 9780071481274.
- ^ a b c Carroll ME, Smethells JR (febrero de 2016). "Diferencias de sexo en el control del comportamiento: papel en la drogadicción y nuevos tratamientos" . Fronteras en psiquiatría . 6 : 175. doi : 10.3389 / fpsyt.2015.00175 . PMC 4745113 . PMID 26903885 .
Ejercicio físico
Hay evidencia cada vez más clara de que el ejercicio físico es un tratamiento útil para prevenir y reducir la adicción a las drogas ... En algunas personas, el ejercicio tiene sus propios efectos gratificantes y puede producirse una interacción económica conductual, de modo que las recompensas físicas y sociales del ejercicio pueden sustituir a los efectos gratificantes del abuso de drogas. ... El valor de esta forma de tratamiento para la adicción a las drogas en animales de laboratorio y humanos es que el ejercicio, si puede sustituir los efectos gratificantes de las drogas, podría mantenerse por sí mismo durante un período prolongado de tiempo. El trabajo realizado hasta la fecha en [animales de laboratorio y humanos] con respecto al ejercicio como tratamiento para la adicción a las drogas apoya esta hipótesis. ... La investigación en humanos y animales sobre el ejercicio físico como tratamiento para la adicción a estimulantes indica que este es uno de los tratamientos más prometedores en el horizonte. - ^ Perez-Mana C, Castells X, Torrens M, Capella D, Farre M (septiembre de 2013). "Eficacia de los psicoestimulantes para el abuso o dependencia de anfetaminas". Base de datos Cochrane de revisiones sistemáticas . 9 (9): CD009695. doi : 10.1002 / 14651858.CD009695.pub2 . PMID 23996457 .
- ^ "Anfetaminas: uso y abuso de drogas" . Merck Manual Home Edition . Merck. Febrero de 2003. Archivado desde el original el 17 de febrero de 2007 . Consultado el 28 de febrero de 2007 .
- ^ a b c d Shoptaw SJ, Kao U, Heinzerling K, Ling W (abril de 2009). Shoptaw SJ (ed.). "Tratamiento para la abstinencia de anfetaminas" . Base de datos Cochrane de revisiones sistemáticas (2): CD003021. doi : 10.1002 / 14651858.CD003021.pub2 . PMC 7138250 . PMID 19370579 .
La prevalencia de este síndrome de abstinencia es extremadamente común (Cantwell 1998; Gossop 1982) con 87,6% de 647 individuos con dependencia de anfetaminas que informan seis o más signos de abstinencia de anfetaminas enumerados en el DSM cuando el fármaco no está disponible (Schuckit 1999) ... La gravedad de los síntomas de abstinencia es mayor en los individuos dependientes de anfetaminas que son mayores y que tienen trastornos más extensos por el uso de anfetaminas (McGregor 2005). Los síntomas de abstinencia generalmente se presentan dentro de las 24 horas posteriores al último uso de anfetamina, con un síndrome de abstinencia que involucra dos fases generales que pueden durar 3 semanas o más. La primera fase de este síndrome es el "colapso" inicial que se resuelve en aproximadamente una semana (Gossop 1982; McGregor 2005) ...
- ↑ a b Spiller HA, Hays HL, Aleguas A (junio de 2013). "Sobredosis de fármacos para el trastorno por déficit de atención con hiperactividad: presentación clínica, mecanismos de toxicidad y manejo". Medicamentos para el SNC . 27 (7): 531–543. doi : 10.1007 / s40263-013-0084-8 . PMID 23757186 . S2CID 40931380 .
La anfetamina, la dextroanfetamina y el metilfenidato actúan como sustratos para el transportador de monoaminas celulares, especialmente el transportador de dopamina (DAT) y menos el transportador de norepinefrina (NET) y serotonina. El mecanismo de toxicidad se relaciona principalmente con el exceso de dopamina, norepinefrina y serotonina extracelulares.
- ^ Colaboradores (2015). "Mortalidad global, regional y nacional por todas las causas y por causas específicas por edad y sexo por 240 causas de muerte, 1990-2013: un análisis sistemático para el Estudio de la carga mundial de enfermedades de 2013" (PDF) . The Lancet . 385 (9963): 117-171. doi : 10.1016 / S0140-6736 (14) 61682-2 . hdl : 11655/15525 . PMC 4340604 . PMID 25530442 . Consultado el 3 de marzo de 2015 .
Trastornos por consumo de anfetaminas ... 3,788 (3,425–4,145)
- ^ Albertson TE (2011). "Anfetaminas". En Olson KR, Anderson IB, Benowitz NL, Blanc PD, Kearney TE, Kim-Katz SY, Wu AH (eds.). Envenenamiento y sobredosis de drogas (6ª ed.). Nueva York: McGraw-Hill Medical. págs. 77–79. ISBN 9780071668330.
- ^ Advokat C (julio de 2007). "Actualización sobre la neurotoxicidad de las anfetaminas y su relevancia para el tratamiento del TDAH". Revista de trastornos de la atención . 11 (1): 8–16. doi : 10.1177 / 1087054706295605 . PMID 17606768 . S2CID 7582744 .
- ↑ a b c d Bowyer JF, Hanig JP (noviembre de 2014). "Hipertermia inducida por anfetaminas y metanfetaminas: implicaciones de los efectos producidos en la vasculatura cerebral y los órganos periféricos para la neurotoxicidad del prosencéfalo" . Temperatura . 1 (3): 172–182. doi : 10.4161 / 23328940.2014.982049 . PMC 5008711 . PMID 27626044 .
La hipertermia sola no produce neurotoxicidad similar a la de las anfetaminas, pero las exposiciones a AMPH y METH que no producen hipertermia (≥40 ° C) son mínimamente neurotóxicas. Es probable que la hipertermia mejore la neurotoxicidad de AMPH y METH directamente a través de la alteración de la función de las proteínas, los canales iónicos y una mayor producción de ROS. ... La hipertermia y la hipertensión producidas por altas dosis de anfetaminas son una causa principal de rupturas transitorias en la barrera hematoencefálica (BHE) que resultan en neurodegeneración regional y neuroinflamación concomitantes en animales de laboratorio. ... En modelos animales que evalúan la neurotoxicidad de AMPH y METH, está bastante claro que la hipertermia es uno de los componentes esenciales necesarios para la producción de signos histológicos de daño terminal de dopamina y neurodegeneración en corteza, estriado, tálamo e hipocampo.
- ^ "Anfetamina" . Biblioteca Nacional de Medicina de los Estados Unidos - Red de datos de toxicología . Banco de datos de sustancias peligrosas. Archivado desde el original el 2 de octubre de 2017 . Consultado el 2 de octubre de 2017 .
El daño tóxico directo a los vasos parece improbable debido a la dilución que ocurre antes de que el fármaco llegue a la circulación cerebral.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 15: Refuerzo y trastornos adictivos". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2ª ed.). Nueva York, Estados Unidos: McGraw-Hill Medical. pag. 370. ISBN 9780071481274.
A diferencia de la cocaína y la anfetamina, la metanfetamina es directamente tóxica para las neuronas dopaminérgicas del mesencéfalo.
- ^ Sulzer D, Zecca L (febrero de 2000). "Síntesis intraneuronal de dopamina-quinona: una revisión". Investigación de neurotoxicidad . 1 (3): 181-195. doi : 10.1007 / BF03033289 . PMID 12835101 . S2CID 21892355 .
- ^ Miyazaki I, Asanuma M (junio de 2008). "Estrés oxidativo específico de neuronas dopaminérgicas causado por la propia dopamina" (PDF) . Acta Medica Okayama . 62 (3): 141–150. doi : 10.18926 / AMO / 30942 . PMID 18596830 .
- ^ Hofmann FG (1983). Un manual sobre el abuso de drogas y alcohol: los aspectos biomédicos (2ª ed.). Nueva York, Estados Unidos: Oxford University Press. pag. 329 . ISBN 9780195030570.
- ^ Hasenhuetl PS, Bhat S, Freissmuth M, Sandtner W (marzo de 2019). "Selectividad funcional y eficacia parcial en los transportadores de monoamina: un modelo unificado de modulación alostérica y liberación de sustrato inducida por anfetaminas" . Farmacología molecular . 95 (3): 303–312. doi : 10.1124 / mol.118.114793 . PMID 30567955 . S2CID 58557130 .
Aunque el ciclo de transporte de monoaminas se ha resuelto con considerable detalle, el conocimiento cinético sobre las acciones moleculares de los moduladores alostéricos sintéticos es aún escaso. Afortunadamente, el ciclo catalítico DAT está modulado alostéricamente por un ligando endógeno (a saber, Zn
2+
; Norregaard y col., 1998). Vale la pena consultar Zn 2+ como un ejemplo instructivo, porque su acción sobre el ciclo catalítico DAT se ha descifrado en gran medida ... La unión de Zn + estabiliza la conformación orientada hacia afuera de DAT ... Esto potencia tanto el transporte hacia adelante modo (es decir, absorción de DA; Li et al., 2015) y el modo de intercambio de sustrato (es decir, liberación de DA inducida por anfetaminas; Meinild et al., 2004; Li et al., 2015). Es importante destacar que el efecto potenciador sobre la absorción de sustrato solo es evidente cuando las concentraciones internas de Na + son bajas ... Si las concentraciones internas de Na + aumentan durante el experimento, el modo de intercambio de sustrato domina y el efecto neto de Zn 2+ sobre la absorción es inhibidor. Por el contrario, Zn 2+acelera la liberación de sustrato inducida por anfetaminas a través de DAT. ... es importante enfatizar que se ha demostrado que Zn 2+ reduce la captación de dopamina en condiciones que favorecen la acumulación intracelular de Na +
Fig. 3. Selectividad funcional por selección conformacional. - ^ Krause J (abril de 2008). "SPECT y PET del transportador de dopamina en el trastorno por déficit de atención / hiperactividad". Revisión de expertos de neuroterapéuticos . 8 (4): 611–625. doi : 10.1586 / 14737175.8.4.611 . PMID 18416663 . S2CID 24589993 .
El zinc se une en ... sitios extracelulares de la DAT [103] y actúa como inhibidor de la DAT. En este contexto, son de interés los estudios controlados doble ciego en niños, que mostraron efectos positivos de la [suplementación] de zinc sobre los síntomas del TDAH [105,106]. Cabe señalar que en este momento [la suplementación] con zinc no está integrada en ningún algoritmo de tratamiento del TDAH.
- ↑ a b Scholze P, Nørregaard L, Singer EA, Freissmuth M, Gether U, Sitte HH (junio de 2002). "El papel de los iones de zinc en el transporte inverso mediado por transportadores de monoaminas" . Revista de Química Biológica . 277 (24): 21505–21513. doi : 10.1074 / jbc.M112265200 . PMID 11940571 . S2CID 10521850 .
El transportador de dopamina humana (hDAT) contiene un
sitio de unión de
Zn
2+
endógeno de alta afinidad
con tres residuos de coordinación en su cara extracelular (His193, His375 y Glu396). ... Aunque Zn
2+
inhibió la captación, Zn
2+
facilitó la liberación de [3H] MPP + inducida por anfetamina, MPP + o despolarización inducida por K + específicamente en hDAT pero no en el transportador de serotonina humana y norepinefrina (hNET). ... Sorprendentemente, este flujo de salida provocado por anfetaminas se mejoró notablemente, en lugar de inhibirse, mediante la adición de Zn 2+ 10 μM al tampón de superfusión (Fig. 2 A, cuadrados abiertos). ... Las concentraciones de Zn 2+ que se muestran en este estudio, necesarias para la estimulación de la liberación de dopamina (así como la inhibición de la captación), cubrieron este rango fisiológicamente relevante, con una estimulación máxima que se produce entre 3 y 30 μM. ... Por lo tanto, cuando el Zn 2+ se libera conjuntamente con el glutamato, puede aumentar en gran medida la salida de dopamina.
- ^ Kahlig KM, Lute BJ, Wei Y, Loland CJ, Gether U, Javitch JA, Galli A (agosto de 2006). "Regulación del tráfico de transportadores de dopamina por anfetamina intracelular". Farmacología molecular . 70 (2): 542–548. doi : 10.1124 / mol.106.023952 . PMID 16684900 . S2CID 10317113 .
La coadministración de Zn (2+) y AMPH redujo constantemente el tráfico de WT-hDAT
- ^ Scassellati C, Bonvicini C, Faraone SV, Gennarelli M (octubre de 2012). "Biomarcadores y trastorno por déficit de atención con hiperactividad: una revisión sistemática y metanálisis". Revista de la Academia Estadounidense de Psiquiatría Infantil y Adolescente . 51 (10): 1003–1019.e20. doi : 10.1016 / j.jaac.2012.08.015 . PMID 23021477 .
Con respecto a la suplementación con zinc, un ensayo controlado con placebo informó que dosis de hasta 30 mg / día de zinc eran seguras durante al menos 8 semanas, pero el efecto clínico fue ambiguo excepto por el hallazgo de una reducción del 37% en la dosis óptima de anfetamina con 30 mg por día de zinc.
110
- ^ a b c d e f g h i j k l m n Eiden LE, Weihe E (enero de 2011). "VMAT2: un regulador dinámico de la función neuronal monoaminérgica del cerebro que interactúa con las drogas de abuso" . Anales de la Academia de Ciencias de Nueva York . 1216 (1): 86–98. doi : 10.1111 / j.1749-6632.2010.05906.x . PMC 4183197 . PMID 21272013 .
VMAT2 es el transportador vesicular del SNC no solo para las aminas biogénicas DA, NE, EPI, 5-HT y HIS, sino probablemente también para las trazas de aminas TYR, PEA y tironamina (THYR) ... [Trazas aminérgicas] neuronas en El SNC de mamíferos sería identificable como neuronas que expresan VMAT2 para almacenamiento y la enzima biosintética aminoácido aromático descarboxilasa (AADC). ... La liberación de AMPH de DA de las sinapsis requiere tanto una acción en VMAT2 para liberar DA al citoplasma como una liberación concertada de DA del citoplasma a través del "transporte inverso" a través de DAT.
- ^ a b c d Sulzer D, Cragg SJ, Rice ME (agosto de 2016). "Neurotransmisión de dopamina estriatal: regulación de liberación y captación" . Ganglios basales . 6 (3): 123-148. doi : 10.1016 / j.baga.2016.02.001 . PMC 4850498 . PMID 27141430 .
A pesar de los desafíos para determinar el pH de la vesícula sináptica, el gradiente de protones a través de la membrana de la vesícula es de fundamental importancia para su función. La exposición de vesículas de catecolaminas aisladas a protonóforos colapsa el gradiente de pH y redistribuye rápidamente el transmisor desde el interior hacia el exterior de la vesícula. ... La anfetamina y sus derivados, como la metanfetamina, son compuestos de base débil que son la única clase de fármacos ampliamente utilizados que se sabe que provocan la liberación del transmisor mediante un mecanismo no exocítico. Como sustratos tanto para DAT como para VMAT, las anfetaminas se pueden llevar al citosol y luego secuestrar en vesículas, donde actúan para colapsar el gradiente de pH vesicular.
- ↑ a b Ledonne A, Berretta N, Davoli A, Rizzo GR, Bernardi G, Mercuri NB (julio de 2011). "Efectos electrofisiológicos de trazas de aminas en neuronas dopaminérgicas mesencefálicas" . Fronteras en neurociencia de sistemas . 5 : 56. doi : 10.3389 / fnsys.2011.00056 . PMC 3131148 . PMID 21772817 .
Recientemente han surgido tres aspectos nuevos e importantes de la acción de los TA: (a) inhibición del disparo debido a una mayor liberación de dopamina; (b) reducción de las respuestas inhibidoras mediadas por el receptor D2 y GABAB (efectos excitadores debidos a la desinhibición); y (c) una activación directa mediada por el receptor TA1 de los canales GIRK que producen hiperpolarización de la membrana celular.
- ^ a b "TAAR1" . GenAtlas . Universidad de Paris. 28 de enero de 2012 . Consultado el 29 de mayo de 2014 .
• activa tónicamente los canales de K (+) rectificadores hacia adentro, lo que reduce la frecuencia de disparo basal de las neuronas de dopamina (DA) del área tegmental ventral (VTA)
- ^ a b c d e f Underhill SM, Wheeler DS, Li M, Watts SD, Ingram SL, Amara SG (julio de 2014). "La anfetamina modula la neurotransmisión excitadora a través de la endocitosis del transportador de glutamato EAAT3 en neuronas de dopamina" . Neurona . 83 (2): 404–416. doi : 10.1016 / j.neuron.2014.05.043 . PMC 4159050 . PMID 25033183 .
El AMPH también aumenta el calcio intracelular (Gnegy et al., 2004) que está asociado con la activación de calmodulina / CamKII (Wei et al., 2007) y la modulación y tráfico del DAT (Fog et al., 2006; Sakrikar et al., 2012). ). ... Por ejemplo, AMPH aumenta el glutamato extracelular en varias regiones del cerebro, incluido el cuerpo estriado, VTA y NAc (Del Arco et al., 1999; Kim et al., 1981; Mora y Porras, 1993; Xue et al., 1996) , pero no se ha establecido si este cambio puede explicarse por una mayor liberación sináptica o por una reducción del aclaramiento de glutamato. ... La captación de EAAT2 sensible a DHK no fue alterada por AMPH (Figura 1A). El transporte de glutamato restante en estos cultivos de mesencéfalo probablemente esté mediado por EAAT3 y este componente disminuyó significativamente por AMPH
- ↑ a b Vaughan RA, Foster JD (septiembre de 2013). "Mecanismos de regulación del transportador de dopamina en estados normales y patológicos" . Tendencias en Ciencias Farmacológicas . 34 (9): 489–496. doi : 10.1016 / j.tips.2013.07.005 . PMC 3831354 . PMID 23968642 .
AMPH y METH también estimulan la salida de DA, que se cree que es un elemento crucial en sus propiedades adictivas [80], aunque los mecanismos no parecen ser idénticos para cada fármaco [81]. Estos procesos son dependientes de PKCβ y CaMK [72, 82], y los ratones knock-out para PKCβ muestran una disminución del flujo de salida inducido por AMPH que se correlaciona con una reducción de la locomoción inducida por AMPH [72].
- ↑ a b Maguire JJ, Davenport AP (2 de diciembre de 2014). " Receptor TA 1 " . Base de datos IUPHAR . Unión Internacional de Farmacología Básica y Clínica . Consultado el 8 de diciembre de 2014 .
- ^ Borowsky B, Adham N, Jones KA, Raddatz R, Artymyshyn R, Ogozalek KL, Durkin MM, Lakhlani PP, Bonini JA, Pathirana S, Boyle N, Pu X, Kouranova E, Lichtblau H, Ochoa FY, Branchek TA, Gerald C (julio de 2001). "Trazas de aminas: identificación de una familia de receptores acoplados a proteína G de mamíferos" . Actas de la Academia Nacional de Ciencias . 98 (16): 8966–8971. Código Bibliográfico : 2001PNAS ... 98.8966B . doi : 10.1073 / pnas.151105198 . PMC 55357 . PMID 11459929 .
- ^ a b "Familia SLC18 de transportadores de amina vesicular" . Base de datos IUPHAR . Unión Internacional de Farmacología Básica y Clínica . Consultado el 13 de noviembre de 2015 .
- ^ a b c d "Familia 1 del portador de soluto SLC1A1 (transportador de glutamato de alta afinidad neuronal / epitelial, sistema Xag), miembro 1 [Homo sapiens (humano)]" . NCBI Gene . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 11 de noviembre de 2014 .
La anfetamina modula la neurotransmisión excitadora a través de la endocitosis del transportador de glutamato EAAT3 en las neuronas de dopamina. ... la internalización de EAAT3 desencadenada por la anfetamina aumenta la señalización glutamatérgica y, por lo tanto, contribuye a los efectos de la anfetamina en la neurotransmisión.
- ^ Zhu HJ, Appel DI, Gründemann D, Markowitz JS (julio de 2010). "Interacción del transportador de cationes orgánicos 3 (SLC22A3) y anfetamina" . Revista de neuroquímica . 114 (1): 142-149. doi : 10.1111 / j.1471-4159.2010.06738.x . PMC 3775896 . PMID 20402963 .
- ^ Rytting E, Audus KL (enero de 2005). "Captación de carnitina mediada por transportador de cationes orgánicos nuevo 2 en células de coriocarcinoma placentario (BeWo)". Revista de Farmacología y Terapéutica Experimental . 312 (1): 192-198. doi : 10.1124 / jpet.104.072363 . PMID 15316089 . S2CID 31465243 .
- ^ Inazu M, Takeda H, Matsumiya T (agosto de 2003). "[El papel de los transportadores de monoamina gliales en el sistema nervioso central]". Nihon Shinkei Seishin Yakurigaku Zasshi (en japonés). 23 (4): 171-178. PMID 13677912 .
- ↑ a b c Vicentic A, Jones DC (febrero de 2007). "El sistema CART (transcripción regulada por cocaína y anfetaminas) en el apetito y la adicción a las drogas". Revista de Farmacología y Terapéutica Experimental . 320 (2): 499–506. doi : 10.1124 / jpet.105.091512 . PMID 16840648 . S2CID 14212763 .
La importancia fisiológica de CART se comprobó aún más en numerosos estudios en humanos que demuestran un papel de CART tanto en la alimentación como en la adicción a los psicoestimulantes. ... Los estudios de colocalización también apoyan el papel de CART en las acciones de los psicoestimulantes. ... Las transcripciones de los receptores CART y DA se colocalizan (Beaudry et al., 2004). En segundo lugar, las terminales nerviosas dopaminérgicas en la sinapsis NAc en neuronas que contienen CART (Koylu et al., 1999), por lo tanto, proporcionan la proximidad requerida para la señalización de neurotransmisores. Estos estudios sugieren que la DA juega un papel en la regulación de la expresión del gen CART posiblemente a través de la activación de CREB.
- ^ Zhang M, Han L, Xu Y (junio de 2012). "Funciones de la transcripción regulada por cocaína y anfetaminas en el sistema nervioso central". Farmacología y Fisiología Clínica y Experimental . 39 (6): 586–592. doi : 10.1111 / j.1440-1681.2011.05642.x . PMID 22077697 . S2CID 25134612 .
Recientemente, se demostró que el CART, como péptido neurotrófico, tenía un efecto cerebroprotector contra el ictus isquémico focal e inhibía la neurotoxicidad de la proteína β-amiloide, lo que centró la atención en el papel del CART en el sistema nervioso central (SNC) y las enfermedades neurológicas. ... La literatura indica que son muchos los factores, como la regulación del sistema inmunológico y la protección frente al fallo energético, que pueden estar implicados en la protección cerebral que ofrece CART
- ^ a b Rogge G, Jones D, Hubert GW, Lin Y, Kuhar MJ (octubre de 2008). "Péptidos CART: reguladores del peso corporal, recompensa y otras funciones" . Nature Reviews Neurociencia . 9 (10): 747–758. doi : 10.1038 / nrn2493 . PMC 4418456 . PMID 18802445 .
Varios estudios sobre la señalización celular inducida por péptidos CART (transcripción regulada por cocaína y anfetaminas) han demostrado que los péptidos CART activan al menos tres mecanismos de señalización. Primero, CART 55-102 inhibió los canales de Ca2 + tipo L dependientes de voltaje ...
- ^ Lin Y, Hall RA, Kuhar MJ (octubre de 2011). "Estimulación del péptido CART de la señalización mediada por proteína G en células PC12 diferenciadas: identificación de PACAP 6-38 como un antagonista del receptor CART" . Neuropéptidos . 45 (5): 351–358. doi : 10.1016 / j.npep.2011.07.006 . PMC 3170513 . PMID 21855138 .
- ^ "Monoamino oxidasa (Homo sapiens)" . BRENDA . Technische Universität Braunschweig. 1 de enero de 2014 . Consultado el 4 de mayo de 2014 .
- ^ a b c "Objetivos". Anfetamina . T3DB . Universidad de Alberta . Consultado el 24 de febrero de 2015 .
- ^ a b Toll L, Berzetei-Gurske IP, Polgar WE, Brandt SR, Adapa ID, Rodriguez L, Schwartz RW, Haggart D, O'Brien A, White A, Kennedy JM, Craymer K, Farrington L, Auh JS (marzo 1998). "Ensayos de unión y funcionales estándar relacionados con las pruebas de división de desarrollo de medicamentos para posibles medicamentos de tratamiento narcóticos de cocaína y opiáceos". Monografía de investigación del NIDA . 178 : 440–466. PMID 9686407 .
- ^ a b Finnema SJ, Scheinin M, Shahid M, Lehto J, Borroni E, Bang-Andersen B, Sallinen J, Wong E, Farde L, Halldin C, Grimwood S (noviembre de 2015). "Aplicación de imágenes de PET de especies cruzadas para evaluar la liberación de neurotransmisores en el cerebro" . Psicofarmacología . 232 (21-22): 4129-4157. doi : 10.1007 / s00213-015-3938-6 . PMC 4600473 . PMID 25921033 .
Más recientemente, Colasanti y sus colegas informaron que una elevación inducida farmacológicamente en la liberación de opioides endógenos redujo [
11
Unión de C] carfentanilo en varias regiones del cerebro humano, incluidos los ganglios basales, la corteza frontal y el tálamo (Colasanti et al. 2012). La administración oral de d-anfetamina, 0,5 mg / kg, 3 h antes de la inyección de [ 11 C] carfentanilo, redujo los valores de BPND en un 2 a 10%. Los resultados se confirmaron en otro grupo de sujetos (Mick et al. 2014). Sin embargo, Guterstam y sus colegas no observaron cambios en la unión de [ 11 C] carfentanil cuando se administró d-anfetamina, 0.3 mg / kg, por vía intravenosa directamente antes de la inyección de [ 11C] carfentanilo (Guterstam et al. 2013). Se ha planteado la hipótesis de que esta discrepancia puede estar relacionada con aumentos retardados en las concentraciones de péptidos opioides extracelulares después de la liberación de monoaminas evocadas por anfetaminas (Colasanti et al. 2012; Mick et al. 2014).
- ↑ a b Loseth GE, Ellingsen DM, Leknes S (diciembre de 2014). "Modulación de la motivación social μ-opioide dependiente del estado" . Fronteras en neurociencia del comportamiento . 8 : 430. doi : 10.3389 / fnbeh.2014.00430 . PMC 4264475 . PMID 25565999 .
Se informaron patrones de activación de MOR similares durante el estado de ánimo positivo inducido por un videoclip divertido (Koepp et al., 2009) y después de la administración de anfetaminas en humanos (Colasanti et al., 2012).
- ^ a b Colasanti A, Searle GE, Long CJ, Hill SP, Reiley RR, Quelch D, Erritzoe D, Tziortzi AC, Reed LJ, Lingford-Hughes AR, Waldman AD, Schruers KR, Matthews PM, Gunn RN, Nutt DJ, Rabiner EA (septiembre de 2012). "Liberación de opioides endógenos en el sistema de recompensa del cerebro humano inducida por la administración aguda de anfetaminas". Psiquiatría biológica . 72 (5): 371–377. doi : 10.1016 / j.biopsych.2012.01.027 . PMID 22386378 . S2CID 18555036 .
- ↑ a b c Gunne LM (2013). "Efectos de las anfetaminas en humanos" . Drogadicción II: Dependencia de anfetaminas, psicógenos y marihuana . Berlín, Alemania; Heidelberg, Alemania: Springer. págs. 247–260. ISBN 9783642667091. Consultado el 4 de diciembre de 2015 .
- ^ a b c Oswald LM, Wong DF, McCaul M, Zhou Y, Kuwabara H, Choi L, Brasic J, Wand GS (abril de 2005). "Relaciones entre la liberación de dopamina del estriado ventral, la secreción de cortisol y las respuestas subjetivas a la anfetamina" . Neuropsicofarmacología . 30 (4): 821–832. doi : 10.1038 / sj.npp.1300667 . PMID 15702139 . S2CID 12302237 .
Los resultados de varias investigaciones previas han demostrado que los niveles plasmáticos de glucocorticoides y ACTH aumentan con la administración aguda de AMPH tanto en roedores como en humanos.
- ^ a b c d e f g h i j Angeli A, Vaiano F, Mari F, Bertol E, Supuran CT (diciembre de 2017). "Las sustancias psicoactivas pertenecientes a la clase de las anfetaminas activan potentemente las isoformas VA, VB, VII y XII de la anhidrasa carbónica cerebral" . Revista de inhibición de enzimas y química medicinal . 32 (1): 1253-1259. doi : 10.1080 / 14756366.2017.1375485 . PMC 6009978 . PMID 28936885 .
Aquí, presentamos el primer estudio de este tipo, que muestra que la anfetamina, la metanfetamina, la fentermina, la mefentermina y la clorfenteramina activan de manera potente varias isoformas de CA, algunas de las cuales son muy abundantes en el cerebro, donde desempeñan funciones importantes relacionadas con la cognición y la memoria, entre otras. otros26,27. ... Investigamos aminas psicotrópicas basadas en el andamio de fenetilamina, como anfetamina 5, metanfetamina 6, fentermina 7, mefentermina 8 y la clorfenteramina 9 estructuralmente diversa, por sus efectos activadores sobre 11 isoformas de CA de origen humano ... hCA I y II, el hCA VI secretado, así como el hCA XIII citosólico y el hCA IX y XIV unidos a la membrana se activaron pobremente por estas aminas, mientras que el hCA IV extracelular, las enzimas mitocondriales hCA VA / VB, el hCA VII citosólico ,y la isoforma transmembrana hCA XII se activaron de forma potente. Algunas de estas enzimas (hCA VII, VA, VB, XII) son abundantes en el cerebro, lo que plantea la posibilidad de que algunos de los efectos cognitivos de dichas sustancias psicoactivas puedan estar relacionados con la activación de estas enzimas. ... Los AAC comenzaron a considerarse solo recientemente para posibles aplicaciones farmacológicas en la terapia de la memoria / cognición27. Este trabajo puede aportar nuevas luces sobre la intrincada relación entre la activación de CA por este tipo de compuestos y la multitud de acciones farmacológicas que pueden provocar.Los AAC comenzaron a considerarse solo recientemente para posibles aplicaciones farmacológicas en la terapia de la memoria / cognición27. Este trabajo puede aportar nuevas luces sobre la intrincada relación entre la activación de CA por este tipo de compuestos y la multitud de acciones farmacológicas que pueden provocar.Los AAC comenzaron a considerarse solo recientemente para posibles aplicaciones farmacológicas en la terapia de la memoria / cognición27. Este trabajo puede aportar nuevas luces sobre la intrincada relación entre la activación de CA por este tipo de compuestos y la multitud de acciones farmacológicas que pueden provocar.
Tabla 1: Activación de CA de las isoformas hCA I, II, IV, VII y XIII [5: anfetamina]
Tabla 2: Activación de CA de las isoformas hCA VA, VB, VI, IX, XII y XIV [5: anfetamina] - ^ a b Lewin AH, Miller GM, Gilmour B (diciembre de 2011). "El receptor 1 asociado a trazas de amina es un sitio de unión estereoselectivo para compuestos de la clase de las anfetaminas" . Química bioorgánica y medicinal . 19 (23): 7044–7048. doi : 10.1016 / j.bmc.2011.10.007 . PMC 3236098 . PMID 22037049 .
- ^ a b Maguire JJ, Parker WA, Foord SM, Bonner TI, Neubig RR, Davenport AP (marzo de 2009). "Unión Internacional de Farmacología. LXXII. Recomendaciones para la nomenclatura del receptor de trazas de amina" . Revisiones farmacológicas . 61 (1): 1–8. doi : 10.1124 / pr.109.001107 . PMC 2830119 . PMID 19325074 .
- ^ Revel FG, Moreau JL, Gainetdinov RR, Bradaia A, Sotnikova TD, Mory R, Durkin S, Zbinden KG, Norcross R, Meyer CA, Metzler V, Chaboz S, Ozmen L, Trube G, Pouzet B, Bettler B, Caron MG, Wettstein JG, Hoener MC (mayo de 2011). "La activación de TAAR1 modula la neurotransmisión monoaminérgica, previniendo la actividad hiperdopaminérgica e hipoglutamatérgica" . Actas de la Academia Nacional de Ciencias . 108 (20): 8485–8490. doi : 10.1073 / pnas.1103029108 . PMC 3101002 . PMID 21525407 .
- ^ a b "Anfetamina: actividad biológica" . Guía de farmacología IUPHAR / BPS . Unión Internacional de Farmacología Básica y Clínica . Consultado el 31 de diciembre de 2019 .
- ↑ a b Bozdag M, Altamimi AA, Vullo D, Supuran CT, Carta F (2019). "Estado del arte en moduladores de anhidrasa carbónica para fines biomédicos". Química Medicinal Actual . 26 (15): 2558-2573. doi : 10.2174 / 0929867325666180622120625 . PMID 29932025 .
INHIBIDORES DE ANHIDRASAS CARBÓNICAS (CAI). El diseño y desarrollo de los CAI representan el área más prolífica dentro del campo de investigación de CA. Desde la introducción de los CAI en el uso clínico en los años 40, siguen siendo la primera opción para el tratamiento del edema [9], el mal de altura [9], el glaucoma [7] y la epilepsia [31]. ... ACTIVADORES DE ANHIDRASAS CARBÓNICAS (AAC) ... La clase emergente de AAC ha ganado atractivo recientemente a medida que se demostró en modelos animales que la mejora de las propiedades cinéticas en los hCA expresados en el SNC es beneficiosa para el tratamiento tanto cognitivo como de la memoria discapacidades. Así, los AAC tienen una enorme potencialidad en química médica para ser desarrollados para el tratamiento de síntomas asociados al envejecimiento, trauma o deterioro de los tejidos del SNC.
- ^ a b c d e f "Vyvanse- cápsula de dimesilato de lisdexanfetamina Vyvanse- tableta de dimesilato de lisdexanfetamina, masticable" . DailyMed . Shire US Inc.30 de octubre de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ "Resumen compuesto" . p-hidroxianfetamina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Resumen compuesto" . p-hidroxinorefedrina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Resumen compuesto" . Fenilpropanolamina . Base de datos compuesta de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Farmacología y bioquímica" . Anfetamina . Base de datos compuesta de Pubchem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 12 de octubre de 2013 .
- ↑ a b c Sjoerdsma A, von Studnitz W (abril de 1963). "Actividad de la dopamina-beta-oxidasa en el hombre, utilizando hidroxianfetamina como sustrato" . Revista británica de farmacología y quimioterapia . 20 : 278-284. doi : 10.1111 / j.1476-5381.1963.tb01467.x . PMC 1703637 . PMID 13977820 .
Se administró hidroxianfetamina por vía oral a cinco sujetos humanos ... Dado que la conversión de hidroxianfetamina en hidroxinorefedrina se produce in vitro por la acción de la dopamina-β-oxidasa, se sugiere un método simple para medir la actividad de esta enzima y el efecto de sus inhibidores en el hombre . ... La falta de efecto de la administración de neomicina a un paciente indica que la hidroxilación se produce en los tejidos corporales. ... una parte importante de la β-hidroxilación de la hidroxianfetamina se produce en el tejido no suprarrenal. Desafortunadamente, en la actualidad no se puede estar completamente seguro de que la hidroxilación de la hidroxianfetamina in vivo se lleve a cabo mediante la misma enzima que convierte la dopamina en noradrenalina.
- ↑ a b Badenhorst CP, van der Sluis R, Erasmus E, van Dijk AA (septiembre de 2013). "Conjugación de glicina: importancia en el metabolismo, el papel de la glicina N-aciltransferasa y factores que influyen en la variación interindividual". Opinión de expertos sobre metabolismo y toxicología de fármacos . 9 (9): 1139-1153. doi : 10.1517 / 17425255.2013.796929 . PMID 23650932 .
Figura 1. Conjugación de glicina del ácido benzoico. La vía de conjugación de glicina consta de dos pasos. El primer benzoato se liga a CoASH para formar el tioéster de benzoil-CoA de alta energía. Esta reacción es catalizada por el ácido de cadena media HXM-A y HXM-B: CoA ligasas y requiere energía en forma de ATP. ... El benzoil-CoA luego se conjuga con glicina por GLYAT para formar ácido hipúrico, liberando CoASH. Además de los factores enumerados en los recuadros, los niveles de ATP, CoASH y glicina pueden influir en la velocidad general de la vía de conjugación de glicina.
- ^ Horwitz D, Alexander RW, Lovenberg W, Keizer HR (mayo de 1973). "Dopamina-β-hidroxilasa de suero humano. Relación con la hipertensión y la actividad simpática". Investigación de circulación . 32 (5): 594–599. doi : 10.1161 / 01.RES.32.5.594 . PMID 4713201 .
La importancia biológica de los diferentes niveles de actividad de DβH en suero se estudió de dos formas. En primer lugar, se comparó la capacidad in vivo para β-hidroxilar el sustrato sintético hidroxianfetamina en dos sujetos con baja actividad de DβH en suero y dos sujetos con actividad media. ... En un estudio, se administró hidroxianfetamina (Paredrine), un sustrato sintético para DβH, a sujetos con niveles bajos o medios de actividad de DβH en suero. El porcentaje de fármaco hidroxilado a hidroxinorefedrina fue comparable en todos los sujetos (6,5-9,62) (Tabla 3).
- ^ Freeman JJ, Sulser F (diciembre de 1974). "Formación de p-hidroxinorefedrina en el cerebro después de la administración intraventricular de p-hidroxianfetamina". Neurofarmacología . 13 (12): 1187-1190. doi : 10.1016 / 0028-3908 (74) 90069-0 . PMID 4457764 .
En especies en las que la hidroxilación aromática de la anfetamina es la principal vía metabólica, la
p
-hidroxianfetamina (POH) y la
p
-hidroxinorrefedrina (PHN) pueden contribuir al perfil farmacológico del fármaco original. ... La ubicación de la
p
Las reacciones de -hidroxilación y β-hidroxilación son importantes en especies donde la hidroxilación aromática de anfetamina es la vía predominante de metabolismo. Después de la administración sistémica de anfetamina a ratas, se ha encontrado POH en orina y plasma.
La falta observada de una acumulación significativa de PHN en el cerebro después de la administración intraventricular de (+) - anfetamina y la formación de cantidades apreciables de PHN a partir de (+) - POH en tejido cerebral in vivo respalda la opinión de que la hidroxilación aromática de anfetamina después de su administración sistémica ocurre predominantemente en la periferia, y entonces la POH es transportada a través de la barrera hematoencefálica, captada por neuronas noradrenérgicas en el cerebro, donde la (+) - POH se convierte en las vesículas de almacenamiento por la dopamina β-hidroxilasa en PHN. - ^ Matsuda LA, Hanson GR, Gibb JW (diciembre de 1989). "Efectos neuroquímicos de los metabolitos de las anfetaminas en los sistemas central dopaminérgico y serotoninérgico". Revista de Farmacología y Terapéutica Experimental . 251 (3): 901–908. PMID 2600821 .
El metabolismo de
p
-OHA a
p
-OHNor está bien documentado y la dopamina-β hidroxilasa presente en las neuronas noradrenérgicas podría convertir fácilmente
p
-OHA en
p
-OHN o después de la administración intraventricular.
- ^ a b c d e f ElRakaiby M, Dutilh BE, Rizkallah MR, Boleij A, Cole JN, Aziz RK (julio de 2014). "Pharmacomicrobiomics: el impacto de las variaciones del microbioma humano en la farmacología de sistemas y la terapéutica personalizada" . Omics . 18 (7): 402–414. doi : 10.1089 / omi.2014.0018 . PMC 4086029 . PMID 24785449 .
Los cien billones de microbios y virus que residen en cada cuerpo humano, que superan en número a las células humanas y aportan al menos 100 veces más genes que los codificados en el genoma humano (Ley et al., 2006), ofrecen una inmensa reserva de accesorios para la genética interindividual. variación que ha sido subestimada y en gran parte inexplorada (Savage, 1977; Medini et al., 2008; Minot et al., 2011; Wylie et al., 2012). ... Mientras tanto, desde hace mucho tiempo se dispone de una gran cantidad de literatura sobre la biotransformación de xenobióticos, especialmente por bacterias intestinales (revisado en Sousa et al., 2008; Rizkallah et al., 2010; Johnson et al., 2012; Haiser y Turnbaugh , 2013). Esta valiosa información se refiere principalmente al metabolismo de fármacos por microbios desconocidos asociados con los seres humanos; sin embargo, solo se han documentado unos pocos casos de variaciones de microbiomas interindividuales [p. ej.,digoxina (Mathan et al., 1989) y acetaminofén (Clayton et al., 2009)].
- ^ a b c Cho I, Blaser MJ (marzo de 2012). "El microbioma humano: en la interfaz de la salud y la enfermedad" . Nature Reviews Genética . 13 (4): 260–270. doi : 10.1038 / nrg3182 . PMC 3418802 . PMID 22411464 .
La composición del microbioma varía según el sitio anatómico (Figura 1). El principal determinante de la composición de la comunidad es la ubicación anatómica: la variación interpersonal es sustancial
23,24
y es mayor que la variabilidad temporal observada en la mayoría de los sitios en un solo individuo
25
. ... ¿Cómo afecta el microbioma a la farmacología de los medicamentos? ¿Podemos "micro-tipificar" personas para mejorar la farmacocinética y / o reducir la toxicidad? ¿Podemos manipular el microbioma para mejorar la estabilidad farmacocinética?
- ^ Hutter T, Gimbert C, Bouchard F, Lapointe FJ (2015). "Ser humano es un presentimiento" . Microbioma . 3 : 9. doi : 10.1186 / s40168-015-0076-7 . PMC 4359430 . PMID 25774294 .
Algunos estudios metagenómicos han sugerido que menos del 10% de las células que componen nuestro cuerpo son células de Homo sapiens. El 90% restante son células bacterianas. La descripción de este llamado microbioma humano es de gran interés e importancia por varias razones. Por un lado, nos ayuda a redefinir lo que es un individuo biológico. Sugerimos que un individuo humano ahora se describe mejor como un superindividuo en el que coexisten un gran número de especies diferentes (incluido el Homo sapiens).
- ^ a b c d Kumar K, Dhoke GV, Sharma AK, Jaiswal SK, Sharma VK (enero de 2019). "Aclaración mecanicista del metabolismo de la anfetamina por tiramina oxidasa de la microbiota intestinal humana mediante simulaciones de dinámica molecular". Revista de bioquímica celular . 120 (7): 11206–11215. doi : 10.1002 / jcb.28396 . PMID 30701587 . S2CID 73413138 .
Particularmente en el caso del intestino humano, que alberga una gran diversidad de especies bacterianas, las diferencias en la composición microbiana pueden alterar significativamente la actividad metabólica en el lumen intestinal.
4
La actividad metabólica diferencial debida a las diferencias en las especies microbianas intestinales se ha relacionado recientemente con diversos trastornos y enfermedades metabólicas. 5-12 Además del impacto de la diversidad microbiana intestinal o disbiosis en diversas enfermedades humanas, existe una cantidad creciente de evidencia que muestra que los microbios intestinales pueden afectar la biodisponibilidad y eficacia de varias moléculas de fármacos administradas por vía oral a través de un metabolismo enzimático promiscuo. 13,14 ... El presente estudio sobre los detalles atomísticos de la unión de la anfetamina y la afinidad de unión a la tiramina oxidasa junto con la comparación con dos sustratos naturales de esta enzima, a saber, la tiramina y la fenilalanina, proporciona una fuerte evidencia del metabolismo basado en la promiscuidad de la anfetamina por la tiramina oxidasa. enzima de E. coli. Los resultados obtenidos serán cruciales en el diseño de una molécula sustituta de anfetamina que pueda ayudar a mejorar la eficacia y biodisponibilidad del fármaco anfetamínico a través de la inhibición competitiva o al rediseño del fármaco para obtener mejores efectos farmacológicos. Este estudio también tendrá implicaciones clínicas útiles en la reducción de la variación causada por la microbiota intestinal en la respuesta al fármaco entre diferentes poblaciones.
- ↑ a b Khan MZ, Nawaz W (octubre de 2016). "Los roles emergentes de trazas de aminas humanas y receptores asociados a aminas de trazas humanas (hTAAR) en el sistema nervioso central". Biomedicina y Farmacoterapia . 83 : 439–449. doi : 10.1016 / j.biopha.2016.07.002 . PMID 27424325 .
- ↑ a b c d e Lindemann L, Hoener MC (mayo de 2005). "Un renacimiento en trazas de aminas inspirado en una nueva familia GPCR". Tendencias en Ciencias Farmacológicas . 26 (5): 274–281. doi : 10.1016 / j.tips.2005.03.007 . PMID 15860375 .
- ^ "Determinación de que las tabletas y cápsulas de Delcobese (adipato de anfetamina, sulfato de anfetamina, adipato de dextroanfetamina, sulfato de dextroanfetamina) no se retiraron de la venta por razones de seguridad o eficacia" . Registro Federal . 10 de noviembre de 2003 . Consultado el 3 de enero de 2020 .
- ^ "Clorhidrato de anfetamina" . Base de datos compuesta de Pubchem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 8 de noviembre de 2013 .
- ^ "Fosfato de anfetamina" . Base de datos compuesta de Pubchem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 8 de noviembre de 2013 .
- ^ Cavallito, John (23 de agosto de 1960). "Tanato de anfetamina. Solicitud de patente nº 2.950.309" (PDF) . Oficina de Patentes de Estados Unidos .
- ^ Brussee J, Jansen AC (mayo de 1983). "Una síntesis altamente estereoselectiva de s (-) - [1,1'-binaftaleno] -2,2'-diol". Letras de tetraedro . 24 (31): 3261–3262. doi : 10.1016 / S0040-4039 (00) 88151-4 .
- ↑ a b Schep LJ, Slaughter RJ, Beasley DM (agosto de 2010). "La toxicología clínica de la metamfetamina". Toxicología clínica . 48 (7): 675–694. doi : 10.3109 / 15563650.2010.516752 . ISSN 1556-3650 . PMID 20849327 . S2CID 42588722 .
- ^ Lillsunde P, Korte T (marzo de 1991). "Determinación de anfetaminas sustituidas en anillo y N como derivados de heptafluorobutirilo". Internacional de Ciencias Forenses . 49 (2): 205–213. doi : 10.1016 / 0379-0738 (91) 90081-s . PMID 1855720 .
- ^ a b c d "Reseña histórica de la metanfetamina" . Departamento de Salud de Vermont . Gobierno de Vermont. Archivado desde el original el 5 de octubre de 2012 . Consultado el 29 de enero de 2012 .
- ↑ a b c Allen A, Ely R (abril de 2009). "Revisión: métodos sintéticos de anfetamina" (PDF) . Escena del crimen . Asociación del Noroeste de Científicos Forenses. 37 (2): 15-25 . Consultado el 6 de diciembre de 2014 .
- ↑ a b c Allen A, Cantrell TS (agosto de 1989). "Reducciones sintéticas en laboratorios clandestinos de anfetaminas y metanfetaminas: una revisión". Internacional de Ciencias Forenses . 42 (3): 183-199. doi : 10.1016 / 0379-0738 (89) 90086-8 .
- ^ a b c d "Métodos recomendados para la identificación y análisis de anfetamina, metanfetamina y sus análogos de anillo sustituido en materiales incautados" (PDF) . Oficina de las Naciones Unidas contra la Droga y el Delito . Naciones Unidas. 2006. págs. 9-12 . Consultado el 14 de octubre de 2013 .
- ^ Pollard CB, Young DC (mayo de 1951). "El mecanismo de la reacción de Leuckart". La Revista de Química Orgánica . 16 (5): 661–672. doi : 10.1021 / jo01145a001 .
- ^ Patente estadounidense 2276508 , Nabenhauer FP, "Método para la separación de alfa-metilfenetilamina ópticamente activa", publicada el 17 de marzo de 1942, asignada a Smith Kline French
- ↑ a b Gray DL (2007). "Tratamientos aprobados para el trastorno por déficit de atención con hiperactividad: anfetamina (Adderall), metilfenidato (Ritalin) y atomoxetina (Straterra)" . En Johnson DS, Li JJ (eds.). El arte de la síntesis de fármacos . Nueva York, Estados Unidos: Wiley-Interscience. pag. 247. ISBN 9780471752158.
- ^ Patrick TM, McBee ET, Hass HB (junio de 1946). "Síntesis de arilpropilaminas; a partir de cloruro de alilo". Revista de la Sociedad Química Estadounidense . 68 (6): 1009–1011. doi : 10.1021 / ja01210a032 . PMID 20985610 .
- ^ Ritter JJ, Kalish J (diciembre de 1948). "Una nueva reacción de nitrilos; síntesis de t-carbinaminas". Revista de la Sociedad Química Estadounidense . 70 (12): 4048–4050. doi : 10.1021 / ja01192a023 . PMID 18105933 .
- ^ Krimen LI, Cota DJ (marzo de 2011). "La reacción de Ritter". Reacciones orgánicas . 17 . pag. 216. doi : 10.1002 / 0471264180.or017.03 . ISBN 9780471264187.
- ^ Patente estadounidense 2413493 , Bitler WP, Flisik AC, Leonard N, "Síntesis de éster metílico de bencilmetil acetoacético sin isómeros", publicada el 31 de diciembre de 1946, asignada a Kay Fries Chemicals Inc.
- ^ Collins M, Salouros H, Cawley AT, Robertson J, Heagney AC, Arenas-Queralt A (junio de 2010). "Relaciones de isótopos δ 13 C y δ 2 H en anfetamina sintetizada a partir de benzaldehído y nitroetano". Comunicaciones rápidas en espectrometría de masas . 24 (11): 1653-1658. doi : 10.1002 / rcm.4563 . PMID 20486262 .
- ^ Kraemer T, Maurer HH (agosto de 1998). "Determinación de anfetaminas, metanfetaminas y medicamentos de diseño derivados de anfetaminas o medicamentos en sangre y orina". Journal of Chromatography B . 713 (1): 163–187. doi : 10.1016 / S0378-4347 (97) 00515-X . PMID 9700558 .
- ^ Kraemer T, Paul LD (agosto de 2007). "Procedimientos bioanalíticos para la determinación de drogas de abuso en sangre". Química analítica y bioanalítica . 388 (7): 1415-1435. doi : 10.1007 / s00216-007-1271-6 . PMID 17468860 . S2CID 32917584 .
- ^ Goldberger BA, Cone EJ (julio de 1994). "Pruebas confirmatorias de fármacos en el lugar de trabajo mediante cromatografía de gases-espectrometría de masas". Journal of Chromatography A . 674 (1–2): 73–86. doi : 10.1016 / 0021-9673 (94) 85218-9 . PMID 8075776 .
- ^ a b "Pruebas clínicas de drogas en atención primaria" (PDF) . Universidad de Colorado Denver . Serie de publicaciones de asistencia técnica 32. Departamento de Salud y Servicios Humanos de los Estados Unidos - Administración de Servicios de Salud Mental y Abuso de Sustancias. 2012. p. 55. Archivado (PDF) desde el original el 14 de mayo de 2018 . Consultado el 31 de octubre de 2013 .
Se puede detectar una sola dosis de anfetamina o metanfetamina en la orina durante aproximadamente 24 horas, según el pH de la orina y las diferencias metabólicas individuales. Las personas que lo usan de forma crónica y en dosis altas pueden seguir teniendo muestras de orina positivas durante 2 a 4 días después del último uso (SAMHSA, 2010b).
- ↑ a b c d e Paul BD, Jemionek J, Lesser D, Jacobs A, Searles DA (septiembre de 2004). "Separación enantiomérica y cuantificación de (±) -anfetamina, (±) -metanfetamina, (±) -MDA, (±) -MDMA y (±) -MDEA en muestras de orina por GC-EI-MS después de derivatizar con ( R ) - (-) - o ( S ) - (+) - α-metoxi-α- (trifluorometil) fenilacetilo (MTPA) " . Revista de Toxicología Analítica . 28 (6): 449–455. doi : 10.1093 / jat / 28.6.449 . PMID 15516295 .
- ^ "Parte 341 - productos para el resfriado, tos, alergias, broncodilatadores y antiasmáticos para uso humano sin receta" . Código de Regulaciones Federales Título 21: Subcapítulo D - Medicamentos para uso humano . Administración de Drogas y Alimentos de los Estados Unidos . 1 de abril de 2019. Archivado desde el original el 25 de diciembre de 2019 . Consultado el 24 de diciembre de 2019 .
Descongestionantes nasales tópicos - (i) Para productos que contienen levmetamfetamina identificados en 341.20 (b) (1) cuando se usan en una forma de dosificación inhalable. El producto entrega en cada 800 mililitros de aire de 0.04 a 0.150 miligramos de levmetamfetamina.
- ^ "Identificación" . Levometanfetamina . Base de datos compuesta de Pubchem . Biblioteca Nacional de Medicina de los Estados Unidos - Centro Nacional de Información Biotecnológica . Consultado el 2 de enero de 2014 .
- ↑ a b Verstraete AG, Heyden FV (agosto de 2005). "Comparación de la sensibilidad y especificidad de seis inmunoensayos para la detección de anfetaminas en orina" . Revista de Toxicología Analítica . 29 (5): 359–364. doi : 10.1093 / jat / 29.5.359 . PMID 16105261 .
- ^ Baselt RC (2011). Disposición de drogas y sustancias químicas tóxicas en el hombre (9ª ed.). Seal Beach, Estados Unidos: Publicaciones biomédicas. págs. 85–88. ISBN 9780962652387.
- ↑ a b Musshoff F (febrero de 2000). "¿Uso ilegal o legítimo? Compuestos precursores de anfetamina y metanfetamina". Reseñas de metabolismo de fármacos . 32 (1): 15–44. doi : 10.1081 / DMR-100100562 . PMID 10711406 . S2CID 20012024 .
- ↑ a b Cody JT (mayo de 2002). "Medicamentos precursores como fuente de metanfetamina y / o resultados positivos de las pruebas de drogas de anfetamina". Revista de Medicina Ambiental y Ocupacional . 44 (5): 435–450. doi : 10.1097 / 00043764-200205000-00012 . PMID 12024689 . S2CID 44614179 .
- ^ "Prevalencia anual del uso de drogas, por región y globalmente, 2016" . Informe mundial sobre las drogas 2018 . Oficina de Drogas y Crimen de las Naciones Unidas. 2018 . Consultado el 7 de julio de 2018 .
- ^ Rassool GH (2009). Uso indebido de alcohol y drogas: manual para estudiantes y profesionales de la salud . Londres, Inglaterra: Routledge. pag. 113. ISBN 9780203871171.
- ↑ a b Sulzer D, Sonders MS, Poulsen NW, Galli A (abril de 2005). "Mecanismos de liberación de neurotransmisores por anfetaminas: una revisión". Progresos en neurobiología . 75 (6): 406–433. doi : 10.1016 / j.pneurobio.2005.04.003 . PMID 15955613 . S2CID 2359509 .
- ^ Rasmussen N (agosto de 2011). "La ciencia médica y el ejército: el uso de anfetaminas por los aliados durante la Segunda Guerra Mundial". Revista de Historia Interdisciplinaria . 42 (2): 205–233. doi : 10.1162 / JINH_a_00212 . PMID 22073434 . S2CID 34332132 .
- ^ Defalque RJ, Wright AJ (abril de 2011). "Metanfetamina para la Alemania de Hitler: 1937 a 1945". Boletín de Historia de la Anestesia . 29 (2): 21-24, 32. doi : 10.1016 / s1522-8649 (11) 50016-2 . PMID 22849208 .
- ^ "Ley de sustancias controladas" . Administración de Drogas y Alimentos de los Estados Unidos. 11 de junio de 2009. Archivado desde el original el 2 de marzo de 2017 . Consultado el 4 de noviembre de 2013 .
- ^ "Horarios de sustancias controladas" . División de Control de Desvío de la DEA . Consultado el 25 de diciembre de 2019 .
- ^ Gyenis A. "Cuarenta años de On the Road 1957-1997" . wordsareimportant.com . Latido de DHARMA. Archivado desde el original el 14 de febrero de 2008 . Consultado el 18 de marzo de 2008 .
- ^ Wilson A (2008). "Mezcla de la medicina: la consecuencia involuntaria del control de anfetaminas en la escena del alma del norte" (PDF) . Revista de Criminología de Internet . Archivado desde el original (PDF) el 13 de julio de 2011 . Consultado el 25 de mayo de 2013 .
- ^ Hill J (4 de junio de 2004). "Paul Erdos, genio matemático, humano (en ese orden)" (PDF) . Consultado el 2 de noviembre de 2013 .
- ^ a b c Mohan J, ed. (Junio de 2014). "Informe mundial sobre las drogas 2014" (PDF) . Oficina de las Naciones Unidas contra la Droga y el Delito . pag. 3 . Consultado el 18 de agosto de 2014 .
- ^ "Boletín estadístico 2018 - prevalencia del uso de drogas" . Observatorio Europeo de las Drogas y las Toxicomanías . Consultado el 5 de febrero de 2019 .
- ^ a b Informe europeo sobre drogas 2014: Tendencias y desarrollos (PDF) (Informe). Lisboa, Portugal: Observatorio Europeo de las Drogas y las Toxicomanías. Mayo de 2014. págs. 13, 24. doi : 10.2810 / 32306 . ISSN 2314-9086 . Consultado el 18 de agosto de 2014 .
1,2 millones o el 0,9% de los adultos jóvenes (de 15 a 34 años) consumieron anfetaminas en el último año
- ^ Oficina de las Naciones Unidas contra la Droga y el Delito (2007). Prevención del uso de estimulantes de tipo anfetamínico entre los jóvenes: guía de políticas y programación (PDF) . Nueva York, Estados Unidos: Naciones Unidas. ISBN 9789211482232. Consultado el 11 de noviembre de 2013 .
- ^ "Lista de sustancias psicotrópicas sometidas a fiscalización internacional" (PDF) . Junta Internacional de Fiscalización de Estupefacientes . Naciones Unidas. Agosto de 2003. Archivado desde el original (PDF) el 5 de diciembre de 2005 . Consultado el 19 de noviembre de 2005 .
- ^ "Importar o traer medicamentos a Japón para uso personal" . Ministerio de Salud, Trabajo y Bienestar de Japón . 1 de abril de 2004 . Consultado el 3 de noviembre de 2013 .
- ^ "Ley de sustancias y drogas controladas" . Sitio web de leyes de justicia canadiense . Gobierno de Canadá. Archivado desde el original el 22 de noviembre de 2013 . Consultado el 11 de noviembre de 2013 .
- ^ "Opiumwet" . Gobierno de los Países Bajos . Consultado el 3 de abril de 2015 .
- ^ "Programa 8" . Estándar de venenos . Departamento de Salud del Gobierno de Australia. Octubre de 2015 . Consultado el 15 de diciembre de 2015 .
- ^ "Tabla de estupefacientes controlados según la Ley de estupefacientes de Tailandia" (PDF) . Administración de Alimentos y Medicamentos de Tailandia . 22 de mayo de 2013. Archivado desde el original (PDF) el 8 de marzo de 2014 . Consultado el 11 de noviembre de 2013 .
- ^ "Drogas de clase A, B y C" . Ministerio del Interior, Gobierno del Reino Unido . Archivado desde el original el 4 de agosto de 2007 . Consultado el 23 de julio de 2007 .
- ^ a b "Tableta de anfetamina Adzenys XR-ODT-, que se desintegra por vía oral" . DailyMed . Neos Therapeutics, Inc. 9 de febrero de 2018 . Consultado el 22 de diciembre de 2019 .
ADZENYS XR-ODT (tableta de anfetamina de liberación prolongada de desintegración oral) contiene una proporción de 3 a 1 de d- a l-anfetamina, un estimulante del sistema nervioso central.
- ^ "Mydayis- sulfato de dextroanfetamina, sacarato de dextroanfetamina, monohidrato de aspartato de anfetamina y cápsula de sulfato de anfetamina, liberación prolongada" . DailyMed . Shire US Inc. 11 de octubre de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ "Paquete de aprobación de medicamentos: Mydayis (sales mixtas de un producto de anfetamina de entidad única)" . Administración de Drogas y Alimentos de los Estados Unidos . 6 de junio de 2018 . Consultado el 22 de diciembre de 2019 .
- ^ "Adzenys ER- suspensión de anfetamina, liberación prolongada" . DailyMed . Neos Therapeutics, Inc. 8 de diciembre de 2017 . Consultado el 25 de diciembre de 2019 .
- ^ "Paquete de aprobación de medicamentos: Adzenys XR-ODT (anfetamina)" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 22 de diciembre de 2019 .
- ^ "Evekeo" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 11 de agosto de 2015 .
- ^ "Evekeo ODT- tableta de sulfato de anfetamina, desintegración oral" . DailyMed . Arbor Pharmaceuticals, LLC. El 7 de junio de 2019 . Consultado el 25 de diciembre de 2019 .
- ^ "Tableta de sulfato de zenzedi- dextroanfetamina" . DailyMed . Arbor Pharmaceuticals, LLC. 14 de agosto de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ "Paquete de aprobación de medicamentos: Vyvanse (Lisdexanfetamina Dimesylate) NDA # 021977" . Administración de Drogas y Alimentos de los Estados Unidos . 24 de diciembre de 1999 . Consultado el 22 de diciembre de 2019 .
- ^ "Calculadora de peso molecular" . Lenntech . Consultado el 19 de agosto de 2015 .
- ^ a b "Sulfato de dextroanfetamina USP" . Mallinckrodt Pharmaceuticals. Marzo de 2014 . Consultado el 19 de agosto de 2015 .
- ^ a b "Sulfato de D-anfetamina" . Tocris. 2015 . Consultado el 19 de agosto de 2015 .
- ^ a b "Sulfato de anfetamina USP" . Mallinckrodt Pharmaceuticals. Marzo de 2014 . Consultado el 19 de agosto de 2015 .
- ^ "Sacarato de dextroanfetamina" . Mallinckrodt Pharmaceuticals. Marzo de 2014 . Consultado el 19 de agosto de 2015 .
- ^ "Aspartato de anfetamina" . Mallinckrodt Pharmaceuticals. Marzo de 2014 . Consultado el 19 de agosto de 2015 .
enlaces externos
- "Anfetamina" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de los Estados Unidos.
- CID 5826 de PubChem - Dextroanfetamina
- CID 32893 de PubChem - Levoanfetamina
- Entrada comparativa de la base de datos de toxicogenómica: anfetamina
- Entrada comparativa de la base de datos de toxicogenómica: CARTPT