| Hipertensión intracraneal idiopática | |
|---|---|
| Otros nombres | Hipertensión intracraneal benigna (BIH), [1] pseudotumor cerebral (PTC) [2] |
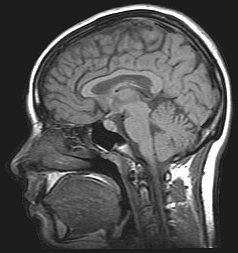 | |
| Para el diagnóstico, se deben realizar escáneres cerebrales (como una resonancia magnética) para descartar otras causas potenciales | |
| Especialidad | Neurología |
| Síntomas | Dolor de cabeza , problemas de visión, zumbido en los oídos con los latidos del corazón [1] [2] |
| Complicaciones | Pérdida de visión [2] |
| Inicio habitual | 20 a 50 años [2] |
| Factores de riesgo | Sobrepeso, tetraciclina [1] [2] |
| Método de diagnóstico | Según los síntomas, punción lumbar , imágenes cerebrales [1] [2] |
| Diagnóstico diferencial | Tumor cerebral , aracnoiditis , meningitis [3] |
| Tratamiento | Dieta saludable, restricción de sal, ejercicio, cirugía [2] |
| Medicamento | Acetazolamida [2] |
| Pronóstico | Variable [2] |
| Frecuencia | 2 por 100.000 por año [4] |
La hipertensión intracraneal idiopática ( HII ), anteriormente conocida como pseudotumor cerebral e hipertensión intracraneal benigna , es una afección caracterizada por un aumento de la presión intracraneal (presión alrededor del cerebro) sin una causa detectable. [2] Los síntomas principales son dolor de cabeza , problemas de visión, zumbido en los oídos con los latidos del corazón y dolor de hombro. [1] [2] Las complicaciones pueden incluir pérdida de la visión . [2]
Los factores de riesgo incluyen el sobrepeso o un reciente aumento de peso. [1] La tetraciclina también puede desencadenar la afección. [2] El diagnóstico se basa en los síntomas y una presión intracraneal alta que se encuentra durante una punción lumbar sin una causa específica encontrada en un escáner cerebral . [1] [2]
El tratamiento incluye una dieta saludable, restricción de sal y ejercicio. [2] La cirugía bariátrica también se puede utilizar para ayudar con la pérdida de peso. [2] El medicamento acetazolamida también se puede usar junto con las medidas anteriores. [2] Un pequeño porcentaje de personas puede requerir cirugía para aliviar la presión. [2]
Aproximadamente 2 de cada 100.000 personas se ven afectadas por año. [4] La afección afecta con mayor frecuencia a mujeres de 20 a 50 años. [2] Las mujeres se ven afectadas 20 veces más a menudo que los hombres. [2] La condición se describió por primera vez en 1897. [1]
Signos y síntomas [ editar ]
El síntoma más común de IIH es la cefalea, que se presenta en casi todos los casos (92 a 94%). Es característicamente peor por la mañana, de carácter generalizado y de naturaleza palpitante. Puede estar asociado con náuseas y vómitos. El dolor de cabeza puede empeorar con cualquier actividad que aumente aún más la presión intracraneal , como toser y estornudar . El dolor también se puede experimentar en el cuello y los hombros. [5] Muchos tienen tinnitus pulsátil , una sensación de silbido en uno o ambos oídos (64 a 87%); este sonido está sincronizado con el pulso. [5] [6] Varios otros síntomas, como entumecimiento de las extremidades, debilidad generalizada, pérdida del olfato ypérdida de coordinación , se informan más raramente; ninguno es específico para IIH. [5] En los niños, pueden presentarse numerosos signos y síntomas inespecíficos. [7]
El aumento de presión conduce a la compresión y tracción de los nervios craneales , un grupo de nervios que surgen del tronco del encéfalo y que irrigan la cara y el cuello. Más comúnmente, el nervio abducens (sexto nervio) está involucrado. Este nervio inerva el músculo que tira del ojo hacia afuera. Aquellos con parálisis del VI par craneal, por tanto, experimentan visión doble horizontal, que empeora cuando se mira hacia el lado afectado. Más raramente, el nervio oculomotor y el nervio troclear ( parálisis del tercer y cuarto par , respectivamente) se ven afectados; ambos juegan un papel en los movimientos oculares. [7] [8] El nervio facial(séptimo par craneal) se ve afectado ocasionalmente - el resultado es una debilidad total o parcial de los músculos de la expresión facial en uno o ambos lados de la cara. [5]
El aumento de presión conduce a papiledema , que es la hinchazón del disco óptico , el lugar donde el nervio óptico entra en el globo ocular . Esto ocurre en prácticamente todos los casos de HII, pero no todo el mundo experimenta síntomas de esto. Aquellos que experimentan síntomas típicamente informan "oscurecimientos visuales transitorios", episodios de dificultad para ver que ocurren en ambos ojos pero no necesariamente al mismo tiempo. El edema de papila no tratado a largo plazo conduce a una pérdida visual, inicialmente en la periferia pero progresivamente hacia el centro de la visión. [5] [9]
El examen físico del sistema nervioso suele ser normal, aparte de la presencia de edema de papila, que se observa al examinar el ojo con un pequeño dispositivo llamado oftalmoscopio o, con más detalle, con una cámara de fondo de ojo . Si hay anomalías de los pares craneales, estas pueden notarse en el examen ocular en forma de estrabismo (parálisis del tercer, cuarto o sexto par craneal) o como parálisis del nervio facial. Si el edema de papila ha sido de larga duración, los campos visuales pueden estar restringidos y la agudeza visual puede estar disminuida. Pruebas de campo visual automatizadas ( Humphrey) Se recomienda la perimetría ya que otros métodos de prueba pueden ser menos precisos. El papiledema de larga duración conduce a la atrofia óptica , en la que el disco se ve pálido y la pérdida visual tiende a ser avanzada. [5] [9]
Causas [ editar ]
"Idiopático" significa de causa desconocida. Por lo tanto, la HII solo se puede diagnosticar si no existe una explicación alternativa para los síntomas. La presión intracraneal puede aumentar debido a medicamentos como derivados de la vitamina A en dosis altas (p. Ej., Isotretinoína para el acné ), antibióticos de tetraciclina a largo plazo (para una variedad de afecciones de la piel) y anticonceptivos hormonales .
Existen muchas otras enfermedades, en su mayoría afecciones raras, que pueden provocar hipertensión intracraneal. Si hay una causa subyacente, la afección se denomina "hipertensión intracraneal secundaria". [5] Las causas comunes de hipertensión intracraneal secundaria incluyen apnea obstructiva del sueño (un trastorno respiratorio relacionado con el sueño), lupus eritematoso sistémico (LES), enfermedad renal crónica y enfermedad de Behçet . [9]
Mecanismo [ editar ]
Se desconoce la causa de la HII. La regla de Monro-Kellie establece que la presión intracraneal está determinada por la cantidad de tejido cerebral, líquido cefalorraquídeo (LCR) y sangre dentro de la bóveda craneal ósea. Por lo tanto, existen tres teorías sobre por qué la presión podría aumentar en IIH: un exceso de producción de LCR, aumento del volumen de sangre o tejido cerebral u obstrucción de las venas que drenan sangre del cerebro . [5]
La primera teoría, la del aumento de la producción de líquido cefalorraquídeo, se propuso en las primeras descripciones de la enfermedad. Sin embargo, no hay datos experimentales que apoyen un papel para este proceso en IIH. [5]
La segunda teoría postula que el aumento del flujo sanguíneo al cerebro o el aumento del tejido cerebral en sí pueden provocar un aumento de la presión. Se ha acumulado poca evidencia para apoyar la sugerencia de que el aumento del flujo sanguíneo juega un papel, pero recientemente Bateman et al. en los estudios de ARM de contraste de fase han cuantificado el flujo sanguíneo cerebral (FSC) in vivo y sugieren que el FSC está anormalmente elevado en muchas personas con IIH. Tanto las muestras de biopsia como varios tipos de escáneres cerebrales han mostrado un mayor contenido de agua en el tejido cerebral. No está claro por qué podría ser así. [5]
La tercera teoría sugiere que el drenaje venoso restringido del cerebro puede verse afectado y provocar congestión. Muchas personas con HII tienen un estrechamiento de los senos transversales . [10] No está claro si este estrechamiento es la patogenia de la enfermedad o un fenómeno secundario. Se ha propuesto que puede existir un bucle de biorretroalimentación positiva, donde la PIC elevada ( presión intracraneal ) provoca un estrechamiento venoso en los senos transversales , lo que da como resultado hipertensión venosa (presión venosa elevada), disminución de la resorción de LCR a través de la granulación aracnoidea y un aumento adicional de la PIC. [11]
Diagnóstico [ editar ]
El diagnóstico puede sospecharse sobre la base de la historia y el examen. Para confirmar el diagnóstico, además de excluir causas alternativas, se requieren varias investigaciones; Se pueden realizar más investigaciones si la historia no es típica o si es más probable que la persona tenga un problema alternativo: niños, hombres, ancianos o mujeres que no tienen sobrepeso. [8]
Investigaciones [ editar ]
La neuroimagen , generalmente con tomografía computarizada (CT / CAT) o imagen por resonancia magnética (MRI), se usa para excluir cualquier lesión de masa. En la IIH, estas exploraciones suelen parecer normales, aunque los ventrículos son pequeños o en forma de hendidura , la dilatación y el pandeo [13] de las vainas del nervio óptico y el " signo de la silla turca vacía " (aplanamiento de la glándula pituitaria debido al aumento de la presión) y agrandamiento de la enfermedad de Meckel. se pueden ver cuevas.
En la mayoría de los casos, también se realiza un venograma por resonancia magnética para excluir la posibilidad de estenosis / obstrucción del seno venoso o trombosis del seno venoso cerebral . [5] [7] [8] Una exploración MRV con contraste (ATECO) tiene una alta tasa de detección de estenosis de los senos transversales anormales. [10] Estas estenosis pueden identificarse y evaluarse de manera más adecuada con una venografía cerebral y una manometría con catéter. [11] El pandeo de los nervios ópticos bilaterales con aumento de líquido perineural también se observa a menudo en las imágenes de resonancia magnética.
La punción lumbar se realiza para medir la presión de apertura, así como para obtener líquido cefalorraquídeo (LCR) para excluir diagnósticos alternativos. Si se aumenta la presión de apertura, se puede extraer LCR para un alivio transitorio (ver más abajo). [8] El LCR se examina en busca de células anormales, infecciones, niveles de anticuerpos, nivel de glucosa y niveles de proteínas . Por definición, todos estos están dentro de sus límites normales en IIH. [8]Ocasionalmente, la medición de la presión del LCR puede ser normal a pesar de síntomas muy sugerentes. Esto puede atribuirse al hecho de que la presión del LCR puede fluctuar en el transcurso del día normal. Si la sospecha de problemas sigue siendo alta, puede ser necesario realizar una monitorización más prolongada de la PIC mediante un catéter de presión. [8]
Clasificación [ editar ]
Los criterios originales para IIH fueron descritos por Dandy en 1937. [14]
| 1 Signos y síntomas de aumento de la PIC: presión del LCR> 25 cmH 2 O |
| 2 Sin signos de localización a excepción de la parálisis del nervio abducens |
| 3 Composición normal del LCR |
| 4 Ventrículos normales a pequeños (hendiduras) en las imágenes sin masa intracraneal |
Fueron modificados por Smith en 1985 para convertirse en los "criterios Dandy modificados". Smith incluyó el uso de imágenes más avanzadas: Dandy había requerido ventriculografía , pero Smith reemplazó esto con tomografía computarizada . [15] En un artículo de 2001, Digre y Corbett enmendaron aún más los criterios de Dandy. Agregaron el requisito de que la persona esté despierta y alerta, ya que el coma impide una evaluación neurológica adecuada y requiere la exclusión de la trombosis del seno venoso como causa subyacente. Además, agregaron el requisito de que no se encuentre ninguna otra causa para el aumento de la PIC. [5] [9] [16]
| 1 Síntomas de presión intracraneal elevada (dolor de cabeza, náuseas, vómitos, oscurecimientos visuales transitorios o papiledema) |
| 2 Sin signos de localización a excepción de la parálisis del nervio abducens (sexto) |
| 3 El paciente está despierto y alerta. |
| 4 Hallazgos normales de CT / MRI sin evidencia de trombosis |
| 5 LP presión de apertura de> 25 cmH 2 O y composición bioquímica y citológica normal del LCR |
| 6 No hay otra explicación para la presión intracraneal elevada |
En una revisión de 2002, Friedman y Jacobson proponen un conjunto alternativo de criterios, derivados del de Smith. Éstos requieren la ausencia de síntomas que no podrían explicarse con un diagnóstico de IIH, pero no requieren la presencia real de ningún síntoma (como dolor de cabeza) atribuible a IIH. Estos criterios también requieren que la punción lumbar se realice con la persona acostada de lado, ya que una punción lumbar realizada en posición sentada erguida puede conducir a mediciones de presión artificialmente altas. Friedman y Jacobson tampoco insisten en la venografía por RM para todas las personas; más bien, esto solo es necesario en casos atípicos (ver "diagnóstico" más arriba). [8]
Tratamiento [ editar ]
El objetivo principal del tratamiento de la HII es la prevención de la pérdida visual y la ceguera, así como el control de los síntomas. [9] La HII se trata principalmente mediante la reducción de la presión del LCR y. La HII puede resolverse después del tratamiento inicial, puede entrar en remisión espontánea (aunque aún puede recaer en una etapa posterior) o puede continuar de forma crónica. [5] [8]
Punción lumbar [ editar ]
El primer paso en el control de los síntomas es el drenaje del líquido cefalorraquídeo mediante punción lumbar. Si es necesario, esto se puede realizar al mismo tiempo que un LP de diagnóstico (como en la búsqueda de una infección de LCR). En algunos casos, esto es suficiente para controlar los síntomas y no se necesita ningún tratamiento adicional. [7] [9]
El procedimiento se puede repetir si es necesario, pero esto generalmente se toma como una pista de que pueden ser necesarios tratamientos adicionales para controlar los síntomas y preservar la visión. Las personas consideran que las punciones lumbares repetidas son desagradables y presentan el peligro de introducir infecciones de la columna si se realizan con demasiada frecuencia. [5] [7] A veces se necesitan punciones lumbares repetidas para controlar la PIC con urgencia si la visión de la persona se deteriora rápidamente. [9]
Medicación [ editar ]
El tratamiento médico mejor estudiado para la hipertensión intracraneal es la acetazolamida (Diamox), que actúa inhibiendo la enzima anhidrasa carbónica y reduce la producción de LCR entre un seis y un 57 por ciento. Puede causar los síntomas de hipopotasemia (niveles bajos de potasio en sangre), que incluyen debilidad muscular y hormigueo en los dedos. La acetazolamida no puede usarse durante el embarazo, ya que se ha demostrado que causa anomalías embrionarias en estudios con animales. Además, en los seres humanos se ha demostrado que causa acidosis metabólica y alteraciones en los niveles de electrolitos en sangre de los recién nacidos. El diurético furosemidaa veces se usa para un tratamiento si no se tolera la acetazolamida, pero este medicamento a veces tiene poco efecto sobre la PIC. [5] [9]
Se pueden usar varios analgésicos (analgésicos) para controlar los dolores de cabeza de la hipertensión intracraneal. Además de los agentes convencionales como el paracetamol , una dosis baja del antidepresivo amitriptilina o el anticonvulsivo topiramato han mostrado algún beneficio adicional para el alivio del dolor. [9]
El uso de esteroides en el intento de reducir la PIC es controvertido. Estos pueden usarse en papiledema severo, pero por lo demás se desaconseja su uso. [5]
Colocación de un stent en el seno venoso [ editar ]
Las estenosis de los senos venosos que conducen a la hipertensión venosa parecen desempeñar un papel importante en relación con el aumento de la PIC , y la colocación de un stent en un seno transverso puede resolver la hipertensión venosa, lo que conduce a una mejor reabsorción de LCR , disminución de la PIC, curación del papiledema y otros síntomas de la HII. [11]
Un stent de metal autoexpandible se despliega permanentemente dentro del seno transversal dominante a través de la estenosis bajo anestesia general. En general, las personas son dadas de alta al día siguiente. Las personas requieren terapia antiplaquetaria doble por un período de hasta 3 meses después del procedimiento y terapia con aspirina por hasta 1 año.
En un análisis sistemático de 19 estudios con 207 casos, hubo una mejora del 87% en la tasa general de síntomas y una tasa de curación del 90% para el tratamiento del papiledema. Las complicaciones mayores solo ocurrieron en 3/207 personas (1,4%). [17] En la serie más grande de colocación de endoprótesis en el seno transverso, hubo una tasa de recurrencia de 11% después de una endoprótesis, que requirió la colocación de más endoprótesis. [11]
Debido a la permanencia del stent y al riesgo pequeño pero definido de complicaciones, la mayoría de los expertos recomendarán que la persona con HII debe tener edema de papila y haber fallado el tratamiento médico o ser intolerante a la medicación antes de emprender la colocación del stent.
Cirugía [ editar ]
Existen dos procedimientos quirúrgicos principales en el tratamiento de la HII: descompresión de la vaina del nervio óptico y fenestración y derivación . Normalmente, la cirugía solo se ofrecería si la terapia médica no tiene éxito o no se tolera. [7] [9] La elección entre estos dos procedimientos depende del problema predominante en IIH. Ninguno de los procedimientos es perfecto: ambos pueden causar complicaciones importantes y, eventualmente, ambos pueden fallar en el control de los síntomas. No existen ensayos controlados aleatorios para orientar la decisión sobre qué procedimiento es mejor. [9]
La fenestración de la vaina del nervio óptico es una operación que implica la realización de una incisión en el revestimiento del tejido conectivo del nervio óptico en su parte detrás del ojo. No está del todo claro cómo protege el ojo de la presión elevada, pero puede ser el resultado de la desviación del LCR hacia la órbita o la creación de un área de tejido cicatricial que reduce la presión. [9] Los efectos sobre la presión intracraneal en sí son más modestos. Además, el procedimiento puede dar lugar a complicaciones importantes, incluida la ceguera en el 1-2%. [5]Por lo tanto, el procedimiento se recomienda principalmente en aquellos que tienen síntomas limitados de dolor de cabeza pero edema de papila significativo o visión amenazada, o en aquellos que han sido sometidos a un tratamiento infructuoso con una derivación o tienen una contraindicación para la cirugía de derivación. [9]
La cirugía de derivación, generalmente realizada por neurocirujanos , implica la creación de un conducto por el cual el líquido cefalorraquídeo puede drenarse hacia otra cavidad corporal. El procedimiento inicial suele ser una derivación lumboperitoneal (LP) , que conecta el espacio subaracnoideo de la columna lumbar con la cavidad peritoneal . [18] Generalmente, se incluye una válvula de presión en el circuito para evitar un drenaje excesivo cuando la persona está erecta. La derivación LP proporciona alivio a largo plazo en aproximadamente la mitad de los casos; otros requieren la revisión de la derivación, a menudo en más de una ocasión, generalmente debido a una obstrucción de la derivación. Si la derivación lumboperitoneal necesita revisiones repetidas, una derivación ventriculoauricular o ventriculoperitonealpuede ser considerado. Estas derivaciones se insertan en uno de los ventrículos laterales del cerebro, generalmente mediante cirugía estereotáctica , y luego se conectan a la aurícula derecha del corazón o la cavidad peritoneal, respectivamente. [5] [9] Dada la menor necesidad de revisiones en las derivaciones ventriculares, es posible que este procedimiento se convierta en el tipo de tratamiento de derivación de primera línea. [5]
Se ha demostrado que en personas obesas, la cirugía bariátrica (y especialmente la cirugía de bypass gástrico ) puede llevar a la resolución de la afección en más del 95%. [5]
Pronóstico [ editar ]
No se sabe qué porcentaje de personas con IIH remitirán espontáneamente y qué porcentaje desarrollará una enfermedad crónica. [9]
La IIH normalmente no afecta la esperanza de vida. Las principales complicaciones de la HII surgen del papiledema no tratado o resistente al tratamiento . En varias series de casos, se informa que el riesgo a largo plazo de que la visión se vea afectada significativamente por la IIH se encuentra entre el 10 y el 25%. [5] [9]
Epidemiología [ editar ]
En promedio, la IIH ocurre en aproximadamente una de cada 100,000 personas y puede ocurrir en niños y adultos. La mediana de edad en el momento del diagnóstico es de 30 años. La HII se presenta predominantemente en mujeres, especialmente en las edades de 20 a 45, que tienen de cuatro a ocho veces más probabilidades de verse afectadas que los hombres. El sobrepeso y la obesidad predisponen fuertemente a una persona a la HII: las mujeres que están más del diez por ciento por encima de su peso corporal ideal tienen trece veces más probabilidades de desarrollar HII, y esta cifra aumenta hasta diecinueve veces en las mujeres que están más del veinte por ciento por encima de su peso ideal. peso corporal. En los hombres también existe esta relación, pero el aumento es solo de cinco veces en aquellos que superan en un 20 por ciento su peso corporal ideal. [5]
A pesar de varios informes de IIH en familias, no existe una causa genética conocida para IIH. Las personas de todas las etnias pueden desarrollar IIH. [5] En los niños, no hay diferencia en la incidencia entre hombres y mujeres. [7]
A partir de las bases de datos nacionales de ingresos hospitalarios, parece que la necesidad de intervención neuroquirúrgica para la HII ha aumentado notablemente durante el período comprendido entre 1988 y 2002. Esto se ha atribuido, al menos en parte, al aumento de la prevalencia de la obesidad, [19] aunque parte de este aumento puede explicarse por la creciente popularidad de la derivación sobre la fenestración de la vaina del nervio óptico. [9]
Historia [ editar ]
El primer informe de IIH fue del médico alemán Heinrich Quincke , quien lo describió en 1893 con el nombre de meningitis serosa. [20] El término "pseudotumor cerebral" fue introducido en 1904 por su compatriota Max Nonne . [21] Posteriormente, aparecieron numerosos otros casos en la literatura; en muchos casos, el aumento de la presión intracraneal puede ser el resultado de afecciones subyacentes. [22] Por ejemplo, la hidrocefalia otítica informada por el neurólogo londinense Sir Charles Symonds puede haber sido el resultado de una trombosis del seno venoso causada por una infección del oído medio . [22] [23]Los criterios de diagnóstico para HII fueron desarrollados en 1937 por el neurocirujano de Baltimore Walter Dandy ; Dandy también introdujo la cirugía descompresiva subtemporal en el tratamiento de la afección. [14] [22]
Los términos "benigno" y "pseudotumor" se derivan del hecho de que el aumento de la presión intracraneal puede estar asociado con tumores cerebrales . Por tanto, a las personas en las que no se encontró tumor se les diagnosticó "pseudotumor cerebri" (una enfermedad que imita un tumor cerebral). La enfermedad pasó a llamarse hipertensión intracraneal benigna en 1955 para distinguirla de la hipertensión intracraneal debida a enfermedades potencialmente mortales (como el cáncer); [24] sin embargo, esto también se consideró engañoso porque cualquier enfermedad que pueda cegar a una persona no debe considerarse benigna, por lo que el nombre se modificó en 1989 a "hipertensión intracraneal idiopática (sin causa identificable)". [25] [26]
La cirugía de derivación se introdujo en 1949; inicialmente se utilizaron derivaciones ventriculoperitoneales. En 1971, se informaron buenos resultados con la derivación lumboperitoneal. Los informes negativos sobre la derivación en la década de 1980 llevaron a un breve período (1988-1993) durante el cual la fenestración del nervio óptico (que inicialmente se había descrito en una condición no relacionada en 1871) fue más popular. Desde entonces, la derivación se recomienda predominantemente, con excepciones ocasionales. [5] [9]
Referencias [ editar ]
- ↑ a b c d e f g h Wall, M (febrero de 2017). "Actualización sobre hipertensión intracraneal idiopática" . Clínicas neurológicas . 35 (1): 45–57. doi : 10.1016 / j.ncl.2016.08.004 . PMC 5125521 . PMID 27886895 .
- ^ a b c d e f g h i j k l m n o p q r s t "Hipertensión intracraneal idiopática" . Instituto Nacional del Ojo . Abril de 2014 . Consultado el 8 de noviembre de 2017 .
- ^ "Hipertensión intracraneal idiopática" . NORD (Organización Nacional de Enfermedades Raras) . 2015 . Consultado el 8 de noviembre de 2017 .
- ^ a b Wakerley, BR; Tan, MH; Ting, EY (marzo de 2015). "Hipertensión intracraneal idiopática". Cephalalgia: An International Journal of Headache . 35 (3): 248–61. doi : 10.1177 / 0333102414534329 . PMID 24847166 . S2CID 28592337 .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y Binder DK, Horton JC, Lawton MT, McDermott MW (marzo de 2004). "Hipertensión intracraneal idiopática". Neurocirugía . 54 (3): 538–51, discusión 551–2. doi : 10.1227 / 01.NEU.0000109042.87246.3C . PMID 15028127 . S2CID 297003 .
- ^ Sismanis A (julio de 1998). "Acúfenos pulsátiles. Una experiencia de 15 años". Revista estadounidense de otología . 19 (4): 472–7. PMID 9661757 .
- ↑ a b c d e f g Soler D, Cox T, Bullock P, Calver DM, Robinson RO (enero de 1998). "Diagnóstico y tratamiento de la hipertensión intracraneal benigna" . Archivos de enfermedades en la infancia . 78 (1): 89–94. doi : 10.1136 / adc.78.1.89 . PMC 1717437 . PMID 9534686 .
- ↑ a b c d e f g h Friedman DI, Jacobson DM (2002). "Criterios diagnósticos de hipertensión intracraneal idiopática". Neurología . 59 (10): 1492-1495. doi : 10.1212 / 01.wnl.0000029570.69134.1b . PMID 12455560 . S2CID 21999073 .
- ^ a b c d e f g h i j k l m n o p q r Acheson JF (2006). "Hipertensión intracraneal idiopática y función visual" . Boletín médico británico . 79–80 (1): 233–44. CiteSeerX 10.1.1.131.9802 . doi : 10.1093 / bmb / ldl019 . PMID 17242038 .
- ^ a b Farb, RI; Vanek, yo; Scott, JN; Mikulis, DJ; Willinsky, RA; Tomlinson, G; terBrugge, KG (13 de mayo de 2003). "Hipertensión intracraneal idiopática: la prevalencia y morfología de la estenosis sinovenosa". Neurología . 60 (9): 1418–24. doi : 10.1212 / 01.wnl.0000066683.34093.e2 . PMID 12743224 . S2CID 34459740 .
- ^ a b c d Ahmed, RM; Wilkinson, M; Parker, GD; Thurtell, MJ; Macdonald, J; McCluskey, PJ; Allan, R; Dunne, V; Hanlon, M; Owler, BK; Halmagyi, GM (septiembre de 2011). "Colocación de stent de seno transversal para hipertensión intracraneal idiopática: una revisión de 52 pacientes y de las predicciones del modelo" . AJNR. Revista estadounidense de neurorradiología . 32 (8): 1408-14. doi : 10.3174 / ajnr.a2575 . PMC 7964366 . PMID 21799038 .
- ^ "UOTW # 5 - Ultrasonido de la semana" . Ecografía de la semana . 17 de junio de 2014 . Consultado el 27 de mayo de 2017 .
- ^ Peter P, Philip N, Singh Y (2012). "Reversión de hallazgos de resonancia magnética después de drenaje de LCR en hipertensión intracraneal idiopática". Neurol India . 60 (2): 267–8. doi : 10.4103 / 0028-3886.96440 . PMID 22626730 .
- ^ a b c Dandy WE (octubre de 1937). "Presión intracraneal sin tumor cerebral - diagnóstico y tratamiento" . Annals of Surgery . 106 (4): 492–513. doi : 10.1097 / 00000658-193710000-00002 . PMC 1390605 . PMID 17857053 .
- ^ Smith JL (1985). "¿De dónde proviene el pseudotumor cerebri?". Revista de neurooftalmología clínica . 5 (1): 55–6. PMID 3156890 .
- ↑ a b Digre KB, Corbett JJ (2001). "Hipertensión intracraneal idiopática (pseudotumor cerebri): una reevaluación". Neurólogo . 7 : 2-67. doi : 10.1097 / 00127893-200107010-00002 .
- ^ Teleb, MS; Cziep, ME; Lazzaro, MA; Gheith, A; Asif, K; Remler, B; Zaidat, OO (2013). "Hipertensión intracraneal idiopática. Un análisis sistemático de la implantación de stents en el seno transverso" . Neurología intervencionista . 2 (3): 132–143. doi : 10.1159 / 000357503 . PMC 4080637 . PMID 24999351 .
- ^ Yadav, YadR; Parihar, Vijay; Sinha, Mallika (1 de enero de 2010). "Derivación peritoneal lumbar". Neurology India . 58 (2): 179–84. doi : 10.4103 / 0028-3886.63778 . PMID 20508332 .
- ^ Curry WT, Butler WE, Barker FG (2005). "Incidencia en rápido aumento de procedimientos de derivación de líquido cefalorraquídeo para la hipertensión intracraneal idiopática en los Estados Unidos, 1988-2002". Neurocirugía . 57 (1): 97–108, discusión 97–108. doi : 10.1227 / 01.NEU.0000163094.23923.E5 . PMID 15987545 . S2CID 38715388 .
- ↑ Quincke HI (1893). "Meningitis serosa". Sammlung Klinischer Vorträge . 67 : 655.
- ^ Nonne M (1904). "Ueber Falle vom Symptomkomplex" Tumor Cerebri "mit Ausgang en Heilung (Pseudotumor Cerebri)". Deutsche Zeitschrift für Nervenheilkunde (en alemán). 27 (3–4): 169–216. doi : 10.1007 / BF01667111 . S2CID 31708166 .
- ↑ a b c Johnston I (2001). "El desarrollo histórico del concepto de pseudotumor" . Enfoque neuroquirúrgico . 11 (2): 1–9. doi : 10.3171 / foc.2001.11.2.3 . PMID 16602675 .
- ^ Symonds CP (1931). "Hidrocefalia otítica" . Cerebro . 54 : 55–71. doi : 10.1093 / cerebro / 54.1.55 .También impreso en Symonds CP (enero de 1932). "Hidrocefalia otítica" . Br Med J . 1 (3705): 53–4. doi : 10.1136 / bmj.1.3705.53 . PMC 2519971 . PMID 20776602 .
- ^ Foley J (1955). "Formas benignas de hipertensión intracraneal; hidrocefalia tóxica y otítica". Cerebro . 78 (1): 1–41. doi : 10.1093 / cerebro / 78.1.1 . PMID 14378448 .
- ^ Corbett JJ, Thompson HS (octubre de 1989). "El manejo racional de la hipertensión intracraneal idiopática". Archivos de Neurología . 46 (10): 1049–51. doi : 10.1001 / archneur.1989.00520460025008 . PMID 2679506 .
- ^ Bandyopadhyay S (2001). "Pseudotumor cerebri". Archivos de Neurología . 58 (10): 1699–701. doi : 10.1001 / archneur.58.10.1699 . PMID 11594936 .
Enlaces externos [ editar ]
| Clasificación | D
|
|---|---|
| Recursos externos |
|
- Hipertensión intracraneal idiopática en Curlie