 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC (2 R , 3 S ) -2- (3,4-Dihidroxifenil) -3,4-dihidro- 2H -cromeno-3,5,7-triol | |
| Otros nombres Cianidanol Cianidanol (+) - catequina D-Catequina Ácido catequínico Ácido catechuico Cianidol Dexcianidanol (2 R , 3 S ) -Catequina 2,3- trans -Catequina (2 R , 3 S ) -Flavan-3,3 ′, 4 ′, 5,7-pentol | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| 3DMet | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Número CE |
|
| KEGG | |
PubChem CID | |
| UNII |
|
| |
| |
| Propiedades | |
| C 15 H 14 O 6 | |
| Masa molar | 290,271 g · mol −1 |
| Apariencia | Sólido incoloro |
| Punto de fusion | 175 a 177 ° C (347 a 351 ° F; 448 a 450 K) |
| UV-vis (λ máx. ) | 276 nanómetro |
Rotación quiral ([α] D ) | + 14,0 ° |
| Peligros | |
| Principales peligros | Mutagénico para células somáticas de mamíferos, mutagénico para bacterias y levaduras |
| Ficha de datos de seguridad | Sciencelab AppliChem [ enlace muerto permanente ] |
| Pictogramas GHS |  |
| Palabra de señal GHS | Advertencia |
| H315 , H319 , H335 | |
| P261 , P264 , P271 , P280 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis mediana ) | (+) - catequina: 10,000 mg / kg en rata (RTECS) 10,000 mg / kg en ratón 3,890 mg / kg en rata (otra fuente) |
| Farmacología | |
| Oral | |
| Farmacocinética : | |
| Orinas | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
La catequina / k æ t ɪ tʃ ɪ n / es un flavan-3-ol , un tipo de fenol natural y antioxidante . Es un metabolito secundario vegetal . Pertenece al grupo de los flavan-3-oles (o simplemente flavonoides ), parte de la familia química de los flavonoides .
El nombre de la familia química de las catequinas deriva de catechu , que es el jugo tánico o extracto hervido de Mimosa catechu ( Acacia catechu Lf). [1]
Química [ editar ]
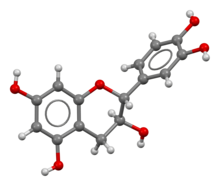
La catequina posee dos anillos de benceno (llamados anillos A y B) y un heterociclo de dihidropirano (el anillo C) con un grupo hidroxilo en el carbono 3. El anillo A es similar a un resto de resorcinol mientras que el anillo B es similar a un resto de catecol . Hay dos centros quirales en la molécula de los carbonos 2 y 3. Por lo tanto, tiene cuatro diastereoisómeros . Dos de los isómeros están en configuración trans y se denominan catequina y los otros dos están en configuración cis y se denominan epicatequina .
El isómero de catequina más común es la (+) - catequina. El otro estereoisómero es (-) - catequina o ent -catequina. El isómero de epicatequina más común es (-) - epicatequina (también conocida con los nombres de L-epicatequina, epicatequina, (-) - epicatequina, l-acacatequina, l-epicatequina, epi-catequina, 2,3-cis-epicatequina o ( 2 R , 3 R ) - (-) - epicatequina).
Los diferentes epímeros se pueden distinguir usando cromatografía en columna quiral . [2]
Haciendo referencia a ningún isómero en particular, la molécula puede llamarse simplemente catequina. Las mezclas de los diferentes enantiómeros se pueden llamar (+/-) - catequina o DL-catequina y (+/-) - epicatequina o DL-epicatequina.
La catequina y la epicatequina son los componentes básicos de las proantocianidinas , un tipo de tanino condensado.
- Galería de diastereoisómeros
(+) - catequina (2 R , 3 S )
(-) - catequina (2 S , 3 R )
(-) - epicatequina (2 R , 3 R )
(+) - epicatequina (2 S , 3 S )
Además, la flexibilidad del anillo C permite dos isómeros de conformación , colocando el anillo B en una posición pseudoecuatorial (conformador E) o en una posición pseudoaxial (conformador A). Los estudios confirmaron que la (+) - catequina adopta una mezcla de conformadores A y E en solución acuosa y su equilibrio conformacional se ha evaluado en 33:67. [3]
Como flavonoides, las catequinas pueden actuar como antioxidantes cuando están en alta concentración in vitro , pero en comparación con otros flavonoides, su potencial antioxidante es bajo. [4] La capacidad para apagar el oxígeno singlete parece estar en relación con la estructura química de la catequina, con la presencia del resto catecol en el anillo B y la presencia de un grupo hidroxilo que activa el doble enlace en el anillo C. [5]
Oxidación [ editar ]
Los experimentos electroquímicos muestran que el mecanismo de oxidación de (+) - catequina procede en pasos secuenciales, relacionados con los grupos catecol y resorcinol y la oxidación depende del pH. La oxidación de los grupos donantes de electrones de catecol 3 ', 4'-dihidroxilo ocurre primero, a potenciales positivos muy bajos, y es una reacción reversible. Se demostró que los grupos hidroxilo del resto de resorcinol oxidado posteriormente experimentan una reacción de oxidación irreversible. [6]
El sistema lacasa / ABTS oxida (+) - catequina a productos oligoméricos [7] de los cuales la proantocianidina A2 es un dímero.
Datos espectrales [ editar ]
| UV-Vis | |
|---|---|
| Lambda-max : | 276 nanómetro |
| Coeficiente de extinción (log ε) | 4.01 |
| IR | |
| Bandas de absorción principales | 1600 cm −1 (anillos de benceno) |
| RMN | |
| RMN de protones
| δ : 2,49 (1H, dd, J = 16,0, 8,6 Hz, H-4a), |
| RMN de carbono 13 | |
| Otros datos de RMN | |
| SRA | |
| Masas de fragmentos principales | IEN-EM [M + H] + m / z: 291,0
|
Acontecimientos naturales [ editar ]
(+) - Catequina y (-) - epicatequina, así como sus conjugados de ácido gálico, son componentes ubicuos de las plantas vasculares y componentes frecuentes de los remedios tradicionales a base de hierbas , como Uncaria rhynchophylla . Los dos isómeros se encuentran principalmente como componentes del cacao y del té , así como en las uvas Vitis vinifera . [9] [10] [11]
En comida [ editar ]
Las principales fuentes dietéticas de catequinas en Europa y Estados Unidos son el té y las frutas de pepita . [12] [13]
Las catequinas y epicatequinas se encuentran en el cacao , [14] que, según una base de datos, tiene el mayor contenido (108 mg / 100 g) de catequinas entre los alimentos analizados, seguido del jugo de ciruela pasa (25 mg / 100 ml) y la vaina de habas (16 mg / 100 g). [15] El aceite de açaí , obtenido del fruto de la palma de açaí ( Euterpe oleracea ), contiene (+) - catequinas (67 mg / kg). [dieciséis]
Las catequinas son diversas entre los alimentos, [15] desde melocotones [17] hasta té verde y vinagre . [15] [18] Las catequinas se encuentran en el grano de cebada, donde son el principal compuesto fenólico responsable de la decoloración de la masa . [19] El sabor asociado con la (+) - catequina o (-) - epicatequina monomérica se describe como ligeramente astringente , pero no amarga. [20]
Metabolismo [ editar ]
Biosíntesis [ editar ]
La biosíntesis de la catequina comienza con una unidad inicial de ma 4-hidroxicinamoil CoA que sufre una extensión de cadena mediante la adición de tres malonil-CoAs a través de una ruta PKSIII. La 4-hidroxicinamoil CoA se biosintetiza a partir de L-fenilalanina a través de la vía Shikimate. La L-fenilalanina se desamina primero por la fenilalanina amoniaco liasa (PAL) formando ácido cinámico que luego se oxida a ácido 4-hidroxicinámico por la cinamato 4-hidroxilasa. La calcona sintasa luego cataliza la condensación de 4-hidroxicinamoil CoA y tres moléculas de malonil-CoA para formar calcona . La chalcona luego se isomeriza a naringenina por la chalcona isomerasa que se oxida aeriodictyol por flavonoide 3'-hidroxilasa y luego oxidado a taxifolina por flavanona 3-hidroxilasa. Luego, la taxifolina se reduce mediante dihidroflavanol 4-reductasa y leucoantocianidina reductasa para producir catequina. La biosíntesis de la catequina se muestra a continuación [21] [22] [23]
La leucocianidina reductasa (LCR) utiliza 2,3-trans-3,4-cis- leucocianidina para producir (+) - catequina y es la primera enzima en la vía específica de las proantocianidinas (PA). Su actividad se ha medido en hojas, flores y semillas de las leguminosas Medicago sativa , Lotus japonicus , Lotus uliginosus , Hedysarum sulfurescens y Robinia pseudoacacia . [24] La enzima también está presente en Vitis vinifera (uva). [25]
Biodegradación [ editar ]
La catequina oxigenasa, una enzima clave en la degradación de la catequina, está presente en hongos y bacterias. [26]
Entre las bacterias, Acinetobacter calcoaceticus puede lograr la degradación de (+) - catequina . La catequina se metaboliza a ácido protocatecuico (PCA) y ácido floroglucinol carboxílico (PGCA). [27] También es degradado por Bradyrhizobium japonicum . El ácido floroglucinol carboxílico se descarboxila más a floroglucinol , que se deshidroxila a resorcinol . El resorcinol se hidroxila a hidroxiquinol . El ácido protocatecuico y el hidroxiquinol experimentan escisión intradiol a través de la protocatecuato 3,4-dioxigenasa yhidroxiquinol 1,2-dioxigenasa para formar β-carboxi cis, ácido cis-mucónico y acetato de maleilo . [28]
Entre los hongos, Chaetomium cupreum puede lograr la degradación de la catequina . [29]
Metabolismo en humanos [ editar ]
Las catequinas se metabolizan al ser absorbidas por el tracto gastrointestinal , en particular el yeyuno , [31] y en el hígado , dando lugar a los denominados metabolitos de epicatequina estructuralmente relacionados (SREM). [32] Las principales vías metabólicas para SREMs son glucuronidación , sulfatación y la metilación de la catecol grupo por la catecol-O-metil , con sólo pequeñas cantidades detectados en plasma. [33] [30] Sin embargo, la mayoría de las catequinas de la dieta son metabolizadas por el microbioma colónico a gamma-valerolactonasy ácidos hipúricos que experimentan una mayor biotransformación , glucuronidación , sulfatación y metilación en el hígado . [33]
La configuración estereoquímica de las catequinas tiene un fuerte impacto en su captación y metabolismo, ya que la captación es más alta para (-) - epicatequina y más baja para (-) - catequina. [34]
Biotransformación [ editar ]
La biotransformación de (+) - catequina en taxifolina mediante una oxidación en dos pasos puede lograrse mediante Burkholderia sp. [35]
(+) - Catequina y (-) - epicatequina son transformadas por el hongo filamentoso endofítico Diaporthe sp. en los derivados de 3,4-cis-dihidroxiflavana, (+) - (2R, 3S, 4S) -3,4,5,7,3 ', 4'-hexahidroxiflavana (leucocianidina) y (-) - (2R, 3R , 4R) -3,4,5,7,3 ', 4'-hexahidroxiflavano , respectivamente, mientras que (-) - catequina y (+) - epicatequina con un grupo 2S-fenilo resistieron la biooxidación. [36]
La leucoantocianidina reductasa (LAR) utiliza (2 R , 3 S ) -catequina, NADP + y H 2 O para producir 2,3-trans-3,4-cis- leucocianidina , NADPH y H + . Su expresión genética se ha estudiado en el desarrollo de bayas de uva y hojas de vid. [37]
Glucósidos [ editar ]
- El (2R, 3S) -catequina-7-O-β-D-glucopiranósido se puede aislar de cebada ( Hordeum vulgare L.) y malta. [38]
- El epigeósido (catequina-3-O-alfa-L-ramnopiranosil- (1-4) -beta-D-glucopiranosil- (1-6) -beta-D-glucopiranósido) se puede aislar de los rizomas de Epigynum auritum . [39]
Investigación [ editar ]
Función vascular [ editar ]
Solo la evidencia limitada de estudios dietéticos indica que las catequinas pueden afectar la vasodilatación dependiente del endotelio, lo que podría contribuir a la regulación normal del flujo sanguíneo en humanos. [41] [42] Las catequinas del té verde pueden mejorar la presión arterial, especialmente cuando la presión arterial sistólica es superior a 130 mmHg. [43] [44]
Debido al extenso metabolismo durante la digestión, se desconoce el destino y la actividad de los metabolitos de las catequinas responsables de este efecto en los vasos sanguíneos, así como el modo de acción real. [33] [45]
La Autoridad Europea de Seguridad Alimentaria estableció que los flavonoides del cacao tienen un efecto sobre la función vascular en adultos sanos al concluir: "Los flavonoides del cacao ayudan a mantener la vasodilatación dependiente del endotelio, lo que contribuye al flujo sanguíneo normal". [46] Para que se produzca tal efecto, el consumo diario de 200 mg de flavonoides de cacao, posiblemente de 2,5 g de cacao en polvo con alto contenido de flavanol o 10 g de chocolate negro con alto contenido de flavanol, debe realizarse dentro de una dieta equilibrada. [46]
Otros datos de estudios de cohortes observacionales no mostraron una asociación consistente entre la ingesta de flavan-3-ol y el riesgo de enfermedades cardiovasculares. [40] Un metaanálisis también indicó que las catequinas del té verde pueden afectar favorablemente el colesterol . [43]
Otro [ editar ]
Un metanálisis limitado mostró que aumentar el consumo de té verde y sus catequinas a siete tazas por día proporcionó una pequeña reducción en el cáncer de próstata . [47] Los métodos de nanopartículas están bajo investigación preliminar como posibles sistemas de administración de catequinas. [48]
Efectos botánicos [ editar ]
Las catequinas liberadas al suelo por algunas plantas pueden dificultar el crecimiento de sus vecinas, una forma de alelopatía . [49] Centaurea maculosa , la mala hierba manchada a menudo estudiada para este comportamiento, libera isómeros de catequina en el suelo a través de sus raíces, potencialmente teniendo efectos como antibiótico o herbicida . Una hipótesis es que provoca una onda de especies reactivas de oxígeno a través de la raíz de la planta objetivo para matar las células de la raíz por apoptosis . [50] La mayoría de las plantas del ecosistema europeo tienen defensas contra la catequina, pero pocas plantas están protegidas contra ella en el ecosistema norteamericano donde Centaurea maculosaes una maleza invasora y descontrolada. [49]
La catequina actúa como un factor inhibidor de infecciones en las hojas de fresa. [51] La epicatequina y la catequina pueden prevenir la enfermedad del fruto del café al inhibir la melanización apresora de Colletotrichum kahawae . [52]
Referencias [ editar ]
- ^ "Origen vegetal cutch y catechu" . Organización de las Naciones Unidas para la Agricultura y la Alimentación. 5 de noviembre de 2011.
- ^ Rinaldo D, Batista JM, Rodrigues J, et al. (Agosto de 2010). "Determinación de diastereómeros de catequinas de las hojas de la especie Byrsonima mediante HPLC-PAD-CD quiral". Quiralidad . 22 (8): 726–33. doi : 10.1002 / chir.20824 . PMID 20143413 .
- ^ Kríz Z, Koca J, Imberty A, Charlot A, Auzély-Velty R (julio de 2003). "Investigación de la complejación de (+) - catequina por β-ciclodextrina mediante una combinación de técnicas de RMN, microcalorimetría y modelado molecular". Org. Biomol. Chem . 1 (14): 2590–5. doi : 10.1039 / B302935M . PMID 12956082 .
- ^ Pietta, PG (2000). "Flavonoides como antioxidantes". Revista de productos naturales . 63 (7): 1035–42. doi : 10.1021 / np9904509 . PMID 10924197 .
- ^ Tournaire C, Croux S, Maurette MT, et al. (Agosto de 1993). "Actividad antioxidante de los flavonoides: eficiencia de la extinción del oxígeno singlete ( 1 Δ g )". J. Photochem. Photobiol. B, Biol . 19 (3): 205–15. doi : 10.1016 / 1011-1344 (93) 87086-3 . PMID 8229463 .
- ↑ Janeiro, Patricia; Oliveira Brett, Ana Maria (2004). "Mecanismos de oxidación electroquímica de catequinas". Analytica Chimica Acta . 518 (1–2): 109-115. doi : 10.1016 / j.aca.2004.05.038 . hdl : 10316/5128 .
- ^ Osman, AM; Wong, KKY; Fernyhough, A. (2007). "El sistema lacasa / ABTS oxida (+) - catequina a productos oligoméricos". Tecnología enzimática y microbiana . 40 (5): 1272-1279. doi : 10.1016 / j.enzmictec.2006.09.018 .
- ^ Lin, Yi-Pei; Chen, Tai-Yuan; Tseng, Hsiang-Wen; Lee, Mei-Hsien; Chen, Shui-Tein (2009). "Compuestos protectores de células neuronales aislados de Phoenix hanceana var. Formosana". Fitoquímica . 70 (9): 1173–81. doi : 10.1016 / j.phytochem.2009.06.006 . PMID 19628235 .
- ^ Aizpurua-Olaizola, Oier; Ormazabal, Markel; Vallejo, Asier; Olivares, Maitane; Navarro, Patricia; Etxebarria, Nestor; Usobiaga, Aresatz (1 de enero de 2015). "Optimización de extracciones consecutivas de fluidos supercríticos de ácidos grasos y polifenoles de residuos de uva Vitis vinifera". Revista de ciencia de los alimentos . 80 (1): E101 – E107. doi : 10.1111 / 1750-3841.12715 . ISSN 1750-3841 . PMID 25471637 .
- ^ Freudenberg, Karl; Cox, Richard FB; Braun, Emil (1932). "La catequina del grano de cacao1". Revista de la Sociedad Química Estadounidense . 54 (5): 1913-1917. doi : 10.1021 / ja01344a026 .
- ^ "Michiyo Tsujimura (1888-1969)" . Consultado el 10 de noviembre de 2015 .
- ^ Chun, está bien; Chung, SJ; Song, WO (2007). "Ingesta estimada de flavonoides en la dieta y principales fuentes de alimentos de los adultos estadounidenses" . La Revista de Nutrición . 137 (5): 1244–52. doi : 10.1093 / jn / 137.5.1244 . PMID 17449588 .
- ^ Vogiatzoglou, A; Mulligan, AA; Lentjes, MA; Luben, RN; Spencer, JP; Schroeter, H; Khaw, KT; Kuhnle, GG (2015). "Ingesta de flavonoides en adultos europeos (18 a 64 años)" . PLOS ONE . 10 (5): e0128132. doi : 10.1371 / journal.pone.0128132 . PMC 4444122 . PMID 26010916 .
- ^ Kwik-Uribe C, Bektash RM (2008). "Flavanoles del cacao - medición, biodisponibilidad y bioactividad" (PDF) . Asia Pac J Clin Nutr . 17 (Supl. 1): 280–3. PMID 18296356 .
- ^ a b c "Polifenoles en infusión de té verde" . Phenol-Explorer, v 3.5. 2014 . Consultado el 1 de noviembre de 2014 .
- ^ Pacheco-Palencia LA, Mertens-Talcott S, Talcott ST (junio de 2008). "Composición química, propiedades antioxidantes y estabilidad térmica de un aceite enriquecido con fitoquímicos de Acai (Euterpe oleracea Mart.)". J. Agric. Food Chem . 56 (12): 4631–6. doi : 10.1021 / jf800161u . PMID 18522407 .
- ^ Cheng, Guiwen W .; Crisosto, Carlos H. (1995). "Potencial de pardeamiento, composición fenólica y actividad polifenoloxidasa de extractos tampón de tejido de piel de melocotón y nectarina" (PDF) . Mermelada. Soc. Hort. Sci . 120 (5): 835–838. doi : 10.21273 / JASHS.120.5.835 . Archivado desde el original (PDF) el 14 de mayo de 2014 . Consultado el 26 de febrero de 2012 .
- ^ Gálvez, Miguel Carrero; Barroso, Carmelo García; Pérez-Bustamante, Juan Antonio (1994). "Análisis de compuestos polifenólicos de diferentes muestras de vinagre". Zeitschrift für Lebensmittel-Untersuchung und -Forschung . 199 (1): 29–31. doi : 10.1007 / BF01192948 .
- ^ Quinde-Axtell, Zory; Baik, Byung-Kee (2006). "Compuestos fenólicos de grano de cebada y su implicación en la decoloración de productos alimenticios". J. Agric. Food Chem . 54 (26): 9978–9984. doi : 10.1021 / jf060974w . PMID 17177530 .
- ^ Kielhorn, S; Thorngate Iii, JH (1999). "Sensaciones orales asociadas a los flavan-3-ols (+) - catequina y (-) - epicatequina". Calidad y preferencia alimentaria . 10 (2): 109-116. doi : 10.1016 / S0950-3293 (98) 00049-4 .
- ^ Rani, Arti; Singh, Cachemira; Ahuja, Paramvir S .; Kumar, Sanjay (2012). "Regulación molecular de la biosíntesis de catequinas en té [ Camellia sinensis (L.) O. Kuntze]". Gene . 495 (2): 205–10. doi : 10.1016 / j.gene.2011.12.029 . PMID 22226811 .
- ^ Punyasiri, PAN; Abeysinghe, ISB; Kumar, V .; Treutter, D .; Duy, D .; Gosch, C .; Martens, S .; Forkmann, G .; Fischer, TC (2004). "Biosíntesis de flavonoides en la planta de té Camellia sinensis: propiedades de las enzimas de las rutas prominentes de epicatequina y catequina". Archivos de Bioquímica y Biofísica . 431 (1): 22-30. doi : 10.1016 / j.abb.2004.08.003 . PMID 15464723 .
- ^ Dewick, Paul M. (2009). Productos medicinales naturales: un enfoque biosintético (3ª ed.). Reino Unido: John Wiley & Sons. ISBN 978-0-470-74167-2.[ página necesaria ]
- ^ Skadhauge, Birgitte; Gruber, Margaret Y .; Thomsen, Karl Kristian; Von Wettstein, Diter (abril de 1997). "Actividad de la leucocianidina reductasa y acumulación de proantocianidinas en el desarrollo de tejidos leguminosos". Revista estadounidense de botánica . 84 (4): 494–503. doi : 10.2307 / 2446026 . JSTOR 2446026 .
- ^ Maugé C, Granier T, d'Estaintot BL, et al. (Abril de 2010). "Estructura cristalina y mecanismo catalítico de la leucoantocianidina reductasa de Vitis vinifera". J. Mol. Biol . 397 (4): 1079–91. doi : 10.1016 / j.jmb.2010.02.002 . PMID 20138891 .
- ^ Biodegradación de catequina. M Arunachalam, M Mohan Raj, N Mohan y A Mahadevan, Proc. Indian natn Sci Acad. B69 No. 4 págs. 353–370 (2003) Archivado el 16 de marzo de 2012 en la Wayback Machine.
- ^ Arunachalam, M; Mohan, N; Sugadev, R; Chellappan, P; Mahadevan, A (2003). "Degradación de (+) - catequina por Acinetobacter calcoaceticus MTC 127". Biochimica et Biophysica Acta (BBA) - Temas generales . 1621 (3): 261–265. doi : 10.1016 / S0304-4165 (03) 00077-1 . PMID 12787923 .
- ^ Hopper, Waheeta; Mahadevan, A. (1997). "Degradación de la catequina por Bradyrhizobium japonicum". Biodegradación . 8 (3): 159-165. doi : 10.1023 / A: 1008254812074 .
- ↑ Sambandam, T .; Mahadevan, A. (1993). "Degradación de la catequina y purificación y caracterización parcial de la catequina oxigenasa de Chaetomium cupreum". Revista mundial de microbiología y biotecnología . 9 (1): 37–44. doi : 10.1007 / BF00656513 . PMID 24419836 .
- ^ a b c d Ottaviani, JI; Borges, G; Momma, TY; Spencer, JP; Keen, CL; Crozier, A; Schroeter, H (2016). "El metaboloma de 2- (14) C (-) - epicatequina en humanos: implicaciones para la evaluación de la eficacia, seguridad y mecanismos de acción de los bioactivos polifenólicos" . Informes científicos . 6 : 29034. Bibcode : 2016NatSR ... 629034O . doi : 10.1038 / srep29034 . PMC 4929566 . PMID 27363516 .
- ^ Actis-Goretta, L; Lévèques, A; Rein, M; Teml, A; Schäfer, C; Hofmann, U; Li, H; Schwab, M; Eichelbaum, M; Williamson, G (2013). "Absorción, metabolismo y excreción intestinal de (-) - epicatequina en humanos sanos evaluados mediante una técnica de perfusión intestinal" . Revista estadounidense de nutrición clínica . 98 (4): 924–33. doi : 10.3945 / ajcn.113.065789 . PMID 23864538 .
- ^ Ottaviani, JI; Momma, TY; Kuhnle, GK; Keen, CL; Schroeter, H (2012). "Estructuralmente relacionados (-) - metabolitos de epicatequina en humanos: evaluación utilizando estándares auténticos sintetizados químicamente de novo" . Biología y Medicina de Radicales Libres . 52 (8): 1403–12. doi : 10.1016 / j.freeradbiomed.2011.12.010 . PMID 22240152 .
- ^ a b c "Flavonoides" . Instituto Linus Pauling, Universidad Estatal de Oregon, Corvallis. 2016 . Consultado el 24 de julio de 2016 .
- ^ Ottaviani, JI; Momma, TY; Heiss, C; Kwik-Uribe, C; Schroeter, H; Keen, CL (2011). "La configuración estereoquímica de los flavonoides influye en el nivel y el metabolismo de los flavonoides en humanos y su actividad biológica in vivo". Biología y Medicina de Radicales Libres . 50 (2): 237–44. doi : 10.1016 / j.freeradbiomed.2010.11.005 . PMID 21074608 .
- ^ Matsuda M, Otsuka Y, Jin S, et al. (Febrero de 2008). "Biotransformación de (+) - catequina en taxifolina mediante una oxidación en dos pasos: etapa primaria del metabolismo de (+) - catequina por una nueva bacteria (+) - degradante de catequina, Burkholderia sp. KTC-1, aislada de turba tropical" . Biochem. Biophys. Res. Comun . 366 (2): 414–9. doi : 10.1016 / j.bbrc.2007.11.157 . PMID 18068670 .
- ^ Shibuya H, Agusta A, Ohashi K, Maehara S, Simanjuntak P (julio de 2005). "Biooxidación de (+) - catequina y (-) - epicatequina en derivados 3,4-dihidroxiflavanos por el hongo endofítico Diaporthe sp. Aislado de una planta de té" . Chem. Pharm. Bull . 53 (7): 866–7. doi : 10.1248 / cpb.53.866 . PMID 15997157 .
- ^ Bogs J, Downey MO, Harvey JS, Ashton AR, Tanner GJ, Robinson SP (octubre de 2005). "Síntesis de proantocianidina y expresión de genes que codifican leucoantocianidina reductasa y antocianidina reductasa en el desarrollo de uvas y hojas de vid" . Plant Physiol . 139 (2): 652–63. doi : 10.1104 / pp.105.064238 . JSTOR 4281902 . PMC 1255985 . PMID 16169968 .
- ^ Friedrich, Wolfgang; Galensa, Rudolf (2002). "Identificación de un nuevo glucósido de flavanol de cebada (Hordeum vulgare L.) y malta". Investigación y tecnología alimentaria europea . 214 (5): 388–393. doi : 10.1007 / s00217-002-0498-x .
- ^ Jin QD, Mu QZ (1991). "[Estudio sobre los componentes glucosidales de Epigynum auritum]". Yao Xue Xue Bao (en chino). 26 (11): 841–5. PMID 1823978 .
- ^ a b Vogiatzoglou, A; Mulligan, AA; Bhaniani, A; Lentjes, MA; McTaggart, A; Luben, RN; Heiss, C; Kelm, M; Merx, MW; Spencer, JP; Schroeter, H; Khaw, KT; Kuhnle, GG (2015). "Asociaciones entre la ingesta de flavan-3-ol y el riesgo de ECV en la cohorte de Norfolk de la investigación prospectiva europea sobre el cáncer (EPIC-Norfolk)" . Biología y Medicina de Radicales Libres . 84 : 1-10. doi : 10.1016 / j.freeradbiomed.2015.03.005 . PMC 4503814 . PMID 25795512 .
- ^ Hooper, L; Kay, C; Abdelhamid, A; Kroon, PA; Cohn, JS; Rimm, EB; Cassidy, A (2012). "Efectos del chocolate, el cacao y los flavan-3-ols sobre la salud cardiovascular: una revisión sistemática y un metanálisis de ensayos aleatorizados" . Revista estadounidense de nutrición clínica . 95 (3): 740–51. doi : 10.3945 / ajcn.111.023457 . PMID 22301923 .
- ^ Ellinger, S; Reusch, A; Stehle, P; Helfrich, HP (2012). "La epicatequina ingerida a través de productos de cacao reduce la presión arterial en humanos: un modelo de regresión no lineal con un enfoque bayesiano" . Revista estadounidense de nutrición clínica . 95 (6): 1365–77. doi : 10.3945 / ajcn.111.029330 . PMID 22552030 .
- ^ a b Khalesi, S; Sun, J; Compra, N; Jamshidi, A; Nikbakht-Nasrabadi, E; Khosravi-Boroujeni, H (2014). "Las catequinas del té verde y la presión arterial: una revisión sistemática y un metanálisis de ensayos controlados aleatorios". Revista europea de nutrición . 53 (6): 1299–311. doi : 10.1007 / s00394-014-0720-1 . PMID 24861099 .
- ↑ Aprotosoaie, A. C; Miron, A; Trifan, A; Luca, V. S; Costache, I. I (2016). "Los efectos cardiovasculares de los polifenoles del cacao: una descripción general" . Enfermedades . 4 (4): 39. doi : 10.3390 / disease4040039 . PMC 5456324 . PMID 28933419 .
- ^ Schroeter, H; Heiss, C; Balzer, J; Kleinbongard, P; Keen, CL; Hollenberg, NK; Sies, H; Kwik-Uribe, C; Schmitz, HH; Kelm, M (2006). "(-) - La epicatequina media los efectos beneficiosos del cacao rico en flavanol sobre la función vascular en los seres humanos" . Actas de la Academia Nacional de Ciencias . 103 (4): 1024–9. Código Bibliográfico : 2006PNAS..103.1024S . doi : 10.1073 / pnas.0510168103 . PMC 1327732 . PMID 16418281 .
- ^ a b Panel de la EFSA sobre productos dietéticos, nutrición y alergias (2012). "Opinión científica sobre la justificación de una declaración de propiedades saludables relacionada con los flavonoides del cacao y el mantenimiento de la vasodilatación normal dependiente del endotelio de conformidad con el artículo 13, apartado 5, del Reglamento (CE) nº 1924/2006" . Revista EFSA . 10 (7): 2809. doi : 10.2903 / j.efsa.2012.2809 . Consultado el 25 de julio de 2016 .
- ^ Guo, Y; Zhi, F; Chen, P; Zhao, K; Xiang, H; Mao, Q; Wang, X; Zhang, X (2017). "El té verde y el riesgo de cáncer de próstata: una revisión sistemática y un metanálisis" . Medicina . 96 (13): e6426. doi : 10.1097 / MD.0000000000006426 . PMC 5380255 . PMID 28353571 .
- ^ Ye, J. H; Augustin, M. A (2018). "Nano y micropartículas para la liberación de catequinas: rendimiento físico y biológico". Revisiones críticas en ciencia de los alimentos y nutrición . 59 (10): 1563-1579. doi : 10.1080 / 10408398.2017.1422110 . PMID 29345975 .
- ↑ a b Amanda K. Broz y Jorge M. Vivanco (2006). "Metabolitos secundarios y alelopatía en invasiones de plantas: un estudio de caso de Centaurea maculosa" . Asociados Sinauer; Fisiología y desarrollo vegetal, Ed. 6; Lincoln Taiz, Eduardo Zeiger, Ian M. Møller y Angus Murphy, editores.
- ^ Bais HP, Vepachedu R, Gilroy S, Callaway RM, Vivanco JM (septiembre de 2003). "Alelopatía e invasión de plantas exóticas: de moléculas y genes a interacciones de especies". Ciencia . 301 (5638): 1377–80. Código Bibliográfico : 2003Sci ... 301.1377B . doi : 10.1126 / science.1083245 . PMID 12958360 .
- ^ Yamamoto M, Nakatsuka S, Otani H, Kohmoto K, Nishimura S (junio de 2000). "(+) - catequina actúa como factor inhibidor de infecciones en la hoja de fresa" . Fitopatología . 90 (6): 595–600. doi : 10.1094 / PHYTO.2000.90.6.595 . PMID 18944538 .
- ^ Chen Z, Liang J, Zhang C, Rodrigues CJ (octubre de 2006). "La epicatequina y la catequina pueden prevenir la enfermedad de la baya del café mediante la inhibición de la melanización apresora de Colletotrichum kahawae". Biotechnol. Lett . 28 (20): 1637–40. doi : 10.1007 / s10529-006-9135-2 . PMID 16955359 .
Enlaces externos [ editar ]
| Busque Catechin o catechine en Wiktionary, el diccionario gratuito. |
- Medios relacionados con la catequina en Wikimedia Commons