 | |
| Identificadores | |
|---|---|
| |
Modelo 3D ( JSmol ) | |
| |
| |
| Propiedades | |
| (C 4 H 4 ) Fe (CO) 3 | |
| Apariencia | sólido amarillo |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
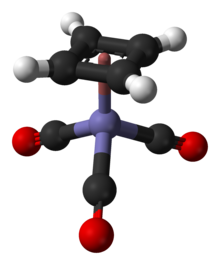
Cyclobutadieneiron tricarbonyl o (C 4 H 4 ) Fe (CO) 3 es un compuesto de organohierro con la fórmula Fe (C 4 H 4 ) (CO) 3 . Es un sólido amarillo que es soluble en solventes orgánicos. Se ha utilizado en química orgánica como precursor del ciclobutadieno , que es una especie esquiva en estado libre. [1]
Preparación y estructura [ editar ]
Fue preparado por primera vez en 1965 por Pettit a partir de 3,4-diclorociclobuteno y diiron nonacarbonyl : [2] [3]
- C 4 H 4 Cl 2 + 2 Fe 2 (CO) 9 → (C 4 H 4 ) Fe (CO) 3 + 2 Fe (CO) 5 + 2 CO + 2 FeCl 2
El compuesto es un ejemplo de un complejo de taburetes de piano . Las distancias CC son 1.426 Å. [4]
Propiedades [ editar ]
La descomplejación oxidativa del ciclobutadieno se logra tratando el complejo de tricarbonilo con nitrato de amonio cérico . El ciclobutadieno liberado queda atrapado con una quinona , que funciona como dienófilo . [5]
Cyclobutadieneiron tricarbonyl muestra aromaticidad como lo demuestran algunas de sus reacciones, que pueden clasificarse como sustitución aromática electrofílica : [6]
Se somete a acilación de Friedel-Crafts con cloruro de acetilo y cloruro de aluminio para dar el derivado de acilo 2 , con formaldehído y ácido clorhídrico al derivado de clorometilo 3 , en una reacción de Vilsmeier-Haack con N-metilformanilida y oxicloruro de fósforo al formilo 4 , y en una reacción de Mannich al derivado de amina 5 .
El mecanismo de reacción es idéntico al de EAS:
Compuestos relacionados [ editar ]
Varios años antes del trabajo de Petit, (C 4 Ph 4 ) Fe (CO) 3 se había preparado a partir de la reacción de carbonilo de hierro y difenilacetileno . [7]
(Butadieno) hierro tricarbonilo es isoelectrónico con ciclobutadieno hierro tricarbonilo.
Referencias [ editar ]
- ^ D. Seyferth "(ciclobutadieno) hierro tricarbonilo - un caso de teoría antes del experimento" Organometallics 2003, volumen 22, 2-20.
- ^ Complejos de ciclobutadieno y benzociclobutadieno-tricarbonilo de hierro GF Emerson, L. Watts, R. Pettit; Mermelada. Chem. Soc. ; 1965 ; 87 (1); 131-133. Primera página
- ^ Pettit, R .; Henery, J. (1970). "Cyclobutadieneiron Tricarbonyl". Síntesis orgánicas . 50 : 21. doi : 10.15227 / orgsyn.050.0021 .
- ^ PD Harvey; WP Schaefer; HB gris; DFR Gilson; IS Butler (1988). "Estructura de tricarbonil (η 4- ciclobutadienil) hierro (0) a -45 ° C". Inorg. Chem. 27 (1): 57–59. doi : 10.1021 / ic00274a013 .
- ^ L. Brener, JS Mckennis, R. Pettit (1976). "Ciclobutadieno en síntesis: endo- triciclo [4.4.0.02,5] deca-3,8-dieno-7,10-diona". Org. Synth . 55 : 43. doi : 10.15227 / orgsyn.055.0043 .Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Cyclobutadieneiron Tricarbonyl. Un nuevo sistema aromático JD Fitzpatrick, L. Watts, GF Emerson, R. Pettit J. Am. Chem. Soc. ; 1965 , vol. 87, 3254-3255 Resumen
- ^ RP Dodge, V. Schomaker, "Estructura cristalina del tetrafenilciclobutadieno hierro tricarbonilo", Nature 1960, vol. 186, 798-799. ‹Ver Tfd› doi : 10.1038 / 186798b0

