Cianogeno
El cianógeno es el compuesto químico con la fórmula ( C N ) 2 . Es un incoloro , tóxico gas con un penetrante olor . La molécula es un pseudohalógeno . Moléculas de cianógeno consisten en dos grupos CN - análogos a las moléculas diatómicas halógeno, tales como Cl 2 , pero mucho menos oxidante. Los dos ciano grupos están unidos entre sí en sus carbono átomos: N≡C-C≡N, aunque se han detectado otros isómeros. [6] El nombre también se utiliza para el radical CN, [7]y por tanto se utiliza para compuestos tales como bromuro de cianógeno (NCBr). [8]
El cianógeno se genera típicamente a partir de compuestos de cianuro. Un método de laboratorio implica la descomposición térmica del cianuro de mercurio :
Alternativamente, se pueden combinar soluciones de sales de cobre (II) (tales como sulfato de cobre (II) ) con cianuros; se forma un cianuro de cobre (II) inestable que se descompone rápidamente en cianuro de cobre (I) y cianógeno. [10]
Industrialmente, se crea mediante la oxidación de cianuro de hidrógeno , generalmente usando cloro sobre un catalizador de dióxido de silicio activado o dióxido de nitrógeno sobre una sal de cobre . También se forma cuando el nitrógeno y el acetileno reaccionan por una chispa o descarga eléctrica. [11]
El cianógeno es NCCN. Hay isómeros menos estables en los que el orden de los átomos difiere. El isocianógeno (o cianoisocianógeno) es NCNC, el diisocianógeno es CNNC y el diazodicarbono [ cita requerida ] es CCNN.
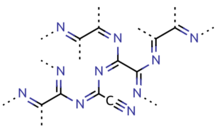
El paracianógeno es un polímero de cianógeno. Se puede preparar mejor calentando cianuro de mercurio. También se puede preparar por calentamiento de cianuro de plata , cianato de plata , yoduro de cianógeno o yoduro cianúrico. [12] También se puede preparar mediante la polimerización de cianógeno de 300 a 500 ° C (572 a 932 ° F) en presencia de trazas de impurezas. El paracianógeno también se puede convertir nuevamente en cianógeno calentando a 800 ° C (1470 ° F). [9] Basado en evidencia experimental, se cree que la estructura de este material polimérico es bastante irregular, siendo la mayoría de los átomos de carbono del tipo sp 2 y dominios localizados de conjugación π. [13]