 | |
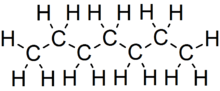 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Heptano [2] | |
| Otros nombres Septano [1] | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| 1730763 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Número CE |
|
| 49760 | |
| Malla | n-heptano |
PubChem CID | |
| Número RTECS |
|
| UNII | |
| un numero | 1206 |
| |
| |
| Propiedades | |
| C 7 H 16 | |
| Masa molar | 100,205 g · mol −1 |
| Apariencia | Líquido incoloro |
| Olor | Petrolico |
| Densidad | 0,6795 g cm −3 [3] |
| Punto de fusion | −90.549 [3] ° C (−130.988 ° F; 182.601 K) |
| Punto de ebullición | 98,38 [3] ° C (209,08 ° F; 371,53 K) |
| 0,0003% (20 ° C) [4] | |
| log P | 4.274 |
| Presión de vapor | 5,33 kPa (a 20,0 ° C) |
Constante de la ley de Henry ( k H ) | 12 nmol Pa −1 kg −1 |
| -85,24 · 10 −6 cm 3 / mol | |
Índice de refracción ( n D ) | 1.3855 [3] |
| Viscosidad | 0,389 mPa · s [5] |
| 0,0 D | |
| Termoquímica | |
Capacidad calorífica ( C ) | 224,64 JK −1 mol −1 |
Entropía molar estándar ( S | 328.57 JK −1 mol −1 |
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −225,2–−223,6 kJ mol −1 |
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | −4,825–−4,809 MJ mol −1 |
| Peligros | |
| Pictogramas GHS | |
| Palabra de señal GHS | Peligro |
Declaraciones de peligro GHS | H225 , H304 , H315 , H336 , H410 |
Consejos de prudencia del SGA | P210 , P261 , P273 , P301 + 310 , P331 |
| NFPA 704 (diamante de fuego) |  1 3 0 |
| punto de inflamabilidad | -4,0 ° C (24,8 ° F; 269,1 K) |
autoignición temperatura | 223,0 ° C (433,4 ° F; 496,1 K) |
| Límites explosivos | 1,05–6,7% |
| Dosis o concentración letal (LD, LC): | |
LC 50 ( concentración media ) | 17,986 ppm (ratón, 2 h) [6] |
LC Lo ( más bajo publicado ) | 16.000 ppm (humano) 15.000 ppm (ratón, 30 min) [6] |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
PEL (permitido) | TWA 500 ppm (2000 mg / m 3 ) [4] |
REL (recomendado) | TWA 85 ppm (350 mg / m 3 ) C 440 ppm (1800 mg / m 3 ) [15 minutos] [4] |
IDLH (peligro inmediato) | 750 ppm [4] |
| Compuestos relacionados | |
Alcanos relacionados |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El heptano o n- heptano es el alcano de cadena lineal con la fórmula química H 3 C (CH 2 ) 5 CH 3 o C 7 H 16 , y es uno de los componentes principales de la gasolina (gasolina). Cuando se utiliza como componente de combustible de prueba en motores de prueba antidetonantes , un combustible de heptano al 100% es el punto cero de la escala de octanaje (el punto 100 es 100% iso-octano). El número de octano equivale a las cualidades antidetonantes de una mezcla de comparación de heptano e isooctano, que se expresa como el porcentaje de isooctano en el heptano y se indica en las bombas para gasolina (gasolina) distribuidas a nivel mundial.
Usos [ editar ]
El heptano (y sus numerosos isómeros) se utiliza ampliamente en los laboratorios como disolvente no polar . Como líquido , es ideal para transporte y almacenamiento. En la prueba de la mancha de grasa, se usa heptano para disolver una mancha de aceite para mostrar la presencia previa de compuestos orgánicos en un papel manchado. Esto se hace agitando el papel manchado en una solución de heptano durante aproximadamente medio minuto. [ cita requerida ]
El bromo acuoso se puede distinguir del yodo acuoso por su apariencia después de la extracción en heptano. En el agua, tanto el bromo como el yodo aparecen de color marrón . Sin embargo, el yodo se vuelve violeta cuando se disuelve en heptano, mientras que la solución de bromo permanece marrón.
El heptano está disponible comercialmente como isómeros mixtos para su uso en pinturas y revestimientos, como el solvente de cemento de caucho "Bestine", el combustible de estufa exterior "Powerfuel" de Primus, como n- heptano puro para investigación y desarrollo y fabricación farmacéutica y como componente menor de gasolina.
El heptano también se utiliza como removedor de adhesivo por los coleccionistas de sellos . Desde 1974, el Servicio Postal de los Estados Unidos ha emitido sellos autoadhesivos que algunos coleccionistas encuentran difícil de separar de los sobres mediante el método tradicional de remojo en agua. Los productos a base de heptano como Bestine, así como los productos a base de limoneno , se han convertido en solventes populares para quitar sellos con mayor facilidad. [7]
Escala de octanaje [ editar ]
El n- heptano se define como el punto cero de la escala de octanaje . Es un componente más ligero en la gasolina , se quema más explosivamente , causando motor de pre-encendido ( golpeando ) en su forma pura, a diferencia de octano isómeros, que se queman más lentamente y dan menos golpeteo. Originalmente se eligió como el punto cero de la escala debido a la disponibilidad de n- heptano de muy alta pureza , sin mezclar con otros isómeros de heptano u otros alcanos, destilado de la resina de pino Jeffrey y del fruto de Pittosporum resiniferum . Otras fuentes de heptano y octano, producidas a partir depetróleo crudo , contiene una mezcla de diferentes isómeros con clasificaciones muy diferentes y no dan un punto cero tan preciso.
Isómeros y enantiómeros [ editar ]
El heptano tiene nueve isómeros , u once si se cuentan los enantiómeros :
- Heptano ( n- heptano), H 3 C – CH 2 –CH 2 –CH 2 –CH 2 –CH 2 –CH 3 ,
- 2- Metilhexano (isoheptano), H 3 C – CH (CH 3 ) –CH 2 –CH 2 –CH 2 –CH 3 ,
- 3-metilhexano , H 3 C – CH 2 –C * H (CH 3 ) –CH 2 –CH 2 –CH 3 ( quiral ),
- 2,2-dimetilpentano (neoheptano), H 3 C – C (CH 3 ) 2 –CH 2 –CH 2 –CH 3 ,
- 2,3-dimetilpentano , H 3 C – CH (CH 3 ) –C * H (CH 3 ) –CH 2 –CH 3 ( quiral ),
- 2,4-dimetilpentano , H 3 C – CH (CH 3 ) –CH 2 –CH (CH 3 ) –CH 3 ,
- 3,3-dimetilpentano , H 3 C – CH 2 –C (CH 3 ) 2 –CH 2 –CH 3 ,
- 3-etilpentano , H 3 C – CH 2 –CH (CH 2 CH 3 ) –CH 2 –CH 3 ,
- 2,2,3-trimetilbutano , H 3 C – C (CH 3 ) 2 –CH (CH 3 ) –CH 3 , este isómero también se conoce como pentametiletano y triptano. [8]
Preparación [ editar ]
El n- heptano lineal se puede obtener del aceite de pino Jeffrey . [9] Los seis isómeros ramificados sin un carbono cuaternario se pueden preparar creando un alcohol secundario o terciario adecuado mediante la reacción de Grignard , convirtiéndolo en un alqueno por deshidratación e hidrogenando este último. [9] El isómero de 2,2-dimetilpentano se puede preparar haciendo reaccionar cloruro de terc -butilo con bromuro de n -propil magnesio. [9] El isómero de 3,3-dimetilpentano se puede preparar a partir de cloruro de terc -amilo y bromuro de etilmagnesio.[9]
Riesgos para la salud [ editar ]
Esta sección necesita expansión . Puede ayudar agregando más . ( Junio de 2015 ) |
La exposición aguda a los vapores de heptano puede causar mareos , estupor, falta de coordinación, pérdida de apetito, náuseas, dermatitis, neumonitis química o pérdida del conocimiento, posible neuropatía periférica. [10]
Referencias [ editar ]
- ↑ Hofmann, August Wilhelm Von (1 de enero de 1867). "I. Sobre la acción del tricloruro de fósforo sobre las sales de las monaminas aromáticas". Actas de la Royal Society de Londres . 15 : 54–62. doi : 10.1098 / rspl.1866.0018 .
- ^ "n-heptano - Resumen de compuestos" . Compuesto PubChem . EE.UU .: Centro Nacional de Información Biotecnológica. 16 de septiembre de 2004. Identificación y registros relacionados . Consultado el 2 de enero de 2012 .
- ↑ a b c d Haynes, William M., ed. (2011). Manual CRC de Química y Física (92ª ed.). Boca Raton, FL: CRC Press . pag. 3.290. ISBN 1439855110.
- ^ a b c d Guía de bolsillo de NIOSH sobre peligros químicos. "# 0312" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Dymond, JH; Oye, HA (1994). "Viscosidad de n-alcanos líquidos seleccionados". Revista de datos de referencia físicos y químicos . 23 (1): 41–53. doi : 10.1063 / 1.555943 . ISSN 0047-2689 .
- ^ a b "n-heptano" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Mayordomo, Peter. "Es como magia: quitar sellos autoadhesivos del papel" (PDF) . Sociedad Filatélica Estadounidense . Consultado el 15 de junio de 2020 .
- ^ Isómeros . Members.optushome.com.au. Consultado el 4 de marzo de 2012.
- ^ a b c d Graham Edgar, George Calingaert y RE Marker (1929): "La preparación y propiedades de los heptanos isoméricos. Parte I. Preparación". Revista de la Sociedad Química Estadounidense , volumen 51, número 5, páginas 1483–1491. doi : 10.1021 / ja01380a027
- ^ Patty, FA; Yant, WP (1929). "Intensidad del olor y síntomas producidos por vapor comercial de propano, butano, pentano, hexano y heptano" . Informe de Investigaciones . Departamento de Comercio de EE. UU., Oficina de Minas de EE. UU. No. 2979 (diciembre): 1–10.
Enlaces externos [ editar ]
- Tarjeta internacional de seguridad química 0657 ( n- heptano)
- Tarjeta internacional de seguridad química 0658 (2-metilhexano)
- Guía de bolsillo de NIOSH sobre peligros químicos
- Hoja de datos de seguridad del material para heptano
- Entrada de la base de datos de fitoquímicos