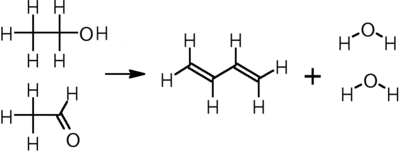
Butadieno
El 1,3-butadieno ( / ˌ b juː t ə ˈ d aɪ iː n / ) [7] es el compuesto orgánico de fórmula (CH 2 =CH) 2 . Es un gas incoloro que se condensa fácilmente a líquido. Es importante industrialmente como precursor del caucho sintético . La molécula puede verse como la unión de dos grupos vinilo . Es el dieno conjugado más simple .
Aunque el butadieno se descompone rápidamente en la atmósfera, se encuentra en el aire ambiente de áreas urbanas y suburbanas como consecuencia de su constante emisión por parte de los vehículos de motor . [8]
El nombre butadieno también puede referirse al isómero , 1,2-butadieno , que es un dieno acumulado con estructura H 2 C=C=CH−CH 3 . Este aleno no tiene importancia industrial.
En 1863, el químico francés E. Caventou aisló el butadieno a partir de la pirólisis del alcohol amílico . [9] Este hidrocarburo fue identificado como butadieno en 1886, después de que Henry Edward Armstrong lo aislara de entre los productos de pirólisis del petróleo. [10] En 1910, el químico ruso Sergei Lebedev polimerizó butadieno y obtuvo un material con propiedades similares al caucho. Sin embargo, se encontró que este polímero era demasiado blando para reemplazar el caucho natural en muchas aplicaciones, especialmente en neumáticos de automóviles.
La industria del butadieno se originó en los años previos a la Segunda Guerra Mundial. Muchas de las naciones beligerantes se dieron cuenta de que, en caso de guerra, podrían quedar aisladas de las plantaciones de caucho controladas por el Imperio Británico y buscaron reducir su dependencia del caucho natural. [11] En 1929, Eduard Tschunker y Walter Bock , que trabajaban para IG Farben en Alemania, fabricaron un copolímero de estireno y butadieno que podía utilizarse en neumáticos de automóviles. La producción mundial se produjo rápidamente, con butadieno producido a partir de alcohol de grano en la Unión Soviética y los Estados Unidos, y de acetileno derivado del carbón en Alemania.
En los Estados Unidos, Europa occidental y Japón, el butadieno se produce como subproducto del proceso de craqueo al vapor utilizado para producir etileno y otros alquenos . Cuando se mezclan con vapor y se calientan brevemente a temperaturas muy altas (a menudo por encima de los 900 °C), los hidrocarburos alifáticos liberan hidrógeno para producir una mezcla compleja de hidrocarburos insaturados, incluido el butadieno. La cantidad de butadieno producido depende de los hidrocarburos utilizados como alimentación. Las alimentaciones ligeras, como el etano , dan principalmente etileno cuando se craquean, pero las alimentaciones más pesadas favorecen la formación de olefinas, butadieno e hidrocarburos aromáticos más pesados .