Los flavonoides (o bioflavonoides ; de la palabra latina flavus , que significa amarillo, su color en la naturaleza) son una clase de metabolitos secundarios polifenólicos que se encuentran en las plantas y, por lo tanto, se consumen comúnmente en las dietas. [1]
Químicamente, los flavonoides tienen la estructura general de un esqueleto de 15 carbonos, que consta de dos anillos de fenilo (A y B) y un anillo heterocíclico (C, el anillo que contiene el oxígeno incrustado ). [1] [2] Esta estructura de carbono puede abreviarse C6-C3-C6. Según la nomenclatura de la IUPAC , [3] [4] se pueden clasificar en:
- flavonoides o bioflavonoides
- isoflavonoides , derivados de la estructura de 3- fenilcromen-4-ona (3-fenil-1,4- benzopirona )
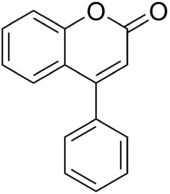
- neoflavonoids , derivados de 4-fenil cumarina (4-fenil-1,2- benzopirona estructura)
Las tres clases de flavonoides anteriores son todos compuestos que contienen cetonas y, como tales, antoxantinas ( flavonas y flavonoles ). [1] Esta clase fue la primera en denominarse bioflavonoides. Los términos flavonoide y bioflavonoide también se han utilizado de manera más vaga para describir compuestos de polihidroxi polifenol no cetónicos, que se denominan más específicamente flavonoides. Los tres ciclos o heterociclos en la cadena principal de flavonoides generalmente se denominan anillo A, B y C. [2] El anillo A generalmente muestra un patrón de sustitución de floroglucinol .
Biosíntesis [ editar ]
Los flavonoides son metabolitos secundarios sintetizados principalmente por plantas. La estructura general de los flavonoides es un esqueleto de 15 carbonos, que contiene 2 anillos de benceno conectados por una cadena de enlace de 3 carbonos. [1] Por lo tanto, se describen como compuestos C6-C3-C6. Dependiendo de la estructura química, el grado de oxidación y la insaturación de la cadena de enlace (C3), los flavonoides se pueden clasificar en diferentes grupos, como antocianidinas, calconas, flavonoles, flavanonas, flavan-3-oles, flavanonoles, flavonas e isoflavonoides. . [1] Además, los flavonoides se pueden encontrar en plantas en formas agliconas libres y unidas a glucósidos. La forma unida a glucósidos es la forma de flavona y flavonol más común consumida en la dieta. [1]
Funciones de los flavonoides en las plantas [ editar ]
Los flavonoides se encuentran ampliamente distribuidos en las plantas y cumplen muchas funciones. [1] Los flavonoides son los pigmentos vegetales más importantes para la coloración de las flores y producen pigmentación amarilla o roja / azul en los pétalos diseñados para atraer a los animales polinizadores . En las plantas superiores, los flavonoides están involucrados en la filtración UV, la fijación simbiótica de nitrógeno y la pigmentación floral. También pueden actuar como mensajeros químicos, reguladores fisiológicos e inhibidores del ciclo celular. Los flavonoides secretados por la raíz de su planta huésped ayudan a Rhizobia en la etapa de infección de su relación simbiótica con legumbres como guisantes, frijoles, trébol y soja. Los rizobios que viven en el suelo son capaces de sentir los flavonoides y esto desencadena la secreción deLos factores Nod , que a su vez son reconocidos por la planta huésped y pueden provocar la deformación del pelo de la raíz y varias respuestas celulares, como los flujos de iones y la formación de un nódulo radicular . Además, algunos flavonoides tienen actividad inhibidora contra organismos que causan enfermedades de las plantas, por ejemplo, Fusarium oxysporum . [5]
Subgrupos [ editar ]
Se han caracterizado más de 5000 flavonoides naturales de varias plantas. Se han clasificado de acuerdo con su estructura química y, por lo general, se subdividen en los siguientes subgrupos (para obtener más información, consulte [6] ):
Antocianidinas [ editar ]
Las antocianidinas son las agliconas de las antocianinas ; utilizan el esqueleto iónico de flavilio (2-fenilcromenilo). [1]
- Ejemplos : cianidina , delfinidina , malvidina , pelargonidina , peonidina , petunidina
Antoxantinas [ editar ]
Las antoxantinas se dividen en dos grupos: [7]
| Grupo | Esqueleto | Ejemplos de | |||
|---|---|---|---|---|---|
| Descripción | Grupos funcionales | Fórmula estructural | |||
| 3-hidroxilo | 2,3-dihidro | ||||
| Flav uno | 2-fenilcromos - 4-uno | ✗ | ✗ | Luteolina , apigenina , mandaritina | |
| Flav on ol o 3-hydroxy flav one | 3-hidroxi - 2-fenilcromenos - 4-uno | ✓ | ✗ | La quercetina , kaempferol , miricetina , fisetina , Galangina , isorhamnetina , pachypodol , Rhamnazin , Pyranoflavonols , Furanoflavonols , | |
Flavanones [ editar ]
Flavanones
| Grupo | Esqueleto | Ejemplos de | |||
|---|---|---|---|---|---|
| Descripción | Grupos funcionales | Fórmula estructural | |||
| 3-hidroxilo | 2,3-dihidro | ||||
| Flav un uno | 2,3-dihidro - 2-fenilcromen - 4-ona | ✗ | ✓ | Hesperetina , naringenina , eriodictyol , homoeriodictyol | |
Flavanonols [ editar ]
Flavanonoles
| Grupo | Esqueleto | Ejemplos de | |||
|---|---|---|---|---|---|
| Descripción | Grupos funcionales | Fórmula estructural | |||
| 3-hidroxilo | 2,3-dihidro | ||||
| Flav una en ol o 3-hidroxi Flav un uno o 2,3-dihidro flav en ol | 3-hidroxi - 2,3-dihidro - 2-fenilcromen - 4-ona | ✓ | ✓ | Taxifolina (o dihidroquercetina ), dihidrokaempferol | |
Flavans [ editar ]
Incluya flavan-3-ols (flavanoles), flavan-4-oles y flavan-3,4-dioles .
| Esqueleto | Nombre |
|---|---|
| Flavan-3-ol (flavanol) | |
| Flavan-4-ol | |
| Flavan-3,4-diol (leucoantocianidina) |
- Flavan-3-ols (flavonoides)
- Flav an - 3-ols utilizan el esqueleto 2-fenil- 3,4-dihidro -2 H -cromen- 3-ol
- Ejemplos : catequina (C), galocatequina (GC), catequina 3-galato (CG), galocatequina 3-galato (GCG), epicatequinas ( epicatequina (EC)), epigalocatequina (EGC), la epicatequina 3-galato (ECG), la epigalocatequina 3-galato (EGCg)
- Theaflavin
- Ejemplos : Theaflavin-3-galato , Theaflavin-3'-galato , Theaflavin-3,3'-digallate
- Thearubigin
- Las proantocianidinas son dímeros, trímeros, oligómeros o polímeros de los flavonoides.
Isoflavonoides [ editar ]
- Isoflavonoides
- Las isoflavonas usan el esqueleto 3-fenilcromen- 4-ona (sin sustitución de grupos hidroxilo en el carbono en la posición 2)
- Ejemplos : genisteína , daidzeína , gliciteína
- Isoflavanos
- Isoflavandiol
- Isoflavenos
- Coumestans
- Pterocarpanos
Fuentes dietéticas [ editar ]
Los flavonoides (específicamente los flavonoides como las catequinas ) son "el grupo más común de compuestos polifenólicos en la dieta humana y se encuentran ubicuamente en las plantas". [1] [8] Los flavonoles, los bioflavonoides originales como la quercetina , también se encuentran en todas partes, pero en menores cantidades. La amplia distribución de los flavonoides, su variedad y su toxicidad relativamente baja en comparación con otros compuestos vegetales activos (por ejemplo, alcaloides ) significa que muchos animales, incluidos los humanos , ingieren cantidades significativas en su dieta. [1] Los alimentos con un alto contenido de flavonoides incluyen el perejil., [9] cebollas , [9] arándanos y otras bayas , [9] té negro , [9] té verde y té oolong , [9] plátanos , todos los cítricos , Ginkgo biloba , vino tinto , espinos amarillos , trigo sarraceno , [10] y chocolate negro con un contenido de cacao del 70% o más.
Perejil [ editar ]
El perejil , tanto fresco como seco, contiene flavonas . [9]
Arándanos [ editar ]
Los arándanos son una fuente dietética de antocianidinas . [9] [11]
Té negro [ editar ]
El té negro es una rica fuente de flavan-3-ols en la dieta . [9]
Cítricos [ editar ]
Los flavonoides cítricos incluyen hesperidina (un glucósido de la flavanona hesperetina ), quercitrina , rutina (dos glucósidos del flavonol quercetina ) y la flavona mandaritina . Los flavonoides están mucho menos concentrados en la pulpa que en las cáscaras (por ejemplo, 165 frente a 1156 mg / 100 g en pulpa frente a piel de mandarina satsuma , y 164 frente a 804 mg / 100 g en pulpa frente a piel de clementina ). [12]
Vino [ editar ]
Cacao [ editar ]
Los flavonoides existen naturalmente en el cacao , pero debido a que pueden ser amargos, a menudo se eliminan del chocolate , incluso del chocolate negro . [13] Aunque los flavonoides están presentes en el chocolate con leche, la leche puede interferir con su absorción; [14] sin embargo, esta conclusión ha sido cuestionada. [15]
Maní [ editar ]
La piel de maní (roja) contiene un contenido significativo de polifenoles, incluidos los flavonoides. [16] [17]
| Fuente de comida | Flavonas | Flavonoles | Flavanones |
|---|---|---|---|
| cebolla roja | 0 | 4 - 100 | 0 |
| Perejil, fresco | 24 - 634 | 8 - 10 | 0 |
| Tomillo fresco | 56 | 0 | 0 |
| Jugo de limón, fresco | 0 | 0 - 2 | 2 - 175 |
Unidad: mg / 100g [1]
Ingesta dietética [ editar ]
Los datos de composición de los alimentos para los flavonoides fueron proporcionados por la base de datos del USDA sobre flavonoides. [9] En la encuesta NHANES de Estados Unidos , la ingesta media de flavonoides fue de 190 mg / d en adultos, con flavan-3-ols como el principal contribuyente. [19] En la Unión Europea , según los datos de la EFSA , la ingesta media de flavonoides fue de 140 mg / día, aunque hubo diferencias considerables entre los países individuales. [18] El principal tipo de flavonoides consumidos en la UE y EE. UU. Fueron los 3-flavonoides (80% para los adultos estadounidenses), principalmente de té o cacao en el chocolate, mientras que la ingesta de otros flavonoides fue considerablemente menor. [1] [18] [19]
Investigación [ editar ]
Ni la Administración de Alimentos y Medicamentos (FDA) ni la Autoridad Europea de Seguridad Alimentaria (EFSA) han aprobado ninguna declaración de propiedades saludables para los flavonoides ni han aprobado flavonoides como medicamentos recetados . [1] [20] [21] [22] La FDA de EE. UU. Ha advertido a numerosas empresas de suplementos dietéticos sobre la publicidad ilegal y las declaraciones de propiedades saludables engañosas. [23] [24]
Metabolismo y excreción [ editar ]
Los flavonoides se absorben mal en el cuerpo humano (menos del 5%), luego se metabolizan rápidamente en fragmentos más pequeños con propiedades desconocidas y se excretan rápidamente. [1] [22] [25] [26] Los flavonoides tienen una actividad antioxidante insignificante en el cuerpo, y el aumento en la capacidad antioxidante de la sangre que se observa después del consumo de alimentos ricos en flavonoides no es causado directamente por los flavonoides, sino por la producción de ácido úrico. resultante de la despolimerización y excreción de flavonoides . [1] El metabolismo microbiano es un factor importante que contribuye al metabolismo general de los flavonoides de la dieta. [1] [27]Se desconoce el efecto de la ingesta habitual de flavonoides en el microbioma intestinal humano. [1] [28]
Inflamación [ editar ]
La inflamación ha sido implicada como un posible origen de numerosas enfermedades locales y sistémicas, como el cáncer , [29] trastornos cardiovasculares , [30] diabetes mellitus , [31] y enfermedad celíaca . [32] No hay evidencia clínica de que los flavonoides de la dieta afecten a alguna de estas enfermedades. [1]
Cáncer [ editar ]
Los estudios clínicos que investigan la relación entre el consumo de flavonoides y la prevención / desarrollo del cáncer son contradictorios para la mayoría de los tipos de cáncer, probablemente porque la mayoría de los estudios en humanos tienen diseños débiles, como un tamaño de muestra pequeño . [1] [33] Hay poca evidencia que indique que los flavonoides de la dieta afectan el riesgo de cáncer en humanos en general, pero los estudios observacionales y los ensayos clínicos sobre cánceres dependientes de hormonas (mama y próstata) han mostrado beneficios. [1] Una revisión reciente ha sugerido que la ingesta dietética de flavonoides se asocia con un riesgo reducido de diferentes tipos de cáncer, incluido el cáncer gástrico, de mama, de próstata y colorrectal.[34]
Enfermedades cardiovasculares [ editar ]
Aunque no se ha encontrado una asociación significativa entre la ingesta de flavan-3-ol y la mortalidad por enfermedades cardiovasculares, los ensayos clínicos han demostrado una mejor función endotelial y una reducción de la presión arterial (con algunos estudios que muestran resultados inconsistentes). [1] Las revisiones de los estudios de cohortes en 2013 encontraron que los estudios tenían demasiadas limitaciones para determinar una posible relación entre el aumento de la ingesta de flavonoides y la disminución del riesgo de enfermedad cardiovascular, aunque existía una tendencia hacia una relación inversa. [1] [35]
In vitro [ editar ]
Los estudios de laboratorio en células aisladas o cultivos celulares in vitro indican que los flavonoides pueden afectar la enfermedad crónica inhibiendo selectivamente las quinasas , pero los resultados in vivo podrían diferir debido a la baja biodisponibilidad . [1]
Síntesis, detección, cuantificación y alteraciones semisintéticas [ editar ]
Espectro de color [ editar ]
La síntesis de flavonoides en las plantas es inducida por espectros de color de luz con radiaciones de alta y baja energía. Las radiaciones de baja energía son aceptadas por el fitocromo , mientras que las radiaciones de alta energía son aceptadas por los carotenoides , flavinas , criptocromos además de los fitocromos. El proceso fotomorfogénico de la biosíntesis de flavonoides mediada por fitocromos se ha observado en amaranto , cebada , maíz , sorgo y nabo . La luz roja promueve la síntesis de flavonoides. [36]
Disponibilidad a través de microorganismos [ editar ]
Varios artículos de investigación recientes han demostrado la producción eficiente de moléculas de flavonoides a partir de microorganismos modificados genéticamente. [37] [38] [39] y el proyecto SynBio4Flav [40] [41] tiene como objetivo proporcionar una alternativa rentable a la producción actual de flavonoides descomponiendo sus complejas vías biosintéticas en partes específicas estandarizadas, que pueden transferirse a microorganismos diseñados dentro de Consorcios microbianos sintéticos para promover el ensamblaje de flavonoides mediante catálisis distribuida .
Pruebas de detección [ editar ]
- Prueba de Shinoda
Se añaden cuatro trozos de limaduras de magnesio al extracto etanólico seguido de unas gotas de ácido clorhídrico concentrado . Un color rosa o rojo indica la presencia de flavonoides. [42] colores que varían del naranja al rojo indicados flavonas , rojo carmesí flavonoides indicados, carmesí a magenta indica flavononas .
- Prueba de hidróxido de sodio
Aproximadamente 5 mg del compuesto se disuelven en agua, se calienta y se filtra. Se añade hidróxido de sodio acuoso al 10% a 2 ml de esta solución. Esto produce una coloración amarilla. Un cambio de color de amarillo a incoloro al agregar ácido clorhídrico diluido es una indicación de la presencia de flavonoides. [43]
- Prueba de p-dimetilaminocinamaldehído
Se ha desarrollado un ensayo colorimétrico basado en la reacción de los anillos A con el cromógeno p-dimetilaminocinamaldehído (DMACA) para los flavonoides en la cerveza que puede compararse con el procedimiento de la vainillina . [44]
Cuantificación [ editar ]
Lamaison y Carnet han diseñado una prueba para la determinación del contenido total de flavonoides de una muestra ( método AlCI 3 ). Después de mezclar correctamente la muestra y el reactivo, la mezcla se incuba durante 10 minutos a temperatura ambiente y se lee la absorbancia de la solución a 440 nm. El contenido de flavonoides se expresa en mg / g de quercetina. [45]
Alteraciones semisintéticas [ editar ]
La lipasa de Candida antarctica inmovilizada se puede utilizar para catalizar la acilación regioselectiva de flavonoides. [46]
Ver también [ editar ]
- Fitoquímico
- Lista de antioxidantes en los alimentos
- Lista de fitoquímicos en los alimentos
- Fitoquímica
- Metabolitos secundarios
- Homoisoflavonoides , sustancias químicas relacionadas con un esqueleto de 16 carbonos
Referencias [ editar ]
- ^ a b c d e f g h i j k l m n o p q r s t u v w Delage B (noviembre de 2015). "Flavonoides" . Instituto Linus Pauling , Universidad Estatal de Oregon , Corvallis, Oregon . Consultado el 26 de enero de 2021 .
- ↑ a b de Souza Farias SA, da Costa KS, Martins JB (abril de 2021). "Análisis de propiedades conformacionales, estructurales, magnéticas y electrónicas relacionadas con la actividad antioxidante: revisando Flavan, antocianidina, flavanona, flavonol, isoflavona, flavona y flavan-3-ol" . ACS Omega . 6 (13): 8908–8918. doi : 10.1021 / acsomega.0c06156 . PMC 8028018 . PMID 33842761 .
- ^ McNaught AD, Wilkinson A (1997), Compendio de terminología química de la IUPAC (2a ed.), Oxford: Blackwell Scientific, doi : 10.1351 / goldbook.F02424 , ISBN 978-0-9678550-9-7
- ^ Nič M, Jirát J, Košata B, Jenkins A, McNaught A, eds. (2009). "Flavonoides (isoflavonoides y neoflavonoides)" . El libro de oro . doi : 10.1351 / goldbook . ISBN 978-0-9678550-9-7. Consultado el 16 de septiembre de 2012 .
- ^ Galeotti F, Barile E, Curir P, Dolci M, Lanzotti V (2008). "Flavonoides del clavel (Dianthus caryophyllus) y su actividad antifúngica". Letras de fitoquímica . 1 : 44–48. doi : 10.1016 / j.phytol.2007.10.001 .
- ^ Ververidis F, Trantas E, Douglas C, Vollmer G, Kretzschmar G, Panopoulos N (octubre de 2007). "Biotecnología de flavonoides y otros productos naturales derivados de fenilpropanoides. Parte I: Diversidad química, impactos en la biología vegetal y la salud humana". Revista de biotecnología . 2 (10): 1214–34. doi : 10.1002 / biot.200700084 . PMID 17935117 . S2CID 24986941 .
- ^ Aislamiento de una UDP-glucosa: gen de flavonoide 5-O-glucosiltransferasa y análisis de expresión de genes biosintéticos de antocianina en peonía herbácea (Paeonia lactiflora Pall.). Da Qiu Zhao, Chen Xia Han, Jin Tao Ge y Jun Tao, Electronic Journal of Biotechnology , 15 de noviembre de 2012, Volumen 15, Número 6, doi : 10.2225 / vol15-número6-fulltext-7
- ^ Spencer JP (mayo de 2008). "Flavonoides: ¿moduladores de la función cerebral?" . La Revista Británica de Nutrición . 99 E Suppl 1 (E-S1): ES60-77. doi : 10.1017 / S0007114508965776 . PMID 18503736 .
- ^ a b c d e f g h i Base de datos del USDA sobre el contenido de flavonoides
- ^ Oomah BD, Mazza G (1996). "Flavonoides y actividades antioxidantes en alforfón". Revista de Química Agrícola y Alimentaria . 44 (7): 1746-1750. doi : 10.1021 / jf9508357 .
- ^ Ayoub M, de Camargo AC, Shahidi F (abril de 2016). "Antioxidantes y bioactividades de fenólicos libres, esterificados e insolubles ligados a partir de harinas de semillas de bayas". Química de los alimentos . 197 (Parte A): 221–32. doi : 10.1016 / j.foodchem.2015.10.107 . PMID 26616944 .
- ^ Levaj B; otros (2009). "Determinación de flavonoides en pulpa y cáscara de frutos de mandarina (tabla 1)" (PDF) . Agriculturae Conspectus Scientificus . 74 (3): 223.
- ^ "El diablo en el chocolate negro". Lancet . 370 (9605): 2070. Diciembre de 2007. doi : 10.1016 / S0140-6736 (07) 61873-X . PMID 18156011 . S2CID 41271401 .
- ^ Serafini M, Bugianesi R, Maiani G, Valtuena S, De Santis S, Crozier A (agosto de 2003). "Antioxidantes plasmáticos del chocolate". Naturaleza . 424 (6952): 1013. Código Bibliográfico : 2003Natur.424.1013S . doi : 10.1038 / 4241013a . PMID 12944955 . S2CID 4381941 .
- ^ Roura E, Andrés-Lacueva C, Estruch R, Mata-Bilbao ML, Izquierdo-Pulido M, Waterhouse AL, Lamuela-Raventós RM (2007). "La leche no afecta la biodisponibilidad del flavonoide del cacao en polvo en humanos sanos". Annals of Nutrition & Metabolism . 51 (6): 493–8. doi : 10.1159 / 000111473 . PMID 18032884 . S2CID 25993668 . [ enlace muerto permanente ]
- ↑ de Camargo AC, Regitano-d'Arce MA, Gallo CR, Shahidi F (2015). "Cambios inducidos por irradiación gamma en el estado microbiológico, perfil fenólico y actividad antioxidante de la piel de maní" . Revista de alimentos funcionales . 12 : 129-143. doi : 10.1016 / j.jff.2014.10.034 .
- ^ Chukwumah Y, Walker LT, Verghese M (noviembre de 2009). "Color de la piel del maní: un biomarcador del contenido polifenólico total y las capacidades antioxidantes de los cultivares de maní" . Revista Internacional de Ciencias Moleculares . 10 (11): 4941–52. doi : 10.3390 / ijms10114941 . PMC 2808014 . PMID 20087468 .
- ^ a b c d Vogiatzoglou A, Mulligan AA, Lentjes MA, Luben RN, Spencer JP, Schroeter H, et al. (2015). "Ingesta de flavonoides en adultos europeos (18 a 64 años)" . PLOS ONE . 10 (5): e0128132. Código bibliográfico : 2015PLoSO..1028132V . doi : 10.1371 / journal.pone.0128132 . PMC 4444122 . PMID 26010916 .
- ^ a b Chun OK, Chung SJ, Song WO (mayo de 2007). "Ingesta estimada de flavonoides en la dieta y principales fuentes de alimentos de los adultos estadounidenses" . La Revista de Nutrición . 137 (5): 1244–52. doi : 10.1093 / jn / 137.5.1244 . PMID 17449588 .
- ^ "Productos farmacéuticos aprobados por la FDA" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 8 de noviembre de 2013 .
- ^ "Reclamaciones de salud que cumplen un acuerdo científico significativo" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 8 de noviembre de 2013 .
- ^ a b Panel de la EFSA sobre productos dietéticos, nutrición y alergias (NDA) (2010). "Opinión científica sobre la sustanciación de las declaraciones de propiedades saludables relacionadas con varios alimentos / constituyentes de los alimentos y la protección de las células contra el envejecimiento prematuro, la actividad antioxidante, el contenido de antioxidantes y las propiedades antioxidantes, y la protección del ADN, las proteínas y los lípidos del daño oxidativo de conformidad con el artículo 13, apartado 1, del Reglamento (CE) no 1924/20061 " . Revista EFSA . 8 (2): 1489. doi : 10.2903 / j.efsa.2010.1489 .
- ^ "Inspecciones, cumplimiento, ejecución e investigaciones penales (ciencias flavonoides)" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 8 de noviembre de 2013 .
- ^ "Inspecciones, cumplimiento, ejecución e investigaciones criminales (Unilever, Inc.)" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 25 de octubre de 2013 .
- ^ Lotito SB, Frei B (diciembre de 2006). "Consumo de alimentos ricos en flavonoides y aumento de la capacidad antioxidante del plasma en humanos: ¿causa, consecuencia o epifenómeno?". Biología y Medicina de Radicales Libres . 41 (12): 1727–46. doi : 10.1016 / j.freeradbiomed.2006.04.033 . PMID 17157175 .
- ^ Williams RJ, Spencer JP, Rice-Evans C (abril de 2004). "Flavonoides: ¿antioxidantes o moléculas de señalización?". Biología y Medicina de Radicales Libres . 36 (7): 838–49. doi : 10.1016 / j.freeradbiomed.2004.01.001 . PMID 15019969 .
- ^ Hidalgo M, Oruna-Concha MJ, Kolida S, Walton GE, Kallithraka S, Spencer JP, de Pascual-Teresa S (abril de 2012). "Metabolismo de las antocianinas por la microflora intestinal humana y su influencia en el crecimiento bacteriano intestinal". Revista de Química Agrícola y Alimentaria . 60 (15): 3882–90. doi : 10.1021 / jf3002153 . PMID 22439618 .
- ^ Ivey KL, Chan AT, Izard J, Cassidy A, Rogers GB, Rimm EB (septiembre de 2019). "Papel de los compuestos flavonoides dietéticos en los patrones de conducción de la asamblea de la comunidad microbiana" . mBio . 10 (5). doi : 10.1128 / mBio.01205-19 . PMC 6759757 . PMID 31551328 .
- ^ Ravishankar D, Rajora AK, Greco F, Osborn HM (diciembre de 2013). "Flavonoides como compuestos prospectivos para la terapia contra el cáncer". La Revista Internacional de Bioquímica y Biología Celular . 45 (12): 2821–31. doi : 10.1016 / j.biocel.2013.10.004 . PMID 24128857 .
- ^ Manach C, Mazur A, Scalbert A (febrero de 2005). "Polifenoles y prevención de enfermedades cardiovasculares". Opinión actual en lipidología . 16 (1): 77–84. doi : 10.1097 / 00041433-200502000-00013 . PMID 15650567 . S2CID 794383 .
- ^ Babu PV, Liu D, Gilbert ER (noviembre de 2013). "Avances recientes en la comprensión de las acciones antidiabéticas de los flavonoides dietéticos" . La Revista de Bioquímica Nutricional . 24 (11): 1777–89. doi : 10.1016 / j.jnutbio.2013.06.003 . PMC 3821977 . PMID 24029069 .
- ^ Ferretti G, Bacchetti T, Masciangelo S, Saturni L (abril de 2012). "Enfermedad celíaca, inflamación y daño oxidativo: un enfoque nutrigenético" . Nutrientes . 4 (4): 243–57. doi : 10.3390 / nu4040243 . PMC 3347005 . PMID 22606367 .
- ^ Romagnolo DF, Selmin OI (2012). "Flavonoides y prevención del cáncer: una revisión de la evidencia". Revista de Nutrición en Gerontología y Geriatría . 31 (3): 206–38. doi : 10.1080 / 21551197.2012.702534 . PMID 22888839 . S2CID 205960210 .
- ^ Rodríguez-García C, Sánchez-Quesada C, J Gaforio J (mayo de 2019). "Flavonoides dietéticos como agentes quimiopreventivos del cáncer: una revisión actualizada de estudios humanos" . Antioxidantes . 8 (5): 137. doi : 10.3390 / antiox8050137 . PMC 6562590 . PMID 31109072 .
- ^ Wang X, Ouyang YY, Liu J, Zhao G (enero de 2014). "Ingesta de flavonoides y riesgo de ECV: una revisión sistemática y metanálisis de estudios de cohortes prospectivos" . La Revista Británica de Nutrición . 111 (1): 1–11. doi : 10.1017 / S000711451300278X . PMID 23953879 .
- ↑ Sinha RK (1 de enero de 2004). Fisiología vegetal moderna . Prensa CRC. pag. 457. ISBN 9780849317149.
- ^ Hwang EI, Kaneko M, Ohnishi Y, Horinouchi S (mayo de 2003). "Producción de flavanonas específicas de plantas por Escherichia coli que contienen un grupo de genes artificiales" . Microbiología aplicada y ambiental . 69 (5): 2699–706. doi : 10.1128 / AEM.69.5.2699-2706.2003 . PMC 154558 . PMID 12732539 .
- ^ Trantas E, Panopoulos N, Ververidis F (noviembre de 2009). "Ingeniería metabólica de la vía completa que conduce a la biosíntesis heteróloga de varios flavonoides y estilbenoides en Saccharomyces cerevisiae". Ingeniería metabólica . 11 (6): 355–66. doi : 10.1016 / j.ymben.2009.07.004 . PMID 19631278 .
- ^ Ververidis F, Trantas E, Douglas C, Vollmer G, Kretzschmar G, Panopoulos N (octubre de 2007). "Biotecnología de flavonoides y otros productos naturales derivados de fenilpropanoides. Parte II: Reconstrucción de vías multienzimáticas en plantas y microbios". Revista de biotecnología . 2 (10): 1235–49. doi : 10.1002 / biot.200700184 . PMID 17935118 . S2CID 5805643 .
- ^ "SynBio4Flav | impulsando la estandarización de partes biológicas sintéticas de alta complejidad" . synbio4flav.eu . Consultado el 16 de noviembre de 2020 .
- ^ "Plataforma basada en consorcios microbianos sintéticos para la producción de flavonoides utilizando biología sintética | H2020 | Comisión Europea" .
- ^ Yisa, Jonathan (2009). "Análisis fitoquímico y actividad antimicrobiana de Scoparia Dulcis y Nymphaea Lotus" . Revista Australiana de Ciencias Básicas y Aplicadas . 3 (4): 3975–3979. Archivado desde el original el 17 de octubre de 2013.
- ^ Bello IA, Ndukwe GI, Audu OT, Habila JD (octubre de 2011). "Un flavonoide bioactivo de Pavetta crassipes K. Schum" . Letras de Química Orgánica y Medicinal . 1 (1): 14. doi : 10.1186 / 2191-2858-1-14 . PMC 3305906 . PMID 22373191 .
- ^ Delcour JA (1985). "Un nuevo ensayo colorimétrico para flavonoides en cervezas Pilsner" . Revista del Instituto de Elaboración de la Cerveza . 91 : 37–40. doi : 10.1002 / j.2050-0416.1985.tb04303.x .
- ^ Lamaison, JL; Carnet, A (1991). "Teneurs en principaux flavonoides des fleurs de Cratageus monogyna Jacq et de Cratageus Laevigata (Poiret DC) en Fonction de la Vegetable". Plantes Medicinales Phytotherapie . 25 : 12-16.
- ^ Passicos E, Santarelli X, Coulon D (julio de 2004). "Acilación regioselectiva de flavonoides catalizada por lipasa de Candida antarctica inmovilizada a presión reducida". Cartas de biotecnología . 26 (13): 1073–6. doi : 10.1023 / B: BILE.0000032967.23282.15 . PMID 15218382 . S2CID 26716150 .
Lectura adicional [ editar ]
- Andersen ØM, Markham KR (2006). 'Flavonoides: Química, Bioquímica y Aplicaciones . Boca Raton, FL: CRC Press, Taylor & Francis. ISBN 978-0-8493-2021-7.
- Grotewold E (2006). La ciencia de los flavonoides . Nueva York: Springer. ISBN 978-0-387-74550-3.
- Harborne JB (1967). Bioquímica comparada de los flavonoides .
- retraso (1971). "La identificación sistemática de flavonoides". Revista de estructura molecular . 10 (2): 320. doi : 10.1016 / 0022-2860 (71) 87109-0 .
| Wikimedia Commons tiene medios relacionados con los flavonoides . |
Bases de datos [ editar ]
- Base de datos del USDA para el contenido de flavonoides de alimentos seleccionados, versión 3.1 (diciembre de 2013); datos para 506 alimentos en las 5 subclases de flavonoides proporcionados en un PDF separado actualizado en mayo de 2014
- FlavoDB, Centro de Bioinformática, India, noviembre de 2019