 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Dovprela |
| Otros nombres | PA-824 |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a619056 |
| Datos de licencia |
|
| Vías de administración | Oral |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Datos químicos y físicos | |
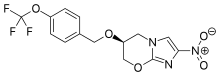
| Fórmula | C 14 H 12 F 3 N 3 O 5 |
| Masa molar | 359,261 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
La pretomanida es un medicamento antibiótico que se utiliza para el tratamiento de la tuberculosis multirresistente que afecta a los pulmones . [3] [4] Generalmente se usa junto con bedaquilina y linezolid . [3] Se toma por vía oral . [3]
Los efectos secundarios más comunes incluyen daño a los nervios , acné , vómitos, dolor de cabeza, niveles bajos de azúcar en sangre , diarrea e inflamación del hígado . [3] Es en el nitroimidazol clase de medicamentos. [5]
La pretomanida fue aprobada para uso médico en los Estados Unidos en agosto de 2019, [3] [6] y en la Unión Europea en julio de 2020. [2] La pretomanida fue desarrollada por TB Alliance . [7] [3] [8] La Administración de Drogas y Alimentos de los Estados Unidos (FDA) lo considera un medicamento de primera clase . [9]
Usos médicos
Pretomanid está indicado en combinación con bedaquilina y linezolid, en adultos, para el tratamiento de la tuberculosis (TB) pulmonar extensamente resistente a fármacos (XDR), intolerante al tratamiento o que no responde a múltiples fármacos (MDR). [2] [1]
Historia
Pretomanid es el nombre genérico común del novedoso compuesto de fármaco antibacteriano anteriormente llamado PA-824. [10] La pretomanida se denomina "Pa" en las abreviaturas del régimen, como BPaL. El prefijo "preto" del nombre del compuesto hace honor a Pretoria, Sudáfrica, el hogar de una oficina de desarrollo clínico de TB Alliance donde tuvo lugar gran parte del desarrollo del fármaco. El sufijo "manid" se utiliza para agrupar compuestos con estructuras químicas similares. Esta clase de fármaco se conoce como nitroimidazoles., nitroimidazooxazinas o nitroimidazopiranos. El desarrollo de este compuesto se inició debido a la urgente necesidad de nuevos fármacos antibacterianos eficaces contra cepas resistentes de tuberculosis. Además, los fármacos antituberculosos actuales son principalmente eficaces contra las bacterias replicantes y metabólicamente activas, lo que genera la necesidad de fármacos eficaces contra las infecciones bacterianas persistentes o latentes, como ocurre a menudo en los pacientes con tuberculosis. [11]
Descubrimiento y desarrollo preclínico
La pretomanida se identificó por primera vez en 2000, en una serie de 100 derivados de nitroimidazopirano sintetizados y probados para determinar su actividad antituberculosa, por PathoGenesis (ahora una subsidiaria de Novartis). [12] Es importante destacar que la pretomanida tiene actividad contra los aislados estáticos de M. tuberculosis que sobreviven en condiciones anaeróbicas, con una actividad bactericida comparable a la del fármaco existente metronidazol . La pretomanida requiere activación metabólica por parte de Mycobacterium para la actividad antibacteriana. La pretomanida no fue el compuesto más potente de la serie contra cultivos de M. tuberculosis, pero fue el más activo en ratones infectados después de la administración oral. La pretomanida oral fue activa contra la tuberculosis en ratones y cobayas en dosis toleradas de forma segura durante un máximo de 28 días. [11]
Aprobación limitada de la FDA
La Administración de Drogas y Alimentos de los Estados Unidos (FDA) aprobó la pretomanida solo en combinación con bedaquilina y linezolid para el tratamiento de una población limitada y específica de adultos con tuberculosis pulmonar resistente a múltiples medicamentos , intolerante al tratamiento o que no responde . [3] La pretomanida fue aprobada bajo la vía de población limitada (vía LPAD) para fármacos antibacterianos y antifúngicos. [3] La vía LPAD fue establecida por el Congreso bajo la Ley de Curas del Siglo XXI para acelerar el desarrollo y aprobación de antibacterianos y antifúngicosmedicamentos para tratar infecciones graves o potencialmente mortales en una población limitada de pacientes con necesidades insatisfechas. La pretomanida es solo el tercer fármaco contra la tuberculosis en recibir la aprobación de la FDA en más de 40 años. [3] [8]
La FDA otorgó la revisión de prioridad a Pretomanid y la designación de medicamento huérfano . [3] La FDA otorgó a The Global Alliance for TB Drug Development ( TB Alliance ) la aprobación de Pretomanid y un vale de revisión de prioridad de enfermedades tropicales. [3]
Referencias
- ^ a b "Tableta de pretomanida" . DailyMed . 15 de septiembre de 2019 . Consultado el 25 de septiembre de 2020 .
- ^ a b c "EPAR de Pretomanid FGK" . Agencia Europea de Medicamentos (EMA) . 24 de marzo de 2020 . Consultado el 25 de septiembre de 2020 .El texto se copió de esta fuente que es © Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ a b c d e f g h i j k "La FDA aprueba un nuevo fármaco para las formas de tuberculosis resistentes al tratamiento que afectan a los pulmones" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa). 14 de agosto de 2019 . Consultado el 28 de agosto de 2019 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ "Instantáneas de ensayos de drogas: Pretomanid" . EE.UU. Administración de Drogas y Alimentos (FDA) . 14 de agosto de 2019 . Consultado el 17 de marzo de 2020 .
- ^ "Nuestro oleoducto" . TB Alliance . Consultado el 18 de abril de 2019 .
- ^ "Paquete de aprobación de medicamentos: pretomanida" . EE.UU. Administración de Drogas y Alimentos (FDA) . 12 de septiembre de 2019 . Consultado el 25 de septiembre de 2020 .
- ^ "Pretomanid de la medicina de la tuberculosis entra en proceso de revisión reglamentaria en los Estados Unidos" . TB Alliance . Consultado el 18 de abril de 2019 .
- ↑ a b Abutaleb Y (14 de agosto de 2019). "Nuevo antibiótico aprobado para tuberculosis farmacorresistente" . The Washington Post .
- ^ "Aprobaciones de nuevas terapias farmacológicas 2019" . Administración de Drogas y Alimentos de EE. UU . 31 de diciembre de 2019 . Consultado el 15 de septiembre de 2020 .
- ^ "PA-824 tiene un nuevo nombre genérico: Pretomanid" . TB Alliance . Consultado el 18 de abril de 2019 .
- ^ a b Lenaerts AJ, Gruppo V, Marietta KS, Johnson CM, Driscoll DK, Tompkins NM, Rose JD, Reynolds RC, Orme IM (junio de 2005). "Pruebas preclínicas del nitroimidazopiran PA-824 para la actividad contra Mycobacterium tuberculosis en una serie de modelos in vitro e in vivo" . Agentes antimicrobianos y quimioterapia . 49 (6): 2294-301. doi : 10.1128 / AAC.49.6.2294-2301.2005 . PMC 1140539 . PMID 15917524 .
- ^ Stover CK, Warrener P, VanDevanter DR, Sherman DR, Arain TM, Langhorne MH, Anderson SW, Towell JA, Yuan Y, McMurray DN, Kreiswirth BN, Barry CE, Baker WR (2000). "Un candidato a fármaco nitroimidazopirano de molécula pequeña para el tratamiento de la tuberculosis". Naturaleza . 405 (6789): 962–6. Código bibliográfico : 2000Natur.405..962S . doi : 10.1038 / 35016103 . PMID 10879539 . S2CID 4428584 .
Enlaces externos
- "Pretomanid" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.