Saltar a navegación Saltar a búsqueda
Los inhibidores del proteasoma son fármacos que bloquean la acción de los proteasomas , complejos celulares que descomponen las proteínas . Están en estudio para el tratamiento del cáncer ; y tres están aprobados para su uso en el tratamiento del mieloma múltiple .
Mecanismo [ editar ]
Es probable que estén implicados múltiples mecanismos, pero la inhibición del proteasoma puede prevenir la degradación de factores proapoptóticos como la proteína p53 , permitiendo la activación de la muerte celular programada en células neoplásicas dependiente de la supresión de las vías proapoptóticas. Por ejemplo, bortezomib provoca un cambio rápido y dramático en los niveles de péptidos intracelulares. [1]
Ejemplos [ editar ]
- El primer inhibidor no peptídico del proteasoma descubierto fue el producto natural lactacistina . [2]
- Se ha propuesto el disulfiram como otro inhibidor del proteasoma. [3] [4] [5]
- También se ha propuesto epigalocatequina-3-galato . [6]
- Marizomib (salinosporamida A) ha iniciado ensayos clínicos para el mieloma múltiple .
- Oprozomib (ONX-0912), delanzomib (CEP-18770) también han comenzado ensayos clínicos. [7]
- La epoxomicina es un inhibidor selectivo de origen natural. [8]
- MG132 es un péptido sintetizado comúnmente utilizado para estudios in vitro .
- El beta-hidroxi beta-metilbutirato es un inhibidor del proteasoma en el músculo esquelético humano [9] [10] in vivo . [11]
Medicamentos aprobados [ editar ]
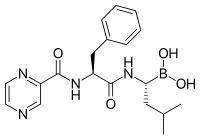
- Bortezomib ( Velcade ) fue aprobado en 2003. Este fue el primer inhibidor del proteasoma aprobado para su uso en los EE. UU. Su átomo de boro se une al sitio catalítico del proteasoma 26S . [12]
- El carfilzomib ( Kyprolis ) fue aprobado por la FDA para el mieloma múltiple en recaída y refractario en 2012. [13] Se une de manera irreversible e inhibe la actividad similar a la quimotripsina del proteasoma 20S .
- Ixazomib ( Ninlaro ) fue aprobado por la FDA en 2015 para su uso en combinación con lenalidomida y dexametasona para el tratamiento del mieloma múltiple después de al menos una terapia previa. Es el primer inhibidor del proteasoma disponible por vía oral [14]
Referencias [ editar ]
- ^ Gelman JS, Sironi J, Berezniuk I, Dasgupta S, Castro LM, Gozzo FC, Ferro ES, Fricker LD (2013). "Alteraciones del peptidoma intracelular en respuesta al inhibidor del proteasoma bortezomib" . PLOS ONE . 8 (1): e53263. doi : 10.1371 / journal.pone.0053263 . PMC 3538785 . PMID 23308178 .
- ^ Fenteany G, Standaert RF, Lane WS, Choi S, Corey EJ, Schreiber SL (1995). "Inhibición de las actividades del proteasoma y modificación de la treonina amino-terminal específica de la subunidad por lactacistina". Ciencia . 268 (5211): 726–31. doi : 10.1126 / science.7732382 . PMID 7732382 .
- ^ Lövborg H, Oberg F, Rickardson L, Gullbo J, Nygren P, Larsson R (marzo de 2006). "Inhibición de la actividad del proteasoma, translocación del factor nuclear-KappaB y supervivencia celular por el fármaco antialcoholismo disulfiram" . Revista Internacional de Cáncer . 118 (6): 1577–80. doi : 10.1002 / ijc.21534 . PMID 16206267 .
- ^ Wickström M, Danielsson K, Rickardson L, et al. (Enero de 2007). "Perfil farmacológico de disulfiram utilizando líneas de células tumorales humanas y células tumorales humanas de pacientes". Farmacología bioquímica . 73 (1): 25–33. doi : 10.1016 / j.bcp.2006.08.016 . PMID 17026967 .
- ^ Cvek B, Dvorak Z (agosto de 2008). "El valor de la inhibición del proteasoma en el cáncer. ¿Puede el antiguo fármaco, el disulfiram, tener un futuro brillante como un nuevo inhibidor del proteasoma?". Descubrimiento de drogas hoy . 13 (15-16): 716-22. doi : 10.1016 / j.drudis.2008.05.003 . PMID 18579431 .
- ^ Osanai K, Landis-Piwowar KR, Dou QP, Chan TH (agosto de 2007). "Un sustituyente para-amino en el anillo D del té verde polifenol epigalocatequina-3-galato como un nuevo inhibidor de proteasoma e inductor de apoptosis de células cancerosas" . Bioorg. Medicina. Chem . 15 (15): 5076–82. doi : 10.1016 / j.bmc.2007.05.041 . PMC 2963865 . PMID 17544279 .
- ^ "Avances actuales en enfoques basados en nuevos inhibidores de proteasoma para el tratamiento del mieloma múltiple en recaída / refractario" . 2011.
- ^ Meng, L .; et al. (1999). "La epoxomicina, un inhibidor del proteasoma potente y selectivo, exhibe actividad antiinflamatoria in vivo" . Proc. Natl. Acad. Sci. USA . 96 (18): 10403–10408. doi : 10.1073 / pnas.96.18.10403 . PMC 17900 . PMID 10468620 .
- ^ Wilson JM, Fitschen PJ, Campbell B, Wilson GJ, Zanchi N, Taylor L, Wilborn C, Kalman DS, Stout JR, Hoffman JR, Ziegenfuss TN, Lopez HL, Kreider RB, Smith-Ryan AE, Antonio J (febrero de 2013 ). "Stand de posición de la sociedad internacional de nutrición deportiva: beta-hidroxi-beta-metilbutirato (HMB)" . J. Int. Soc. Deportes. Nutr . 10 (1): 6. doi : 10.1186 / 1550-2783-10-6 . PMC 3568064 . PMID 23374455 .
La proteólisis del músculo esquelético aumenta en estados catabólicos como el ayuno, la inmovilización, el envejecimiento y las enfermedades [77]. Se ha demostrado que el HMB reduce la degradación de las proteínas del músculo esquelético tanto in vitro [72,73] como in vivo [78]. ... De hecho, se ha demostrado que el HMB disminuye la expresión del proteasoma [72] y la actividad [72,78-80] durante los estados catabólicos, atenuando así la degradación de las proteínas del músculo esquelético a través de la vía ubiquitina-proteasoma.
- ^ Suerte F, Pandey MC, Radhakrishna K (2015). "Efectos de los derivados de aminoácidos sobre las actividades físicas, mentales y fisiológicas". Crit. Rev. Food Sci. Nutr . 55 (13): 1793–1807. doi : 10.1080 / 10408398.2012.708368 . PMID 24279396 .
HMB, un derivado de la leucina, previene el daño muscular y aumenta la fuerza muscular al reducir la proteólisis inducida por el ejercicio en los músculos y también ayuda a aumentar la masa corporal magra.
- ^ Wilkinson DJ, Hossain T, Hill DS, Phillips BE, Crossland H, Williams J, Loughna P, Churchward-Venne TA, Breen L, Phillips SM, Etheridge T, Rathmacher JA, Smith K, Szewczyk NJ, Atherton PJ (junio de 2013 ). "Efectos de la leucina y su metabolito β-hidroxi-β-metilbutirato sobre el metabolismo de la proteína del músculo esquelético humano" (PDF) . J. Physiol . 591 (11): 2911–2923. doi : 10.1113 / jphysiol.2013.253203 . PMC 3690694 . PMID 23551944 . Consultado el 27 de mayo de 2016 .
aunque el HMB administrado por vía oral no produjo un aumento de la insulina plasmática, sí provocó una depresión en el MPB (-57%). Normalmente, las disminuciones posprandiales en MPB (de ~ 50%) se atribuyen a los efectos ahorradores de nitrógeno de la insulina, ya que el pinzamiento de la insulina en concentraciones posabsorbentes (5 μU ml − 1) mientras que la infusión continua de AA (18 gh − 1) no suprimió MPB (Greenhaff et al. 2008), por lo que optamos por no medir MPB en el grupo Leu, debido a una hiperinsulinemia anticipada (Fig. 3C). Por lo tanto, HMB reduce la MPB de una manera similar, pero independiente de, la insulina. Estos hallazgos están en línea con los informes de los efectos anticatabólicos del HMB que suprime el MPB en modelos preclínicos, mediante la atenuación de la proteólisis mediada por proteasoma en respuesta al LPS (Eley et al. 2008).
[ enlace muerto permanente ] - ^ Bonvini P, Zorzi E, Basso G, Rosolen A (2007). "La inhibición del proteasoma 26S mediada por bortezomib provoca la detención del ciclo celular e induce la apoptosis en el linfoma anaplásico de células grandes CD-30 +" . Leucemia . 21 (4): 838–42. doi : 10.1038 / sj.leu.2404528 . PMID 17268529 .
- ^ "Anuncios de prensa - la FDA aprueba Kyprolis para algunos pacientes con mieloma múltiple" . Administración de Drogas y Alimentos de los Estados Unidos. 20 de julio de 2012 . Consultado el 24 de abril de 2016 .
- ^ "Anuncios de prensa - la FDA aprueba Ninlaro, nuevo medicamento oral para tratar el mieloma múltiple" . Administración de Drogas y Alimentos de los Estados Unidos . Consultado el 24 de abril de 2016 .