 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / K æ p t ə p r ɪ l / |
| Nombres comerciales | Capoten, otros |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a682823 |
Categoría de embarazo |
|
| Vías de administración | Oral |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 70–75% |
| Metabolismo | Hígado |
| Vida media de eliminación | 1,9 horas |
| Excreción | Riñón |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Ligando PDB | |
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.057.806 |
| Datos químicos y físicos | |
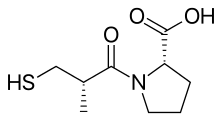
| Fórmula | C 9 H 15 N O 3 S |
| Masa molar | 217,28 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| (verificar) | |
El captopril , vendido bajo la marca Capoten entre otros, es un inhibidor de la enzima convertidora de angiotensina (ECA) que se usa para el tratamiento de la hipertensión y algunos tipos de insuficiencia cardíaca congestiva .
Fue patentado en 1976 y aprobado para uso médico en 1980. [2]
Usos médicos [ editar ]
Los principales usos de captopril se basan en su vasodilatación e inhibición de algunas actividades de la función renal. Estos beneficios se ven más claramente en: 1) Hipertensión 2) Condiciones cardíacas como insuficiencia cardíaca congestiva y después de un infarto de miocardio 3) Preservación de la función renal en la nefropatía diabética .
Además, ha mostrado propiedades que mejoran el estado de ánimo en algunos pacientes. Esto es consistente con la observación de que los modelos de cribado en animales indican una supuesta actividad antidepresiva para este compuesto, aunque un estudio ha sido negativo. No se han informado ensayos clínicos formales en pacientes deprimidos. [4]
También se ha investigado para su uso en el tratamiento del cáncer. [5] También se informó que los estereoisómeros de captopril inhiben algunas metalo -β-lactamasas . [6]
Efectos adversos [ editar ]
Los efectos adversos del captopril incluyen tos debido al aumento de los niveles plasmáticos de bradicinina, angioedema , agranulocitosis , proteinuria , hiperpotasemia , alteración del gusto , teratogenicidad , hipotensión postural , insuficiencia renal aguda y leucopenia . [7] A excepción de la hipotensión postural, que se produce debido al modo de acción corto y rápido del captopril, la mayoría de los efectos secundarios mencionados son comunes para todos los inhibidores de la ECA. Entre estos, la tos es el efecto adverso más común. Hiperpotasemiapuede ocurrir, especialmente si se usa con otros medicamentos que elevan el nivel de potasio en sangre, como los diuréticos ahorradores de potasio . Otros efectos secundarios son:
- Picor
- Dolor de cabeza
- Taquicardia
- Dolor de pecho
- Palpitaciones
- Debilidad
El perfil de reacciones adversas a medicamentos (RAM) de captopril es similar al de otros inhibidores de la ECA , siendo la tos la RAM más común. [8] Sin embargo, el captopril también se asocia comúnmente con erupciones cutáneas y alteraciones del gusto (metálicas o pérdida del gusto), que se atribuyen a la única fracción tiol . [9]
El captopril también tiene un perfil farmacocinético relativamente pobre. La corta vida media requiere dos o tres dosis diarias, lo que puede reducir el cumplimiento del paciente .
Sobredosis [ editar ]
La sobredosis de inhibidores de la ECA se puede tratar con naloxona . [10] [11] [12]
Historia [ editar ]
A finales de la década de 1960, John Vane, del Royal College of Surgeons of England, estaba trabajando en los mecanismos mediante los cuales el cuerpo regula la presión arterial. [13] Se le unió Sérgio Henrique Ferreira de Brasil, que había estado estudiando el veneno de una víbora brasileña, la jararaca ( Bothrops jararaca ) , y trajo una muestra del veneno de la víbora. El equipo de Vane descubrió que uno de los péptidos del veneno inhibía selectivamente la acción de la enzima convertidora de angiotensina.(ACE), que se pensaba que funcionaba en la regulación de la presión arterial; el veneno de serpiente funciona deprimiendo gravemente la presión arterial. Durante la década de 1970, se descubrió que la ECA elevaba la presión arterial al controlar la liberación de agua y sales de los riñones.
El captopril, un análogo del péptido inhibidor de la ECA del veneno de serpiente, fue sintetizado por primera vez en 1975 por tres investigadores de la compañía farmacéutica estadounidense ER Squibb & Sons Pharmaceuticals (ahora Bristol-Myers Squibb ): Miguel Ondetti, Bernard Rubin y David Cushman. Squibb solicitó la protección de patente de EE. UU. Para el medicamento en febrero de 1976, la patente de EE. UU. 4.046.889 se otorgó en septiembre de 1977 y el captopril fue aprobado para uso médico en 1980. [2] Fue el primer inhibidor de la ECA desarrollado y se consideró un gran avance tanto por su mecanismo de acción y también por el proceso de desarrollo. [14] [15] En la década de 1980, Vane recibió el premio Nobel y fue nombrado caballero por su trabajo y Ferreira recibió la Orden Nacional al Mérito Científico. desde Brasil.
El desarrollo de captopril fue uno de los primeros éxitos del revolucionario concepto de diseño de fármacos basado en ligandos . El sistema renina-angiotensina-aldosterona había sido ampliamente estudiado a mediados del siglo XX, y este sistema presentaba varios objetivos oportunos en el desarrollo de nuevos tratamientos para la hipertensión. Los dos primeros objetivos que se intentaron fueron renina y ACE . Captopril fue la culminación de los esfuerzos de los laboratorios de Squibb para desarrollar un inhibidor de la ECA.
Ondetti, Cushman y sus colegas se basaron en el trabajo realizado en la década de 1960 por un equipo de investigadores dirigido por John Vane en el Royal College of Surgeons of England . El primer avance lo realizó Kevin KF Ng [16] [17] [18] en 1967, cuando descubrió que la conversión de angiotensina I en angiotensina II tenía lugar en la circulación pulmonar en lugar de en el plasma . Por el contrario, Sergio Ferreira [19] encontró que la bradicinina desaparecía en su paso por la circulación pulmonar. Se pensó que la conversión de angiotensina I en angiotensina II y la inactivación de bradicinina estaban mediadas por la misma enzima.
En 1970, utilizando el factor potenciador de bradicinina (BPF) proporcionado por Sergio Ferreira, [20] Ng y Vane encontraron que la conversión de angiotensina I en angiotensina II se inhibía durante su paso a través de la circulación pulmonar. Más tarde se descubrió que el BPF era un péptido en el veneno de una víbora cabeza de lanza ( Bothrops jararaca ) , que era un "inhibidor de producto recolectado" de la enzima convertidora. El captopril se desarrolló a partir de este péptido después de que se descubrió mediante una modificación basada en QSAR que el resto sulfhidrilo terminal del péptido proporcionaba una alta potencia de inhibición de la ECA . [21]
El captopril obtuvo la aprobación de la FDA el 6 de abril de 1981. El fármaco se convirtió en un medicamento genérico en los EE. UU. En febrero de 1996, cuando expiró la exclusividad de mercado de Bristol-Myers Squibb para el captopril.
Síntesis química [ editar ]
En la figura se muestra una síntesis química de captopril mediante el tratamiento de L -prolina con cloruro de (2S) -3-acetiltio-2-metilpropanoilo en condiciones básicas (NaOH), seguida de aminólisis del grupo acetilo protector para desenmascarar el tiol libre del fármaco figura a la derecha. [22]
| Síntesis de captopril 1 | Síntesis de captopril 2 |
|---|---|
Síntesis de captopril de Shimazaki, Watanabe, et al. | Patentes: [23] Diseño y síntesis: [24] [25] Síntesis mejorada: [26] |
Procedimiento 2 sacado de la patente US4105776. Consulte los ejemplos 28, 29a y 36.
Mecanismo de acción [ editar ]
El captopril bloquea la conversión de angiotensina I en angiotensina II y previene la degradación de las prostaglandinas vasodilatadoras , inhibiendo así la vasoconstricción y promoviendo la vasodilatación sistémica . [27]
Farmacocinética [ editar ]
A diferencia de la mayoría de los inhibidores de la ECA, captopril no se administra como profármaco (el único otro es lisinopril ). [28] Aproximadamente el 70% del captopril administrado por vía oral se absorbe. La biodisponibilidad se reduce por la presencia de alimentos en el estómago. Se metaboliza parcialmente y se excreta parcialmente sin cambios en la orina . [29]
Ver también [ editar ]
- Prueba de provocación con captopril
- Prueba de supresión de captopril
Referencias [ editar ]
- ^ https://www.ema.europa.eu/documents/psusa/captopril-list-nationally-authorised-medicinal-products-psusa/00000535/202004_en.pdf
- ↑ a b Fischer J, Ganellin CR (2006). Descubrimiento de fármacos de base análoga . John Wiley e hijos. pag. 467. ISBN 9783527607495.
- ^ Akif M, Georgiadis D, Mahajan A, Dive V, Sturrock ED, Isaac RE, Acharya KR (julio de 2010). "Estructuras cristalinas de alta resolución de la enzima convertidora de angiotensina de Drosophila melanogaster en complejo con nuevos inhibidores y fármacos antihipertensivos". Revista de Biología Molecular . 400 (3): 502-17. doi : 10.1016 / j.jmb.2010.05.024 . PMID 20488190 .
- ^ Murphy DL, Mitchell PB, Potter WZ. "Nuevos enfoques farmacológicos para el tratamiento de la depresión" . Archivado desde el original el 12 de mayo de 2008.
- ^ Attoub S, Gaben AM, Al-Salam S, Al Sultan MA, John A, Nicholls MG, et al. (Septiembre de 2008). "Captopril como potencial inhibidor del crecimiento de tumores pulmonares y metástasis". Anales de la Academia de Ciencias de Nueva York . 1138 (1): 65–72. Código bibliográfico : 2008NYASA1138 ... 65A . doi : 10.1196 / annals.1414.011 . PMID 18837885 . S2CID 24210204 .
- ^ Brem J, van Berkel SS, Zollman D, Lee SY, Gileadi O, McHugh PJ, et al. (Enero de 2016). "Base estructural de la inhibición de metalo-β-lactamasa por estereoisómeros de captopril" . Agentes antimicrobianos y quimioterapia . 60 (1): 142–50. doi : 10.1128 / AAC.01335-15 . PMC 4704194 . PMID 26482303 .
- ^ "Captopril (inhibidor de la ECA): efectos secundarios" . abrazador de vida. 2008-07-09. Archivado desde el original el 14 de agosto de 2009 . Consultado el 2 de mayo de 2009 .
- ^ Rossi S, ed. (2006). Manual de medicamentos de Australia . Adelaide: Manual de medicamentos de Australia.
- ^ Atkinson AB, Robertson JI (octubre de 1979). "Captopril en el tratamiento de la hipertensión clínica y la insuficiencia cardíaca". Lancet . 2 (8147): 836–9. doi : 10.1016 / S0140-6736 (79) 92186-X . PMID 90928 . S2CID 32209360 .
- ^ Nelson L, Howland MA, Lewin NA, Smith SW, Goldfrank R, Hoffman RS, Flomenbaum N (2019). Emergencias toxicológicas de Goldfrank . Nueva York: McGraw-Hill Education. pag. 953. ISBN 978-1-259-85961-8.
- ^ Efectos secundarios de analgésicos y antiinflamatorios de Meyler, Jeffrey K. Aronson, página 120.
- ^ Ajayi AA, Campbell BC, Rubin PC, Reid JL (noviembre de 1985). "Efecto de la naloxona sobre las acciones de captopril". Farmacología clínica y terapéutica . 38 (5): 560–5. doi : 10.1038 / clpt.1985.224 . PMID 2996820 . S2CID 35799800 .
- ^ Cuervo, James Mitchell. "Drogas con mordedura: los poderes curativos de los venenos" . Nuevo científico . Consultado el 30 de julio de 2020 .
- ^ Bryan J (2009). "Desde el veneno de serpiente hasta el inhibidor de la ECA, el descubrimiento y el aumento de captopril" . Revista farmacéutica . Consultado el 8 de enero de 2015 .
- ^ Blankley CJ (septiembre de 1985). "Crónicas del descubrimiento de drogas, vol. 2". Revista de Ciencias Farmacéuticas . 74 (9): 1029-30. doi : 10.1002 / jps.2600740942 .
- ^ Ng KK, Vane JR (noviembre de 1967). "Conversión de angiotensina I en angiotensina II". Naturaleza . 216 (5117): 762–6. Código bibliográfico : 1967Natur.216..762N . doi : 10.1038 / 216762a0 . PMID 4294626 . S2CID 4289093 .
- ^ Ng KK, Vane JR (abril de 1968). "Destino de la angiotensina I en la circulación". Naturaleza . 218 (5137): 144–50. Código Bibliográfico : 1968Natur.218..144N . doi : 10.1038 / 218144a0 . PMID 4296306 . S2CID 4174541 .
- ^ Ng KK, Vane JR (marzo de 1970). "Algunas propiedades de la enzima convertidora de angiotensina en el pulmón in vivo". Naturaleza . 225 (5238): 1142–4. Código Bibliográfico : 1970Natur.225.1142N . doi : 10.1038 / 2251142b0 . PMID 4313869 . S2CID 4200012 .
- ^ Ferreira SH, Vane JR (junio de 1967). "La desaparición de bradicinina y eledoisina en la circulación y los lechos vasculares del gato" . Revista británica de farmacología y quimioterapia . 30 (2): 417–24. doi : 10.1111 / j.1476-5381.1967.tb02148.x . PMC 1557274 . PMID 6036419 .
- ^ Smith CG, Vane JR (mayo de 2003). "El descubrimiento del captopril". Revista FASEB . 17 (8): 788–9. doi : 10.1096 / fj.03-0093life . PMID 12724335 . S2CID 45232683 .
- ^ Patlak M (marzo de 2004). "Del veneno de víbora al diseño de fármacos: tratamiento de la hipertensión". Revista FASEB . 18 (3): 421. doi : 10.1096 / fj.03-1398bkt . PMID 15003987 . S2CID 1045315 .
- ↑ Shimazaki M, Hasegawa J, Kan K, Nomura K, Nose Y, Kondo H, Ohashi T, Watanabe K (1982). "Síntesis de captopril a partir de un .BETA.-hidroxiácido ópticamente activo" . Chem. Pharm. Bull . 30 (9): 3139–3146. doi : 10.1248 / cpb.30.3139 .
- ^ MA Ondetti, DW Cushman, DE 2703828 ; eidem, Patente de EE.UU. 4.046.889 y Patente de EE.UU. 4.105.776 (1977, 1977, 1978, todas de Squibb).
- ^ Ondetti MA, Rubin B, Cushman DW (abril de 1977). "Diseño de inhibidores específicos de la enzima convertidora de angiotensina: nueva clase de antihipertensivos activos por vía oral". Ciencia . 196 (4288): 441–4. Código Bibliográfico : 1977Sci ... 196..441O . doi : 10.1126 / science.191908 . PMID 191908 .
- ^ Cushman DW, Cheung HS, Sabo EF, Ondetti MA (diciembre de 1977). "Diseño de potentes inhibidores competitivos de la enzima convertidora de angiotensina. Aminoácidos carboxialcanoílicos y mercaptoalcanoílicos". Bioquímica . 16 (25): 5484–91. doi : 10.1021 / bi00644a014 . PMID 200262 .
- ^ Nam DH, Lee CS, Ryu DD (diciembre de 1984). "Una síntesis mejorada de captopril". Revista de Ciencias Farmacéuticas . 73 (12): 1843–4. doi : 10.1002 / jps.2600731251 . PMID 6396401 .
- ↑ Vallerand AH, Sanoski CA, Deglin JH (5 de junio de 2014). Guía de medicamentos de Davis para enfermeras (decimocuarta ed.). Filadelfia. ISBN 978-0-8036-4085-6. OCLC 881473728 .
- ^ Brown NJ, Vaughan DE (abril de 1998). "Inhibidores de la enzima convertidora de angiotensina" . Circulación . 97 (14): 1411-20. doi : 10.1161 / 01.cir.97.14.1411 . PMID 9577953 .
- ^ Duchin KL, McKinstry DN, Cohen AI, Migdalof BH (abril de 1988). "Farmacocinética del captopril en sujetos sanos y en pacientes con enfermedades cardiovasculares". Farmacocinética clínica . 14 (4): 241–59. doi : 10.2165 / 00003088-198814040-00002 . PMID 3292102 . S2CID 46614471 .
Enlaces externos [ editar ]
- "Captopril" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- Patente de Estados Unidos 4.046.889