 | |
_carbonate.jpg/440px-Cobalt(2)_carbonate.jpg) | |
| Nombres | |
|---|---|
| Nombre IUPAC Carbonato de cobalto (II) | |
| Otros nombres Carbonato cobaltoso; sal de cobalto (II) | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.007.428 |
PubChem CID | |
| UNII |
|
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| CoCO 3 | |
| Masa molar | 118,941 g / mol |
| Apariencia | cristales rojos / rosados (anhidros) polvo cristalino rosado, violeta, rojo (hexahidrato) |
| Densidad | 4,13 g / cm 3 |
| Punto de fusion | 427 ° C (801 ° F; 700 K) [2] se descompone antes de fundirse en óxido de cobalto (II) (anhidro) 140 ° C (284 ° F; 413 K) se descompone (hexahidrato) |
| El carbonato de cobalto (II) es insoluble en agua destilada. | |
Producto de solubilidad ( K sp ) | 1.0 · 10 −10 [1] |
| Solubilidad | soluble en ácido insignificante en alcohol , acetato de metilo insoluble en etanol |
Índice de refracción ( n D ) | 1.855 |
| Estructura | |
Trigonal romboédrico (anhidro) (hexahidrato) | |
| Termoquímica | |
Entropía molar estándar ( S | 79,9 J / mol · K [2] |
| −722,6 kJ / mol [2] | |
Energía libre de Gibbs (Δ f G ˚) | -651 kJ / mol [2] |
| Peligros | |
| Pictogramas GHS | [3] |
| Palabra de señal GHS | Advertencia |
Declaraciones de peligro GHS | H302 , H315 , H317 , H319 , H335 , H351 [3] |
Consejos de prudencia del SGA | P261 , P280 , P305 + 351 + 338 [3] |
| NFPA 704 (diamante de fuego) |  2 0 0 |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis mediana ) | 640 mg / kg (oral, ratas) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El carbonato de cobalto (II) es el compuesto inorgánico de fórmula CoCO 3 . Este sólido paramagnético rojizo es un intermedio en la purificación hidrometalúrgica del cobalto de sus minerales. Es un pigmento inorgánico y un precursor de los catalizadores . [4] El carbonato de cobalto (II) también se presenta como el raro mineral rojo / rosa esferocobaltita . [5]
Preparación y estructura [ editar ]
Se prepara combinando soluciones de sulfato cobaltoso y bicarbonato de sodio :
- CoSO 4 + 2 NaHCO 3 → CoCO 3 + Na 2 SO 4 + H 2 O + CO 2
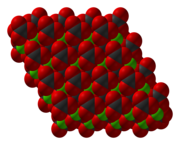
El CoCO 3 adopta una estructura similar a la calcita , que consiste en cobalto en una geometría de coordinación octaédrica . [6]
Reacciones [ editar ]
Calentando el carbonato, se procede de manera típica a la calcinación , excepto que el material está parcialmente oxidado:
- 6 CoCO 3 + O 2 → 2 Co 3 O 4 + 6 CO 2
El Co 3 O 4 resultante se convierte reversiblemente en CoO a altas temperaturas. [7] Como la mayoría de los carbonatos de metales de transición, el carbonato de cobalto es insoluble en agua, pero es fácilmente atacado por ácidos minerales:
- CoCO 3 + 2 HCl + 5 H 2 O → [Co (H 2 O) 6 ] Cl 2 + CO 2
Se utiliza para preparar muchos complejos de coordinación. La reacción de carbonato de cobalto (II) y acetilacetona en presencia de peróxido de hidrógeno da tris (acetilacetonato) cobalto (III) . [8] Estos complejos son quirales y, a menudo, pueden resolverse en los enantiómeros individuales.
Usos [ editar ]
El carbonato de cobalto es un precursor del carbonilo de cobalto y varias sales de cobalto. Es un componente de los complementos alimenticios ya que el cobalto es un elemento esencial . Es un precursor de los esmaltes de cerámica azul, famoso en el caso de Delftware .
Ocurrencia natural [ editar ]
La esferocobaltita moderadamente rara es la forma natural del carbonato de cobalto, con buenos ejemplares procedentes especialmente de la República del Congo . La cobaltocalcita es una variedad de calcita cobaltífera que tiene un hábito bastante similar a la esferocobaltita. [5]
Seguridad [ editar ]
El compuesto es nocivo si se ingiere e irrita los ojos y la piel. [ aclaración necesaria ]
Referencias [ editar ]
- ^ "Copia archivada" . Archivado desde el original el 15 de junio de 2012 . Consultado el 17 de mayo de 2012 . CS1 maint: parámetro desaconsejado ( enlace ) CS1 maint: copia archivada como título ( enlace )
- ^ a b c d http://chemister.ru/Database/properties-en.php?dbid=1&id=573
- ^ a b c Sigma-Aldrich Co. , Carbonato de cobalto (II) . Consultado el 6 de mayo de 2014.
- ^ John Dallas Donaldson, Detmar Beyersmann, "Cobalto y compuestos de cobalto" en Enciclopedia de química industrial de Ullmann, Wiley-VCH, Weinheim, 2005. doi : 10.1002 / 14356007.a07_281.pub2
- ^ a b "Esferocobaltita: información y datos del mineral de esferocobaltita" . www.mindat.org . Consultado el 7 de agosto de 2018 . CS1 maint: discouraged parameter (link)
- ^ Pertlik, F. (1986). "Estructuras de carbonato de cobalto (II) y carbonato de níquel (II) sintetizados hidrotermalmente". Acta Crystallographica Sección C . 42 : 4-5. doi : 10.1107 / S0108270186097524 .
- ^ GA El-Shobaky, AS Ahmad, AN Al-Noaimi y HG El-Shobaky Journal of Thermal Analysis and Calorimetry 1996, Volumen 46, Número 6, pp.1801-1808. resumen en línea
- ^ Bryant, Burl E .; Fernelius, W. Conard (1957). "Acetilacetonato de cobalto (III)". Síntesis inorgánica . págs. 188-189. doi : 10.1002 / 9780470132364.ch53 . ISBN 9780470132364.
Enlaces externos [ editar ]
- Medios relacionados con el carbonato de cobalto (II) en Wikimedia Commons