Lisina
La lisina (símbolo Lys o K ) [2] es un α-aminoácido que se utiliza en la biosíntesis de proteínas . Contiene un α-amino grupo (que se encuentra en la protonado -NH 3 + forma en condiciones biológicas), un grupo de ácido α-carboxílico (que está en la -COO desprotonada - forma en condiciones biológicas), y una lisil cadena lateral ( (CH 2 ) 4 NH 2 ), clasificándolo como un aminoácido alifático básico , cargado (a pH fisiológico) . Está codificado por los codones.AAA y AAG. Como casi todos los demás aminoácidos, el carbono α es quiral y la lisina puede referirse a un enantiómero o una mezcla racémica de ambos. Para el propósito de este artículo, lisina se referirá al enantiómero biológicamente activo L-lisina, donde el carbono α está en la configuración S.
El cuerpo humano no puede sintetizar lisina. Es esencial en el ser humano y debe obtenerse de la dieta. En los organismos que la lisina sintetizan, tiene dos principales rutas biosintéticas , las diaminopimelato y a-aminoadipato vías, que emplean distintas enzimas y sustratos y se encuentran en diversos organismos. El catabolismo de la lisina se produce a través de una de varias vías, la más común de las cuales es la vía de la sacaropina .
La lisina desempeña varias funciones en los seres humanos, principalmente la proteinogénesis , pero también en la reticulación de los polipéptidos de colágeno , la absorción de nutrientes minerales esenciales y la producción de carnitina , que es clave en el metabolismo de los ácidos grasos . La lisina también participa a menudo en las modificaciones de las histonas y, por lo tanto, afecta al epigenoma . El grupo ε- amino participa a menudo en la formación de puentes de hidrógeno y como base general en la catálisis . El grupo ε- amonio (NH 3 + ) está unido al cuarto carbono del carbono α, que está unido al grupo carboxilo (C = OOH). [3]
Debido a su importancia en varios procesos biológicos, la falta de lisina puede conducir a varios estados patológicos que incluyen tejidos conectivos defectuosos, metabolismo deficiente de los ácidos grasos, anemia y deficiencia sistémica de proteínas y energía. Por el contrario, una sobreabundancia de lisina, causada por un catabolismo ineficaz, puede provocar graves trastornos neurológicos .
La lisina fue aislada por primera vez por el químico biológico alemán Ferdinand Heinrich Edmund Drechsel en 1889 a partir de la proteína caseína en la leche. [4] Lo llamó " lisina ". [5] En 1902, los químicos alemanes Emil Fischer y Fritz Weigert determinaron la estructura química de la lisina sintetizándola. [6]
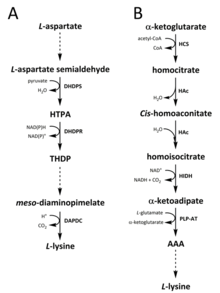
En la naturaleza se han identificado dos vías para la síntesis de lisina. La vía del diaminopimelato (DAP) pertenece a la familia biosintética derivada del aspartato , que también participa en la síntesis de treonina , metionina e isoleucina . [7] [8] Considerando que la vía del α-aminoadipato (AAA) es parte de la familia biosintética del glutamato . [9] [10]