La mecánica molecular utiliza la mecánica clásica para modelar sistemas moleculares . Se asume que la aproximación de Born-Oppenheimer es válida y la energía potencial de todos los sistemas se calcula en función de las coordenadas nucleares utilizando campos de fuerza . La mecánica molecular se puede utilizar para estudiar sistemas de moléculas que varían en tamaño y complejidad desde pequeños a grandes sistemas biológicos o conjuntos de materiales con muchos miles a millones de átomos.
Los métodos de mecánica molecular totalmente atomistas tienen las siguientes propiedades:
- Cada átomo se simula como una partícula.
- A cada partícula se le asigna un radio (generalmente el radio de van der Waals ), polarizabilidad y una carga neta constante (generalmente derivada de cálculos cuánticos y / o experimentos)
- Las interacciones enlazadas se tratan como resortes con una distancia de equilibrio igual a la longitud de enlace experimental o calculada
Son posibles variantes sobre este tema. Por ejemplo, muchas simulaciones han utilizado históricamente una representación de átomos unidos en la que cada grupo metilo terminal o unidad de metileno intermedia se consideraba una partícula, y los sistemas de proteínas grandes se simulan comúnmente utilizando un modelo de perlas que asigna de dos a cuatro partículas por aminoácido .
Forma funcional [ editar ]
Esta sección no cita ninguna fuente . ( Diciembre de 2017 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
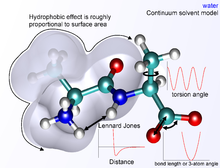
La siguiente abstracción funcional, denominada función potencial interatómica o campo de fuerza en química, calcula la energía potencial (E) del sistema molecular en una conformación dada como una suma de términos de energía individuales.
donde los componentes de las contribuciones covalentes y no covalentes vienen dados por las siguientes sumas:
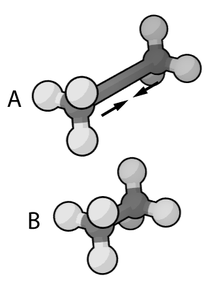
La forma funcional exacta de la función potencial , o campo de fuerza, depende del programa de simulación particular que se utilice. Generalmente, los términos de enlace y ángulo se modelan como potenciales armónicos centrados en valores de equilibrio de longitud de enlace derivados de experimentos o cálculos teóricos de la estructura electrónica realizados con software que hace cálculos de tipo ab-initio como Gaussian . Para una reproducción precisa de los espectros vibracionales, el potencial Morsese puede utilizar en su lugar, a un costo computacional. Los términos diédricos o torsionales suelen tener múltiples mínimos y, por lo tanto, no pueden modelarse como osciladores armónicos, aunque su forma funcional específica varía con la implementación. Esta clase de términos puede incluir términos diédricos impropios , que funcionan como factores de corrección para desviaciones fuera del plano (por ejemplo, se pueden usar para mantener planos los anillos de benceno o para corregir la geometría y quiralidad de los átomos tetraédricos en una representación de átomos unidos ).
Los términos no enlazados son mucho más costosos computacionalmente para calcularlos en su totalidad, ya que un átomo típico está enlazado solo con algunos de sus vecinos, pero interactúa con todos los demás átomos de la molécula. Afortunadamente, el término van der Waals decae rápidamente. Por lo general, se modela utilizando un potencial de Lennard-Jones de 6-12 , lo que significa que las fuerzas de atracción disminuyen con la distancia como r -6 y las fuerzas repulsivas como r -12 , donde r representa la distancia entre dos átomos. La parte repulsiva r −12Sin embargo, no es físico, porque la repulsión aumenta exponencialmente. La descripción de las fuerzas de van der Waals por el potencial de Lennard-Jones 6–12 introduce inexactitudes, que se vuelven significativas en distancias cortas. [1] Generalmente, se utiliza un radio de corte para acelerar el cálculo, de modo que los pares de átomos cuyas distancias son mayores que el corte tengan una energía de interacción de van der Waals de cero.
Los términos electrostáticos son notoriamente difíciles de calcular bien porque no disminuyen rápidamente con la distancia, y las interacciones electrostáticas de largo alcance son a menudo características importantes del sistema en estudio (especialmente para las proteínas ). La forma funcional básica es el potencial de Coulomb , que solo cae cuando r −1. Se utilizan diversos métodos para abordar este problema, siendo el más simple un radio de corte similar al utilizado para los términos de van der Waals. Sin embargo, esto introduce una fuerte discontinuidad entre los átomos del interior y los átomos fuera del radio. Las funciones de conmutación o escalado que modulan la energía electrostática aparente son métodos algo más precisos que multiplican la energía calculada por un factor de escala que varía suavemente de 0 a 1 en los radios de corte exterior e interior. Otros métodos más sofisticados pero computacionalmente intensivos son la malla de partículas Ewald (PME) y el algoritmo multipolar .
Además de la forma funcional de cada término de energía, se deben asignar parámetros a una función de energía útil para las constantes de fuerza, los multiplicadores de van der Waals y otros términos constantes. Estos términos, junto con los valores de enlace de equilibrio, ángulo y diedro, valores de carga parcial, masas y radios atómicos y definiciones de funciones de energía, se denominan colectivamente campo de fuerza . La parametrización se realiza típicamente por acuerdo con los valores experimentales y los resultados de los cálculos teóricos. El campo de fuerza de Norman L.Allinger en la última versión MM4 calcula los calores de formación de hidrocarburos con un error rms de 0.35 kcal / mol, espectros vibracionales con un error rms de 24 cm −1 , barreras rotacionales con un error rms de 2.2 °, Longitudes de enlace CC dentro de 0,004 Å y ángulos CCC dentro de 1 ° . [2] Las versiones posteriores de MM4 también cubren compuestos con heteroátomos como las aminas alifáticas. [3]
Cada campo de fuerza está parametrizado para ser coherente internamente, pero los parámetros generalmente no son transferibles de un campo de fuerza a otro.
Áreas de aplicación [ editar ]
El uso principal de la mecánica molecular se encuentra en el campo de la dinámica molecular . Este utiliza el campo de fuerza para calcular las fuerzas que actúan sobre cada partícula y un integrador adecuado para modelar la dinámica de las partículas y predecir trayectorias. Con un muestreo suficiente y sujeto a la hipótesis ergódica , las trayectorias de dinámica molecular se pueden utilizar para estimar los parámetros termodinámicos de un sistema o sondear las propiedades cinéticas, como las velocidades y los mecanismos de reacción.
Otra aplicación de la mecánica molecular es la minimización de energía, por lo que el campo de fuerza se utiliza como criterio de optimización . Este método utiliza un algoritmo apropiado (por ejemplo, el descenso más pronunciado) para encontrar la estructura molecular de un mínimo de energía local. Estos mínimos corresponden a confórmeros estables de la molécula (en el campo de fuerza elegido) y el movimiento molecular se puede modelar como vibraciones e interconversiones entre estos confórmeros estables. Por lo tanto, es común encontrar métodos de minimización de energía local combinados con optimización de energía global, para encontrar el mínimo de energía global (y otros estados de baja energía). A temperatura finita, la molécula pasa la mayor parte de su tiempo en estos estados bajos, que dominan así las propiedades moleculares. La optimización global se puede lograr mediante el recocido simulado , el algoritmo Metropolis y otros métodos de Monte Carlo., o utilizando diferentes métodos deterministas de optimización discreta o continua. Si bien el campo de fuerza representa solo el componente entálpico de la energía libre (y solo este componente se incluye durante la minimización de energía), es posible incluir el componente entrópico mediante el uso de métodos adicionales, como el análisis en modo normal .
Las funciones de energía potencial de la mecánica molecular se han utilizado para calcular las constantes de unión, [4] [5] [6] [7] [8] cinética de plegamiento de proteínas, [9] equilibrios de protonación, [10] coordenadas del sitio activo , [6] [11 ] y diseñar sitios de enlace . [12]
Medio ambiente y solvatación [ editar ]
Esta sección no cita ninguna fuente . ( Diciembre de 2017 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
En mecánica molecular, existen varias formas de definir el entorno que rodea a una molécula o moléculas de interés. Un sistema se puede simular en el vacío (lo que se denomina simulación en fase gaseosa) sin un entorno circundante, pero esto generalmente no es deseable porque introduce artefactos en la geometría molecular, especialmente en moléculas cargadas. Las cargas superficiales que normalmente interactuarían con las moléculas de disolvente, en cambio, interactúan entre sí, produciendo conformaciones moleculares que es poco probable que estén presentes en cualquier otro entorno. La mejor manera de solvatar un sistema es colocar moléculas de agua explícitas en el cuadro de simulación con las moléculas de interés y tratar las moléculas de agua como partículas interactuantes como las de la molécula. Una variedad de modelos de agua.existen con niveles crecientes de complejidad, representando el agua como una simple esfera dura (un modelo de átomos unidos), como tres partículas separadas con ángulos de enlace fijos, o incluso como cuatro o cinco centros de interacción separados para dar cuenta de los electrones no apareados en el átomo de oxígeno. A medida que los modelos de agua se vuelven más complejos, las simulaciones relacionadas se vuelven más intensivas en computación. Se ha encontrado un método de compromiso en la solvatación implícita, que reemplaza las moléculas de agua representadas explícitamente con una expresión matemática que reproduce el comportamiento promedio de las moléculas de agua (u otros disolventes como los lípidos). Este método es útil para prevenir los artefactos que surgen de las simulaciones de vacío y reproduce bien las propiedades del solvente a granel, pero no puede reproducir situaciones en las que las moléculas de agua individuales tienen interacciones interesantes con las moléculas en estudio.
Paquetes de software [ editar ]
Ésta es una lista limitada; hay muchos más paquetes disponibles.
- Abulón
- ACEMD - GPU MD [13]
- ÁMBAR
- Diseñador Ascalaph [14]
- PATRÓN
- CHARMM
- COSMOS [15]
- CP2K
- Químico
- GROMACS
- GROMOS
- Mecánica de coordenadas internas (ICM)
- LAMPARAS
- MacroModel
- MDynaMix
- Entorno operativo molecular (MOE)
- NAMD
- Q
- Q-Chem
- espartano
- StruMM3D (STR3DI32) [16]
- Gitano
- X-PLOR
- Yasara
- Zodiaco [17]
Ver también [ editar ]
- Gráficos moleculares
- Dinámica molecular
- Editor de moléculas
- Campo de fuerza (química)
- Comparación de implementaciones de campos de fuerza
- Software de diseño molecular
- Modelado molecular en GPU
- Comparación de software para modelado de mecánica molecular
- Lista de software para el modelado molecular de Monte Carlo
Referencias [ editar ]
- ^ Zgarbova M, et al. (2010). "Compensación a gran escala de errores en campos de fuerza empíricos aditivos por pares: comparación de términos intermoleculares AMBER con cálculos rigurosos de DFT-SAPT". Phys. Chem. Chem. Phys . 12 (35): 10476–10493. Código Bibliográfico : 2010PCCP ... 1210476Z . doi : 10.1039 / C002656E . PMID 20603660 .
- ^ Allinger, NL; Chen, K .; Lii, J.-H. J. Comput. Chem. 1996 , 17, 642 https://onlinelibrary.wiley.com/doi/abs/10.1002/%28SICI%291096-987X%28199604%2917%3A5/6%3C642%3A%3AAID-JCC6%3E3.0.CO% 3B2-U
- ^ Kuo-Hsiang Chen, Jenn-Huei Lii, Yi Fan, Norman L. Allinger J. Comput. Chem. 2007 , 28, 2391 https://onlinelibrary.wiley.com/doi/full/10.1002/jcc.20737
- ^ Kuhn B, Kollman PA (octubre de 2000). "Unión de un conjunto diverso de ligandos a avidina y estreptavidina: una predicción cuantitativa precisa de sus afinidades relativas mediante una combinación de mecánica molecular y modelos de disolvente continuo". Revista de Química Medicinal . 43 (20): 3786–91. doi : 10.1021 / jm000241h . PMID 11020294 .
- ^ Huo S, Massova I, Kollman PA (enero de 2002). "Exploración computacional de alanina del complejo receptor de hormona de crecimiento humano 1: 1". J Comput Chem . 23 (1): 15-27. doi : 10.1002 / jcc.1153 . PMID 11913381 .
- ^ a b Mobley DL, Graves AP, Chodera JD, McReynolds AC, Shoichet BK, Dill KA (agosto de 2007). "Predicción de energías libres de unión de ligando absoluto a un sitio modelo simple" . J Mol Biol . 371 (4): 1118–34. doi : 10.1016 / j.jmb.2007.06.002 . PMC 2104542 . PMID 17599350 .
- ^ Wang J, Kang X, Kuntz ID, Kollman PA (abril de 2005). "Pruebas de bases de datos jerárquicas para la transcriptasa inversa del VIH-1 utilizando un modelo de farmacóforo, acoplamiento rígido, acoplamiento de solvatación y MM-PB / SA". Revista de Química Medicinal . 48 (7): 2432–44. doi : 10.1021 / jm049606e . PMID 15801834 .
- ^ Kollman PA, Massova I, Reyes C, et al. (Diciembre de 2000). "Cálculo de estructuras y energías libres de moléculas complejas: combinando mecánica molecular y modelos continuos". Acc Chem Res . 33 (12): 889–97. CiteSeerX 10.1.1.469.844 . doi : 10.1021 / ar000033j . PMID 11123888 .
- ^ Snow CD, Nguyen H, Pande VS, Gruebele M (noviembre de 2002). "Comparación absoluta de la dinámica de plegamiento de proteínas simulada y experimental". Naturaleza . 420 (6911): 102–6. Código Bibliográfico : 2002Natur.420..102S . doi : 10.1038 / nature01160 . PMID 12422224 .
- ^ Barth P, Alber T, Harbury PB (marzo de 2007). "Predicciones precisas, dependientes de la conformación de los efectos del solvente sobre las constantes de ionización de proteínas" . Proc Natl Acad Sci USA . 104 (12): 4898–903. Código bibliográfico : 2007PNAS..104.4898B . doi : 10.1073 / pnas.0700188104 . PMC 1829236 . PMID 17360348 .
- ^ Chakrabarti R, Klibanov AM, Friesner RA (julio de 2005). "Predicción computacional de secuencias de sitios activos enzimáticos y de unión a ligandos de proteínas nativas" . Proc Natl Acad Sci USA . 102 (29): 10153–8. Código Bibliográfico : 2005PNAS..10210153C . doi : 10.1073 / pnas.0504023102 . PMC 1177389 . PMID 15998733 .
- ^ Boas FE, Harbury PB (julio de 2008). "Diseño de unión proteína-ligando basado en el modelo energético de la mecánica molecular" . J Mol Biol . 380 (2): 415–24. doi : 10.1016 / j.jmb.2008.04.001 . PMC 2569001 . PMID 18514737 .
- ^ ACEMD - GPU MD
- ^ Ascalaph
- ^ COSMOS
- ^ StruMM3D (STR3DI32)
- ^ Zodiac Archivado el 16 de diciembre de 2009 en la Wayback Machine.
- Allinger NL, Burkert U (1982). Mecánica molecular . Publicación de la American Chemical Society. ISBN 978-0-8412-0885-8.
- Box VG (marzo de 1997). "La mecánica molecular de los enlaces de valencia cuantificados". Modelo J Mol . 3 (3): 124–41. doi : 10.1007 / s008940050026 .
- Box VG (12 de noviembre de 1998). "El efecto anomérico de los monosacáridos y sus derivados. Conocimientos del nuevo campo de fuerza de la mecánica molecular QVBMM" . Heterociclos . 48 (11): 2389–417. doi : 10.3987 / REV-98-504 .
- Recuadro VG (2004). "Efectos estereoelectrónicos en polinucleótidos y sus dobles hélices". J Mol Struct . 689 (1–2): 33–41. Código Bibliográfico : 2004JMoSt.689 ... 33B . doi : 10.1016 / j.molstruc.2003.10.019 .
- Becker OM (2001). Bioquímica y biofísica computacional . Nueva York, NY: Marcel Dekker. ISBN 978-0-8247-0455-1.
- Mackerell AD (octubre de 2004). "Campos de fuerza empíricos para macromoléculas biológicas: descripción general y problemas". J Comput Chem . 25 (13): 1584–604. doi : 10.1002 / jcc.20082 . PMID 15264253 .
- Schlick T (2002). Modelado y simulación molecular: una guía interdisciplinaria . Berlín: Springer. ISBN 978-0-387-95404-2.
- Krishnan Namboori; Ramachandran, KS; Deepa Gopakumar (2008). Química Computacional y Modelado Molecular: Principios y Aplicaciones . Berlín: Springer. ISBN 978-3-540-77302-3.
Enlaces externos [ editar ]
- Métodos de simulación de dinámica molecular revisados
- Mecánica molecular: es simple